从确认靶点到获批上市肺癌药crizotinib诞生记
一发现就是晚期!全球共有哪些胃癌靶向药物获批上市?
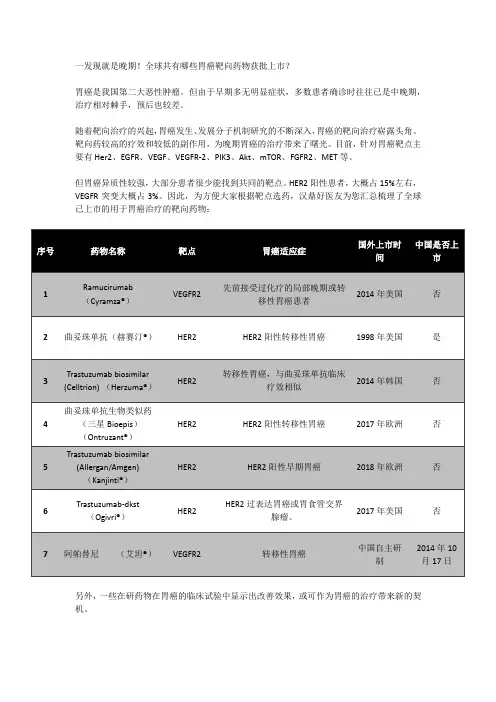
一发现就是晚期!全球共有哪些胃癌靶向药物获批上市?胃癌是我国第二大恶性肿瘤。
但由于早期多无明显症状,多数患者确诊时往往已是中晚期,治疗相对棘手,预后也较差。
随着靶向治疗的兴起,胃癌发生、发展分子机制研究的不断深入,胃癌的靶向治疗崭露头角。
靶向药较高的疗效和较低的副作用,为晚期胃癌的治疗带来了曙光。
目前,针对胃癌靶点主要有Her2、EGFR、VEGF、VEGFR-2、PIK3、Akt、mTOR、FGFR2、MET等。
但胃癌异质性较强,大部分患者很少能找到共同的靶点。
HER2阳性患者,大概占15%左右,VEGFR突变大概占3%。
因此,为方便大家根据靶点选药,汉鼎好医友为您汇总梳理了全球已上市的用于胃癌治疗的靶向药物:另外,一些在研药物在胃癌的临床试验中显示出改善效果,或可作为胃癌的治疗带来新的契机。
注:未完全统计近年来,以免疫检查点抑制剂为代表的免疫治疗已经彻底颠覆了晚期肿瘤的治疗模式。
在胃癌组织中也观察到了PD-L1的过表达,使抑制PD-1通路成为治疗胃或胃食管结合部癌患者的新靶点。
帕博利珠单抗(Keytruda):在既往接受治疗的胃癌患者中,具有抗肿瘤活性和可控的安全性。
由于疗效良好,获FDA批准用于治疗表达PD-L1(CPS≥1)的接受两种或以上治疗后进展的复发性局部晚期或转移性胃或胃食管结合部腺癌患者。
2018年7月中国获批上市,用于一线治疗失败的不可切除或转移性黑色素瘤,针对胃癌国内有临床试验在研。
纳武利尤单抗(Opdivo):在日本已获批用于化疗后进展的不可切除的晚期或复发性胃癌,无论患者的PD-L1状态。
此外,在美国,基于KEYNOTE-059研究,获批用于PD-L1表达阳性的胃癌和胃食管交界部癌。
2018年6月中国获批上市,用于治疗非小细胞肺癌,针对胃癌国内有临床试验在研。
12月17日,首个国产PD-1单抗——特瑞普利单抗注射液(商品名:拓益)上市,用于治疗既往标准治疗失败后的局部进展或转移性黑色素瘤。
2021.v5版非小细胞肺癌NCCN指南新鲜出炉!十大靶点治疗方案更新解读!

2021.v5版⾮⼩细胞肺癌NCCN指南新鲜出炉!⼗⼤靶点治疗⽅案更新解读!NCCN全称美国国⽴综合癌症⽹络(National Comprehensive Cancer Network ),每年都会发布各种恶性肿瘤临床实践指南,已成为全球临床医师遵循和认可的临床治疗标准和参考,意义重⼤。
2021年6⽉,NCCN官⽹将⾮⼩细胞肺癌(NSCLC)的临床实践指南更新⾄第五版,主要是两⼤重磅抗癌新药JNJ-6372和AMG510接连提前获批上市,实现了EGFR 20ins和KRAS两⼤靶点0靶向药的突破,对肿瘤患者意义重⼤,指南及时将这些抗癌“特药”纳⼊指南,给病友们带来新的选择和希望。
全球肿瘤医⽣⽹医学部为病友们整理了指南更新的最新治疗⽅案,希望给⼤家带来帮助。
NCCN指南:⾮⼩细胞肺癌需要检测的⼗⼤靶点⽬前,⾮⼩细胞肺癌NCCN指南推荐肺癌患者应检测的靶点为EGFR(19del和L858R)、EGFR 20ins、KRAS G12C、ALK、ROS1、BRAF、NTRK1/2/3、MET、RET、PD-L1⼗⼤靶点。
注:最新版指南推荐的检测中,将敏感的EGFR突变阳性,分为EGFR突变阳性(19del和L858R),以及EGFR 20外显⼦插⼊突变阳性,此靶点之前没有专门获批的靶向药物,4代EGFR药物Amivantamab-vmjw上市,使得其成为可⽤药靶点,这是EGFR外显⼦20插⼊突变肺癌患者的⾸款靶向疗法,是医学届对于这部分患者的⼀项重⼤进步,具有⾥程碑式的意义!最新版指南推荐的检测中,增加了KRAS G12C阳性突变,此靶点堪称史上“最难治”靶点,研发40年终于在今年迎来新药AMG510这款重磅药物上市。
肺癌NCCN指南⼗⼤靶点治疗⽅案更新解读EGFREGFR(epidermal growth factor receptor,ErbB-1或HER1)全称表⽪⽣长因⼦受体。
主要在肺腺癌、亚裔、⾮吸烟及⼥性患者中,⼤约有 15% 的⽩种⼈和 30-50% 的亚洲⼈中有 EGFR 基因突变。
6年来FDA首次批准上市肺癌药物-Xalkori

6年来FDA首次批准上市肺癌药物-Xalkori
佚名
【期刊名称】《药学与临床研究》
【年(卷),期】2011(19)5
【摘要】美国FDA日前通过简化程序批准了美国辉瑞公司研制的一种肺癌新药上市。
这是6年来FDA首次批准肺癌药物上市。
新药名为Xalkori,是一种激酶抑制剂,适用于间变型淋巴瘤激酶基因表达异常的晚期或局部转移的非小细胞肺癌患者,可以通过阻断对肿瘤细胞生长和存活起关键作用的多种细胞通路,使肿瘤保持稳定或消退。
【总页数】1页(P456-456)
【关键词】美国FDA;肺癌患者;药物上市;批准上市;肿瘤细胞生长;激酶抑制剂;基因表达异常;新药上市
【正文语种】中文
【中图分类】R95
【相关文献】
1.FDA批准首例用于治疗巨细胞动脉炎药物Actemra/FDA批准首个治疗ADHD
仿制药/FDA批准Ceritinib用于一线治疗ALK阳性的转移性非小细胞肺癌 [J],
2.降胆固醇药物立普妥的仿制药首次获FDA批准上市 [J],
3.美国FDA批准Xalkori(crizotinib)治疗一种罕见肺癌 [J], 夏训明
4.FDA首次批准艾滋病预防药物上市 [J],
5.FDA首次批准由转基因动物生产药物上市 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。
肿瘤分子靶向药物简介历史及上市药物

肿瘤的靶向药物选择——国内外已经上市的分子靶向(MTT)药物...一、靶向药物(targeted medicine)简介靶向药物是目前最先进的用于医治癌症的药物,是随着今世分子生物学、细胞生物学的发展产生的高科技药物。
靶向药物与常规化疗药物最大的不同在于其作用机理:常规化疗药物通过对细胞的迫害发挥作用,由于不能准确识别肿瘤细胞,因此在杀灭肿瘤细胞的同时也会殃及正常细胞,所以产生了较大的毒副作用。
而靶向药物是针对肿瘤基因开发的,它能够识别肿瘤细胞上由肿瘤细胞特有的基因所决定的特征性位点,通过与之结合(或类似的其他机制),阻断肿瘤细胞内控制细胞生长、增殖的信号传导通路,从而杀灭肿瘤细胞、阻止其增殖。
由于这样的特点,靶向药物不仅效果好,而且副作用要比常规的化疗方式小得多。
靶向药物可以分为以下几类:(一)小分子药物小分子药物一般是信号传导抑制剂,它能够特异性地阻断肿瘤生长、增殖进程中所必需的信号传导通路,从而达到医治的目的。
例如诺华制药生产的格列卫(Gleevec,通用名Imitinib)、阿斯利康生产的易瑞沙(Iressa,通用名Gefitinib)均属此类;(二)细胞凋亡诱导药物通过特异性地诱导肿瘤细胞凋亡,达到医治的目的。
如美国千年制药公司生产的Velcade (通用名bortezomib)、Genta公司生产的Genasense(oblimersen);(三)单克隆抗体例如赫塞汀(Herceptin,通用名Trastuzumab),用于医治HER2基因阳性(过量表达)的乳腺癌。
这种药物是通过抗原抗体的特异性结合来识别肿瘤细胞的。
除上述列举的已经进入临床利用的靶向药物外,另外还有多种靶向药物正在开发中。
二、肿瘤的靶向药物上市历史回顾:■白血病费城染色体开启靶向医治之门早在1960年,美国费城的研究者发现慢性髓性白血病(CML)患者中存在一个染色体异样。
数年后,研究者发现这是9号和22号染色体长臂易位的结果。
鲁先平:平衡药物靶点药效和副作用的创新药研发思路剖析

鲁先平:平衡药物靶点药效和副作用的创新药研发思路剖析药品是一种特殊商品,关系人命,应立足于科学,而非政治、宗教和商业利益。
作为海归团队中的一分子,我们享受在创新研发中,用自己学习掌握的科学智慧去治病救人、服务于社会的过程。
虽然我国医药产业与发达国家的差距暂时还很大,但我们在原创新药、原料药和制剂的国际化方面,以及生物医药的知识产权和金融交易方面,都实现了从无到有,并不断发展和攀升。
我相信,在“大众创业,万众创新”浪潮中,高科技企业将迎来发展的春天,中国将涌现出更多原创企业和创新团队。
——鲁先平汇聚中国精神,研发经济可及原创药15年前,时任Galderma北美研发中心主任鲁先平博士及Nanogen项目首席科学家程京博士提议创建基于化学基因组学的新型药物发现公司。
3年后的2001年3月21日,由清华大学鲁先平教授、程京教授(2009年当选中国工程院院士)、宁志强博士等5位资深留美的跨国药企高管和大学教授在深圳成立微芯生物——一家生物高科技领先企业,专注于原创小分子药物研发,满足尚未满足的临床需求。
微芯的理念是“原创、安全、优效、中国”,致力于为患者提供经济可承受、全新机制的新颖药物。
“我们想做中国真正的原创药。
然而,原创药的开发风险是最大的,周期也是最长的。
理想很美好,过程很艰辛。
”深圳微芯生物科技有限责任公司的主要发起和筹建人,总裁兼首席科学官鲁先平说。
2001年我国国内生产总值(GDP)9.59万亿元,医药工业总产值2767亿元,医药工业总产值占GDP的2.88%,而美国和发展中国家的这一数字分别是9.0%和4.2%。
《药物发现自然评论》(Nature Reviews Drug Discovery)杂志2011年的文献显示,2003~2010年187个新药中,源自中国的新药(国家食品药品监督管理总局统计数字)有70种,但其中真正的原创药(First-in-class)寥若晨星。
2003~2010年,相关国际化合物专利授权的我国在研1.1类和1-2类化学药及1类生物药,在美国或欧洲获准进入临床研究阶段的仅有2个。
克唑替尼中文说明书

【药物名】Xalkori【商品名】Crizotinib(克唑替尼)【美国上市时间】o ROS-1阳性非小细胞肺癌;o FDA 批准的检测方法确定的间变性淋巴瘤激酶(ALK)阳性的局部晚期患者;上市时间:2011年【类别】酪氨酸酶抑制剂【靶点】ALK【分子结构】分子式:C21H22C l2FN5O化学名:(R)-3-[1-(2,6-Dichloro-3-fluorophenyl)ethoxy]-5-[1-(piperidin-4-yl)-1H-pyrazol-4-yl]pyridin-2-amine结构式为:分子量为:KDa【生产公司】Pfizer 辉瑞公司【购买地】美国【剂型和规格】口服胶囊,剂量为250mg和200mg。
250mg胶囊:硬明胶胶囊,大小0,粉色不透明帽和体,在帽上有“Pfizer”和体上“CRZ 250” ,60胶囊瓶:NDC 0069-8140-20。
200mg胶囊:硬明胶胶囊,大小1,白色不透明体和粉色不透明帽,帽上有“Pfizer”和体上“CRZ 200”,60胶囊瓶:NDC 0069-8141-20。
【本质】克唑蒂尼胶囊硬壳含250 mg或200 mg的克唑蒂尼胶体二氧化硅,微晶纤维素,无水磷酸氢钙,羟基乙酸淀粉钠,硬脂酸镁和硬胶囊胶囊壳为无活性成分。
粉红色不透明胶囊壳组分含明胶,二氧化钛,和氧化铁红。
白色不透明胶囊壳组分含明胶和二氧化钛。
印刷油墨含有虫胶,丙二醇,强氨水溶液,氢氧化钾,和黑色氧化铁。
【作用机理】克唑替尼是酪氨酸激酶受体包括ALK,肝细胞生长因子受体(HGFR, c-Met),ROS1(c-ros),和酪氨酸激酶(RON)的一种抑制剂。
易位可影响ALK基因导致致癌融合蛋白的表达。
ALK融合蛋白的形成导致激活和基因表达和增加细胞增殖有贡献信号的调节异常而生存肿瘤表达这些蛋白。
克唑蒂尼就是通过阻断对肿瘤细胞生长与存活起关键作用的多种细胞通路,导致肿瘤的稳定或消退。
2024年克唑替尼市场需求分析
2024年克唑替尼市场需求分析1. 介绍克唑替尼(Crizotinib)是一种常用的抗癌药物,属于酪氨酸激酶抑制剂(TKI)类药物。
它主要用于治疗ALK(成纤维母细胞生长因子受体激酶)重排阳性的非小细胞肺癌(NSCLC)和ROS1(ROS receptor tyrosine kinase)重排阳性的晚期非小细胞肺癌。
本文将对克唑替尼市场需求进行分析,为相关企业制定市场策略提供基础数据。
2. 市场规模克唑替尼是肺癌治疗领域的重要药物之一,其市场规模受多个因素影响。
根据数据显示,全球每年新确诊的非小细胞肺癌病例超过百万,其中约有5-7%的患者具有ALK或ROS1重排。
而这一患者群体中,大约有50%的患者适合使用克唑替尼进行治疗。
因此,克唑替尼在全球的市场潜力巨大。
3. 市场竞争目前,关于ALK或ROS1重排阳性的非小细胞肺癌治疗的选择有限,其中包括克唑替尼在内的几种药物,如氟西汀(Alectinib)和雷莫芦单抗(Ramucirumab)。
这些药物在临床研究和数据支持方面存在差异,因此在市场上存在一定程度的竞争。
除了药物本身的竞争,市场还受到价格、渠道和医保政策等因素的影响。
克唑替尼的价格较高,患者承担的治疗费用较大,这对市场需求带来一定压力。
此外,不同地区的医保政策对克唑替尼的报销情况也存在差异,这在一定程度上影响了患者的购买意愿和药物的市场份额。
4. 市场趋势近年来,克唑替尼的市场趋势呈现以下几个方面的特点:a. 个体化治疗需求增加随着分子生物学技术的发展,越来越多的肺癌患者能够通过基因检测明确其ALK或ROS1的重排情况,从而确定是否适合使用克唑替尼进行个体化治疗。
这使得克唑替尼在临床应用中的需求有所增加。
b. 临床研究不断深入克唑替尼作为一种新型抗癌药物,其在临床研究方面还有很大的发展空间。
目前,研究人员正在探索克唑替尼在其他肿瘤类型中的应用,如转移性胃肠道起源的肿瘤和乳腺癌等。
这些研究结果将进一步拓宽克唑替尼的市场需求。
肺腺癌基因突变靶点
肺腺癌基因突变靶点全文共四篇示例,供读者参考第一篇示例:肺腺癌是一种常见的恶性肿瘤,属于呼吸系统肿瘤的一种。
据统计,肺腺癌在所有恶性肿瘤中的发病率和死亡率均排名第一。
肺腺癌的发病机制十分复杂,其中基因突变是导致肺腺癌发生和发展的重要原因之一。
而基因突变靶点是允许医生精准干预的重要标志。
本文将对肺腺癌基因突变靶点进行详细介绍。
第一篇文章是关于EGFR基因突变靶点的研究。
EGFR(表皮生长因子受体)是肿瘤细胞生长和分化的重要信号传导通路之一,EGFR基因突变是肺腺癌中最常见的突变之一。
通过对EGFR基因的突变进行检测,可以明确患者对EGFR抑制剂的治疗反应,为临床治疗提供重要依据。
研究表明,EGFR基因突变靶点在肺腺癌的个体化治疗中具有重要作用,并且与肺腺癌的预后密切相关。
第二篇文章是关于ALK基因突变靶点的研究。
ALK(酪蛋白激酶)是一种重要的蛋白激酶,在肺腺癌中ALk基因突变是少数能够激活信号通路的突变之一。
目前,临床已经开发出针对ALK基因突变的靶向治疗药物,比如克唑替尼(Crizotinib)。
通过对ALK基因突变的检测,可以明确患者对靶向治疗的治疗效果,提高治疗的成功率,延长患者的生存期。
通过对肺腺癌基因突变靶点的研究,不仅可以更准确地评估患者的病情和预后,还能为临床治疗提供更为个体化的治疗方案。
随着对肿瘤基因突变的深入研究,相信肺腺癌的治疗水平将不断提高,患者的生存期也将得到进一步延长。
希望本文可以帮助更多的医生和患者了解肺腺癌基因突变靶点的重要性,推动肺腺癌的个体化治疗进程。
第二篇示例:肺腺癌是肺癌中最常见的一种类型,它起源于肺部的腺体组织。
肺腺癌的发病率逐年上升,给患者和家庭带来了严重的健康负担。
为了更好地了解和治疗肺腺癌,科学家们对其基因突变靶点进行了深入研究。
基因突变是导致肺腺癌发生的重要原因之一。
在肺腺癌的发展过程中,一系列基因的突变和异常表达会导致正常细胞发生恶性变化,最终形成肿瘤。
肺癌分子靶向药物治疗的研究进展
肺癌分子靶向药物治疗的研究进展分子靶向治疗是指针对参与肿瘤发生、发展过程的细胞信号转导和其他生物学途径的治疗手段,具有高效和低不良反应的特点。
随着近年来肿瘤相关研究的不断进步,在恶性肿瘤的个体化治疗和靶向治疗方面取得了令人瞩目的进展。
本文主要针对肺癌的分子靶向治疗研究进展进行概括总结。
标签:肺癌;血管内皮生长因子受体;表皮生长因子受体;肿瘤干细胞;肿瘤抑制基因肺癌是当前发病率和死亡率最高的肿瘤之一,80%以上患者就诊时已处于晚期,失去手术机会。
目前,肿瘤化疗已经处于治疗瓶颈,毒副反应大,有效率低,5年生存率不足15%。
近年来发展起来的靶向治疗,具备高效、低副反应等特点,已成为目前肺癌治疗的研究热点。
其作用靶点包括细胞内信号转导通道中重要的蛋白质、酶、细胞表面的生长因子受体,而广义的分子靶点则包括参与肿瘤细胞分化、凋亡、迁移、浸润、淋巴结转移、全身转移等过程的从DNA到蛋白酶水平的任何亚细胞分子。
1 血管内皮生成因子(VEGF)VEGF是一种细胞因子,它能诱导内皮细胞增生、蛋白酶的表达、抗内皮细胞凋亡和细胞重组,最终形成毛细血管。
在病理血管生成方面,它还能增强血管的通透性,形成不成熟的血管网络。
血管上皮生长因子能够刺激血管内皮细胞的增生,在大多数人体肿瘤组织中,VEGF的表达大大高于其他正常组织[1]。
研究证实贝伐单抗以VEGF作为靶点,具有一定的抗肿瘤作用[2]。
VEGF家族包含6个生长因子(VEGF-A、VEGF-B、VEGF-C、VEGF-D、VEGF-E以及胎盘生长因子)和3个受体(VEGFR-1、VEGFR-2(KDR/FIk.1)和VEGFR-3)。
VEGF 的过度表达与肿瘤进展及不良预后相关。
目前针对VEGF途径的治疗包括抗VEGF单克隆抗体和VEGFR-TKI两大类。
1.1贝伐单抗(Bevacizumab)Bevacizumab即重组人抗VEGF单克隆抗体,可与VEGFR结合,阻断肿瘤血管的细胞信号转导,抑制肿瘤血管生长,抑制肿瘤细胞。
ROS1融合基因突变非小细胞肺癌的诊断与ROS1抑制剂研究进展
DOI:10.3969/j.issm1672-9463.2021.04.025•综述. ROS1融合基因突变非小细胞肺癌的诊断与ROS1抑制剂研究进展王大壮王泽雨陈立江王欣近年来随着社会日益进步,人类疾病也越来越复杂。
在众多疾病中,癌症的发病率与日俱增,已成为一种常见的疾病,且治疗难度较大。
诸多癌症中肺癌的发病率和致死率分别可达11.6%和18.4%[1],在我国更是居于首位。
其中非小细胞肺癌(NSCLC)占我国肺癌患者的80%囱,且大多数都是高龄患者,早期不重视,发现较晚,失去了手术机会,5年生存率很低叫常规的治疗方法包括手术、放疗和化疗等,效果欠佳,给患者带来巨大痛苦。
近年来随着个体化治疗理念的普及,靶向治疗非小细胞肺癌成为热点叫随着基因分析和基因检测技术的发展以及对相关致癌基因研究的逐步深入,表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)等肿瘤相关靶点相继被检测出来,针对它们的靶向药物也相继上市。
这些靶向药物在临床中疗效良好,毒副作用明显降低,但也存在着长期使用后出现耐药的问题。
近年来,也不断有一些新的驱动基因被发现,如MET基因、HER-2及R0S1融合基因等,针对它们的靶向药物也在不断研发中。
ROS1基因是上世纪80年代于UR2鸟肉瘤病毒中发现的具有独特致癌作用的原癌基因,野生型的R0S1定位于染色体6q21上,共编码2347个氨基酸[5],尚未发现相应的活化配体,关于ROS1的生理功能也尚不清楚叫目前共发现了包括CD47等22种ROS1基因融合形式叫ROS1基因重排在非小细胞肺癌患者中的发生率为1%~2%,常见于年轻、不吸烟或少量吸烟的腺癌患者中,而且年龄偏小,多为女性、亚裔,与ALK阳性患者表型有着重叠性咲训,且有研究发现ROS1的进化过程与ALK密切相关,两者在激酶结构域内有49%同源性的氨基酸序列[11],目前已上市的ALK靶向抑制剂,大部分能有效控制ROS1融合患者的病情[12]0但由于ROS1基因重排在非小细胞肺癌患者中发生概率较低,这一分子亚型在治疗中常被忽视,目前还没有单纯针对ROS1融合突变的抑制剂,但是每年都出现大量的肺癌新病例,使得研究人员对ROS1抑制剂的开发更加关注,基于ALK和ROS1的激酶结构域的相似性,以及ALK靶向抑制剂对ROS1融合患者的治疗效果,开发ROS1靶向抑制剂或ALK/R0S1双重靶向抑制剂具有高度的可行性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
从确认靶点到获批上市肺癌药crizotinib诞生记
酪氨酸激酶的一种——间变性淋巴瘤激酶(ALK)第一次被认定为潜在的癌症治疗靶点还是约在20年前。
那时,它作为与核仁磷酸蛋白(nucleophosmin)所组成的融合蛋白的一部分,被发现于间变性大细胞淋巴瘤(ALCL)的细胞中。
如今我们已知,这一融合蛋白的形成其实是染色体重排突变导致的,其导致的结果为ALK的异常激活,进而引发癌变。
然而,在肺癌领域,ALK直到2007年才被认为是潜在的治疗靶点。
那时,来自日本自治医科大学的间野博行(Hiroyuki Mano)教授发现,在6.7%的非小细胞肺癌(NSCLC)患者体内,ALK的胞内激酶结构域与EML4蛋白形成了融合蛋白。
在体外实验中,他的研究团队进一步表明,ALK的抑制剂WHI-P154能显着抑制表达有EML4-ALK融合蛋白的BA/F3细胞的生长。
基于这样的结果,间野教授认为,ALK是ALK阳性NSCLC的潜在治疗靶点。
这一成果最终发表在《Nature》期刊上。
形成ALK-EML4融合蛋白的基因重排
巧合的是,就在前一年,另一个ALK的小分子抑制剂刚刚进入临床试验。
这就是PF-02341066,也就是如今的上市药物crizotinib。
不过,crizotinib那时是作为受体酪氨酸激酶c-MET的抑制剂进入临床试验的,尽管人们那时也已知它同样可抑制ALK。
基于上述研究成果,有人认为,ALK在历经基因重排后对于crizotinib的敏感性可显着提高,因此可作为NSCLC的治疗靶点。
当
然,要想证明这一点并不容易,因为我们需要首先能够知道这些患者体内的ALK基因是否发生了重排突变,然后再去测试crizotinib等药物能否对他们起到疗效。
John Iafrate教授
可幸的是,来自麻省总医院(MGH)的John Iafrate教授很快找到了解决方案。
他的研究团队利用荧光原位杂交探针技术,开发出了SNaPshot检测法,能够迅速确定患者的肿瘤中是否存在ALK基因重排突变。
就这样,研究者们对NSCLC肿瘤进行了大规模分析,发现了多个可致癌的重排特征,并筛选出了携带相关突变的患者群体。
终于,在2007年12月,第一个ALK阳性的晚期NSCLC患者在临床试验中服用了crizotinib。
奇迹出现了——这位患者的症状很快就出现了明显缓解!
然而,这还不是此次试验唯一令人称奇的地方。
要知道,这距离间野教授那篇《Nature》论文的发表仅仅才过去四个月!
间野博行教授
就这样,在上述试验结果的激励下,大规模针对ALK阳性NSCLC
患者的筛选和招募工作在全球范围内展开。
他们将陆续进入crizotinib 的1期临床试验,以期获得一次重生的机会。
Crizotinib的有效性和安全性:获得FDA加速批准的基础
果不其然,在接下来的1期和2期临床试验中,crizotinib表现出了显着的疗效。
在一项161名ALK突变阳性NSCLC患者的1期临床试验中,crizotinib的客观响应率达到了61%。
从开始服药到显现疗效的中位数时间仅为8周,给试验者们留下了深刻的印象。
当试验进行到了2007年6月时,患者的中位无进展生存期达到10个月,这与EGFR抑制剂在治疗EGFR突变阳性晚期NSCLC的过程中所取得的数据相近。
紧接着,crizotinib初步的2期临床试验结果被公布于7月的底14届世界肺癌大会(WCLC)上。
在133名ALK阳性晚期NSCLC患者中,crizotinib的客观响应率达51%,12周时的疾病控制率达到74%。
Crizotinib结构
51%和61%,这样的客观响应率数据是十分令人鼓舞的。
要知道,参与上述1期试验中的大部分以及2期中的全部人员均为经治患者,而对于晚期NSCLC患者而言,标准的二线或三线化疗的客观响应率仅为10%。
不仅如此,crizotinib的安全性也是经得起考验的,大多数患者都能够承受它的副作用。
基于这样的结果,美国FDA于2011年8月加速批准了crizotinib 的上市,用于ALK阳性的晚期NSCLC的治疗,而这距离间野教授最初发现NSCLC中的ALK基因重排仅仅才过去四年!相信么?这就是从最初的靶点确认到药物最终上市所需的时间。
在这之后的2013年11月,crizotinib终于获得了FDA的正式批
准,商品名为Xalkori。
更为锦上添花的是,crizotinib的适应症在这之后还得到了进一步拓展。
今年三月,FDA批准该药物用于ROS-1基因突变阳性的晚期NSCLC的治疗,并授予其突破性疗法认定。
与ALK 一样,ROS-1基因同样编码着一种酪氨酸激酶。
Crizotinib带给患者的生存收益如何?
总生存率无疑是显示药物临床收益的最佳指标,同时也是最能反映其疗效的临床终点,crizotinib在这一点上也毫不逊色。
分析显示,1期临床试验中患者的总生存率得到了显着提高。
将crizotinib作为其二线或三线疗法的患者的一年期和二年期的总生存率分别达到了74%和54%。
相比之下,只接受了标准二线疗法的患者的这两项指标分别只有44%和12%,风险比为0.36。
当然你可能会说,也许ALK基因重排突变本身减轻了癌症的严重
性,从而有着更好的预后,而未必是crizotinib。
为了检验这样的可能性,研究者们专门比较了ALK和EGFR基因野生型以及两基因均发生突变的患者,在未服用crizotinib情况下的总生存率。
结果显示,二者之间没有显着区别。
值得注意的是,在NSCLC患者中,这两种基因未发生突变是较为普遍的情形,而这样的患者由于得不到靶向治疗通常预后较差。
我们该如何筛查和治疗ALK阳性的晚期NSCLC患者?
从crizotinib诞生的故事中我们可以看出,该疗法的关键在于能够筛查出ALK基因重排突变阳性的患者,让他们能够接受到高效且安全的治疗。
在很多的大型研究中心,很多晚期NSCLC患者都会接受这样的基因检测,从而为研究者积累了大量的患者数据。
通过对这些数据的分析,我们发现,ALK基因重排突变在某些特定群体中有着较高的发生率,尤其是那些未患有腺癌以及没有/少有吸烟习惯的年轻患者。
当然,ALK基因重排突变阳性在有着吸烟积习的患者群体中也是存在的,而这些患者同样获益于crizotinib。
可导致NSCLC的基因突变的概率分布
因此,我们显然应该尽可能多地为NSCLC患者进行基因检测。
如果实在做不到覆盖所有的患者,那么也应把有限的机会更多地留给不
吸烟或者少有吸烟的患者,除非已知他们携带有可被靶向治疗的EGFR 或KRAS基因的突变。
当被确定为ALK基因重排突变阳性后,这些患者便应当得到crizotinib的治疗。
值得注意的是,FDA并没有指定任何先期治疗作为使用crizotinib的前提条件,这说明任何新确诊的ALK阳性晚期NSCLC患者均可服用该药。
酪氨酸激酶抑制剂的作用机制
不过,像很多其他成功的靶向疗法一样,crizotinib也存在复发的问题,后者通常在开始服用一年后出现。
确实,获得性酪氨酸激酶抑制剂(TKI)抗性给crizotinib等靶向疗法带来了困扰。
如今,数种可导致抗性的机理都已被发现,包括ALK的酪氨酸激酶(TK)结构域上发生了某些新的突变。
要想应对这一问题,我们显然首先要弄清楚究竟发生了什么样的抗性突变,这就要求医生能够持续性地对复发患者进行取样分析。
这些分析结果对于后crizotinib阶段的治疗是至关重要的。
从最初的靶点确认到上市批准,靶向抗癌药物crizotinib只用了四
年,在制药史上留下光辉的一页。
我们希望crizotinib能够更多地造福于全球的癌症患者,继续为精准医疗的发展和推广做出贡献!
参考资料
[1] Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer.
[2] The Crizotinib Story: From Target to FDA Approval and Beyond
[3] FDA expands use of Xalkori to treat rare form of advanced non-small cell lung cancer
[4] FDA Approves Crizotinib。
