麦氏重排
麦氏重排条件
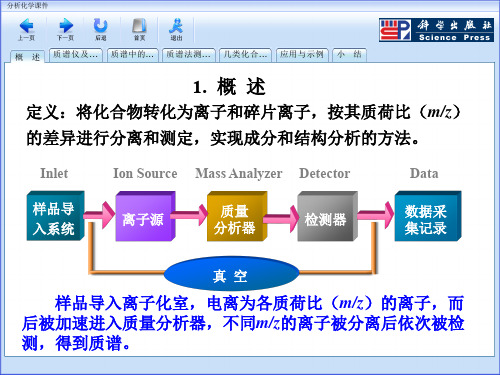
1. 磁偏转 2. 四极杆 3. 离子阱
应用与示例 小 结
1.高能打拿极 2.电子倍增器
样品导 入系统
离子源
质量 分析器
检测器
数据采 集记录
真空
10-3 ~ 10-5 Pa
1. 大量的氧会烧坏离子源的灯丝; 2. 用作加速离子的几千伏高压会引起放电; 3. 引起额外的离子-分子反应,改变裂解模型,使谱图复杂化
分析化学课件
概 述 质谱仪及... 质谱中的... 质谱法测... 几类化合... 应用与示例 小 结
质谱图:棒图 ( bar graph )
100
57
43
71
50
29 41
27
55
99 113
128(M.+)
80
100 120 m/z
横坐标:质荷比 m/z —— 定性;
纵坐标:离子的相对强度 ( 以基峰为100% )—— 定量;
离子源
质量 分析器
检测器
Data
数据采 集记录
真空
样品导入离子化室,电离为各质荷比(m/z)的离子,而 后被加速进入质量分析器,不同m/z的离子被分离后依次被检 测,得到质谱。
分析化学课件
概 述 质谱仪及... 质谱中的... 质谱法测... 几类化合...
1. 直接导入 1. 电子轰击 2. 色质联用 2. 化学电离
MS 的用途:
(1)测定相对分子质量 (2)鉴定化合物( 确定分子式 ) (3)推测未知物结构 (4)测定分子中 Cl、Br 等元素的原子数 (5)与色谱联用
分析化学课件
概 述 质谱仪及... 质谱中的... 质谱法测... 几类化合... 应用与示例 小 结
浅析质谱中的广义麦式重排
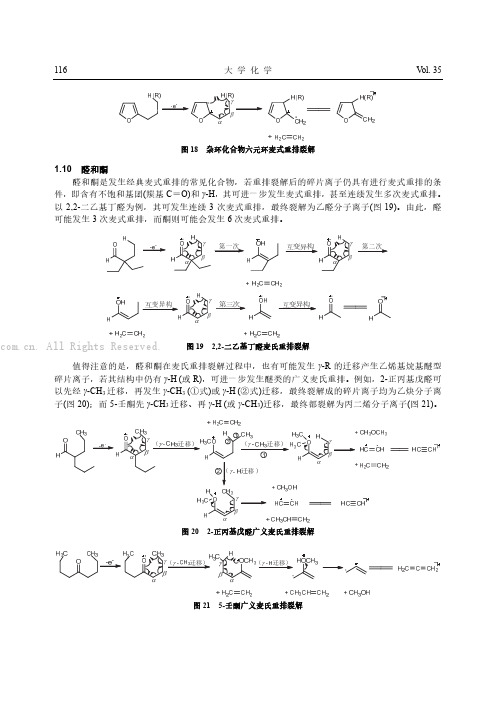
环过渡态发生的协同裂解;此外,有机化合物也可以通过六元环或五元环过渡态进行协同裂解,发
生 γ-H (或 R)、β-H (或 R)的迁移,产生更多的碎片离子,裂解过程合理可行,便于质谱解析。广义
麦式重排是在经典麦式重排基础上的进一步拓展,其裂解方式与规律有助于质谱解析、化合物结构
4 次麦式重排,最终裂解为乙酸分子离子(图 22)。
H
O
H
H
-e-
O
O
H
H
第一次
OH
+ H2C
H
O
H
互变异构
H
H
第三次
OH
+ H2C
图 22
H
第二次
OH
+ H2C
H
互变异构
O
O
OH
第四次
CH2
CH2
OH
O
CH3
+ H2C
CH2
CH3
H
O
CH2
O
O
H
O
O
O
O
互变异构
H
O
CH3
酯类化合物多次麦氏重排裂解
Alum(K); Macroscopic crystallographic planes; Self-normality
不同的晶体具有不同的宏观形状,如理想的胆矾晶体是平行六面体,而理想的明矾晶体为正八
面体。但在培养过程中,晶体常出现截棱或截角的六面体、八面体。本文在 Bravais 原理的基础上,
对晶体的宏观形状及缺陷提出简单的热力学假设,并通过明矾培养实验对理论进行半定量的解释,
有机波谱分析考试题库及答案

第二章:紫外吸收光谱法一、选择1. 频率(MHz)为4.47×108的辐射,其波长数值为(1)670.7nm (2)670.7μ(3)670.7cm (4)670.7m2. 紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了(1)吸收峰的强度(2)吸收峰的数目(3)吸收峰的位置(4)吸收峰的形状3. 紫外光谱是带状光谱的原因是由于(1)紫外光能量大(2)波长短(3)电子能级差大(4)电子能级跃迁的同时伴随有振动及转动能级跃迁的原因4. 化合物中,下面哪一种跃迁所需的能量最高(1)σ→σ*(2)π→π*(3)n→σ*(4)n→π*5. π→π*跃迁的吸收峰在下列哪种溶剂中测量,其最大吸收波长最大(1)水(2)甲醇(3)乙醇(4)正己烷6. 下列化合物中,在近紫外区(200~400nm)无吸收的是(1)(2)(3)(4)7. 下列化合物,紫外吸收λmax值最大的是(1)(2)(3)(4)二、解答及解析题1.吸收光谱是怎样产生的?吸收带波长与吸收强度主要由什么因素决定?2.紫外吸收光谱有哪些基本特征?3.为什么紫外吸收光谱是带状光谱?4.紫外吸收光谱能提供哪些分子结构信息?紫外光谱在结构分析中有什么用途又有何局限性?5.分子的价电子跃迁有哪些类型?哪几种类型的跃迁能在紫外吸收光谱中反映出来?6.影响紫外光谱吸收带的主要因素有哪些?7.有机化合物的紫外吸收带有几种类型?它们与分子结构有什么关系?8.溶剂对紫外吸收光谱有什么影响?选择溶剂时应考虑哪些因素?9.什么是发色基团?什么是助色基团?它们具有什么样结构或特征?10.为什么助色基团取代基能使烯双键的n→π*跃迁波长红移?而使羰基n→π*跃迁波长蓝移?11.为什么共轭双键分子中双键数目愈多其π→π*跃迁吸收带波长愈长?请解释其因。
12.芳环化合物都有B吸收带,但当化合物处于气态或在极性溶剂、非极性溶剂中时,B吸收带的形状有明显的差别,解释其原因。
质谱裂解机理中的特征裂解方式

质谱裂解机理中的特征裂解方式有机质谱中的裂解是极其复杂的,但是通过对其质谱裂解方式和机理的探讨研究,我们可以发现有一些特征结构裂解方式在有机质谱的裂解中是普遍存在的,是世界上的大量质谱学家通过对大量的有机质谱裂解方式进行观察、研究后的概括性总结。
所以其具有很重要的参考价值和应用价值,所以在有机质谱解析过程中,必须予以遵循,如此方能得到合理的质谱裂解方式和解析结果。
通过概括总结我们发现有机质谱中大部分化合物具有以下几种特征裂解方式:α裂解、苄基裂解、烯丙基裂解、麦氏重排裂解、DRA 裂解(逆狄尔斯阿尔德反应),几种特征裂解方式的强弱顺序如下:苄基裂解>α裂解、i 裂解>麦氏重排裂解、DRA 裂解>烯丙基裂解当然这种顺序不是一成不变的,随着化合物的结构发生改变,这些特征裂解方式的顺序有可能会发生改变,有机化合物质谱裂解大致可以分为两类α裂解(均裂)、β裂解,我们上面所讲的苄基裂解、烯丙基裂解、麦氏重排裂解、DRA 裂解都属于β裂解。
下面我们对几种特征裂解方式做以说明。
1、特征裂解方式一、α裂解α裂解是指凡具有C-X 单键基团和C=X 双键基团(其中X=C 、O 、S 、Cl 等)的有机分子,与该基团原子相连接的单键、称之为α键,在电子轰击条件下,该键很容易断裂因而称之为α断裂。
断键时成键的两个原子各自收回一个电子,这是由游离基中心引发的反应,原动力来自游离基的电子强烈配对倾向,所以α断裂属于均裂。
其裂解的机理及通式如下: I 饱和中心R 2C YR +H 2CCH2+ II 不饱和杂原子R RCY +几类化合物的α裂解 (1)H 3CCH 2OH 3H 2COH + (2)H 3CH 2C H 2CCH 3H 2COH 2CCH 3+3(3)CH 3OαO+H 2C CH 3(4)H NOCH 3O αH NO+OCH 3引发α断裂的倾向是由游离基中心给电子的能力决定的,一般来讲N>S 、O 、π、烷基>Cl 、Br>H ,同时α断裂遵循最大烷基游离基丢失的原则。
苯环上的麦氏重排

苯环上的麦氏重排苯环,这一现象被称为“麦氏重排”,作为一种重大的化学现象,一直受到学者的研究。
在20世纪50年代,麦哲伦(F.C.McGuire)及其同事将它发现,并被普遍认可,给整个伦理学界带来了前所未有的冲击。
麦氏重排是指一种通过化学反应将苯环原质及结构重新排列的现象。
麦氏重排发生在苯烯类有机化合物的循环氢还原过程中,以其易分解的中间产物为特征。
其中,以芳香环为核心主题,其中所有的取代基都会发生变化,从而产生一种新的中间体。
麦氏重排的发生,与反应温度与时间有关,可以通过控制温度及时间来调节反应速率,从而获得更高的重排率。
在此基础上,麦氏重排技术最终在药物合成、染料、香料及医药中得到了广泛的应用。
麦氏重排本身也包含了一些重要的化学原理,在伦理学界也受到了诸多的研究与探讨。
早期的发现和研究,将麦氏重排的一些理论及实践应用到了药物合成等化学领域,使其成为一门有趣及重要的学科。
麦氏重排也是一个综合性的研究课题,其中涉及了化学、分子生物学、物理化学、化学工程等多个学科领域。
由于涉及有机合成、芳香环分子还原、稳定性及反应热势等方面,多年来,麦氏重排在学术界有着广泛的研究。
比如,在化学领域里,一些有机合成方法也受到了麦氏重排的影响,其中涉及到了可以进行高稳定的反应的原料的选择,以及稳定的反应方法,当然还包括有效控制反应中产生的热势。
同时,在生物学及分子生物学方面,麦氏重排也受到研究,主要是针对其对一些蛋白质分子的影响。
比如,研究者会研究麦氏重排对一些激酶的影响,以及它对某些药物的作用机理等。
另外,在物理化学的研究中,也有一些涉及到麦氏重排的实验报道,比如在液体结构的研究中,研究者可以从液体的性质中,了解到溶质的结构变化对麦氏重排反应的影响,以及麦氏重排反应中涉及到的一些物理化学参数。
总之,麦氏重排本身由一种基本的化学反应而来,但正是这种简单的化学反应,给学术界带来了巨大的挑战。
它不仅仅是一种重要的化学现象,也给化学领域带来了深刻的影响,比如药物合成、染料制造、香料及医药等。
麦氏重排

单纯裂解:仅一根键发生裂解称为单纯裂解。
其断裂的方式有均裂、异裂和半均裂三种。
①均裂(α断裂):在键断裂后,两个成键电子分别保留在各自的碎片上的过程,通式
为:,反应的动力来自:自由基强烈的电子配对倾向。
例子:a.
b.
②异裂(i断裂):在键断裂后,两个成键的电子全部转移到一个碎片上的裂解过程,通式为:,反应的动力:电荷引发(又称诱导效应)。
例子:a.
b.
③半均裂(σ断裂):离子化键的断裂过程,通式为:。
重排:有些离子不是由单纯裂解产生,而是通过断裂两个或两个以上的键,结构重新排列形成的,这种裂解称重排。
重排的方式很多,其中最常见的是麦氏重排和反Diels-Alder重排。
1.麦氏重排
发生条件:①化合物中含有不饱和中心基团C=X或C≡X (X为O,N,S,C)。
②这个基团相连的键上有γ氢原子。
重排过程:γ氢原子转移到不饱和中心的一个原子上,同时,β键发生断裂,脱掉一个中性分子。
例子:a. 2-戊酮
b. 1-己烯
2.反Diels-Alder重排(RDA反应)
反应条件:分子中存在含一根π键的六元环重排过程:
例子:a.
b.。
有机分子裂解类型与过程新
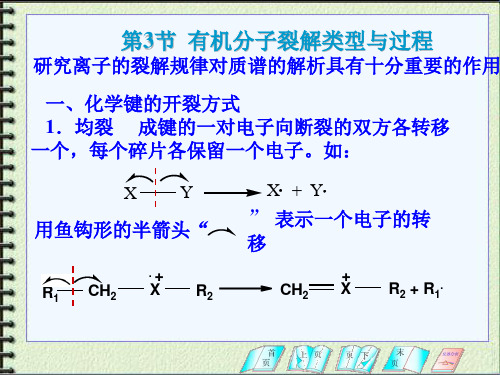
-H
R
+
+
H + -H + R
烷基苯
+
2.逆Diels-Alder反应 (RDA):
RDA(in MS) DA(有机合成)
+
+
.
.
+
.
+
or
+
+
.
+
3、四元过渡重排
常见化合物类型 :醚、酯、酚、胺、酰胺 (1)分子离子的四元环过渡重排
+. Y R z H CH R' R YH
·
·+
羧酸酯
+ OH · OCH3
醛
酮 腈
44
58 41
+NH ·
+ OH ·
·
或
甲酸酯
酰胺 硝基化合物
46
59 61
+ OH · O H + OH
H
+ OH
·
· + NH
NH 2 OH +N · O
R 羰基化合物
H + O R' +
-H
R
O+
+
R'
R' = H, R, OR, OH, NH2 R 烯烃化合物 H
X Y X+ + Y 或 X Y + X + Y
用整箭头形式“
O
R1
”表示一对电子的转移。
O + R1 + C
C
R2
R2
异裂伴随正电荷的 转移,均裂正电荷的位置不变。 3.半异裂 已离子化的σ键发生断裂,仅存的一个 成键电子转移到一个碎片上。
苯环上的麦氏重排

苯环上的麦氏重排
麦氏重排是一种在苯环上的重要的有机反应,被称为是有机反应的永恒主题。
它得到了化学家和研究者们的广泛关注,也受到了国内外大学教授们无穷的研究热情。
麦氏重排是一种由具有一定扭转引发的反应,根据新月钠与羟基冰片反应,通
过加热,能够将一氟三苯乙酰羧酸变为3-芴醛二酢胺(3-Me-2-acetoxybenzoic acid)。
其反应机理为,先在氟原子位置上受到热破解,引发向外扭转,而这种扭
转又受到有机化学的力学原理的支持,出现的新的化合物三-醛二-酢胺就是其最终反应产物。
实际生活中,麦氏重排反应在药物、农药以及某些有机物的制取中,有着重要
的作用。
它历尽沧桑,无论是苯环上的热反应,还是芴醛向羟基苯醛的不对称还原,其突出的性能和可持续性,受到了化学行业界的一致好评。
此外,麦氏重排反应也同时涉及到由热引发及复制反应,而由这类反应得出的
农药成分,能够有效地抑制或杀死害虫,为后代节约自然资源、保护植物。
可以说,推动社会进步的科学技术,就是由这些细微反应组成的。
他们不仅给
化学界提供了许多方法和原理,而且也为我们更好地了解自然,增进了我们对自然的洞察力。
(结束)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
浅谈麦氏重排在质谱解析中的应用
1.前言
麦氏重排是Mclatterty对质谱分析中离子的重排反应提出的经验规则。
麦氏重排(Mclatterty Rearrangement)是有机质谱裂解反应过程中十分重要的一种反应类型。
是指具有不饱和官能团C=X(X为O、S、N、C等)及其γ-H原子结构的化合物,γ-H 原子可以通过六元环空间排列的过渡态,向缺电子(C=X+)的部位转移,发生γ-H的断裂,同时伴随C=X的β键断裂(属于均裂),这种断裂称为McLafferty重排,简称麦氏重排。
反应通式:
R
YH
X
+
+
其中 X=O,NR2,CR2
Y=R,OR,NR2
Z=CR2,O
由于偶电子离子不存在游离基中心,所以只有奇电子离子才发生游离基诱导的重排反应。
由麦氏重排产生的奇电子离子,对质谱的解析及化合物的研究有很重要的意义。
2.麦氏重排在质谱解析中的应用
(1)麦氏重排对同分异构体的判别
同分异构体的识别可根据麦氏重排进行确认。
如,3 -甲基- 2-丁酮2-戊酮,见图1。
这两种化合物的质谱图十分相似,由于3-甲基- 2-丁酮没有γH存在,不符合麦氏重排发生的条件,故其不能发生麦氏重排;而 2-戊酮含有γ-H,符合麦氏重排发生的条件,因此它可以通过麦氏重排产生M/Z=58的奇电子离子。
所以它们能根据有无较弱的M/Z=58碎片离子被区分开。
图1
1000
2000
3000
4000
5000
6000
7000
Inten.
43
2741
86
71
57
3750
3175
6984 2562
1000
2000
3000
4000
5000
6000
Inten.
43
41
86
27
5871
38
2687
5159
316779
63
21
2-戊酮通过麦氏重排形成的M/Z=58碎片离子的途径
O
HγH
OH
+
M/Z=
58
R
e
l
a
c
t
i
v
e
i
n
t
e
n
s
i
t
y
O
O
由麦氏重排所形成的碎片子丰度不高,那么是否有由麦氏重排所形成的基峰离子。
(2)麦氏重排所形成的基峰离子
麦氏重排解释异戊巴比妥质谱图(图2)基峰,异戊巴比妥通过以下反应式可产生高丰度的碎片离子,先通过γ-H重排及随后的
α断裂产生的
N
N
HO OH
O
H离子(M/Z=156),丰度为100%。
图2:
m/z 0
1000
2000
3000
4000
5000
Inten.
156
141
41
55
43
142
197
29
183
69
1898112
97
83211
126
H H
OH
H
H
R
e
l
a
c
t
i
v
e
i
n
t
e
n
s
i
t
y
N
N
O O
O
H
H
N N
HO OH
H
H
N N
HO OH
O
M/Z=141
M/Z=156
(3)麦氏重排在对烷基苯异构的判别
在质谱解析过程中普遍认为:在芳环上取代基的位置异构,一般不会引起质谱图明显的变化,这类化合物不易于用质谱图进行鉴别。
其主要原因是存在位置异构的芳香烃在断裂过程中,发生断裂的各化学键本身没有明显的差异(部分存在邻位效应的化合物除外),因此由这些键断裂而产生的碎片离子也就不会产生明显的区别。
再加上芳环上的氢和碳骨架容易发生攀移,高度攀移会使一些同分异构体在断裂过程中形成结构相同的中间产物,使中间产物进一步丧失掉它们原来的结构特征,结果是它们的谱图十分相似,难以区分。
对芳环位置异构与麦氏重排产生的碎片离子丰度大小的关系进行了考察 ,结果发现不同的位置异构对麦氏重排发生的几率影响很大 ,并可以根据这种几率的不同对物质结构进行鉴别。
通过麦氏重排形成的M/Z=92碎片离子的途径
下表列出各种烷基苯裂解产生M/Z=91与M/Z=92相对的丰度比值结构式M/Z 92/91结构式M/Z 92/91
0.080.8
R
e
l
a
c
t
i
v
e
i
n
t
e
n
s
i
t
y
0.100.6 0.1*0.1* 0.1* 1.2
0.10 1.3
0.6 1.6
0.7
烷基苯被电离后,可通过α断裂产生M/Z=91(100%)的苄基离子,也可通过γ-H重排及随后的α断裂而产生M/Z=92离子。
芳香化合物中麦氏重排裂解反应的主要竞争对象是β开裂反应,哪一种竞争反应在化合物裂解过程中能够占据优势,关键是α碳原子上的正电荷稳定与否。
α碳原子越容易稳定正电荷,就越容易发生游离基中心引发的β开裂而不利于反应过程复杂的麦氏重排,因为麦氏重排要经过几个键的协同断裂才能完成。
(3)麦氏重排解释THC中M/Z=258离子生成
图3 THC质谱图
O
OH
a
c
t
i
v
e
i
n
t
e
n
s
i
t
y
2500
5000
750010000
Inten.299
314
231
271
243
258
91
115
193
77
41
297
174
67128
217
14755
161
通过麦氏重排反应所形成M/Z=258的过程
M/Z=258
3 影响氢重排的因素
氢重排主要受以下因素影响:氢的不稳定性,空间效应,新位置接受氢的能力
对于氢的不稳定性主要有以下因素影响氢的离去能力,对于支化度高的碳原子上的氢来讲比较容易离去,与不饱和键相邻的碳上的氢较容易离去,与电负性原子相连的氢比较容易离去,而对于拉电子基团来讲会降低氢的离去能力。
新位置接受氢的能力,氢重排到带电荷的杂原子上,相当于该杂原子结合一个质子,因此质子亲和力愈大的元素接受转移氢的能力愈大,主要为以下顺序:N>S,O>烯烃,芳烃
4 结论
麦氏重排作为有机裂解反应过程中一个十分重要的反应类型,通过其可以解释在有机裂解过程中的系列质谱碎片的裂解方式,同时可以通过化合物的结构类型是否可以发生麦氏重排对化合物进行进一步的判别,在质谱解析中十分重要,同时麦氏重排还受系列因素的影响,在质谱解析中充分考虑,才可以得到合理的解释。
(注:幼儿教育越显重要,但文档可能无法思考全面,请浏览后下载,供参考。
可复制、编制,期待你的好评与关注)。
