脐血干细胞移植知情同意书
干细胞治疗知情同意书

干细胞治疗知情同意书干细胞治疗知情同意书患者姓名:性别:年龄:住院科室:床号:住院号:治疗前诊断:治疗名称:干细胞治疗治疗方式:局部种植□蛛网膜下腔输注□静脉输注□动脉介入□其他:___治疗须知干细胞治疗是一种创新型临床治疗技术,与其他的临床治疗技术一样,在治疗疾病的同时,有可能会存在一定的风险,特别是由于患者病情异常或者个体差异时,或其他一些不可预知的因素的影响,这些在目前的医学技术领域内完全避免是不现实的,也是目前的科学技术水平所达不到的。
如果治疗您的疾病有其他的方法,我们建议您慎重选择。
如果您接受干细胞治疗您的疾病,我们提醒您可能发生一些意外情况,包括以下但不仅限于以下:1、麻醉意外及其并发症,重危者可能危及生命;2、治疗中血管损伤,致出血不止、大出血休克,危及生命等情况,严重时需输血或另行止血处理;3、发热反应;4、免疫排斥反应;5、局部或全身各种感染及血液制品引起的疾病(如:病毒性肝炎、艾滋病、梅毒、疟疾,巨细胞病毒);6、治疗后效果不明显,临床症状及体征的改善与您的期望存在偏差,甚至治疗无效;7、治疗后症状加重,或临床有效时间较短,原有病情继续进展,症状及体征加重;8、经腰穿治疗,术后脑脊液漏或中枢神经系统感染、发热、头痛、腰背部疼痛等;9、干细胞动员期间,可能会出现“白细胞瘀滞症”,可发生呼吸困难、头晕、言语不清等临床表现或其他心脑血管意外;10、局部治疗,可出现局部组织感染、溃烂、坏死等情况,进而加重病情;11、其他难以预料的危及生命及致残的情况,附注:兹有患者﹍﹍﹍,拟接受干细胞治疗技术,次治疗系自费项目,有关治疗情况及治疗后注意事项已向受治疗者(家属/委托代理人/法定监护人)说明。
谈话医师签名:年月日患者声明我已阅读了上述有关本次治疗的介绍,而且就本次治疗与医生讨论,并提出问题,我提出的所有问题均得到满意的答复。
我已经理解了干细胞治疗的风险和受益,愿意承担由于疾病本身或现有医疗技术所限而致的医疗意外及并发症,并全权负责签字,要求治疗。
医院自体外周干细胞动员,采集及冻存知情同意书模板

2.我理解任何所用药物都可能产生副作用,包括轻度的恶心、皮疹等症状到严重的过敏性休克,甚至危及生命。
3.我理解此治疗可能出现的风险和医生的对策:
1)动员方案的危险和副反应:
大剂量化疗导致的黏膜炎,脏器损害(心脏,肝脏,肾脏等)。血象降低,感染,出血等合并症。
G-CSF应用所后的不良反应,发热,头痛及周身不适感,血栓形成等。
症和风险、可能存在的其它治疗方法并且解答了我关于此次诊治的相关问题。
我同意在诊治中医生可以根据我的病情对我的诊治方式做出调整。
我理解我的诊治需要多位医生共同进行。
我并未得到诊治百分之百成功的许诺。
我授权医师对诊治切除的病变器官、组织或标本进行处置,包括病理学检查、细胞学检查和医疗废物处理等。
患者签名签名日期年月日如果患者无法签署知情同意书,请其授权的亲属在此签名:
其他:
2)自体外周干细胞采集:
采集相关并发症(见PBSCT采集同意书)。
一次采集不够,需要再次动员采集。
动员后出现严重并发症而无法进行采集。
特殊风险或主要高危因素
我理解根据我个人的病情,我可能出现未包括在上述所交待并发症以外的风险:
一旦发生上述风险和意外,医生会采取积极应对措施。
患者知情选择
我的医生已经告知我将要进行的诊治方式、此次诊治及诊治后可能发生的并发
患者授权亲属签名与患者关系签名日期年月日
医生陈述
我已经告知患者将要进行的诊治方式、此次治疗及诊治后可能发生的并发症和风险、可能存在的其它治疗方法并且解答了患者关于此次诊治的相关问题。
医生签名签名日期年月日
自体外周干细胞动员,采集及冻存知情同意书
xx医院
自体外周干细胞动员,采集及冻存知情同意书
临床研究受试者知情同意书模板-中国临床试验注册中心

脐血间充质干细胞静脉注射治疗重症遗传性皮肤病的临床研究知情同意书受试者姓名:________________联系地址:_________________联系电话:__________________研究中心名称:上海交通大学医学院附属新华医院第一部分告知页尊敬的___________ 先生/女士:我们真诚地邀请您的孩子参加“脐血间充质干细胞静脉注射治疗重症遗传性皮肤病的临床研究”。
本研究由上海交通大学医学院附属新华医院皮肤科、血液科联合进行。
在您同意您的孩子参加本项研究之前,请您仔细阅读这份知情同意书,它将提供给您一些信息,帮助您决定和您的孩子是否参加此项研究,如有疑问可以向该项目的研究者咨询。
如果您同意参加本研究,请您签署知情同意书,并且保存一份双方签字的知情同意书。
本研究方案已通过医院医学伦理委员会审查。
1、为什么要参加这项研究?研究背景:迂回线状鱼鳞病(Ichthyosis linearis circumfl exa)是一组致死或致残、严重威胁人类健康的遗传性皮肤病。
目前缺乏有效治疗手段。
迂回性线状鱼鳞病是一种常染色体隐性遗传角化性疾病,最初可表现为严重的先天性泛发性剥脱性红皮病,此后皮疹主要分布于躯干和四肢,为多环状匍行性表现,由于伴随特应性体质,患者全年终生伴剧烈难忍的瘙痒,痛苦不堪。
该疾病在我国患者数多、有多系统受累表现、严重致死致残、目前均无有效治疗措施。
近几年来,间充质干细胞疗法作为一种治疗机体无法自然修复的组织细胞和器官损伤的多种难治性疾病的新方法取得了广泛关注,在多个国家正在开展动物实验和临床I期、II期、III期试验及多中心研究。
目前已经进行各期临床试验的应用领域包括:血液系统疾病(移植物抗宿主病、骨髓增生异常综合征)、心血管系统疾病(心肌梗死、心力衰竭、扩张性心肌病、心肌缺血)、神经系统疾病(脊髓外伤、多发性硬化症等)、胰腺疾病(I-糖尿病、II-糖尿病)、肝脏疾病(肝硬化)、胃肠道疾病(克罗恩病)、肾脏疾病(狼疮性肾炎)、肺疾病(COPD)、骨软骨缺陷、骨关节炎、自身免疫疾病和皮肤疾病(大疱性表皮松解症)(表1),已完成的临床试验均证实MSCs治疗安全有效。
脐血造血干细胞移植

脐血造血干细胞移植脐血造血干细胞移植是一种重要的干细胞移植方式,它利用从新生儿的脐带血中提取的含有造血干细胞的干细胞进行移植治疗。
脐血造血干细胞移植被广泛应用于临床治疗中,具有许多优势,同时也有一些限制和风险。
以下将对脐血造血干细胞移植进行详细介绍。
1. 脐血造血干细胞的特点脐血中含有丰富的造血干细胞,这些干细胞具有自我更新和分化成各类血细胞的潜能,是进行造血干细胞移植的理想来源。
脐血中的干细胞数量相对较多,收获相对容易,存储和移植过程相对简单,同时也少受感染的影响。
2. 临床应用情况脐血造血干细胞移植被广泛应用于治疗一系列的血液病和免疫系统疾病,如白血病、淋巴瘤、再生障碍性贫血等。
在干细胞移植领域,脐血造血干细胞移植的成功率逐渐提高,为许多患者带来了新的希望。
3. 移植过程脐血造血干细胞移植的过程分为捐助、处理、保存和移植等多个环节。
在移植前需要进行充分的检测和筛选,确保干细胞的质量和适用性。
移植后还需密切监测患者的病情和免疫反应,充分防范并发症的发生。
4. 优势和限制脐血造血干细胞移植相比于其他来源的干细胞移植具有许多优势,如来源方便、较少的免疫排斥反应、移植后对供者和受者都较为安全等。
但也存在一些限制,如供应量有限、干细胞数量不足、治疗效果不确定等问题。
5. 风险和并发症脐血造血干细胞移植虽然在治疗许多疾病中取得了成功,但仍然存在着一些风险和并发症,如感染、移植后疾病复发等。
因此,在进行脐血造血干细胞移植时,需谨慎评估患者的情况,并制定个性化的治疗方案。
结语脐血造血干细胞移植作为一种重要的治疗手段,为许多血液病和免疫系统疾病的患者带来了新的希望。
随着技术的不断进步和临床经验的积累,脐血造血干细胞移植的应用前景将会更加广阔,为更多患者带来治疗的可能性。
脐血干细胞移植知情同意书

附件1 与本项目相关的《知情同意书》样本山西医学科学院山西大医院脐血干细胞移植患者知情同意书患者姓名年龄性别住院号疾病介绍和治疗建议:医生已告知我需要进行治疗。
治疗的适应症及术前准备一般流程:1.移植术前讨论参加人员:。
2.目前治疗患者本病的方法:。
3.脐血干细胞移植的适应症:<1>.患者疾病诊断明确;<2>.结合患者的具体情况,目前脐血干细胞移植为治愈疾病的较合适选择;<3>.患者查体无脐血干细胞移植的禁忌症,符合移植要求;<4>. 有可以采用的脐血干细胞来源及必要的经济支持。
4.移植术前的准备:<1>.已对患者病情进行评估,已完成供患者查体,并再次确认HSCT的适应症及移植时机;<2>.根据需要对患者、供者及其家属提供必要的指导;<3>.患者与供者关系:,HLA相合情况:相合。
<4>.预处理方案为:,移植物来源:。
5.移植的一般流程:<1>.患者药浴,进洁净室,行中心静脉插管。
<2>.进行移植前预处理(方案如上所述)。
<3>.按常规进行骨髓和/或外周血造血干细胞输注。
<4>.防治脏器损害、感染及移植物抗宿主病(GVHD)。
<5>.残存白血病监测、免疫重建、远期合并症的防治与随访。
HSCT后的效果:预计非复发死亡率约20%左右,复发率约10%左右,但对于高危白血病,复发率增高。
治疗潜在风险和对策:医生告知我造血干细胞移植可能动发生的一些风险,有些不常见的风险可能没有在此列出,具体的治疗方案根据不同病人的情况有所不同,医生告诉我可与我的医生讨论有关我治疗的具体内容,如果我有特殊的问题可与我的医生讨论。
1.我理解任何治疗都存在风险。
2.我理解任何所用药物都可能产生副作用,包括轻度的恶心、皮疹等症状到严重的过敏性休克,甚至危及生命。
3.我理解此治疗可能发生的风险和医生的对策:1) 主要脏器损害:原因包括既往化疗药物累积毒性、预处理药物毒性、感染、贫血、出血等因素和其它具有使用适应症的药物可能的副作用。
脐带干细胞公共库样品采集要求
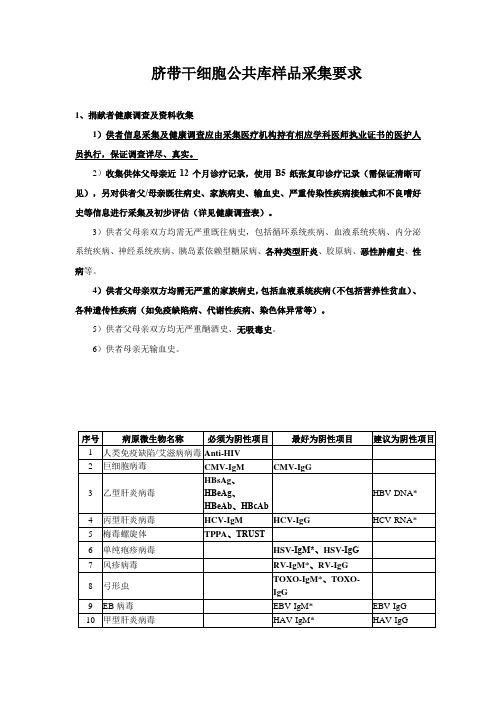
脐带干细胞公共库样品采集要求1、捐献者健康调查及资料收集1)供者信息采集及健康调查应由采集医疗机构持有相应学科医师执业证书的医护人员执行,保证调查详尽、真实。
2)收集供体父母亲近12个月诊疗记录,使用B5纸张复印诊疗记录(需保证清晰可见),另对供者父/母亲既往病史、家族病史、输血史、严重传染性疾病接触式和不良嗜好史等信息进行采集及初步评估(详见健康调查表)。
3)供者父母亲双方均需无严重既往病史,包括循环系统疾病、血液系统疾病、内分泌系统疾病、神经系统疾病、胰岛素依赖型糖尿病、各种类型肝炎、胶原病、恶性肿瘤史、性病等。
4)供者父母亲双方均需无严重的家族病史,包括血液系统疾病(不包括营养性贫血)、各种遗传性疾病(如免疫缺陷病、代谢性疾病、染色体异常等)。
5)供者父母亲双方均无严重酗酒史、无吸毒史。
6)供者母亲无输血史。
7)三个月以内病原微生物检测结果要求如下表(黑色加粗部分为重点调查项目),如供者母亲产检报告中有星号标记项目的检测结果,则必须为阴性。
除此之外,无其它严重传染性疾病,如猪带绦虫病、血吸虫病、丝虫病、鼠疫、霍乱、疟疾和新型冠状病毒肺炎等。
8)供者母亲与艾滋病、性病、鼠疫、霍乱、疟疾和新型冠状病毒/2019-nCoV肺炎等患者无接触史。
9)供者母亲过去12个月内无疫区(如鼠疫、霍乱和疟疾等疫区)旅行、居住和工作史。
10)供者父母亲及其密切接触者健康码均为绿色。
11)供者母亲过去12个月内未注射乙型肝炎免疫球蛋白。
12)供者母亲当前健康状况良好,肝肾功能正常、无各种急性慢性疾病等。
13)供者母亲分娩方式为剖宫产。
14)供者母亲非多胎妊娠。
15)供者母亲妊娠期间未服用对胎儿可能有不良影响的药物。
16)胎儿足月,产检一切正常。
17)新生儿出生时健康、无畸形。
2、签署知情同意书1)供者母亲或其他监护人需签署《脐带样品采集及捐献知情同意书》。
2)知情同意书应由采集医疗机构持有相应学科医师执业证书的医护人员签署声明,并且让供者母亲或其他监护人有充足时间了解和咨询志愿捐献相关内容,保证真实有效。
脐带血造血干细胞储存协议书V2.3
脐带血造血干细胞储存协议书V2.3甲方:(母亲)(父亲)乙方:xx市脐带血造血干细胞库xx市干细胞技术有限公司邮编:xx市干细胞技术有限公司系由xx市红十字会、xx市血液中心等机构经过xx市国资委、xx市卫生局、xx市工商局、xx市科委等委办批准共同出资组建成立的带有慈善性质的高新技术企业,其管理下的xx市脐带血造血干细胞库是经国家卫生部卫医发(2001)225 号和(2005)69 号文批准,并已获得中华人民共和国血站执业许可证,是xx唯一具有开展脐带血采集、制备、检测、冻存、选择、发放等资质的法定机构。
甲乙双方经自愿平等协商,依据《合同法》及相关法律法规,就甲方将其孩子的脐带血交由乙方进行约定的技术处理和储存事宜达成如下一致协议:一、共同声明在签署本《脐带血造血干细胞储存协议书》的同时,甲乙双方已就以下脐带血造血干细胞医学领域的现状和发展前景中的相关问题达成如下共识:1.1 脐带血造血干细胞在临床已被用于治疗许多恶性疾病,但并非每一个人都会患上这些疾病,因此储存脐带血造血干细胞是一种防患于未然的“保险”行为。
1.2 医学研究与临床实践证明,保存一百多年的细胞仍具有活性,骨髓造血干细胞已有几十年的保存历史,医学史上已有脐带血造血干细胞保存15 年后仍有活性且用于临床移植成功的实例;但因为人类医学尚没有充分的时间去证实脐带血造血干细胞能储存多长时间而不丧失其活性,所以不能保证甲方所保存的脐带血造血干细胞永远不丧失活性。
1.3 储存脐带血造血干细胞是一种新型的医学技术,鉴于脐带血取自母亲与子女相连的脐带和胎盘且包含有子女的造血干细胞,其所有权应由母亲和子女共有,其医学利益的最直接受益人应为子女。
考虑到子女刚出生时尚不具备民事行为能力,则此时脐带血造血干细胞所有权由甲方作为其法定监护人代为行使;甲方之子女在符合我国有关民事权利能力和民事行为能力的法律规定时,则应由其本人当然享有。
该权利人有权转让该项权利或许可其他家庭成员及无血缘关系的第三方使用该份脐带血造血干细胞,也可以由合法的继承人依法继承。
脐带样品采集及捐献知情同意书
脐带样品采集及捐献知情同意书我们现在邀请您加入干细胞库脐带干细胞公共库项目(简称项目)。
以下将为您介绍这一项目的目的、作为参与者您将要做的事、潜在风险及利益。
您在决定是否参与之前、或者项目的过程中都享有充分的知情权。
一、项目的目的及意义脐带是胎盘的附属物,一般情况下,胎儿娩出、断脐之后,脐带随着胎盘被丢弃。
科学研究表明,脐带组织中含有大量的干细胞,越来越多的临床研究则表明脐带干细胞对脑瘫、肝硬化、糖尿病、系统性红斑狼疮等众多重大难治性疾病的治疗有非常重大的临床意义。
项目的目的是收集您分娩时将要被丢弃的脐带,从脐带组织中分离、培养获得脐带干细胞并储存,建立脐带干细胞公共库,从而为我国干细胞研究及临床应用提供坚实的资源储备。
您捐献的脐带组织制备的干细胞可能将进行相关科学研究及临床应用,进而为我国医疗事业的发展提供帮助和支持。
二、捐献者参与程序1、了解并签署本知情同意书。
2、配合调查员完成您及您配偶家人的健康史调查并签字确认。
具体问题详见《脐带组织捐献供者父母亲健康调查表》,这些信息将被用来判断脐带干细胞能否储存和用于相关科学研究及临床应用。
3、配合临床医师完成体检、实验室检查。
4、配合采集孕产妇外周血(以下称“母血”)、新生儿脐带血和脐带组织样品。
5、允许对母血、脐带血、脐带干细胞进行相关检测:如HIV、HBV、HCV、CMV等病原微生物检测。
如果检测结果表明该脐带干细胞适合储存,它将被储存,直至被科学研究及临床应用所使用,或直至它不适合继续储存;如果不适合储存,它将被按医疗程序废弃。
6、允许我们在婴儿出生以后大约3~12个月内随访(不排除再次进行外周血检验),以了解产妇/婴儿的健康状况。
三、供者风险产妇分娩时,在保证产妇和婴儿安全、健康的前提下采集脐带,如产妇或婴儿发生紧急情况,医院方和产妇均有权放弃脐带采集。
因为脐带血和脐带组织样品的采集是在脐带、胎盘与母体以及新生儿完全分离以后进行,所以对于母婴均没有任何不良影响,不会增加额外的风险。
干细胞治疗知情同意书
干细胞治疗知情同意书患者姓名:性别:年龄:住院科室:床号:住院号:治疗前诊断:治疗名称:干细胞治疗治疗方式:局部种植□蛛网膜下腔输注□静脉输注□动脉介入□其他:___治疗须知干细胞治疗是一种创新型临床治疗技术,与其他的临床治疗技术一样,在治疗疾病的同时,有可能会存在一定的风险,特别是由于患者病情异常或者个体差异时,或其他一些不可预知的因素的影响,这些在目前的医学技术领域内完全避免是不现实的,也是目前的科学技术水平所达不到的。
如果治疗您的疾病有其他的方法,我们建议您慎重选择。
如果您接受干细胞治疗您的疾病,我们提醒您可能发生一些意外情况,包括以下但不仅限于以下:1、麻醉意外及其并发症,重危者可能危及生命;2、治疗中血管损伤,致出血不止、大出血休克,危及生命等情况,严重时需输血或另行止血处理;3、发热反应;4、免疫排斥反应;5、局部或全身各种感染及血液制品引起的疾病(如:病毒性肝炎、艾滋病、梅毒、疟疾,巨细胞病毒);6、治疗后效果不明显,临床症状及体征的改善与您的期望存在偏差,甚至治疗无效;7、治疗后症状加重,或临床有效时间较短,原有病情继续进展,症状及体征加重;8、经腰穿治疗,术后脑脊液漏或中枢神经系统感染、发热、头痛、腰背部疼痛等;9、干细胞动员期间,可能会出现“白细胞瘀滞症”,可发生呼吸困难、头晕、言语不清等临床表现或其他心脑血管意外;10、局部治疗,可出现局部组织感染、溃烂、坏死等情况,进而加重病情;11、其他难以预料的危及生命及致残的情况,附注:兹有患者﹍﹍﹍,拟接受干细胞治疗技术,次治疗系自费项目,有关治疗情况及治疗后注意事项已向受治疗者(家属/委托代理人/法定监护人)说明。
谈话医师签名:年月日患者声明我已阅读了上述有关本次治疗的介绍,而且就本次治疗与医生讨论,并提出问题,我提出的所有问题均得到满意的答复。
我已经理解了干细胞治疗的风险和受益,愿意承担由于疾病本身或现有医疗技术所限而致的医疗意外及并发症,并全权负责签字,要求治疗。
脐带样品采集及捐献知情同意书
脐带样品采集及捐献知情同意书我们现在邀请您加入干细胞库脐带干细胞公共库项目(简称项目)。
以下将为您介绍这一项目的目的、作为参与者您将要做的事、潜在风险及利益。
您在决定是否参与之前、或者项目的过程中都享有充分的知情权。
一、项目的目的及意义脐带是胎盘的附属物,一般情况下,胎儿娩出、断脐之后,脐带随着胎盘被丢弃。
科学研究表明,脐带组织中含有大量的干细胞,越来越多的临床研究则表明脐带干细胞对脑瘫、肝硬化、糖尿病、系统性红斑狼疮等众多重大难治性疾病的治疗有非常重大的临床意义。
项目的目的是收集您分娩时将要被丢弃的脐带,从脐带组织中分离、培养获得脐带干细胞并储存,建立脐带干细胞公共库,从而为我国干细胞研究及临床应用提供坚实的资源储备。
您捐献的脐带组织制备的干细胞可能将进行相关科学研究及临床应用,进而为我国医疗事业的发展提供帮助和支持。
二、捐献者参与程序1、了解并签署本知情同意书。
2、配合调查员完成您及您配偶家人的健康史调查并签字确认。
具体问题详见《脐带组织捐献供者父母亲健康调查表》,这些信息将被用来判断脐带干细胞能否储存和用于相关科学研究及临床应用。
3、配合临床医师完成体检、实验室检查。
4、配合采集孕产妇外周血(以下称“母血”)、新生儿脐带血和脐带组织样品。
5、允许对母血、脐带血、脐带干细胞进行相关检测:如HIV、HBV、HCV、CMV等病原微生物检测。
如果检测结果表明该脐带干细胞适合储存,它将被储存,直至被科学研究及临床应用所使用,或直至它不适合继续储存;如果不适合储存,它将被按医疗程序废弃。
6、允许我们在婴儿出生以后大约372个月内随访(不排除再次进行外周血检验),以了解产妇/婴儿的健康状况。
三、供者风险产妇分娩时,在保证产妇和婴儿安全、健康的前提下采集脐带, 如产妇或婴儿发生紧急情况,医院方和产妇均有权放弃脐带采集。
因为脐带血和脐带组织样品的采集是在脐带、胎盘与母体以及新生儿完全分离以后进行,所以对于母婴均没有任何不良影响,不会增加额外的风险。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附件 1 与本项目相关的《知情同意书》样本
山西医学科学院山西大医院
脐血干细胞移植患者知情同意书
患者姓名年龄性别住院号
疾病介绍和治疗建议:
医生已告知我需要进行__________________________ 治疗。
治疗的适应症及术
前准备一般流程:
1. ______________________________________________________ 移植术前讨论参加人员: _____________________________________________________ 。
2. ______________________________________________________ 目前治疗患者本病的方法: ___________________________________________________ 。
3.脐血干细胞移植的适应症:
<1>.患者疾病诊断明确;
<2>.结合患者的具体情况,目前脐血干细胞移植为治愈疾病的较合适选择;
<3>.患者查体无脐血干细胞移植的禁忌症,符合移植要求;
<4>.有可以采用的脐血干细胞来源及必要的经济支持。
4.移植术前的准备:
<1>.已对患者病情进行评估,已完成供患者查体,并再次确认HSCT的适
应症及移植时机;
<2>.根据需要对患者、供者及其家属提供必要的指导;
<3>.患者与供者关系: _______________ ,HLA相合情况:_____________ 相合。
<4>.预处理方案为: _____________________ ,移植物来源:_____________ 。
5.移植的一般流程:
<1>.患者药浴,进洁净室,行中心静脉插管。
<2>.进行移植前预处理(方案如上所述)。
<3>.按常规进行骨髓和/或外周血造血干细胞输注。
<4>.防治脏器损害、感染及移植物抗宿主病(GVHD )。
<5>.残存白血病监测、免疫重建、远期合并症的防治与随访。
HSCT后的效果:预计非复发死亡率约20%左右,复发率约10%左右,但
对于咼危白血病,复发率增咼
治疗潜在风险和对策:
医生告知我造血干细胞移植可能动发生的一些风险,有些不常见的风险可能没有在此列出,具体的治疗方案根据不同病人的情况有所不同,医生告诉我可与我的医生讨论有关我治疗的具体内容,如果我有特殊的问题可与我的医生讨论。
1.我理解任何治疗都存在风险。
2.我理解任何所用药物都可能产生副作用,包括轻度的恶心、皮疹等症状到严重的过敏性休克,甚至危及生命。
3.我理解此治疗可能发生的风险和医生的对策:
1)主要脏器损害:原因包括既往化疗药物累积毒性、预处理药物毒性、感染、贫
血、出血等因素和其它具有使用适应症的药物可能的副作用。
心脏、肝、肾、肺、脑等主
要脏器的重度损害可危及生命,轻度脏器损害可恢复。
相应防治措施会尽可能减少上述因素的损害程度,但不能完全杜绝上述损害的发生。
2)干细胞输注过程中可能会发生过敏反应和急性左心衰竭;预防措施为输注前应用抗过敏药物、监测出入量及输液速度;
3)感染:接受移植患者属免疫功能低下人群,易患各种病原导致的感染,内源性病原可活化为活动性感染。
感染的临床表现不典型,不同于免疫功能正常病人,病情变化快,抗感染治疗难度大。
各种抗感染药物及支持措施的应用大大改进了疗效,但重度感染仍可危及生命。
4)移植物抗宿主病(GVHD ):异基因移植急性GVHD发生率50%〜70%, 重度GVHD 死亡率较高。
慢性GVHD 对生活质量有一定影响,少数严重者可危及生命。
抗GVHD 措施包括各种免疫抑制剂、相关感染防治措施和支持治疗。
5)未植入:现行移植方案下异体造血干细胞不植入率约为1%〜4 %。
6)复发:移植后血液病仍存在复发风险。
相应措施包括:定期随访;调整免疫抑制剂;供者淋巴细胞输注(DLI );化疗;二次移植及采用相应靶向药物预防和治疗如格列卫等。
7)其他合并症:PTLD (应用ATG患者发生率稍高为10%-20%),出血性膀胱炎,脑出血;贫血;不育;继发肿瘤等。
应对措施包括血象监测,输血,酌情提前保存生殖细胞,相应化疗等。
4.______________________________________________________ 其他特殊交代事项: ____________________________________________________________ 。
特殊风险或主要高危因素:
我理解根据我个人的病情,我可能出现未包括在上述所交待并发症以外的风险:。
一旦发生上述风险和意外,医生会采取积极应对措施。
患者知情选择:
我的医生已经告知我将要进行的诊治方式、此次诊治及诊治后可能发生的并发症和风险、可能存在的其它治疗方法并且解答了我关于此次诊治的相关问题。
我同意在诊治中医生可以根据我的病情对我的诊治方式做出调整。
我理解我的诊治需要多位医生共同进行。
我并未得到诊治百分之百成功的许诺。
我授权医师对诊治切除的病变器官、组织或标本进行处置,包括病理学检查、细胞学检查和医疗废物处理等。
患者签名 _______________ 签名日期 __________________________ 年_月 _________ 日如果患者无法签署知情同意书,请其授权的亲属在此签名:
患者授权亲属签名 _____________ 与患者关系_____________________
签名日期_______ 年—月—日
医生陈述:
我已经告知患者将要进行的诊治方式、此次治疗及诊治后可能发生的并发症和风险、可能存在的其它治疗方法并且解答了患者关于此次诊治的相关问题。
医生签名______________ 签名日期 __________________________ 年—月 ________ 日。
