2008年第7号文国家食品药品监督管理局关于发布化学药品注射剂和多组分生化药注射剂基本技术要求的通知
注射剂变更申请的研究思路及案例分析_蒋煜

,明
确并大幅提高了注射剂的研发及评价的技术要求, 指导申请人规范、科学开展注射剂的研发工作 ; 2010 年,原卫生部发布了《药品生产质量管理规范
收稿日期:2016-01-20 作者简介:蒋 煜(1975—),男,高级审评员,副主任药师,从事 药品审评工作。 Tel:010-68585566×1545,013910384108 E-mail:jiangyu1975@
DOI:10.16522/ki.cjph.2016.03.022
注射剂系由原料药或原料药与适宜的辅料制成 的供注入人体内的无菌制剂。按照给药途径及给药 方式,可分为皮下注射、皮内注射、肌肉注射、静 脉注射、静脉滴注、鞘内注射和椎管内注射等。按 照药物存在的形式,又可分为溶液型注射液、乳状 液注射液、混悬型注射液、注射用粉末 ( 冻干制剂 或无菌分装制剂 ) 以及注射用浓溶液等
[11]
。
表 3 NDA 以及 ANDA 的比较
NDA申请技术要求 1. 化学部分 2. 生产 3. 质量控制 4. 标签 5. 检验 6. 动物研究 7. 临床研究 8. 生物利用度研究 ANDA申请技术要求 1. 化学部分 2. 生产 3. 质量控制 4. 标签 5. 检验 6. 生物等效性研究
蒋 煜,马 磊
(国家食品药品监督管理总局药品审评中心,北京 100038)
JIANG Yu, MA Lei
(Center for Drug Evaluation, China Food and Drug Adminitration, Beijing 100038) 摘要:基于对注射剂风险控制认识的不断加深,我国药监部门大幅提高了注射剂的研发及评价的技术要求。近年,注射 剂的变更申请数量较大。本文在梳理日常技术审评工作的基础上,结合近年未获得批准的部分注射剂变更申请的案例分 析,对注射剂变更研究的思路、现状和存在的问题进行了分析。 关键词:注射剂;变更申请;研究思路;案例分析;社会管理药学 中图分类号:R95 文献标志码:C 文章编号:1001-8255(2016)03-0355-08
多组分生化药注射剂生产专项整治方案

多组分生化药注射剂生产专项整治方案为加强多组分生化药注射剂生产环节的监管,防止发生系统性、区域性药品安全风险,根据《2015年药品生产监管工作计划》,制定本方案。
一、工作目标通过开展多组分生化药注射剂生产专项整治行动,进一步规范生产行为,消除质量隐患,落实生产企业主体责任,确保多组分生化药注射剂生产质量安全。
二、整治内容(一)企业未按原国家食品药品监督管理局《关于发布化学药品注射剂和多组分生化药注射剂基本技术要求的通知》(国食药监注[2008]7号)要求完成相关研究工作。
(二)企业未对原料建立相应的质量控制标准,未严格按质量控制标准对购入的每批原料进行质量控制;采用外购的中间产品(包括浓缩液等)制备多组分生化注射剂。
(S)企业未严格按照新修订药品GMP及注册的质量标准和生产工艺组织生产,未对产品进行年度质量回顾。
(四)企业未严格执行药品不良反应监测有关规定,未建立完善的药品召回体系。
三、实施步骤(一)企业自查自纠阶段(自本方案印发之日起至2015年7月15日)多组分生化药注射剂生产企业要严格按照本方案要求进行自查自纠,对于自查中发现的问题,要立即整改,并制定有效的风险防控措施。
自查结束后,各企业要将自查自纠情况上报所在地市(州)食品药品监督管理局。
(二)检查抽样阶段(2015年7月16日至10月15日)各市(州)局对辖区内多组分生化药注射剂生产企业进行现场监督检查,对企业上报的自查自纠情况进行核查,对企业在产、库存和留样的全部品种予以监督抽样,每个品种至少抽取一个批次。
(三)总结提升阶段(2015年10月16日至10月31日)各市(州)局要认真总结整治工作,并将工作总结于2015年10月31日前上报省局。
四、工作要求(一)高度重视,精心组织。
由于多组分生化药的原材料来源于人、动物的组织或体液,大多数组成成分不完全明确,来源、工艺条件的细小变化均有可能导致物质基础的变化,而这些质量上的变化较难通过最终产品的质量标准加以控制,从而可能引发不可预测的不良反应,因此,各市(州)局要深刻认识开展多组分生化药注射剂生产专项整治的重要意义,精心组织,深入排查质量风险,做到防患于未然。
关于印发化学药品技术标准等5个药品审评技术标准的通知(国食药监注[2008]271号)
![关于印发化学药品技术标准等5个药品审评技术标准的通知(国食药监注[2008]271号)](https://img.taocdn.com/s3/m/3e26470403d8ce2f006623b0.png)
关于印发化学药品技术标准等5个药品审评技术标准的通知国食药监注[2008]271号2008年06月03日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为做好过渡期品种集中审评工作,按照《过渡期品种集中审评工作方案》和公开、公平、公正的原则,依据《药品注册管理办法》和有关技术指导原则,国家局组织制定了《化学药品技术标准》、《多组分生化药技术标准》、《中药质量标准不明确的判定标准及处理原则》、《含濒危药材中药品种处理原则》和《化学药品研究资料及图谱真实性问题判定标准》。
现予印发,自印发之日起执行。
附件:1.化学药品技术标准2.多组分生化药技术标准3.中药质量标准不明确的判定标准及处理原则4.含濒危药材中药品种处理原则5.化学药品研究资料及图谱真实性问题判定标准国家食品药品监督管理局二○○八年六月三日附件1:化学药品技术标准一、制剂所用原料药和辅料的来源、质量控制《药品注册管理办法》第二十五条规定:单独申请注册药物制剂的,研究用原料药必须具有药品批准文号、《进口药品注册证》或者《医药产品注册证》,该原料药必须通过合法的途径获得。
研究用原料药不具有药品批准文号、《进口药品注册证》或者《医药产品注册证》的,必须经国家食品药品监督管理局批准。
附件2规定:申请制剂的,应提供原料药的合法来源证明文件,包括原料药的批准证明文件、药品标准、检验报告、原料药生产企业的营业执照、《药品生产许可证》、《药品生产质量管理规范》认证证书、销售发票、供货协议等的复印件。
基于该规定,对存在以下情况的注册申请将不予批准:1.单独申请注册药物制剂,提供原料药虚假证明性文件的;申报生产时,原料药如系通过赠送途径获得而未能提供该原料药合法来源证明和供货协议的;2.单独申请注册药物制剂,在药品注册过程中,所用原料药的批准文号已被废止的,或原料药生产企业已被吊销《药品生产许可证》的;3.制剂所用原料药由相同申请人或不同申请人申报,原料药申请已因现场核查被撤回或退回,或因其他各种原因不予不批准或予以退审的;4.所用原料药、辅料的质量控制不能保证药品安全性和有效性的。
药审中心——仿制药相关解答

化药共性问题解答——药学(仿制药相关解答)合成工艺:1.我们有一个化3.2类新药已拿到贵中心下发的生产现场核查通知书,但是在开展相关准备工作时,发现其中一家原料供应商已停产,无法提供原料,我公司是否可以更换另外的一家原料供应商,并将相应的研究资料以补充资料的形式提交给贵中心,待贵中心批准后再进行生产现场检查,不知道这样做是否妥当?答:对于使用已上市原料药并在药物制剂注册过程中变更原料药来源的情况,如确属原料药供应商停产等无法抗拒原因,需要在注册过程中变更制剂使用的原料药来源的,申请人一般应在申报生产时一并提出变更申请,并提交按照相关技术指导原则进行的变更前后的对比研究资料,最迟应当在药品技术审评结束前提出原料药变更申请并同时提交相关支持性研究资料。
变更中涉及管理方面问题应符合注册管理的相关规定。
2. 某个药物,国外研究结果表明存在多晶型及晶型专利,如何对本品晶型进行相关研究。
答:对于仿制多晶型药物时,首先要保证与被仿药物的物质基础一致,晶型也应该和原研产品一致;如果该晶型存在知识产权问题,在进行开发时要对多晶型进行相关的研究,明确晶型的不一致会影响药物的哪些特性(生物学还是物理学特性),在此基础上选择合理的晶型。
3.有一原料药采用进口原料中间体,在国内完成最后一步的合成。
据了解,目前FDA要求合成原料药的反应步数至少应为三步;欧盟要求至少有一步化学反应是在申报企业生产。
我们这样做是否可行?答:这个问题实质上是如何选择起始原料。
起始原料的选择不仅仅是根据反应步骤的长短来选择,由于起始原料的质量对原料药的制备工艺有较大的影响,特别是起始原料结构较复杂,或合成路线较短时更会产生重要影响,一方面起始原料引入的杂质可能会参与后续反应形成一系列副反应杂质或直接残留在终产品中,进而影响终产品的质量;另一方面,外购起始原料的工艺与过程控制的不完善或变更都可能会影响到起始原料的质量。
所以,对起始原料的质量进行控制是原料药质量控制体系的重要组成部分,药物的质量需要从源头考虑的充分体现。
注射制剂变更灭菌工艺的研究思路

注射制剂变更灭菌工艺的研究思路————————————————————————————————作者:————————————————————————————————日期:ﻩ摘要:近期,注射制剂变更灭菌工艺条件的补充申请较为多见。
申请人多根据国食药监注[2008]7号文发布的化学药品注射制剂和多组分生化药注射制剂的基本技术要求,为满足无菌保证水平,对注射制剂提高了灭菌条件。
由于前期研究不足,常导致不批准的现象出现。
为了更好地提高研发和评价效率,本文整理了关于变更灭菌工艺的研究思路和一些研究中应关注的问题。
ﻫ关键词:注射制剂变更灭菌工艺研究思路注射制剂是一类常见剂型,由于给药途径的特殊性,对其的质量要求较高。
注射制剂变更灭菌工艺条件是变更生产工艺中较有代表性的一类,此类变更可能对药品安全性、有效性和质量可控性产生较显著的影响,根据《已上市化学药品变更研究的技术指导原则》的分类原则,属于III类变更,需进行全面的研究和验证工作。
ﻫ当前,注射制剂变更灭菌工艺条件的补充申请较为多见。
部分申请人仅关注了无菌保证水平是否符合要求,却忽视了提高灭菌条件后,使制剂中各组分,包括原料、辅料,以及包装材料都处于更剧烈的温度条件下,由此对产品质量带来的影响。
基于质量源于设计的理念,建议从以下思路进行研究: 首先关注产品的立题合理性,特别是某些早期上市,安全性担忧较大、临床治疗性和用药顺应性,以及剂型规格设计等方面不符合国食药监注[2008]7号文要求的品种,应对其立题合理性进行全面评估。
在立题可行的前提下,要结合原料药的性质、处方中辅料及溶剂的性质、灭菌工艺的特点,包装材料的特性等对产品进行详细的研究和验证工作。
质量对比研究中,采用的质量标准应为当前认可的标准。
ﻫ在此研究思路下,我们对此类变更的研究关注点进行了细化梳理,供研究者参考。
需要说明的是,本文所涉及的仅为采用终端灭菌的注射制剂,暂不涉及采用无菌生产工艺的品种。
化学药品注射剂基本技术要求(试行)

国食药监注[2008]7号化学药品注射剂基本技术要求(试行) 本技术要求适用于化学药品中各种注册分类得注射剂、本技术要求主要针对目前化学药品注射剂研发、生产与使用中存在得突出问题,在遵循一般评价原则得基础上,通过分析可能影响注射剂临床使用安全性得主要因素,结合品种得上市基础等,提出化学药品注射剂审评中得重点关注点与相应得技术要求。
一、化学药品注射剂剂型选择得必要性、合理性(一)选择注射途径给药剂型得必要性、合理性对剂型得必要性、合理性进行评价通常应综合考虑如下因素:1、药物得理化性质、稳定性与生物学特性药物得理化性质(溶解度、pKa、分配系数、吸湿性、晶型等)、稳定性(对光、湿、热得稳定性,固、液状态下得稳定性与配伍稳定性)与生物学特性(吸收、分布、代谢、消除等)可以为剂型得选择提供指导,在有些情况下甚至可能限定剂型得选择。
2、临床治疗得需要在明确药物理化性质及生物学性质得基础上,应结合药物临床治疗需求选择剂型。
例如:用于出血、休克、中毒等急救治疗得药物,需要快速起效,通常选择注射剂。
如口服药物已可满足临床需求,除特殊需要外,不宜再开发注射制剂;如肌肉注射能够满足临床需要,尽量不选择静脉给药。
3、临床用药得顺应性包括医生用药得方便以及患者使用得顺应性。
除此之外,还要考虑制剂工业化生产得可行性及生产成本等。
对于由其她给药途径改为注射给药途径得品种,以及由普通注射剂改为特殊注射剂得品种,应对所改剂型与原剂型进行安全性、有效性、质量可控性方面得比较分析,阐明所改剂型得特点与优势、(二)注射剂不同剂型选择合理性得评价原则注射剂一般包括大容量注射剂(50ml以上)、小容量注射剂(20ml以下)以及粉针剂三种剂型。
在选择确定剂型时,要权衡考虑各种剂型得无菌保证水平、杂质得控制水平、工艺得可行性、临床使用得方便等,从中选择最优剂型。
对于国内外已上市得注射剂,根据当前对注射剂不同剂型选择合理性得认知,如已上市剂型为最优剂型,研制产品一般应首选已上市剂型;如已上市剂型不就是最优剂型,则不宜再仿制该剂型。
注射级聚山梨酯80法规要求

注射级聚山梨酯80法规要求Zhulikou431 内部培训2012 中国谨记纸上得来终觉浅,绝知此事要躬行!---陆游本培训资料参考文献更新至20121001.任何宝贵建议,请联系zhulikou431@.目录(contents)第01章:名词解析第02章:中国药典2010版对聚山梨酯的要求第03章:USP32对聚山梨酯的要求第04章:EP7对聚山梨酯的要求第05章:SFDA对聚山梨酯的法规要求第06章:CDE对聚山梨酯的要求第07章:FDA IIG数据库数据第08章:初步结论注射级聚山梨酯法规要求第01章:名词解析1.1聚山梨酯和吐温1.2司盘和失水山梨醇脂肪酸酯说明:本资料主要介绍法规对聚山梨酯80的要求。
注射级聚山梨酯法规要求1.1聚山梨酯和吐温简述:吐温是(TWEEN)的音译,也叫吐温型乳化剂,为司盘(Span,山梨醇脂肪酸酯)和环氧乙烷的缩合物,为一类非离子型去污剂。
化学名称:聚氧乙烯失水山梨醇脂肪酸酯,简称聚山梨酯(Polysorbate)。
产品系列:由于司盘为山梨醇与不同高级脂肪酸所形成的酯,故吐温实际上是同类型的系列产品,在一般精细化工店或化学试剂公司分20,40,60,80好多种,根据不同的需要来选用。
---来自百度百科注射级聚山梨酯法规要求1.2司盘和失水山梨醇脂肪酸酯药物名:失水山梨醇脂肪酸酯英文名称:Span分子式:C7H11O6-R分子量:346.45~957.46性能:本品为白色或微黄色蜡状物、片状体、粉沫状(≥100目)。
溶于热的乙醇、乙醚、甲醇及四氯化碳,微溶于乙醚、石油醚、能分散于热水中,是w/o型乳化剂,具有很强的乳化、分散、润滑作用,可与各类表面活性剂混用,尤其适应与吐温-60(T-60),复配使用效果更佳。
HLB(亲水亲油平衡)值4.7,熔点52-57℃。
功用作用:为失水山梨醇与不同高级脂肪酸所形成的酯,如司盘-20(SP-20)为月桂酸酯;司盘-80(SP-80)为单油酸酯。
关于化学药品及多组分生化注射剂再注册7号文资料审查的有关事项
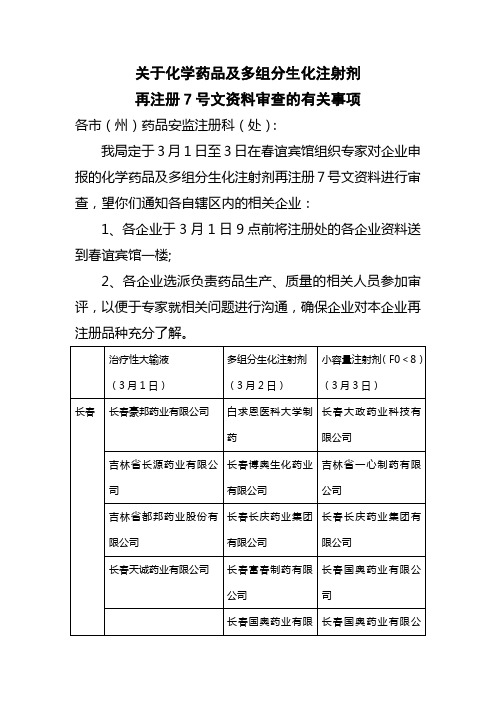
关于化学药品及多组分生化注射剂
再注册7号文资料审查的有关事项
各市(州)药品安监注册科(处):
我局定于3月1日至3日在春谊宾馆组织专家对企业申报的化学药品及多组分生化注射剂再注册7号文资料进行审查,望你们通知各自辖区内的相关企业:
1、各企业于3月1日9点前将注册处的各企业资料送到春谊宾馆一楼;
2、各企业选派负责药品生产、质量的相关人员参加审评,以便于专家就相关问题进行沟通,确保企业对本企业再注册品种充分了解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
国家食品药品监督管理局关于发布化学药品注射剂和多组分生化药注射剂基本技术要求的通知(国食药监注[2008]7号)【收藏】各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为落实国家局制定的《整顿和规范药品研制、生产、流通秩序工作方案》(国食药监办〔2006〕465号),严格审评审批化学药品注射剂、中药注射剂和多组分生化注射剂等安全性风险较大的3类品种。
国家局组织制定了《化学药品注射剂基本技术要求(试行)》和《多组分生化药注射剂基本技术要求(试行)》(以下称《技术要求》),现予发布,请参照执行,并将有关事宜通知如下:一、国家局已受理但尚未批准注册的化学药品注射剂和多组分生化药注射剂应参照《技术要求》进行研究。
二、已经批准注册的化学药品注射剂和多组分生化药注射剂也应参照《技术要求》进行相关研究,并在申报再注册时提供相关研究资料。
三、对已上市化学药品注射剂、多组分生化药注射剂进行仿制、改变剂型或者改变给药途径研究时,研究者应当慎重考虑已上市品种的研究基础。
附件:1.化学药品注射剂基本技术要求(试行)2.多组分生化药注射剂基本技术要求(试行)国家食品药品监督管理局二○○八年一月十日附件1:化学药品注射剂基本技术要求(试行)本技术要求适用于化学药品中各种注册分类的注射剂。
本技术要求主要针对目前化学药品注射剂研发、生产和使用中存在的突出问题,在遵循一般评价原则的基础上,通过分析可能影响注射剂临床使用安全性的主要因素,结合品种的上市基础等,提出化学药品注射剂审评中的重点关注点和相应的技术要求。
一、化学药品注射剂剂型选择的必要性、合理性(一)选择注射途径给药剂型的必要性、合理性对剂型的必要性、合理性进行评价通常应综合考虑如下因素:1.药物的理化性质、稳定性和生物学特性药物的理化性质(溶解度、pKa、分配系数、吸湿性、晶型等)、稳定性(对光、湿、热的稳定性,固、液状态下的稳定性和配伍稳定性)和生物学特性(吸收、分布、代谢、消除等)可以为剂型的选择提供指导,在有些情况下甚至可能限定剂型的选择。
2.临床治疗的需要在明确药物理化性质及生物学性质的基础上,应结合药物临床治疗需求选择剂型。
例如:用于出血、休克、中毒等急救治疗的药物,需要快速起效,通常选择注射剂。
如口服药物已可满足临床需求,除特殊需要外,不宜再开发注射制剂;如肌肉注射能够满足临床需要,尽量不选择静脉给药。
3.临床用药的顺应性包括医生用药的方便以及患者使用的顺应性。
除此之外,还要考虑制剂工业化生产的可行性及生产成本等。
对于由其他给药途径改为注射给药途径的品种,以及由普通注射剂改为特殊注射剂的品种,应对所改剂型与原剂型进行安全性、有效性、质量可控性方面的比较分析,阐明所改剂型的特点和优势。
(二)注射剂不同剂型选择合理性的评价原则注射剂一般包括大容量注射剂(50ml以上)、小容量注射剂(20ml以下)以及粉针剂三种剂型。
在选择确定剂型时,要权衡考虑各种剂型的无菌保证水平、杂质的控制水平、工艺的可行性、临床使用的方便等,从中选择最优剂型。
对于国内外已上市的注射剂,根据当前对注射剂不同剂型选择合理性的认知,如已上市剂型为最优剂型,研制产品一般应首选已上市剂型;如已上市剂型不是最优剂型,则不宜再仿制该剂型。
对于国内外均未上市的注射剂,或依据国内外已上市注射剂改变剂型的产品,在遵循剂型选择一般原则的基础上,从无菌保证水平考虑,剂型选择尚应遵循以下原则:1.首先要考虑被选剂型可采用的灭菌工艺的无菌保证水平的高低。
原则上首选剂型应能采用终端灭菌工艺,并保证SAL≤10-6。
2.对于有充分的依据证明不适宜采用终端灭菌工艺且临床必需注射给药的品种,可考虑选择采用无菌生产工艺的剂型。
通常无菌生产工艺仅限于粉针剂或部分小容量注射剂。
3.大容量注射剂、小容量注射剂和粉针剂之间的互改,如无充分的依据,所改剂型的无菌保证水平不得低于原剂型。
二、化学药品注射剂规格的合理性、必要性(一)未在国内外上市的药物规格确定的一般原则1.根据临床研究确定的用法用量,从方便临床用药、满足临床用药需要的角度确定,可以伴随临床研究进行必要的修订。
2.工艺的可行性(如可能要考虑溶解性、生产设备等的限制)。
(二)在国外和/或国内已上市药物规格确定的一般原则产品规格应根据说明书中规定的用法用量,从方便临床用药、满足临床用药需要的角度确定,并应符合国家有关规定。
对于国内外已上市注射剂,根据当前对注射剂规格选择合理性的认知,如已上市规格合理(被仿制产品无详细临床研究资料,对于规格的合理性尚不能肯定的情况除外),应选择已上市同剂型的相同规格。
对于仿制国内外已上市产品同时增加规格、改变剂型产品的规格选择、对已上市产品增补规格的,应符合以下要求:1.所选规格应在说明书规定的用法用量范围内,一般不得小于单次最小用量,或者大于单次最大用量。
2.所选规格一般应为常规规格(如小容量注射液体积常规为1、2、5、10、20ml;大容量注射液体积常规为50、100、250、500ml等)。
3.所选规格应为临床必需,且能方便医生、护士、病人用药及药剂科对药品的管理。
4.对于新增规格特别是给药浓度发生变化的情况,应有充分数据说明此规格临床使用安全、有效。
如新增规格涉及用药人群/用法用量的改变,一般应进行安全有效性的系统评价。
三、化学药品注射剂原、辅料质量控制及来源(一)原料药质量控制1.未在国内外上市的注射剂未在国内外上市的注射剂原料药的质量应符合注射用原料药的一般要求,并应重点关注以下问题:(1)申报临床时,应关注注射给药途经的非临床安全性研究所用样品的质量。
用于制备临床研究用样品的原料药,在有关物质的种类和含量方面,不得超过非临床安全性研究用样品的相关指标。
(2)申报生产时,应关注临床研究用样品的质量和杂质的安全性研究结果。
原料药的上市质量标准中,有关物质的限度要求原则上不得超过临床研究用样品和安全性评价样品的检测数据。
相关技术要求可参考《化学药物杂质研究的技术指导原则》。
(3)用于粉末直接分装的原料药,工艺中应采用可靠的方法进行灭菌,原料药精制、干燥、包装应在百级环境下进行,质量应达到无菌保证的要求,无菌检查及细菌内毒素检查应符合规定。
2.在国外和/或国内已上市的注射剂(1)采用购买已批准上市的注射用原料药申报注射剂者,应提供原料药合法来源及质量控制的详细资料,包括生产企业、批准文号、执行的质量标准、检验报告、购买发票、供货协议等。
若为进口原料药,还应提供进口注册证。
(2)采用新研制的原料药申报注射剂者,应与制剂同时申报原料药,并应按照注射用原料药的要求提供规范完整的申报资料。
原料药经技术审评符合要求是其注射制剂批准临床注册的必要条件。
(3)有注射用原料药上市的,应使用有合法来源的注射用原料药申报注射剂。
若尚无注射用原料药上市,需对原料药进行精制并制定内控标准,使其达到注射用的质量要求。
在注册申请时,除提供相关的证明性文件外,应提供精制工艺的选择依据、详细的精制工艺及其验证资料、精制前后的质量对比研究资料等。
精制的主要目标是降低杂质含量,使其符合注射用要求,故应对精制后样品按照《化学药品杂质研究的技术指导原则》的要求进行规范的杂质研究。
3.上市后药品改变原料药注射剂经批准上市后,如需更改原料药的生产商或质量标准等,应按补充申请进行申报。
(二)辅料质量控制1.辅料选用的基本原则(1)应采用符合注射用要求的辅料;(2)在满足需要的前提下,注射剂所用辅料的种类及用量应尽可能少;(3)应尽可能采用注射剂常用辅料。
2.使用已批准上市的注射用辅料使用已批准上市的注射用辅料,应提供辅料来源及质量控制的详细资料,包括生产企业、执行的质量标准、检验报告、购买发票、供货协议,有批准文号的还应提供批准文号,进口辅料还应提供进口注册证。
3.使用尚未批准供注射途经使用的辅料使用尚未经国家食品药品监督管理局按注射途径批准生产或进口的辅料,除下述情况外,均应按新辅料与制剂一并申报。
(1)使用国外公司生产,并且已经在国外上市注射剂中使用,但尚未正式批准进口的辅料,在申请临床研究时可暂不要求提供《进口药品注册证》,但须提供该辅料的国外药用依据、执行的质量标准及检验报告。
在制剂批准生产前所用辅料应获得进口注册。
(2)对于注射剂中有使用依据,但尚无符合注射用标准产品生产或进口的辅料,可对非注射途经辅料进行精制使其符合注射用要求,并制定内控标准。
申报资料中应提供详细的精制工艺及其选择依据、内控标准的制定依据。
必要时还应进行相关的安全性试验研究。
4.上市后药品改变辅料注射剂经批准上市后,如需更改辅料的相关内容,例如生产商或质量标准等,应按补充申请进行申报。
为尽量减少注射剂灭菌前的微生物负荷,应考虑对所用原辅料进行相应的微生物控制。
四、化学药品注射剂处方及制备工艺合理性、可行性研究,特别是灭菌工艺的选择及验证研究、工艺稳定性研究等(一)处方研究注射剂处方研究应包括对处方组成(原料药、辅料)的考察、处方设计、处方筛选及优化、处方确定等内容。
1.处方组成的考察(1)原料药:处方设计前应详细调研分析原料药的理化性质(如外观色泽、pH、pKa、熔点、水分、溶解度、油/水分配系数等,以及在固态和/或溶液状态下对光、热、湿、氧等的稳定性情况、所含杂质情况)、生物学性质(如在生理环境下的稳定性、药代动力学性质、毒副作用及治疗窗等),为处方设计提供依据。
(2)辅料:应调研分析拟用辅料的理化性质与合理用量范围,调研分析药物与拟用辅料之间、不同辅料之间的相容性,了解已经明确存在的辅料与辅料间、辅料与药物间相互作用情况,以避免处方设计时选择存在不良相互作用的辅料。
对于缺乏相关研究资料的,应进行相容性研究。
对辅料用量超出常规用量且无文献支持的,需进行必要的药理毒理试验,以验证在所选用量下的安全性。
对于改变给药途径的辅料,应充分证明在注射途径下的安全性。
2.处方设计处方设计应在上述对药物和辅料有关研究的基础上,根据具体剂型的特点及临床应用的需要,结合相关文献及具体工作实践,先设计几种基本合理的处方,然后结合制备工艺研究,以制剂的外观、色泽、澄明度、pH、含量、有关物质、细菌内毒素或热原、不溶性微粒等为评价指标,对不同处方进行考察。
通过考察确定初步处方,并明确影响制剂质量的关键因素。
3.处方筛选和优化处方筛选和优化是在处方设计的基础上,针对确定的影响制剂质量的关键因素,采用各种实验设计(如比较法,正交设计、均匀设计等),做进一步优化,对关键辅料的种类和用量进行最佳选择。
考察评价指标除应包括外观、色泽、澄明度、pH、含量、有关物质、细菌内毒素或热原、不溶性微粒外,还应包括稳定性评价。
处方研究阶段的稳定性评价主要通过影响因素试验进行,对于给药时需使用附带专用溶剂的,或使用前需要用其他溶剂稀释、配液(如静脉滴注用粉针和小水针)的,还需要进行配伍稳定性研究。
