功能科室检查及质量控制SOP详见
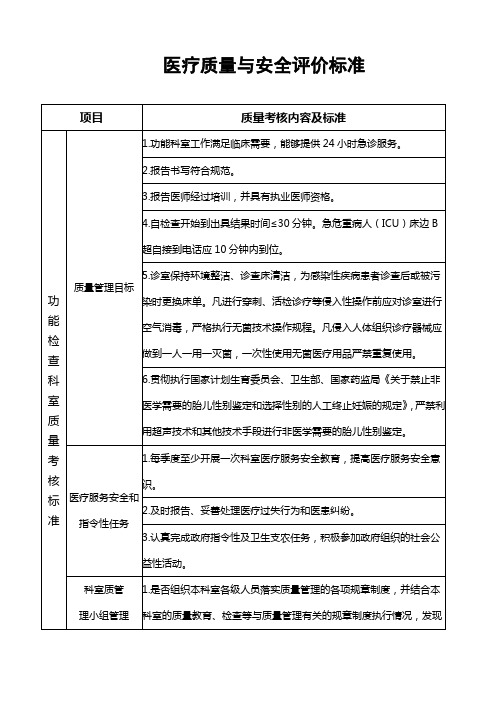
功能检查科室质量考核标准
目标四、
落实“危急值”报告制度
1.落实“危急值”报告制度。
2.“危急值”报告应有可靠途径且检验人员能为临床提供咨询服务。“危急值”报告重点对象是急诊科、手术室、各类重症监护病房等部门的急危重症患者。
3.“危急值”项目可根据医院实际情况认定,至少应包括有脏器破裂大出血、严重心律失常等。
1.在通常诊疗活动中医务人员之间的有效沟通,做到正确执行医嘱,不使用口头或电话通知的医嘱。
2.只有在对危重症患者紧急抢救急的特殊情况下,对医师下达的口头临时医嘱,护士应向医生重述,在执行时实施双重检查。
3.接获口头或电话通知的患者“危急值”或其它重要的检验结果时,接获者必须规范、完整的记录检验结果和报告者的姓名与电话,进行复述确认无误后方可提供医师使用。
医疗质量与安全评价标准
项目
质量考核内容及标准
功
能
检
查
科
室
质
量
考
核
标
准
质量管理目标
1.功能科室工作满足临床需要,能够提供24小时急诊服务。
2.报告书写符合规范。
3.报告医师经过培训,并具有执业医师资格。
4.自检查开始到出具结果时间≤30分钟。急危重病人(ICU)床边B超自接到电话应10分钟内到位。
5.诊室保持环境整洁、诊查床清洁,为感染性疾病患者诊查后或被污染时更换床单。凡进行穿刺、活检诊疗等侵入性操作前应对诊室进行空气消毒,严格执行无菌技术操作规程。凡侵入人体组织诊疗器械应做到一人一用一灭菌,一次性使用无菌医疗用品严禁重复使用。
科室医院
感染管理
1.落实预防和控制医院感染管理规章制度。
2.对医院感染及其相关危险因素进行监测、分析和反馈,针对问题提出控制措施并指导实施。
医院检验科内部质量SOP控制程序

医院检验科内部质量SOP控制程序
检验科内部质量控制程序的目的:对检验程序进行质量控制,以保证检验结果的准确性。
1目的
对检验程序进行质量控制,以保证检验结果的准确性。
2适用范围
开展的检验项目。
3职责
3.1技术负责人负责批准室内质控规则和检验过程的质量控制程序。
3.2各组组长负责制定本组室内质控规则和检验过程的质量控制程序。
3.3检测人员负责执行检验过程的质量控制程序和对本岗位室内质控进行分析和处理。
3.4质量监督员监督本组内是否按照程序文件和作业指导书有检验过程质量控制程序的要求进行。
4工作程序
4.1标本接受的质量控制
检验人员严格按照《样品的核收、登记及保存程序》中的有关规定对标本进行验收和不合格标本处理。
4.2标本前处理的质量控制。
11-科室质量控制SOP
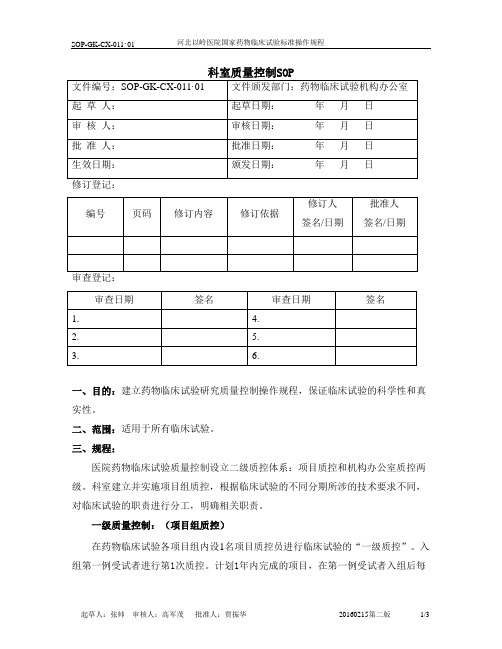
一、目的:建立药物临床试验研究质量控制操作规程,保证临床试验的科学性和真实性。
二、范围:适用于所有临床试验。
三、规程:医院药物临床试验质量控制设立二级质控体系:项目质控和机构办公室质控两级。
科室建立并实施项目组质控,根据临床试验的不同分期所涉的技术要求不同,对临床试验的职责进行分工,明确相关职责。
一级质量控制:(项目组质控)在药物临床试验各项目组内设1名项目质控员进行临床试验的“一级质控”。
入组第一例受试者进行第1次质控。
计划1年内完成的项目,在第一例受试者入组后每月进行1次质控,直至最后一名受试者出组。
计划1年以上完成的项目,在第一例受试者入组后每两月进行1次质控,直至最后一名受试者出组。
待申办方关闭本中心时即项目结束进行最后1次质控。
对照质量控制检查表(见附表),对所质控的病例进行检查。
具体程序如下:1.临床试验的项目负责人指定项目质控员负责本项目的检查。
2. 项目质控人员本着认真负责,严谨的科学态度对试验项目进行定期抽样或全面质量检查。
3.项目质控人员应与被检查病例的观察无关,并熟悉GCP、临床试验方案和相关SOP.4.一级质控检查的病例数要求为:对全部入组病例相关资料进行质控检查和实验室检查溯源。
5. 检查内容(详见《质量控制检查表》):包括研究者对GCP的相关知识、试验方案和相关SOP的熟悉程度;受试者的真实性、与筛选标准的符合性;知情同意书获得情况、试验数据的真实性;不良事件的记录等。
6.检查程序:(1)检查前①审阅试验方案、研究者手册、SOP等资料,了解最新的要求和来自研究中心的信息更新。
②回顾试验进度,查阅以往的检查记录及报告,充分了解完成情况和存在问题。
③与被抽查病例的研究者联系,了解最新情况并确定检查具体时间。
④与研究者讨论检查可能出现的问题和要解决的问题。
⑤准备检查所需文件、表格、报告、资料与物品。
(2)检查中①与研究人员会面,说明本次检查内容,了解试验进展情况,讨论以往问题并了解现存问题。
医院检验科完整SOP程序文件.doc

一、科室设置1、科室各实验室设置及负责人2、科室人员结构3、检验中心平面图4、检验中心工作流程图二、检验中心工作职责(一)检验中心各级人员工作职责1、检验中心主任、副主任工作职责2、主任检验师工作职责3、主管检验师工作职责4、检验师工作职责5、检验士工作职责(二)检验中心各实验室工作职责1、临检室人员岗位职责2、生化室人员岗位职责3、免疫室人员岗位职责4、细菌室人员岗位职责5、骨髓细胞室人员岗位职责6、急诊检验人员岗位职责三、检验中心各项规章制度1、生物安全管理制度2、检验质量管理制度3、血型安全鉴定制度4、差错事故登记制度5、安全制度6、急诊检验制度7、技术管理制度8、工作职责制度9、试剂管理制度10、天平称量制度11、实习生管理制度12、仪器管理制度13、标本管理制度14、档案管理制度15、为民服务公约16、细菌培养室无菌制度17、同位素实验室管理制度18、会议学习制度19、请示报告制度20、保密守则21、职工考勤制度22、人事考核制度23、治安保卫制度24、消防安全制度25、业务学习管理制度26、物资报废制度27、赔偿制度28、奖罚制度29、质量信息反馈制度30、计算机使用管理制度31、血常规复查制度32、卫生制度四、检验中心标准操作规程(一)检验中心各类仪器标准操作规程1、BECKMAN CX9生化操作规程2、日立7600生化仪操作规程3、RA-1000生化仪操作规程4、644电解质仪操作规程5、SP-4430干式生化仪操作规程6、拜耳248血气分析操作规程7、ACCESS化学发光操作规程8、AXSYM化学发光仪操作规程9、Array 360型全自动特定蛋白分析仪操作规程10、BIO-RAD-Model 550酶标仪操作规程11、FJ放射免疫γ计数仪操作规程12、ACL200自动血凝仪操作规程13、CoAg-A-MTX全自动血凝仪操作规程14、HMX全自动血细胞分析仪操作规程15、CD—1700全自动血细胞分析操作规程16、Coulter EPICS XL流式细胞仪操作规程17、MONITOR JI红细胞沉降仪操作规程18、NycoCard Reader II型多功能全定量金标检测仪操作规程19、UF-100全自动尿液分析仪操作规程20、盈东尿十一项化学分析仪操作规程21、ATB 细菌鉴定仪操作规程22、二氧化碳孵箱操作规程23、BacTAlert120全自动血培养操作规程24、伟力彩色精子动态分析仪操作规程25、DiaMed-ID Micro TyPing System达亚美微量定型系统操作规程26、1575型微孔板清洗器操作规程(二)检验中心检测项目标准操作规程A、临检室A1、血常规检验标准操作规程A2、嗜酸性粒细胞直接计数标准操作规程A3、红细胞沉降率测定标准操作规程A4、血型鉴定标准操作规程A5、尿常规标准操作规程A6、一小时尿沉渣计数标准操作规程A7、尿乳糜定性检查标准操作规程A8、大便常规标准操作规程A9、虫卵及包囊浓缩检查标准操作规程A10、隐血试验标准操作规程A11、脑脊液检验标准操作规程A12、浆膜腔积液检查标准操作规程A13、精液检查标准操作规程A14、前列腺液检查标准操作规程A15、阴道分泌物检查标准操作规程A16、胃液检查标准操作规程B、生化室B1、血氨测定标准操作规程B2、17-KS测定标准操作规程B3、17-OH测定标准操作规程B4、VMA标准操作规程B5、Insulin Autoantibadies(IAA) 胰岛素自身抗体标准操作规程B6、Islet Cell Autoantibodies (ICA) 胰岛细胞自身抗体标准操作规程B7、脯氨酸肽酶测定(Prolidase Test Kit) 标准操作规程B8、I型糖尿病检测(诊断酶联试剂盒)标准操作规程B9、血清Ⅳ胶原蛋白(PANASSAY Ⅳ. C)标准操作规程B10、血清蛋白电泳标准操作规程B11、N-乙酰葡萄糖苷酶(NAG) 标准操作规程B12、腺苷脱氨酶(ADA) 标准操作规程B13、尿肌酸测定标准操作规程B14、肌钙蛋白(TNT)测定标准操作规程B15,肿瘤相关物质测定标准操作规程C、免疫室、发光、放免室C1、HAVAbIgM标准操作规程C2、PreS1标准操作规程C3、HBSAg 标准操作规程C4、HBSAb标准操作规程C5、HBEAg标准操作规程C6、HBcAb标准操作规程C7、HBcAbIgM标准操作规程C8、HCVIgG标准操作规程C9、HCVIgM 标准操作规程C10、HDVAg标准操作规程C11、HDVIgG标准操作规程C12、HDVIgM标准操作规程C13、HEVAbIgG标准操作规程C14、HEVAbIgM标准操作规程C15、HGVAb标准操作规程C16、TTV-IgG标准操作规程C17、寒冷凝集反应标准操作规程C18、ENA多肽抗体谱标准操作规程C19、ANA标准操作规程C20、ds-DNA标准操作规程C21、幽门螺杆菌抗体标准操作规程C22、嗜异性凝集试验标准操作规程C23、肥达氏反应标准操作规程C24、胰岛素测定标准操作规程标准操作规程C25、C肽测定标准操作规程标准操作规程C26、胰高血糖素测定标准操作规程标准操作规程C27、α1-微球蛋白测定标准操作规程C28、β2-微球蛋白测定标准操作规程C29、THP-蛋白测定标准操作规程C30、抗TG,TM抗体测定标准操作规程C31、抗INS-抗体测定标准操作规C32、人III型前胶原放射免疫测定标准操作规程C33、逶明质酸放免测定标准操作规程C34、Ⅳ型胶原放免测定标准操作规程C35、内皮素放免测定标准操作规程C36、肺肿瘤标记CY21-1放免测定标准操作规程C37、T3 T4 TSH FT3 FT4 测定标准操作程序(SOP)C38、AFP、CEA、Fer、BR、OV、GI、PSA、 fPSA,Ca-125,Ca-199,Ca-153测定标准操作程序(SOP)C39、HCG、PRL、FSH、LH、E2、P(孕酮)、T(睾酮)测定标准操作程序(SOP)C40、铁蛋白、叶酸、VitB12测定标准操作程序(SOP)C41、CKMB、cTnI、MYO测定标准操作程序(SOP)C42、IgE测定标准操作程序(SOP)C43、地高辛、茶碱、皮质醇、卡马西平、苯巴比妥、苯妥英钠,丙戊酸,安定,环胞霉素标准操作程序C44、DPD测定标准操作程序(SOP)C45、过敏原测定标准操作程序D、血液、骨髓室、FCMD1、D-二聚体标准操作规程D2、3P试验标准操作规程D3、骨髓细胞学检查标准操作规程D4、过氧化物酶(POX)染色标准操作规程D5、苏丹黑B(SBB)染色标准操作规程D6、中性粒细胞碱性磷酸积分(NAP)染色改良GOmorI氏钙钴法标准操作规程D7、中性粒细胞碱性磷酸酶(NAP)染色偶氮偶联法标准操作规程D8、糖原(PAS)染色标准操作规程D9、酯酶染色---中性非特异性脂酶(α-NAE)染色标准操作规程D10、铁染色标准操作规程D11、酸性磷酸酶(ACP)染色标准操作规程D12、红细胞渗透脆性试验标准操作规程D13、自体溶血试验标准操作规程D14、血清酸化溶血试验(Ham试验) 标准操作规程D15、热溶血试验(定性) 标准操作规程D16、蔗糖溶血试验(糖水试验) 标准操作规程D17、变性珠蛋白小体检查(Heinz小体染色) 标准操作规程D18、血浆游离血红蛋白测定标准操作规程D19、淋巴细胞亚群测定标准操作规程D20、HLA B27 / HLA B7 测定标准操作规程D21、活化细胞亚群测定标准操作规程D22、活化血小板测定标准操作规程D23、APO 2.7测定标准操作规程D24、CD25/CD3 测定标准操作规程D25、MDR(P—gP)多药耐药基因)测定标准操作规程D26、TdT(MRD白血病残留病灶)测定标准操作规程D27、血小板糖蛋白测定标准操作规程D28、CD23(Ige低亲和力受体)测定标准操作规程D29、CD95 / Fas 测定标准操作规程D30、FCM试剂配制标准操作规程D31、Bcl-2 测定标准操作规程D32、ANNEXIN V 测定标准操作规程D33、P53 测定标准操作规程D34、λ链测定标准操作规程D35、CD55 测定标准操作规程D36、血小板抗体测定(PAIgG,PAIgM,PAIgA)标准操作规程D37、DNA测定标准操作规程D38、干细胞CD34测定标准操作规程D39、CD34+ 细胞绝对计数标准操作规程D40、纤溶酶原激活剂抑制物(PAI)活性测定(发色底物法) 标准操作规程D41、组织型纤溶酶原激活剂(t-PA)活性测定(发色底物法)标准操作规程D42、血管性假血友病因子(vWF)含量测定(ELISA)标准操作规程E、细菌室E1、革兰氏阴性鉴定卡及药敏卡(GNI及GNS卡的操作步骤)标准操作规程E2、革兰氏阳性鉴定卡及药敏卡(GPI 及GPS卡的操作步骤)标准操作规程E3、酵母菌鉴定卡(YBC卡)标准操作规程F、血库第一章临床输血技术规范第二章输血申请第三章受血者血样采集与送检第四章交叉配血第五章血液入库、核对、贮存第六章发血第七章输血附件一成分输血指南附件二自身输血指南附件三手术及创伤输血指南附件四内科输血指南附件五术中控制性低血压技术指南附件六输血治疗同意书附件七临床输血申请单附件八输血记录单附件九输血不良反应回报单一、科室设置1、科室各实验室设置及负责人4、检验中心工作流程图住院病人就诊检验流程门诊病人就诊检验流程二、检验中心工作职责(一)检验中心各级人员工作职责1、检验中心主任、副主任工作职责(1) 在院长、院党委领导下,负责本科的业务、教学、科研及行政管理工作(2) 负责组织本科业务技术建设规划、年度工作计划和诊断质量监测控制方案的制定、实施、检查和总结。
功能科科医疗质量检查核查标准
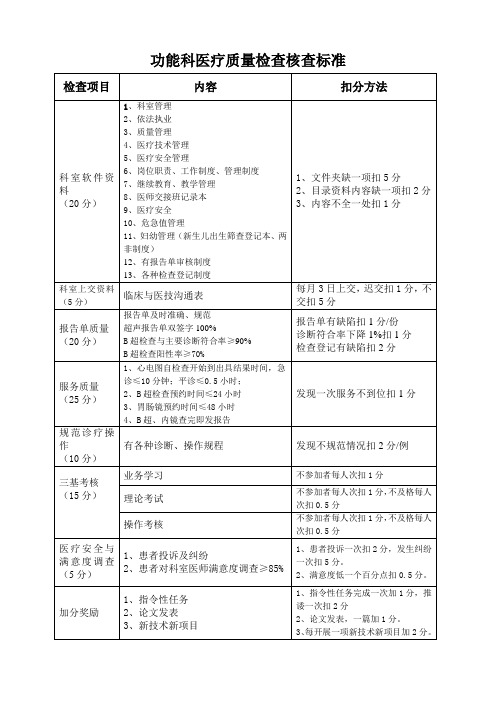
检查项目
内容
扣分方法
科室软件资料
(20分)
1、科室管理
2、依法执业
3、质量管理
4、医疗技术管理
5、医疗安全管理
6、岗位职责、工作制度、管理制度
7、继续教育、教学管理
8、医师交接班记录本
9、医疗安全
10、危急值管理
11、妇幼管理(新生儿出生筛查登记本、两非制度)
12、有报告单审核制度
诊断符合率下降1%扣1分
检查登记有缺陷扣2分
服务质量
(25分)
1、心电图自检查开始到出具结果时间,急诊≤10分钟;平诊≤0.5小时;
2、B超检查预约时间≤24小时
3、胃肠镜预约时间≤48小时
4、B超、内镜查完即发报告
发现一次服务不到位扣1分
规范诊疗操作
(10分)
有各种诊断、操作规程
发现不规范情况扣2分/例
13、各种检查登记制度
1、文件夹缺一项扣5分
2、目录资料内容缺一项扣2分
3、内容不全一处扣1分
科室上交资料(5分)
临床与医技沟通表
每月3日上交,迟交扣1分,不交扣5分
报告单质量
(20分)
报告单及时准确、规范
超声报告单双签字100%
B超检查与主要诊断符合率≥90%
B超检查阳性率≥70%
务
2、论文发表
3、新技术新项目
1、指令性任务完成一次加1分,推诿一次扣2分
2、论文发表,一篇加1分。
3、每开展一项新技术新项目加2分。
三基考核
(15分)
业务学习
不参加者每人次扣1分
理论考试
不参加者每人次扣1分,不及格每人次扣0.5分
功能科室医疗质量检查标准

(1)应急预案,包括处置流程与措施。
(2)有明确的质量与安全管理计划和指标。
(3)有质量与安全培训,对轮转医师培训后上岗。
2.相关人员知晓本部门、本岗位质量与安全管理指标。
3.科室落实质量与安全计划,定期开展质量与安全管理检查,对存在问题及缺陷及时整改。
20
三、由具备专业资质的执业医师出具诊断报告,解读检查结果。
1.有出具诊疗报告,解读检验结果的相关规定。
2.各种诊疗报告签署和发出均由具备专业资质(授权)的执业医师执行。
1.检查相关的规定。
2.抽查“临床诊断报告”,核实签发人资质。
20
四、有检查设备装置操作和维护维修制度与质量保证和检测制度。
1.有设备的操作、维护维修和检测制度,使用者经过培训。
2.有完整的设备使用、维护、检测、维修记录。
3.建立科室大型设备档案,对设备进行日常维护,保证设备正常运行。设备使用与维护有记录。
1.查制度和培训资料。
2.检查设备使用、维护、检测、维修记录。
3.查设备档案、使用、维护记录。
15
五、有质量与安全管理小组并有由专人负责,开展质量与安全管理,有明确的质量与安全管理指标。
功能科室医疗质量检查标准(内镜、脑图、肺功能、心电图)
检查内容
重点要求
检查方法内容
分值
存在问题
得分
一、卫生技术人员要应依法获得相应资质。
各级各类人员依法执业。(1)按照相关规定接受专业技能培训,依法取得执业资格与授权的人员、专业技师,应有专业资格证书。(2)所有人员经过岗前培训
检查特殊检查室人员专业资格证书。检查所有人员经过岗前培训记录或证书。
功能检查科质量控制制度

功能检查科质量控制制度一、引言近年来,随着科技的快速发展,功能检查科已成为医院中不可或缺的重要部门。
功能检查科主要负责对患者进行各类科学、准确的检查,为临床医生提供准确的诊断依据。
为了确保功能检查科能够提供高质量的服务,需要建立科学的质量控制制度。
二、质量控制目标1.提高检查仪器设备的准确性和稳定性;2.提高检查人员的技术水平和专业素养;3.做好检查前后的质量控制工作,保证结果的可靠性;4.加强科室与临床医生的沟通与协作,提高诊断准确率。
三、质量控制措施为了实现上述目标,功能检查科应采取以下质量控制措施:1.仪器设备的质量控制(1)定期维护:对所有重要的仪器设备进行定期的维护和保养,确保其正常工作状态。
(2)仪器校正:定期对仪器设备进行校正,保证其准确度和稳定性。
(3)仪器使用培训:在使用新的仪器设备前,对操作人员进行培训,确保其熟悉操作流程和仪器使用规范。
2.人员培训和质量控制(1)入职培训:对新员工进行系统的入职培训,包括岗位职责、工作流程、质量控制要求等内容。
(2)定期培训:定期组织员工参加相关的培训和学术交流活动,提高其专业知识和技术水平。
(3)考核评估:定期对员工的工作表现进行评估,鼓励优秀员工,及时发现和纠正不足之处。
3.检查过程的质量控制(1)标本采集:规范标本采集程序,确保标本的准确性和完整性。
(2)检查前准备:确保检查前的准备工作完善,如仪器设备的检查和校准、标本的处理等。
(3)检查操作:操作人员应按照规定的方法和流程进行检查操作,确保结果的准确性和可靠性。
(4)结果综合和分析:对检查结果进行综合和分析,及时反馈给临床医生,并参与病情讨论和诊疗方案制定。
4.科室与临床医生的协作(1)加强沟通:科室与临床医生之间应建立良好的沟通渠道,共同讨论和解决问题。
(2)定期会诊:定期组织会诊,就临床医生的需求和建议进行讨论和改进。
(3)诊断回顾:定期组织诊断回顾会议,对疑难病例的诊断结果进行讨论和总结,提高诊断准确率。
检验科SOP_05质量控制SOP

文件审批者:发布日期:操作者从事本项工作前,必须认真学习并掌握本手册的内容,严格按照操作规程操作!学习者:休订书册与增补程序内容与日期:学习者:休订书册与增补程序内容与日期:学习者:SOP_05-1室内质量控制标准操作程序一、目的:规范室内质量控制程序。
二、适用范围:检验科室内质量控制。
三、操作人员:检验科授权工作人员四、操作步骤:1.准备工作1.1建立健全的工作制度(程序、文件)1.2普及质量控制知识(人)1.3仪器的校正和维护(仪器)2.质控图的理论依据2.1正态分布2.2简单图形工具-质控图2.3允许误差范围的确定及有关问题2.4质控规则2.4.1质控规则概述2.4.2常用质控规则的定义2.4.3经典的Westgard多规则质控方法2.4.3.1 Westgard多规则2.4.3.2质控图的绘制2.4.3.3经典Westgard多规则质控方法具体应用的步骤2.4.3.4失控问题的解决3.室内质控的实际操作3.1质控品3.2建立质控图的均值3.3建立质控图的标准差3.4特殊情况的处理3.5更换质控品3.6绘制质控图及记录质控结果3.7质控规则的应用3.8失控情况处理及原因分析3.8.1失控情况处理3.8.2失控原因分析3.9室内质控数据的管理3.9.1每月室内质控数据统计处理3.9.2每月室内质控数据的保存3.9.3每月上报的质控数据图表3.9.4室内质控数据的周期性评价概述:在临床检验中,因工作本身人命关天的性质,较之其他行业,临床检验的管理者和分析人员更需要理解如何在常规操作过程中检测分析过程的质量,也都应懂得如何判断分析批是在控还是失控。
近年来检验技术的迅速发展,为临床检验的质量在测定方法上提供了更可靠的保证。
但决不能因为检验技术和检验方法的改进而错误地对临床检验的质量控制掉以轻心。
一些单位购置了先进的检验仪器后因忽视质控工作,其检验质量反而下降的现象不乏其例。
因此,严格的质量控制是先进的临床检验分析技术真正发挥作用的保证。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
目的:制定临床试验资料档案管理标准操作规程,使文件资料的保存与管理更加规范,保证临床试验文件资料的完整性、安全性。
适用范围:适用于药物临床试验各专业科室及相关部门。
内容:
1. 临床试验文件资料应有专人负责和管理,机构办公室档案管理员负责机构文件资料的分发、归档和保存,各专业科室指定专门的文件资料管理员负责本专业药物临床试验过程中文件资料的接收、保存与保管。
2. 临床试验文件包括:
2.1 临床试验所有标准操作规程;
2.2 临床试验记录文件,包括化验记录/结果、检测记录/结果、不良事件记录、病例报告表等与SOP相关的记录文件;
2.3 临床试验其它文件,如药品监督管理部门批件、伦理委员会批件、试验方案、知情同意书、研究者手册、双方签署的合同等。
3. 文件资料保存与管理的原则:
3.1 按GCP要求保存;
3.2 专人管理;
3.3 及时归档;
3.4 分类管理;
3.5 安全保存。
4. 文件的分发、生效:
4.1 分发:文件获批准后,机构负责向各专业科室发放各类文件,并在机构发文记录本TZRY-JG-AF/SOP-005-2.0上登记。
4.2 执行:新的标准操作规程颁发后,专业科室应及时组织培训,以保证在执行期内实施。
5. 文件的保管、保密、管理和保存:
5.1保管:接收文件后,由专人负责保管,存放在专用的上锁的、防火、防潮、防虫蛀的文件柜里或机构资料档案室内。
文件的保管必须建立完善的登记记录,仅可允许授权人员进入存取文档,不得随便传阅与复印。
查阅仅限于临床试验的研究者、官方检查人员和相关试验项目申办者委派的监查员或稽查员。
所有人员在查阅文件时必须登记查阅时间、原因并签字。
查阅完毕由资料管理员负责检查确定文件完好。
5.2保密:原始资料的记录不得修改和涂抹,任何人未经机构办公室和伦理委员会同意,不得泄漏有关文件内容。
应取出一份存档,其余的及时销毁,不能随意置放。
原始资料不得邮寄,受试者签认代码表和知情同意书不可丢失。
5.3管理:为便于管理和查阅,可以将每项临床试验的资料进行分类管理。
5.4 保存:临床试验必须保存的文件资料的项目,可参照现行GCP附录部分所列出的必须保存的最少文件清单TZRY-JG-AF/ZD-043-2.0。
电子文件可保存在单独的数据管理计算机中(不与网络相连)或移动硬盘、刻录CD等,电子文件要及时备份,必要时打印保存纸质备份。
6. 文件的返还和归档:
试验结束后,临床试验资料经资料管理员整理、项目负责人审核后,提交机构办公室,机构资料管理员验收签字后交机构档案室归档,档案室防火、防盗、防虫、防霉、防光、防尘、防有害生物、防污染等;配备防潮和灭火装置,定期检查以确保正常运转;定期进行通风除湿。
机构应保存临床试验资料至临床试验结束后至少五年,或按试验方案或合同约定的时限保存。
7. 附件
发文登记表 TZRY-JG-AF/SOP-005-2.0
GCP规定的药物临床试验研究者应保存的文件内容 TZRY-JG-AF/ZD-043-2.0
参考文献:
1.《药物临床试验质量管理规范》,2003版。
2. 《医院药物临床试验工作指南》,李斌等编著,人民军医出版社,2011版。
编号:TZRY-JG-AF/SOP-005-2.0
发文登记表
序号文件标题文号发文日期签收部门签收人
编号:TZRY-JG-AF/ZD-043-2.0
GCP规定的药物临床试验研究者应保存的文件内容一、临床试验准备阶段。
