(一)氨基酸及其种类
必须氨基酸的具体种类

必须氨基酸的具体种类氨基酸是构成蛋白质的基本单元,可分为20种常见氨基酸和2种罕见氨基酸。
以下将详细介绍这些氨基酸的具体种类。
一、20种常见氨基酸1.丙氨酸(Ala):无极性,亲水性较强。
2.天冬酰胺(Asn):无极性,亲水性较强。
3.天冬酰胺酸(Asp):有极性,亲水性较强。
4.精氨酸(Arg):有极性,亲水性较强。
5.半胱氨酸(Cys):有极性,亲水性较强。
6.谷氨酰胺(Gln):无极性,亲水性较强。
7.谷氨酰胺酸(Glu):有极性,亲水性较强。
8.甘氨酸(Gly):无极性,亲水性较弱。
9.组氨酸(His):有极性,亲水性较弱。
10.异亮氨酸(Ile):无极性,亲水性较弱。
11.赖氨酸(Lys):有极性,亲水性较强。
12.亮氨酸(Leu):无极性,亲水性较弱。
13.脯氨酸(Pro):无极性,亲水性较弱。
14.丝氨酸(Ser):有极性,亲水性较强。
15.硫氨酸(Cys):有极性,亲水性较弱。
16.苏氨酸(Thr):有极性,亲水性较强。
17.色氨酸(Trp):有极性,亲水性较弱。
18.酪氨酸(Tyr):有极性,亲水性较弱。
19.缬氨酸(Val):无极性,亲水性较弱。
20.蛋氨酸(Met): 有极性, 亲油和亲水都很强。
二、2种罕见氨基酸1.5-羟色胺 (5-HTP) :一种天然的化学物质, 它是一种由色胺合成的前体物质。
它在体内被转化为5-羟色胺 (5-HT) , 这是一种神经递质, 能够对情绪、睡眠、食欲和疼痛敏感性等方面产生影响。
2.甲硫氨酸(Met):这种氨基酸是一种罕见的氨基酸,它在自然界中很少出现。
它是一种必需氨基酸,也是一种硫代谷氨酰胺的前体物质。
甲硫氨酸通常用于治疗肝脏疾病、慢性肾脏疾病和胆囊问题。
三、总结以上就是所有20种常见氨基酸和2种罕见氨基酸的具体种类。
每一种氨基酸都有其特殊的化学结构和生理功能,对于人体健康具有重要意义。
因此,在日常生活中,我们应该注重摄入各类氨基酸,以保持身体健康。
蛋白质的基本组成单位---氨基酸

第一章蛋白质第一节蛋白质的基本组成单位---氨基酸(一)氨基酸的种类蛋白质是重要的生物大分子,其组成单位是氨基酸。
组成蛋白质的氨基酸有20种,均为α-氨基酸。
每个氨基酸的α-碳上连接一个羧基,一个氨基,一个氢原子和一个侧链R 基团。
20种氨基酸结构的差别就在于它们的R基团结构的不同。
根据20种氨基酸侧链R基团的极性,可将其分为四大类:非极性R基氨基酸(8种);不带电荷的极性R基氨基酸(7种);带负电荷的R基氨基酸(2种);带正电荷的R基氨基酸(3种)。
(二)氨基酸的性质氨基酸是两性电解质。
由于氨基酸含有酸性的羧基和碱性的氨基,所以既是酸又是碱,是两性电解质。
有些氨基酸的侧链还含有可解离的基团,其带电状况取决于它们的pK值。
由于不同氨基酸所带的可解离基团不同,所以等电点不同。
除甘氨酸外,其它都有不对称碳原子,所以具有D-型和L-型2种构型,具有旋光性,天然蛋白质中存在的氨基酸都是L-型的。
酪氨酸、苯丙氨酸和色氨酸具有紫外吸收特性,在280nm处有最大吸收值,大多数蛋白质都具有这些氨基酸,所以蛋白质在280nm处也有特征吸收,这是紫外吸收法定量测定蛋白质的基础。
氨基酸的α-羧基和α-氨基具有化学反应性,另外,许多氨基酸的侧链还含有羟基、氨基、羧基等可解离基团,也具有化学反应性。
较重要的化学反应有:(1)茚三酮反应,除脯氨酸外,所有的α-氨基酸都能与茚三酮发生颜色反应,生成蓝紫色化合物,脯氨酸与茚三酮生成黄色化合物。
(2)Sanger反应,α-NH2与2,4-二硝基氟苯作用产生相应的DNB-氨基酸。
(3)Edman反应,α-NH2与苯异硫氰酸酯作用产生相应的氨基酸的苯氨基硫甲酰衍生物(PIT-氨基酸)。
Sanger反应和Edmen反应均可用于蛋白质多肽链N端氨基酸的测定。
氨基酸通过肽键相互连接而成的化合物称为肽,由2个氨基酸组成的肽称为二肽,由3个氨基酸组成的肽称为三肽,少于10个氨基酸肽称为寡肽,由10个以上氨基酸组成的肽称为多肽。
1氨基酸

甲硫氨酸(蛋氨酸)
O C OH
HN
Proline (Pro, P)
脯氨酸
2. 极性但不带电荷的R基氨基酸
这一组中有7种氨基酸 a.侧链的极性是由于它们的羟基造成的
苏氨酸 Thr 丝氨酸 Ser 酪氨酸 Tyr
b.R基极性是它们的酰胺基引起的 天冬酰胺Asn 谷氨酰胺Gln
c.由于含有巯基的缘故 半胱氨酸Cys
脯氨酸的化学结构式
H H2C C COOH H2C NH
C H2
脯氨酸为亚氨基酸
*在空间各原子有两种排列方式:L—构型
与D—构型,它们的关系就像左右手的关 系,互为镜像关系,下图以丙氨酸为例:
二十种氨基酸的名称和结构如图所示:
三、稀有氨基酸:
参加天然蛋白质分子组成的氨基酸,除 了上述20种有遗传密码的基本氨基酸 之外,在少数蛋白质分子中还有一些 不常见的氨基酸,称为稀有氨基酸。
以甘氨酸为例, 从左 向右是用NaOH滴定的 曲线,溶液的pH由小 到大逐渐升高;从右向 左是用HCL滴定的曲线, 溶液的pH由大到小逐 渐降低。曲线中从左向 右第一个拐点是氨基酸 羧基解离50%的状态, 第二个拐点是氨基酸的 等电点,第三个拐点是 氨基酸氨基解离50%的 状态。
参考
通过氨基酸的滴定曲线,可用下列Henderson— Hasselbalch方程求出各解离基团的解离常数(pK,)
O H2N CH C OH
CH2 CO O-
Aspartate (Asp, D)
天门冬氨酸
O
H2N CH C OH CH2 CH2 CO O-
Glutamate (Glu, E)
谷氨酸
4.带正电荷的R基氨基酸 这一类氨基酸在pH=7时携带净正电
20种氨基酸

20种氨基酸的种类名称及它的功能已知基本氨基酸有二十个品种,其中赖氨酸、苏氨酸、亮氨酸、异亮氨酸、缬氨酸、蛋氨酸、色氨酸、苯丙氨酸8种氨基酸,人体不能自己制造,我们称之为必须氨基酸,需要由食物提供。
此外,人体合成精氨酸、组氨酸的力不足于满足自身的需要,需要从食物中摄取一部分,我们称之为半必须氨基酸。
其余的十种氨基酸人体能够自己制造,我们称之为非必须氨基酸。
氨基酸是蛋白质的基本组成单位,大约有200多种,但在动物的营养中起重要作用而且被人们广泛认识的只有20多种,称之为标准氨基酸。
根据动物对氨基酸的营养需要通常分为必需氨基酸和非必需氨基酸两大类,必需氨基酸是指在标准氨基酸中,动物体不能自身合成,或者合成的速度或数量不能满足动物正常生长的需要,必须由饲料提供的一类氨基酸。
非必需氨基酸并不是可要可不要的氨基酸,而是动物体可以自身合成或者需要量较少的一类氨基酸。
必需氨基酸中需要在饲料中补充量最多的称为第一限制性氨基酸,补充量排在后面的称为第二限制氨基酸。
氨基酸对人体的作用一.甘氨酸(GLY)1、降低血液中的胆固醇浓度,防治高血压2、降低血液中的血糖值,防治糖尿病3、能防治血凝、血栓4、提高肌肉活力,防止胃酸过多5、甜味为砂糖的0.8倍,对人体有补益等营养作用二.亮氨酸(LEU)1、降低血液中的血糖值,对治疗头晕有作用2、促进皮肤、伤口及骨头有愈合作用3、如果缺乏时,会停止生长,体重减轻三.蛋氨酸(MET)1、参与胆碱的合成,具有去脂的功能,防治动脉硬化高血脂症2、有提高肌肉活力的功能3、促进皮肤蛋白质和胰岛素的合??四.酪氨酸(TYR)1、造肾上腺激素、甲状腺激素和黑色素的必需氨基酸2、可防治老年痴呆症3、促进新陈代谢,增进食欲4、对治疗胃溃疡等慢性疾病、神经性炎症及发育不良等效果5、与色素形成有关系,缺乏时会利白化症五.组氨酸(HIS)1、参与血球蛋白合成,促进血液生成2、产生组氨、促进血管扩张,增加血管壁的渗透性3、医治胃病、十二指肠等有特效4、促进腺体分泌,对过敏性疫病有效果5、可治疗消化性溃疡、发育不良等症状6、对治疗心功能不全、心绞痛、降低血压、哮喘及类风湿关节炎有效果六.苏氨酸(THR)人体必需,缺乏时会使人消瘦,甚至死亡七.丙氨酸(ALA)1、能促进血液中酒精的代谢(分解)作用增强肝功能,有保肝护肝作用2、甜味为砂糖的1.2倍八.异亮氨酸(ILE)1、能维持机体平衡,治疗精神障碍2、有促进食欲的增加和抗贫血的作用3、如果缺乏时,会出现体力衰竭,昏迷等症状九.色氨酸(TRY)1、促进血红蛋白的合成2、防治癞皮病3、促进生长,增加食欲4、甜味为砂糖的35倍,配制生产的低塘食物等对糖尿病、肥胖病人食用较好十.胱氨酸(CYS)1、有治疗脂肪肝和解毒效果2、治疗皮肤的损伤,对病后、产后脱发有疗效十一.赖氨酸(LYB)1、参与结缔组织、微血管上皮细胞间质的形成,并保持正常的渗透性2、可增加食欲,促进胃蛋白酶的分泌,增强免疫能力,改善发育迟缓,防止蛀牙,促进儿童生长3、提高钙的吸收,促进骨骼生长4、如果缺乏,会降低人的敏感性,妇女会停经,出现贫血、头晕、头昏和恶心等病状十二.天门冬氨酸(ASP)1、降代血氨,对肝有保护作用2、对肌肉有保护作用,可治疗心绞痛,对心肌梗塞等有防治效果3、增加鲜味,促进食欲十三.缬氨酸(VAL)1、促使神经系统功能正常2、如果缺乏时,会造成触觉敏感度特别提高,肌肉的共济运动失调3、可作为肝昏迷的治疗药物十四.苯丙氨酸(PHE)在机体内转变为酪氨酸,促进甲状腺素和肾和肾上腺素的合成十五.脯氨酸(PRO)对高血压有疗效作用十六.丝氨酸(SER)1、降低血液中的胆固醇浓度,防治高血压2、是脑等组织中的丝氨酸磷脂的组成部分3、结核细菌病有效果,可治疗肺病十七.谷氨酸(GLU)1、降低血氨,有解氨毒的作用2、参与脑的蛋白和塘代谢,促进氧化,改善中枢神经活动,有维持和促进脑细胞功能的作用,促进智力的增加3、对严重肝功能不全,肝昏迷,酸中毒,癫痫精神分裂症、神经衰弱等有治疗效果4、对治疗胃溃疡、胃液缺乏、消化不良、食欲不振有效果5、保护皮肤湿润,防治干裂,如配制的洗涤剂、化妆品,对皮肤、粘膜元刺激,适于幼儿及皮肤病患者使用十八.精氨酸(ARG)1、降低血氨,促进体中尿素生成,治疗肝昏迷等2、增加肌肉活力,保持性功能,对治疗精子减少症有作用。
有机化学氨基酸、多肽、蛋白质

6 种异构体 24种异构体
许多种氨基酸按照不同的排列顺序, 构成了自 然界中种类繁多的多肽和蛋白质。
命名多肽时以C-末端的氨基酸残基为母体, 由 N-端叫起, 依次称为某氨酰(基)某氨酸。
O
O
O
H2N CHC NH CH2C NH CHC OH
N-端
CH3
CH2
C-端
丙氨酸残基 甘氨酸残基 苯丙氨酸残基
利用蛋白质分子胶体颗粒大不能透过半透膜 的性质可将蛋白质分离提纯,这种方法称为透析 法(dialysis)。
(三)蛋白质的沉淀和变性
调节蛋白质溶液的pH值至等电点, 再加入适当的脱水剂除去蛋白质分子表 面的水化膜, 可使蛋白质分子聚集而从溶液中沉淀析出。
根据生成紫色化合物颜色的深浅程度,或根据放出
CO2气体的体积,可对 α-氨基酸 进行定量分析。 也常用于层析实验中氨基酸的显色。
第二节 肽肽ຫໍສະໝຸດ 氨基酸残基之间彼此通过酰胺键 (肽键)连 接而成的一类化合物。其通式为:
RO
R’ O
H2N C-C-OH + H N C-C-OH
H
HH
A氨m基ino酸acid
第十四章 氨基酸、蛋白质
第一节 氨基酸
一、氨基酸的分类、命名和构型
氨基酸的结构特点
①都是α-氨基酸(脯氨酸是
α–亚氨基酸); H N
COOH H
R CH COO- 内盐
NH3+
偶极离子
②除甘氨酸外,都是L-氨基酸(左旋);
③各氨基酸侧链R基团不同,氨基酸结构和性质有差异
1、分类
据化学结构:
任何一种蛋白质分子在天然状态下均具有独特 而稳定的构象,这是蛋白质分子在结构上最显著的 特点。为了表示蛋白质分子不同层次的结构,常将 蛋白质分子结构分为一级、二级、三级和四级。一 级结构又称为初级结构或基本结构,二级结构以上 属于构象范畴,称为高级结构。
2021年高中生物 2.2 生命活动的主要承担者 蛋白质知识归纳 新人教版必修1

2021年高中生物 2.2 生命活动的主要承担者蛋白质知识归纳新人教版必修1知识·巧学·升华一、氨基酸及其种类氨基酸是组成蛋白质的基本单位。
对于组成蛋白质的氨基酸必须是至少含有一个氨基和羧基,并且都有一个氨基和羧基连在一个碳原子上。
不同的氨基酸具有不同的R基,组成蛋白质的20种氨基酸的区别在于R基的不同。
如:这20种氨基酸根据人体细胞能否合成划分为两大类,一类是人体细胞不能合成的,必须从外界环境中直接获取的(主要从饮食获得),这些氨基酸叫必需氨基酸,共8种(婴儿有9种),它们是:赖氨酸、色氨酸、苯丙氨酸、亮氨酸、异亮氨酸、苏氨酸、甲硫氨酸、缬氨酸、(组氨酸)。
另一类是人体细胞能够合成的,实用文档叫非必需氨基酸,共12种,它们是:甘氨酸、丙氨酸、天冬氨酸、谷氨酸、半胱氨酸、酪氨酸、精氨酸、脯氨酸、组氨酸、谷氨酰胺、天冬酰胺、丝氨酸。
知识拓展动物蛋白食品要比植物蛋白食品营养价值更高。
因为动物蛋白含的氨基酸种类要比植物蛋白丰富。
另外,动物蛋白所含各种必需氨基酸的比例比植物蛋白更接近人体必需氨基酸的比例。
二、蛋白质的结构及其多样性1.氨基酸分子互相结合的方式是:脱水缩合。
)相连接,一个氨基酸分子的羧基(—COOH)和另一个氨基酸分子的氨基(—NH2同时脱去一分子的水,这种结合方式叫做脱水缩合。
连结两个氨基酸分子的化学键叫做肽键。
肽键的结构为:—NH—CO—(或者)方法点拨关于蛋白质的计算问题,记住下面两个算式即可:(1)肽键数=失水数=氨基酸数-肽链数;(2)蛋白质分子量=氨基酸数×氨基酸平均分子量-18×失水数。
也可以参照下表:实用文档氨基酸数肽键数脱去水分子数氨基数羧基数一条肽链n n-1n-1至少1个至少1个m条肽链n n-m n-m至少m个至少m个在计算多肽分子中含有的氨基和羧基数目时,需要把R基中的氨基和羧基的数目加上。
蛋白质相对分子量的计算公式:n·a-(n-m)·18(其中n为氨基酸总数,a为氨基酸的平均相对分子质量,m 为肽链数)2.蛋白质的结构具有多样性,其原因包括三方面:(1)氨基酸的数目不同:一般蛋白质都含有20种氨基酸,但每种氨基酸的数目是不一样的。
氨基酸及其相关计算
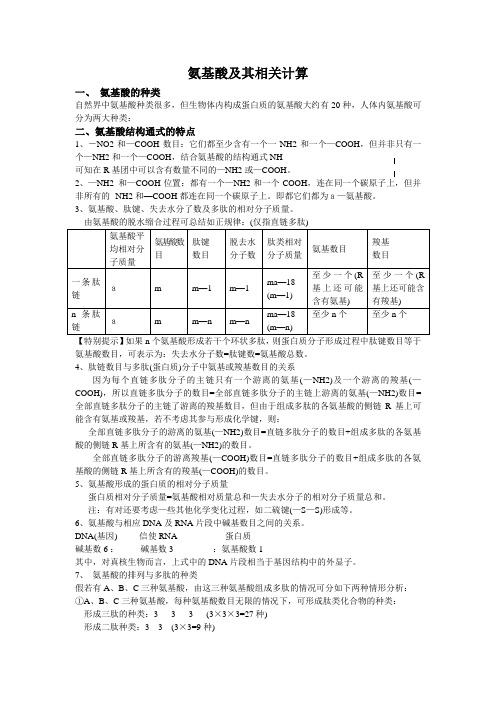
氨基酸及其相关计算一、氨基酸的种类自然界中氨基酸种类很多,但生物体内构成蛋白质的氨基酸大约有20种,人体内氨基酸可分为两大种类:二、氨基酸结构通式的特点1、-NO2和—COOH数目:它们都至少含有一个一NH2和一个—COOH,但并非只有一个—NH2和一个—COOH,结合氨基酸的结构通式NH可知在R基团中可以含有数量不同的—NH2或—COOH。
2、—NH2 和—COOH位置:都有一个—NH2和一个-COOH,连在同一个碳原子上,但并非所有的--NH2和—COOH都连在同一个碳原子上。
即都它们都为a—氨基酸。
3、氨基酸、肽键、失去水分了数及多肽的相对分子质量。
【特别提示】如果n个氨基酸形成若干个环状多肽,则蛋白质分子形成过程中肽键数目等于氨基酸数目,可表示为:失去水分子数=肽键数=氨基酸总数。
4、肽链数目与多肽(蛋白质)分子中氨基或羧基数目的关系因为每个直链多肽分子的主链只有一个游离的氨基(—NH2)及一个游离的羧基(—COOH),所以直链多肽分子的数目=全部直链多肽分子的主链上游离的氨基(—NH2)数目=全部直链多肽分子的主链了游离的羧基数目,但由于组成多肽的各氨基酸的侧链R基上可能含有氨基或羧基,若不考虑其参与形成化学键,则:全部直链多肽分子的游离的氨基(—NH2)数目=直链多肽分子的数目+组成多肽的各氨基酸的侧链R基上所含有的氨基(—NH2)的数目。
全部直链多肽分子的游离羧基(—COOH)数目=直链多肽分子的数目+组成多肽的各氨基酸的侧链R基上所含有的羧基(—COOH)的数目。
5、氨基酸形成的蛋白质的相对分子质量蛋白质相对分子质量=氨基酸相对质量总和—失去水分子的相对分子质量总和。
注:有对还要考虑—些其他化学变化过程,如二硫键(—S—S)形成等。
6、氨基酸与相应DNA及RNA片段中碱基数目之间的关系。
DNA(基因) 信使RNA 蛋白质碱基数6 :碱基数3 :氨基酸数1其中,对真核生物而言,上式中的DNA片段相当于基因结构中的外显子。
2020-2021学年高一生物人教版必修1:第2章 第2节 生命活动的主要承担者——蛋白质

要承担者。
式。
自主 预习 探新 知
一、氨基酸及其种类 1.种类:组成蛋白质的氨基酸大约有 20 种
2.结构
(1)写出图中结构名称 a.氨基;b、d. R基;c.羧基。
(2)比较图中两种氨基酸,写出氨基酸分子的结构通式:
。 (3)氨基酸的结构特点 ①数量关系:至少都含有 一个氨基和 一个羧基。 ②位置关系:都有 一个氨基和一个羧基 连接在同一碳原子上。 ③各种氨基酸之间的区别在于 R基 的不同。
,那么 10 个
氨基酸(同学)形成一条肽链时,脱掉几个水分子?形成几个肽键?
提示:肽键数=失去的水分子数=10-1=9。 (2)若 n 个氨基酸形成 m 条肽链呢?
提示:肽键数=失去水分子数=n-m。
(3)试总结形成肽键数与氨基酸数和肽链条数的关系。
提示:肽键数=失去水分子数=氨基酸数-肽链条数。
4.(1)一条肽链中至少含有多少个游离的—NH2 和—COOH?若 m 条肽链呢?为什么是至少?
质。
()
6.高温会使蛋白质的肽键断裂。
()
7.蛋白质的空间结构破坏后,功能不变。
()
提示:1.× 必需氨基酸是指人体不能合成,必须从外界环境 中直接吸收的氨基酸。
2.√ 3.× 每种氨基酸至少含有一个氨基和一个羧基。 4.× 书写格式应为—NH2,—COOH,—R。
5.× 空间结构不同,蛋白质的结构不同。 6.× 高温破坏蛋白质的空间结构,不破坏肽键。 7.× 蛋白质的空间结构破坏后,功能丧失。
1.关于人体氨基酸的叙述,正确的是( ) A.人体内所有蛋白质都由20种氨基酸构成 B.只要含有氨基和羧基的分子就是组成人体蛋白质的氨基酸 C.不同氨基酸的R基一定不同 D.非必需氨基酸不能在人体中合成
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高二生物学案5 生命活动的主要承担者蛋白质班级姓名
1.写出氨基结构式羧基结构式
酸的R基是半胱氨酸R基是。
(注:
羧基的书写都要有一个游离键)
2.一个氨基酸中是否都只含有一个氨基和一个羧基(二)蛋白质的结构及多样性
1.写出从氨基酸到蛋白质的结构层次。
2. 空间结构:一条或多条肽链通过一定的互
(1)二肽是由两个氨基酸脱水缩合而成,含有
键。
[中卫市第一中学李维宁] [第1 页共2 页] [2019/9/3]
检测题
3、3、2 B.1、2、 C.1、3、2 D.
高二生物学案5 生命活动的主要承担者蛋白质班级姓名[中卫市第一中学李维宁] [第3 页共2 页] [2019/9/3]。
