北京市高中学生高一高二化学竞赛考试及答案
北京市高二化学竞赛试卷及答案

阳离子膜甲乙2013年北京市高中学生化学竞赛试卷(高中二年级)题中可能用到的相对原子质量为:第1题 选择题(12分)(单选或多选,每选2分,错一对一不得分)(1)Na 2SO 3⋅7H 20晶体加热脱水后,强热过程中质量不变。
待固体冷却后溶于水,溶液的碱性比Na 2SO 3 溶液强,所得固体成分可能是( )A .Na 2S Na 2O Na 2SO 3B .Na 2SO 4 Na 2O Na 2SO 3C .Na 2O Na 2S Na 2SO 4D .Na 2S Na 2SO 4 Na 2SO 3(2)右图是一种蓄电池的示意图,被膜隔开的电解质分别为Na 2S 2和NaBr 3。
放电后变为Na 2S 4和NaBr 下面对该装置工作过程中叙述正确的是( ) A .放电过程,甲电极电极反应:2S 22-–2e -= S 42-B .放电过程,电池反应:2S 22-+ Br 3-= S 42-+ 3Br —C .充电过程,阳极室流出NaBr 3溶液D .充电后向阳极室补充Na 2S 4溶液 (3)已知K SP (FeS)=6。
3×10-18, K SP (CuS )=6。
3×10-36,K 1 K 2 (H 2S )=1。
3×10-20。
向0.10mol ⋅L-1Fe 2+ 和0。
10mol ⋅L-1Cu 2+ 的混合溶液中通入H 2S 气体至饱和(c (H 2S ) 0.10mol ⋅L-1).请推断沉淀生成情况是下列哪一种( ) A .先生成CuS 沉淀,后生成FeS 沉淀 B .先生成FeS 沉淀,后生成CuS 沉淀 C .先生成CuS 沉淀,不生成FeS 沉淀D .先生成CuS 沉淀,反应一段时间FeS 和CuS 同时沉淀(4)下面是有关氢硫酸(H 2S 水溶液):①蒸馏水中通入H 2S 至饱和,敞口存放两天,明显失效,但无沉淀;若密闭保存一个月,既不浑浊,也不失效。
高二化学竞赛试题及答案

北京市高中学生化学竞赛试卷(高中二年级)·竞赛时间2小时。
迟到超过30分钟者不得进场。
开赛后1小时内不得离场。
时间到,把试卷纸(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在试卷指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色笔或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
题中可能用到的相对原子质量为:第1题选择题(12分)(多选,每选1.5分)(1)实验室配制SnCl2溶液,必须先用盐酸溶解SnCl2,才能配成澄清溶液,若用这种固体直接溶于水得不到澄清的溶液,用盐酸的目的是()A.利用同离子效应B.缓冲溶液C.抑制盐的水解D.发生氧化还原反应(2)定量分析中可用AgNO3溶液滴定Cl-溶液,加入K2CrO4为指示剂,达到滴定终点时溶液体积为50mL,[Cl-] = 10-5 mol·L-1,AgNO3与CrO42-生成砖红色的Ag2CrO4沉淀。
已知K sp(AgCl) = 1.77×10-10,K sp(AgI)= 8.51×10-17,K sp(Ag2CrO4) = 1.12×10-12下列实验操作正确的是()A.滴定开始时应向含Cl-的溶液中滴加0.1mol/L的K2CrO4溶液4.00mLB.滴定终点时,溶液中CrO42-的浓度约为3.6×10-3 mol·L-1C.滴定开始时,若向试液滴加的K2CrO4溶液超过4.00mL,测定出的Cl-浓度小于实际浓度D.可用0.1 mol·L-1的KI溶液代替K2CrO4做指示(3)向蓝色的CuSO4溶液逐滴加氨水,首先生成蓝色沉淀,而后沉淀溶解成深蓝色溶液;向深蓝色溶液中通入SO2气体,生成白色沉淀;将白色沉淀加入到热的10M/L浓硫酸中,生成红色粉末和SO2气体。
03北京高一化学竞赛试卷及答案

C. S2C 2和NaOH水溶液反口, 氧化与口原口物物口的量之比
D. 13.5gS2Cl 2和NaOH反口口子口移数口
0.1NA
(6)海水中主要含有
Nat、K*、
Mg²*、Ca2*、CI、
1:1 1:1
Br、 SO、HCO 3、
CO3等离子,
排放的烟气可用海水脱硫,其工口流程如下口所示:
含SO2的
H、O的原子数,所以无法
得到口一的原子量。 Cannizzaro根据Avogadro的口点:
“同温度、同口口下,同体口气体中含有相同数的分子”
解决了口定
原子量的口口。 已知A、B、C、D四种化合物中均含有 的数据口算X的原子量(分子中元素原子数只能是整数)
气体口量(g/L)
N2
0.652
A 0.849
(1)
N2O3,写出两种;
(2)NO3F,写出一种
第9口(
10分)
有一口化合物,
AS4. C6H 6, CaH:他口的特征是分子中的每个
或三个C原子形成化学口,口些原子称骨架原子。
(1) 口分口□出以上分子构型的示意口。
(H可不画)
As,或C原子都分口同其他的三个
As,
(2)口分口指出口一口骨架上原子各自的价口子口数。
(2分)
第10口(13分)
(1)
2H202H3O2*+HO2
(2分)
(2) B中的MnO 2作氧化口, 可将口氧化口中的
而A中的口氧化口口生歧化反口,只有一半
故B中放出气体是
A中2倍
-1价氧全部氧化口氧气;
-1价氧被氧化口氧气,
MnO 2+H2O 2+H2SO 4=Mn SO 4+O 2+2H2O
北京高一化学竞赛试卷及答案

北京市高中学生化学竞赛试卷(高中一年级)·竞赛时间2小时。
迟到超过30分钟者不得进场。
开赛后1小时内不得离场。
时间到,把试卷(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在试卷指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
第1题选择题(16分)(每选2分,多选,对一错一不得分,无负分)(1)荧光棒发光的原理是利用H2O2氧化草酸酯产生能量,该能量传递给荧光物质而发光。
草酸酯是一种粘稠度较高的有机化合物。
下列说法不正确...的是()A.荧光棒发光,凑近可燃性气体,会导致气体燃烧B.当荧光棒亮度减弱时,敲打荧光棒亮度可能增强C.荧光棒放入冷冻室亮度可能减弱甚至消失D.荧光棒发光是化学能转化为热能,热能转化为光能(2)碘可能呈金属性,下列事实能说明这一事实的是()A.已经制得I(NO3)3、I(ClO4)3 2H2O等含I3+ 的化合物B.已经制得IBr、ICl 等卤素互化物C.碘易溶于KI溶液形成I3-D.I4O9 可以看成是碘酸盐(3)能正确表示下列反应的离子方程式为()A.向碳酸氢镁溶液中滴加少量石灰水:Mg2+ +2HCO3-+2Ca2+ +4OH-=Mg(OH)2↓+2CaCO3↓+ H2OB.在强碱溶液中,次氯酸钠与氢氧化铁反应生成Na2FeO4:3ClO-+ 2Fe(OH)3 = 2FeO42-+3Cl-+ H2O + 4H+C.向NaAIO2溶液中通入过量的CO2制取AI(OH)3AIO2-+ CO2 + 2H2O = AI(OH)3↓+ HCO3-D.漂白粉[主要成分Ca(ClO)2,Ca(OH)2]在空气中失效:ClO-+ CO2 + H2O = HClO + HCO3-(4)主族元素M和N,M位于短周期,且M2-和N+ 的电子数之差为8,则下列说法正确的是()A.M和N的原子序数之差为11B.M和N的原子序数之和为11C.M和N的最外层电子数之和为8D.M和N的最外层电子数之差为8(5)将Cl2通入熔融的硫磺制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊;S2Cl2与NaOH 溶液反应得到澄清溶液。
北京化学竞赛试题及答案高二
2010年北京市高中学生化学竞赛试卷(高中二年级)·竞赛时间2小时。
迟到超过30分钟者不得进场。
开赛后1小时内不得离场。
时间到,把试卷纸(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在试卷指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色笔或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
第1题选择题(16分)(单选或多选,多选题只答一个或对一错一只扣错答案分)(1)下列现象或应用,不能用胶体知识解释的是()A.肾功能衰竭等疾病的血液中毒,可利用血液透析进行治疗B.可用FeCl3溶液对皮肤小划伤进行应急止血C.氯化铝溶液中加入过量小苏打溶液产生白色沉淀和气体D.水泥、冶金厂常用高压电除去工厂烟尘,减少对空气污染(2)下列溶液中各种微粒的物质的量浓度大小顺序正确的是()A.室温下,向0.01mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性c(Na+)>c(SO42-)>c(NH4+)>c(OH-)= c(H+)B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3)C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)D.0.1mol·L-1的NaHA溶液,其pH=4: c(HA-)>c(H+)>c(H2A)>c(A2-)(3)砷(As)在元素周期表中位于V A族,且As2S3与As2O3均具有还原性,Na2S2与Na2O2均具有氧化性。
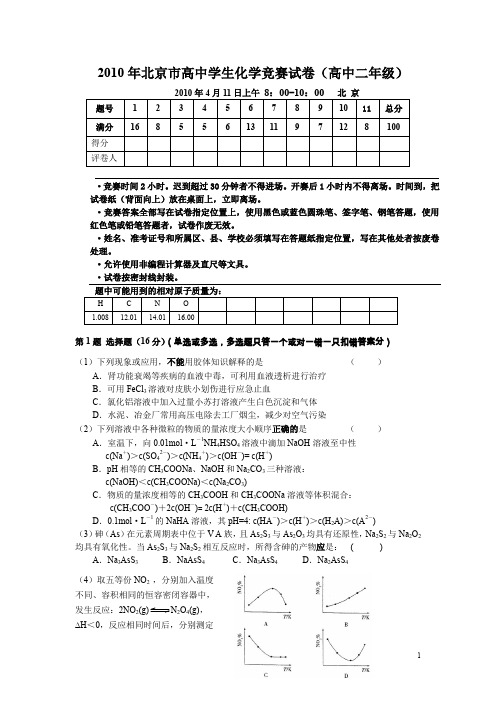
当As2S3与Na2S2相互反应时,所得含砷的产物应是:( ) A.Na3AsS3B.NaAsS4C.Na3AsS4D.Na2AsS4(4)取五等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) N2O4(g),H<0,反应相同时间后,分别测定体系中NO 2的体积分数(NO 2%),并 作随反应温度(T )变化的关系图。
2023年北京高中化学奥林匹克竞赛预赛试题真题(含答案)

2023年高中化学奥林匹克北京地区预选赛试题(2023年4月15日上午8:30–11:30)·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
·竞赛时间3小时。
迟到超过30分钟者不得进场。
开赛后1小时内不得离场。
考试结束后,把试卷(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在答题纸指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色笔或铅笔答题者,试卷作废无效。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
可能用到的元素相对原子质量R = 8.314 J·mol–1·K– 1;温度T(K)= 273.15 + t(℃);F = 96485 C·mol–1;N A= 6.022 × 1023 mol–1第1题选择题(40分)(单选,每题5分)(1)皮蛋是我国独特的传统美食,营养价值高。
传统的腌料配方含生石灰、纯碱、PbO、茶叶、食盐等。
现代食品工业通过研究各成分功能,以人体必需的重金属Zn和Cu代替Pb,成功研制出“无铅皮蛋”。
Pb(OH)-,该离子扩散到蛋壳和蛋膜时,逐渐生成碳酸盐或硫化传统腌料中的PbO能溶于强碱生成24物沉淀,堵塞孔道,从而控制OH–的渗入以达到合适的“成熟度”。
“无铅皮蛋”的腌料将PbO改为ZnSO4和CuSO4,达到同样的效果。
下列说法错误的是A.腌料配制成糊状物时发生反应:CaO +H2O =Ca(OH)2;Ca(OH)2+ Na2CO3=2NaOH+CaCO3 B.蛋膜是一种半透膜,允许离子和小分子通过C.腌制过程中,使蛋白质变性的主要物质是NaOHD.腌制“无铅皮蛋”时,Zn2+和Cu2+直接扩散到蛋膜上形成难溶物(2)某无色溶液....进行如下实验,所得结论正确的是A.滴加NaOH溶液,将湿润红色石蕊试纸置于试管口不变蓝,则原溶液中一定无NH+4 B.洁净铂丝蘸取溶液进行焰色试验,火焰呈黄色,则原溶液中一定有Na+,无K+C.滴加盐酸酸化的BaCl2溶液,有白色沉淀产生,则原溶液中一定含2SO-4D.滴加氯水和CCl4,振荡,静置,下层溶液显紫色,则原溶液中一定含I-(3)已知:反应Ⅰ:N2(g) + 3H2(g)2NH3(g)ΔH1 = a kJ·mol–1反应Ⅱ:C3H8(g)CH2=CHCH3(g) + H2(g)ΔH2 = + 125 kJ·mol–1下列说法不.正确..的是A.NH3中的N与C3H8中的C杂化轨道均为sp3B.反应Ⅰ中a = 92C.反应Ⅱ升高温度可促进反应进行D.通过反应Ⅱ可以计算生成1 mol碳碳π键放出能量271 kJ(4)利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl3·6H2O,主要步骤:用H2O2氧化废蚀刻液、制备氨气、制备碱性蚀刻液[CuCl2 + 4NH3= Cu(NH3)4Cl2]、固液分离、用盐酸溶解沉淀并制备FeCl3·6H2O。
北京高一化学竞赛试题及答案
2Na NH 3 === 2NaNH 2 HCaO 2NH 4Cl === CaCl 22NH H 2O3Mg(NH 2)2 === Mg 3N 2 4NH NH 4Cl NaNH 2 === NaCl 2NH 北京市高中学生化学竞赛试卷(高中一年级)·竞赛时间2小时。
迟到超过30分钟者不得进场。
开赛后1小时内不得离场。
时间到,把试卷(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在试卷指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色笔或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
第1题 选择题( 30 分)(单选或多选,每选5分。
)(1)下列说法正确的是: ( )A .相同质量的热水比冷水含有更多的热量B .化学反应限度大,该反应的速率也大C .在相同条件下,分子破裂为原子所吸收的能量与相应原子结合成分子所放出的能量数值相同D .化石燃料的开采与使用,有利于节能减排与保护环境(2)秤取160 g CuSO 4(160 g/mol )250 g CuSO 4·5H 2O(250 g/mol)分别溶于水时,前者释热66 kJ/mol ,后者吸热11 kJ/mol 。
则CuSO 4(s ) + 5H 2O(l ) = CuSO 4·5H 2O (s ) 的热效应是( )A .释热77 kJ/molB .释热55 kJ/molC .吸热77 kJ/molD .吸热55 kJ/mol(3)从某些性质看,NH 3和H 2O ,NH 4+和H 3O +,OH -和NH 2-,N 3-和O 2-两两相当,据此判断下列反应方程式正确的是 ( ) ① ②③④ A .仅①正确 B .②④正确 C .全部正确 D .正确①②④(4)NaH 是离子化合物,与H 2O 反应,有气体生成,现有NaH 与Al 粉的混合物m g 投入足量水中,全部溶解,生成n g H 2。
北京市年高二化学竞赛组试题新人教版
年北京市高中学生化学竞赛试题(高中二年级)题号 1 2 3 4 5 6 7 8 9 10 11 总分满分7 7 9 9 6 7 5 8 8 17 17 100得分评卷人·竞赛时间2小时。
迟到超过30分钟者不得进场。
1小时内不得离场。
时间到,把答题纸及试题纸(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在答题纸上,使用黑色或蓝色圆珠笔、签字笔或钢笔答题,使用红色或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸上方指定位置,写在他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·答题纸按密封线封装。
H C N O Na F S Fe Cu Cl Si1.008 12.01 14.01 16.00 22.99 19.00 32.07 55.85 63.55 35.45 28.09第一题单选或多选题(共7分)(选对一个答案得1分,多选一个错误答案扣0.5分)1.在抢救大出血的危症病人时,常需静脉点滴以0.9%的氯化钠溶液(俗称“生理盐水”),这是由于人体血液的“矿化度”(即无机盐的含量)为0.9%。
另有研究表明,30亿年前地表原始海水的矿化度即为0.9%。
对此下列猜测或评论不足取的是B。
A) 人类的祖先可能是从原始海洋中逐渐进化到陆地上的B) 人类血液和原始海水矿化度均为0.9%纯属巧合C) 人类血液和原始海水之间存在着某些尚未认识的关系D) 人类血液仍然带有原始海水的某些印记2.某溶液中含有NO3-、SiO32-、AlO2-、S2-等四种离子,若向其中加入过量的盐酸溶液,微热并搅拌,再加入过量的NaOH溶液,则溶液中大量减少的阴离子是 A & D。
A)NO3-B)SiO32-C)AlO2-D)S2-3.A、B为短周期元素,A原子所具有的电子层数是最外层电子数的1/2,B原子次外层电子数是最外层电子数的1/3,A与B能形成多种原子团,其中一定不存在的是D。
2024版高中化学竞赛专区试卷答案
3
关注实际问题
由于试卷中多道题目结合实际问题,学生 需要关注生产、生活等实际问题中的化学 知识应用。可以通过阅读相关书籍、资料 等方式,拓宽视野,增强对实际问题的理 解和分析能力。
2024/1/28
27
下一阶段备考重点提示
要点一
深入理解化学反应原 理
化学反应原理是高中化学的核心内容之 一,也是竞赛考查的重点。学生需要深 入理解化学反应的基本原理、影响因素 等,并能够运用相关知识分析和解决实 际问题。
2024/1/28
11
填空题答案及解析
1. 【答案】
(1) 氢键;
(2) $sp^{3}$;
2024/1/28
12
填空题答案及解析
1
(3) 极性共价键(或共价键);
2
【解析】
2024/1/28
3
(1)电负性较大的$N$、$O$、$F$元素, 能与$H$形成共价键,且分子之间存在 氢键,所以比同周期的其他元素形成的 氢化物沸点高;故答案为:氢键;电负 性较大的$N$、$O$、$F$元素,能与 $H$形成共价键,且分子之间存在氢键, 所以比同周期的其他元素形成的氢化物 沸点高;
2024/1/28
28
感谢您的观看
THANKS
2024/1/28
29
整体难度与往年竞赛试卷相当,符合高中化学竞 赛的选拔要求。
高中化学的主要知识点,包括化学反应原理、物质结构与性质、 有机化学基础、化学实验基础等。
试题注重知识点的综合运用,要求学生能够灵活运用所学知识解决实际问 题。
部分题目涉及了高中化学的拓展知识点,考查了学生的知识广度和深度。
要点二
掌握物质结构与性质
物质结构与性质是高中化学的重要内容 之一,也是竞赛考查的热点。学生需要 掌握常见物质的组成、结构、性质等, 并能够运用相关知识解释和预测物质的 性质和行为。
最新-2018年北京市化学竞赛高二组试题及答案003 精品
A B 2018年北京市高中学生化学竞赛试卷(高中二年级)·竞赛时间2.5小时。
迟到超过30分钟者不得进场。
开赛后1小时内不得离场。
时间到,把试卷纸(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在试卷指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
第一题 单选题(共10 分)(每一个答案得 2 分)1. 下列有关实验现象叙述正确的是 A 。
A . Cu 跟浓HNO 3反应后溶液呈绿色 B . Cu 溶于热、浓H 2SO 4后溶液呈蓝色 C . Na 2SO 4溶液可使苯酚的乳浊液变得澄清 D . Mg 跟盐酸反应放出H 2的速率持续减慢2. 常温下,在溶液中可发生以下反应:①16H + + 10Z -+ 2XO 4-== 2X 2+ + 5Z 2 + 8H 2O ,②2M 2+ + R 2 == 2M 3+ + 2R -,③2 R - + Z 2 == R 2 + 2Z -,由此判断下列说法错误的是 C 。
A . 常温下反应2M 2+ + Z 2 == 2M 3+ + 2Z -可以自发进行 B . Z 元素在反应①中被氧化,在③中被还原C . 氧化性强弱顺序为: XO 4-< Z 2 < R 2 < M 3+D . 还原性强弱顺序为: X 2+ < Z - < R -< M 2+3.以多孔铂为电极,在右图装置中分别在两极区通入CH 3OH 和O 2,发生反应产生电流,经测定,电流方向由b 到a ,下列叙述中正确的是 C 。
A . A 处通入O 2B . 溶液中的阳离子向a 极运动C . 负极的电极反应为:2CH 3OH + 16OH -12e -== 2 CO 32-+ 12H 2O D . 总反应的化学方程式为:2CH 3OH + 3O 2 == 2 CO 2 + 4H 2O4. 某二元酸(H 2A )在水中的电离式为:H 2A == H + + HA -,HA-H+ + A2-,则下列说法正确的是B。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
———————————————————————————————— 作者:
———————————————————————————————— 日期:
ﻩ
2013年北京市高中学生化学竞赛试卷
(高中一年级)
2013年4月14日下午14:00-16:00北京
题号
1
2
3
4ห้องสมุดไป่ตู้
5
A.S2Cl2的结构简式:Cl-S-S-Cl
B.S2Cl2和水反应中,氧化剂还原剂物质的量之比为1:1
C.S2Cl2和NaOH水溶液反应,氧化与还原产物物质的量之比为1:1
D.13.5gS2Cl2和NaOH反应电子转移数为0.1NA
(6)海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示:
有关数据见下表:
Ca(OH)2
Ba(OH)2
CaCO3
BaCO3
溶解度g/100gH2O,25℃
0.165
3.89
0.0002
0.00022
选用哪种饱和液?主要理由是:
第5题(8分)
活泼金属K、Na、Mg都能和CO2反应,但产物不同。请写出下列两个反应方程式并标明得失电子数。
(1)Na和CO2生成Na2CO3。
第4题(7分)
(1)用NaOH(aq)、KOH(aq)吸收CO2。有关数据见下表:
NaOH
KOH
NaHCO3
KHCO3
溶解度 g/100gH2O,20℃
109
112
9.6
33.2
选用哪种试剂(aq)更有效?主要理由是:
(2)用饱和Ca(OH)2、Ba(OH)2溶液检验CO2:
M(OH)2+ CO2=MCO3+H2O
(H2O+H2OH3O++OH-)请写出在液NH3中发生中和反应的离
子方程式。
金属在液NH3中的活动顺序,大体上和金属在水中活动序相似,请写出在液NH3中发生下列化学反应的原因。
Mg+2Na++ 2I-=2Na +MgI2
Al + 3Na++3NH2-=Al(NH2)3+3Na
第3题(9分)
向5.0mL0.20mol/L CuSO4溶液中滴加0.20mol/L的NaOH溶液,当加入7.5mLNaOH溶液时,溶液中Cu2+几乎全部沉淀,请给出沉淀物的化学式。
·允许使用非编程计算器及直尺等文具。
·试卷按密封线封装。
题中可能用到的元素相对原子质量如下:
H
C
N
O
Na
Al
K
S
Cl
Cu
Ag
1.008
12.01
14.01
16.00
22.99
26.98
39.10
32.07
35.45
63.55
107.9
第1题选择题(16分)(每选2分,多选,对一错一不得分,无负分)
(1)荧光棒发光的原理是利用H2O2氧化草酸酯产生能量,该能量传递给荧光物质而发光。草酸酯是一种粘稠度较高的有机化合物。下列说法不正确的是()
A.荧光棒发光,凑近可燃性气体,会导致气体燃烧
B.当荧光棒亮度减弱时,敲打荧光棒亮度可能增强
C.荧光棒放入冷冻室亮度可能减弱甚至消失
D.荧光棒发光是化学能转化为热能,热能转化为光能
(2)碘可能呈金属性,下列事实能说明这一事实的是()
A.已经制得I(NO3)3、I(ClO4)32H2O等含I3+的化合物
(2)K和CO2生成K2C2O4。
第6题(5分)
已知:
前者是酸转化为氧化物(CO),后者是氧化物(CO)转化为盐,为什么CO不是HCOOH的酸酐?
第7题(7分)
19世纪前半叶,测得水中H、O元素的质量比是1:8,因当时不知道水分子中H、O的原子数,所以无法得到统一的原子量。
Cannizzaro根据Avogadro的观点:“同温度、同压强下,同体积气体中含有相同数的分子”。解决了测定原子量的难题。
已知A、B、C、D四种化合物中均含有X元素,300℃时它们都是气体,请根据表中与气体N2相比得到的数据计算X的原子量(分子中元素原子数只能是整数)。
N2
A
B
C
D
气体质量(g/L)
0.652
0.849
6.321
2.731
3.632
X的质量分数(%)
97.3
26.2
6
7
8
9
10
11
总分
满分
16
4
9
7
8
5
7
9
10
13
12
得分
评卷人
·竞赛时间2小时。迟到超过30分钟者不得进场。开赛后1小时内不得离场。时间到,把试卷(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在试卷指定位置上,使用黑色或蓝色圆珠笔、签字笔、钢笔答题,使用红色或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸指定位置,写在其他处者按废卷处理。
(4)主族元素M和N,M位于短周期,且M2-和N+的电子数之差为8,则下列说法正确的是()
A.M和N的原子序数之差为11
B.M和N的原子序数之和为11
C.M和N的最外层电子数之和为8
D.M和N的最外层电子数之差为8
(5)将Cl2通入熔融的硫磺制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊;S2Cl2与NaOH溶液反应得到澄清溶液。S2Cl2在合成橡胶,硬水软化等方面有着重要应用。有关S2Cl2的叙述正确的有()
下列说法错误的是()
A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.氧化主要是氧气将HSO3-,SO32-,H2SO3氧化为SO42-
C.“反应、稀释”的目的是中和、稀释后再排放
D.经稀释“排放”出的废水中SO42-浓度与海水相同
第2题( 4分)
作为溶剂NH3和H2O相似,能发生电离NH3+ NH3NH4++ NH2-
B.已经制得IBr、ICl等卤素互化物
C.碘易溶于KI溶液形成I3-
D.I4O9可以看成是碘酸盐
(3)能正确表示下列反应的离子方程式为()
A.向碳酸氢镁溶液中滴加少量石灰水:
Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+ H2O
B.在强碱溶液中,次氯酸钠与氢氧化铁反应生成Na2FeO4:
3ClO-+ 2Fe(OH)3= 2FeO42-+3Cl-+H2O+4H+
C.向NaAIO2溶液中通入过量的CO2制取AI(OH)3
AIO2-+ CO2+ 2H2O= AI(OH)3↓+ HCO3-
D.漂白粉[主要成分Ca(ClO)2,Ca(OH)2]在空气中失效:
ClO-+ CO2+H2O=HClO+HCO3-
