8-羟基喹啉的合成
8 羟基喹啉的制备

8 羟基喹啉的制备
1. 2-氨基苯酚经过乙醛基化、缩合和环氧化反应得到
2-氨基-1,2-二苯基乙烷醇,再通过羟醛化、脱水和环化反应合成8 羟基喹啉。
该方法中,乙醛和氯化亚砜作为催化剂,可以提高反应速率和收率。
环氧化反应条件需加入亚铁氯化物和过氧化苯乙烯,反应温度在80-100℃,反应时间约为8小时。
2. 对-苯二酚通过三氯化铁氧化反应得到8 羟基喹啉。
该方法中,三氯化铁作为氧化剂,反应条件要求温度在25-30℃,反应时间约为4小时。
得到的产物需要经过结晶纯化,以获得高质量的8 羟基喹啉产品。
3. 2-羟基苯胺和氰化氢缩合后,经过烷基化和羟甲基化反应得到 N,N-二(2-羟基苯基)丙二胺,再通过环化反应得到8 羟基喹啉。
该方法中,烷基化和羟甲基化反应需要加入硫酸三乙酯和过硫酸铵作为催化剂。
环化反应要求温度为150℃,反应时间为12小时。
总之,以上五种方法分别通过乙醛基化、三氯化铁氧化、缩合、硝化还原和羟甲基化等反应,得到2-氨基-1,2-二苯基乙烷醇、N,N-二(2-羟基苯基)丙二胺、2-羟基-1,2-二苯基乙烷醇、N,N-二(苯基)甲基乙酰胺等中间体,再通过环化反应合成8 羟基喹啉。
这些方法均有自己的适用场景和反应条件,可以根据需要进行选择。
8羟基喹啉制备实验报告

8羟基喹啉制备实验报告8羟基喹啉制备实验报告引言:8羟基喹啉是一种重要的有机化合物,具有广泛的应用领域,如药物合成、材料科学等。
本实验旨在通过一系列反应步骤,以苯酚为原料,制备8羟基喹啉。
实验步骤:1. 首先,将苯酚溶解于稀盐酸中,加入硝酸和硫酸作为催化剂。
反应混合物在适当的温度下搅拌反应一段时间,使苯酚发生硝化反应,得到硝基苯酚。
2. 接下来,将硝基苯酚与甲醛反应,生成羟甲基苯酚。
反应条件需要控制得当,以避免产生副反应。
3. 羟甲基苯酚与氨水反应,生成氨基甲基苯酚。
该步骤需要在碱性条件下进行,以促进反应进行。
4. 最后,氨基甲基苯酚与甲醛在碱性条件下缩合反应,生成8羟基喹啉。
该步骤需要控制反应时间和温度,以提高产率和纯度。
实验结果:经过以上步骤,成功合成了8羟基喹啉。
通过红外光谱、核磁共振等仪器分析,确认了产物的结构和纯度。
讨论:本实验中,选择苯酚作为起始原料,是因为其易得且价格相对较低。
同时,苯酚的性质也适合进行后续反应。
在制备过程中,反应条件的选择和控制非常重要。
过高或过低的温度、浓度等因素都会对反应产率和产物纯度产生影响。
在实验过程中,还需要注意安全操作。
苯酚、硝酸等化学品具有一定的毒性和腐蚀性,必须佩戴防护手套、护目镜等个人防护装备,确保实验操作的安全性。
结论:通过本实验,成功合成了8羟基喹啉。
实验结果表明,所得产物的结构和纯度符合预期要求。
实验过程中,合理选择反应条件和注意安全操作是取得良好结果的关键。
展望:虽然本实验成功合成了8羟基喹啉,但仍有一些改进的空间。
例如,可以尝试优化反应条件,提高产率和纯度。
同时,也可以进一步研究8羟基喹啉的应用领域,探索其在药物合成、材料科学等方面的潜力。
总结:本实验通过一系列反应步骤,以苯酚为原料,成功制备了8羟基喹啉。
实验结果表明,所得产物具有良好的结构和纯度。
实验过程中,合理选择反应条件和注意安全操作是取得成功的关键。
通过本实验的实施,对有机合成反应的原理和实践有了更深入的了解,并为进一步研究和应用提供了基础。
8羟基喹啉的制备总结和讨论

8羟基喹啉的制备总结和讨论
8-羟基喹啉(8-Hydroxyquinoline)是一种有机化合物,常用于药物合成、配位化学和光学材料等领域。
下面是关于8-羟基喹啉制备的总结和讨论:
制备方法:
1. 溴化8-氨基喹啉:首先将8-氨基喹啉与溴在适当溶剂中反应,生成溴化8-氨基喹啉。
2. 氧化:将溴化8-氨基喹啉与碱性高锰酸钾(KMnO4)或其他氧化剂反应,进行氧化反应,生成8-羟基喹啉。
讨论:
1. 溴化8-氨基喹啉的反应条件:溴化反应可以在适当的溶剂(如醚类、醇类溶剂)中进行,在适当的温度下进行反应。
反应条件的选择应考虑到反应速率和产率的平衡。
2. 氧化反应的选择:氧化反应可以使用高锰酸钾等常见的氧化剂进行。
其他氧化剂,如过氧化氢(H2O2),也可以用于该反应。
在选择氧化剂时,应考虑到反应条件的温度和反应速率。
3. 产率和纯度:制备8-羟基喹啉的关键是产率和纯度。
反应条件的优化可以提高产率,如反应温度、反应时间、反应物的比例等。
纯度可以通过适当的提纯方法(如结晶、萃取、柱层析等)获得。
总结:
制备8-羟基喹啉的一种常见方法是将8-氨基喹啉与溴反应生成溴化8-氨基喹啉,然后进行氧化反应,生成8-羟基喹啉。
制备过程中需考虑反应条件的选择和优化,以提高产率和纯度。
制备方法的选择还可以根据具体需求和实验条件进行调整和改进。
实验3-38—8-羟基喹啉的制备-甲

8-羟基喹啉的制备一、实验目的1. 学习合成8-羟基喹啉的原理和方法。
2. 巩固回流加热和水蒸汽蒸馏等基本操作。
二、反应原理Skraup反应是合成杂环化合物喹啉及其衍生物最重要的方法,它是用苯胺与无水甘油、浓硫酸及弱氧化剂硝基化合物等一起加热而得,为了避免反应过于剧烈,常加入FeSO4作为氧的载体。
浓硫酸的作用使甘油脱水成丙烯醛,并使苯胺与丙烯醛的加成物脱水成环。
硝基化合物则将1,2-二氢喹啉氧化成喹啉,本身被还原成芳胺也可以参加缩合。
反应中所用的硝基化合物,要与芳胺的结构相对应,否则会导致产生混合物。
8-羟基喹啉形成的过程如下:三、药品试剂、操作步骤在100mL三颈烧瓶中加入1.8g(约0.013mol)邻硝基苯酚、2.8g(约0.025mol)邻氨基苯酚、7.5mL(约9.5g,0.1mol)无水甘油,剧烈振荡,使之混匀。
在不断振荡下慢慢滴入4.5mL浓硫酸,于冷水浴上冷却。
装上回流冷凝管,用小火在石棉网上加热,约15min溶液微沸,即移开火源。
反应大量放热,待反应缓和后,继续小火加热,保持反应物微沸回流1h。
冷却后加入15mL水,充分摇匀,进行简易水蒸气蒸馏,除去未反应的邻硝基苯酚(约30min),直至馏分由浅黄色变为无色为止。
待瓶内液体冷却后,慢慢滴加约7mL1:1(质量比)氢氧化钠溶液,于冷水中冷却,摇匀后,再小心滴加约5mL饱和碳酸钠溶液,使之呈中性。
再加入20mL水进行水蒸气蒸馏,蒸出8-羟基喹啉。
待馏出液充分冷却后,抽滤收集析出物,洗涤,干燥,粗产物约3g。
粗产物用4:1(体积比)乙醇-水混合溶剂25ml 重结晶,得8-羟基喹啉2~2.5g(产率54%~68%)。
纯8-羟基喹啉的mp为72~74℃。
四、操作重点及注意事项1、所用甘油含水量不超过0.5%(d=1.26)。
如果甘油含水量较大,则喹啉的产量不高。
可将其加热到180℃,冷却在100℃左右放入盛有浓H2SO4的干燥器中备用。
8-羟基喹啉

8–羟基喹啉的合成应用化学2008级唐祖建20086129摘要:8-羟基喹啉是白色或淡黄色晶体或结晶性粉末,露光变黑,有石炭酸气味。
8-羟基喹啉是两性的,能溶于强酸、强碱,在碱中电离成负离子,在酸中能结合氢离子,在PH=7时溶解性最小。
8-羟基喹啉广泛用于金属的测定和分离,制染料和药物的中间体,制杀菌剂等。
本实验以邻氨基苯酚、邻硝基酚、无水甘油和浓硫酸为原料合成8-羟基喹啉。
关键词:8-羟基喹啉,水蒸气蒸馏,邻硝基酚,邻氨基酚1 实验部分1.1 实验原理以邻氨基酚、邻硝基酚、无水甘油和浓硫酸为原料合成8-羟基喹啉。
浓硫酸的作用是使甘油脱水生成丙烯醛,并使邻氨基酚和丙烯醛加成物脱水成环。
硝基酚为弱氧化剂,能将成环产物8-羟基–1,2–二氢喹啉氧化成8-羟基喹啉,邻硝基酚本身则还原成邻氨基酚,也可参与缩合反应。
反应历程如下:(1)CH2OHCHOH CH2OH H2SO42CH2HCCHO(2)OHNH2CH2CHCHOOHNHCH2CH CHOHH2SO4OHNHNO2OHNOH1.2 实验药品无水甘油邻硝基苯酚邻氨基苯酚浓硫酸氢氧化钠饱和碳酸钠溶液乙醇1.3 实验仪器圆底烧瓶回流冷凝器水蒸气蒸馏装置锥形瓶滴管烧杯玻璃棒1.4 实验操作在圆底烧瓶中称取19g无水甘油(约0.2mol),并加入3.6g(0.026mol)邻硝基苯酚、5.5g(0.05mol)邻氨基苯酚,使混合均匀。
然后缓缓加入9mL浓硫酸(约16g)。
装上回流冷凝管,在石棉网上用小火加热。
当溶液微沸时,立即移去火源。
反应大量放热,待作用缓和后,继续加热,保持反应物微沸2小时。
稍冷后,进行水蒸气蒸馏,除去未作用的邻硝基苯酚。
瓶内液体冷却后,加入12g氢氧化钠与12mL水的溶液。
再小心滴入饱和碳酸钠溶液,使呈中性。
再进行水蒸气蒸馏。
蒸出8-羟基喹啉(约收集馏液400mL)。
馏出液充分冷却后,抽滤收集析出物,洗涤干燥后的粗产品6g左右。
粗产物用乙醇–水混合溶剂重结晶,得8-羟基喹啉5g左右(产率69﹪)。
有机电致发光材料三(8-羟基喹啉)铝的合成工艺

有机电致发光材料三(8-羟基喹啉)铝(tris(8-hydroxyquinolinato)aluminum, Alq3)是一种常用的有机半导体材料,广泛应用于有机发光二极管(OLED)、有机场效应晶体管(OEFT)和太阳能电池等领域。
其合成方法较为简单,一般采用反相溶剂法,主要步骤如下:1.雄性醇类亲核试剂(如异丙醇)在氧化剂存在下氧化制备出8-羟基喹啉酸(8-hydroxyquinolinol, HQ)。
将醇类亲核试剂(如异丙醇)放入反应釜内,加入氧化剂(如氧气或过氧化氢) 进行氧化反应。
反应的最终产物是8-羟基喹啉酸。
2.在惰性溶剂(如氢氧化钾/钾碳酸钠溶液)中,将8-羟基喹啉酸与氯化铝反应制备出配合物Alq3。
在一个量热容器中加入8-羟基喹啉酸和氯化铝。
在惰性溶剂(如丙酮或四氢呋喃)中在-78°C 的温度下进行反应,控制加入氢氧化钾/钾碳酸钠两者的浓度,使反应物迅速反应形成Alq3中间体。
在反应后,Alq3物质会沉淀在反应溶液中。
为获取纯度高的Alq3,少量的取沉淀物用冷水洗涤,用真空泵吸干。
这些步骤需要多次重复,以确保纯度充分高的Alq3沉淀晶体获得。
3.沉淀的Alq3物质在凉水中反复洗涤、过滤干燥、再经真空干燥得到纯净的Alq3粉末。
取得的Alq3晶体沉淀通过凉水反复洗涤和过滤处理。
这些沉淀晶体然后在高温烘干箱中干燥,也可在真空下在低温下干燥以去除水分。
这样合成得到的Alq3配合物大多数晶体为亮绿黄色,对有机发光二极管的制备有广泛应用。
上述工艺过程比较简单,但需要注意入料顺序、溶剂的选择和反应条件等因素,以保证合成出的Alq3样品物理化学性质良好,达到研究和工程应用的需求。
8-羟基喹啉的制备

五、产物谱图
8-羟基喹啉红外光谱 羟基喹啉红外光谱
8-羟基喹啉的核磁共振氢谱 羟基喹啉的核磁共振氢谱
思考题
1.为什么第一次水蒸气蒸馏要在酸性条件下进行,第二 次却要在中性条件下进行? 2.在反应中,如果用对甲基苯胺作原料,应得到什么产 2. 物,硝基化合物应如何选择?
三、升华的基本原理
升华是纯化固体有机化合物的一种方法。利用升 华可除去不挥发性杂质,或分离不同挥发度的固体混 合物。 升华是指固体物质不经过液态直接转变成蒸气的 现象。对有机化合物的提纯来说,重要的是使物质蒸 气不经过液态而直接转变成固态,因为这样能得到高 纯度的物质。因此,在有机化学实验操作中,不管物 质蒸气是由固态直接气化,还是由液态蒸发而产生的, 只要是物质从蒸气不经过液态而直接转变成固态的过 程都称之为升华。一般说来,对称性较高的固体物质, 具有较高的熔点,且在熔点温度以下具有较高的蒸汽 压,易于用升华来提纯。
实验2 实验2-5
一、实验目的
8-羟基喹啉的合成 8-
1.学习合成8-羟基喹啉的原理和方法 2.巩固回流、水蒸气蒸馏等操作
二、主反应式: 主反应式:
+ HO NH2 OH OH
NO2
OH
OH
N OH
喹啉及其衍生物可用Skraup反应制备,浓硫酸的作 用是使甘油脱水生成丙烯醛,并使邻氨基酚与丙烯醛的 加成物脱水成环;邻硝基酚作为弱氧化剂能将8-羟基1,2-二氢喹啉氧化成8-羟基喹啉,而其本身还原成邻氨 基酚。
2.稍冷后,进行水蒸气蒸馏,除去未作用的邻硝基苯酚。 将3克氢氧化钠溶于6毫升水中,待烧瓶内液体冷却后加 入,用饱和碳酸钠溶液调至中性,再进行第二次水蒸气 蒸馏,蒸出8-羟基喹啉。
3.待馏出液充分冷却后,抽滤收集析出物,即得粗产品。 4.粗产品用4:1(体积)的乙醇-水重结晶。
2014_8-羟基喹啉与AlQ3的合成及发光性能
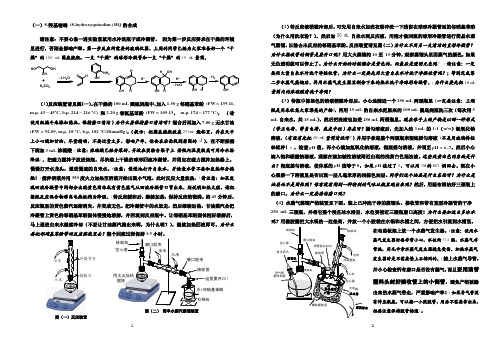
(一)8-羟基喹啉 (8-hydroxyquinoline) HQ 的合成请注意:不要心急一进实验室就用水冲洗瓶子或冷凝管, 因为第一步反应要求在干燥的环境里进行,否则会影响产率。
第一步反应所需要的玻璃仪器,上周的同学已经为大家准备好一个“干燥”的100 mL 圆底烧瓶、一支“干燥”的球形冷凝管和一支“干燥”的10 mL 量筒。
+HOOHOHNH 2ONNH OHH 22H 2SO 4(1)反应装置请见图(一)。
在干燥的100 mL 圆底烧瓶中,加入1.50 g 邻硝基苯酚 (FW = 139.11, m.p. 43 – 45ºC, b.p. 214 – 216 ºC) 和2.20 g 邻氨基苯酚 (FW = 109.13, m.p. 174 – 177 ºC), (请使用纸漏斗来添加药品,保持磨口清洁)为什么要保持磨口清洁呀?混合后再加入7.80 g 无水甘油 (FW = 92.09, m.p. 18 ºC, b.p. 182 ºC/20mmHg),(提示:把圆底烧瓶放在250ml 烧杯里,并在天平上小心滴加甘油,尽量精确,不要过量太多,影响产率。
你会在后面找到原因的 J ),在不断振摇下滴加3 mL 浓硫酸 (注意:浓硫酸已经分装好,并放在实验台架子上,若瓶内温度较高可用冷水浴降温)。
把磁力搅拌子放进烧瓶,尽快装上干燥的球形回流冷凝管,并固定在磁力搅拌加热器上。
慢慢打开水龙头,通进慢速的自来水。
(注意:慢慢地打开自来水,并检查水管不要和发热部分接触!)搅拌溶液并用350度火力加热至溶液开始出现小气泡,此时反应大量放热,(请注意:如果发现回流冷凝管中间部分出现黄色固体或有黄色蒸气从回流冷凝管口冒出来,则说明加热太猛,请把整瓶反应混合物移离电热板稍为降温。
)待反应缓和后,继续加热,保持反应物微沸。
约45分钟后,反应瓶里的黄色蒸汽逐渐消失,并变成无色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8-羟基喹啉的合成
指导老师:邹平
刘玲 20131976
摘要本实验通过设计合成8-羟基喹啉杂环化合物,掌握其合成原理及合成方法。
掌握环合的SKraup反应原理(用苯胺与无水甘油,浓硫酸及弱氧化剂硝基化合物等一起加热)。
在实验过程中进一步巩固回流加热和水蒸气蒸馏等基本操作技能。
关键词 8-羟基喹啉甘油浓硫酸水蒸气蒸馏
8-羟基喹啉是一种白色或淡黄色结晶或结晶性粉末,有石炭酸气味,熔点75-76℃,不溶于水和乙醚,易溶于乙醇、丙酮、氯仿、苯或稀酸,能升华,腐蚀性较小,低毒。
8-羟基喹啉是一种两性物质,能溶于强酸、强碱,在碱中电离成负离子,在酸中能结合氢离子,中性环境下溶解度最小。
由于其能沉淀和分离金属离子,被广泛用于金属的测定和分离,其硫酸盐和铜盐是优良的防腐剂。
此外,它也被用作医药中间体,是合成克泻痢宁、氯碘喹啉、扑喘息敏的原料,也是染料、农药中间体。
本实验以邻氨基酚、邻硝基酚、无水甘油和浓硫酸为原料合成8-羟基喹啉。
浓硫酸的作用是使甘油脱水形成丙烯醛,并使邻氨基酚和丙烯醛加成脱水成环。
硝基酚为弱氧化剂,能将成环产物8-羟基-1,2-二氢喹啉氧化成8-羟基-喹啉,邻硝基酚本身被还原成邻氨基酚,也可参与缩合反应。
反应过程可能为:
1 实验部分
1.1 实验仪器与试剂
圆底烧瓶、电热套、搅拌器、回流冷凝管、蒸馏头、烧杯、量筒、漏斗、电子天平
无水甘油、邻氨基苯酚、邻硝基苯酚、浓硫酸、氢氧化钠、饱和碳酸钠
1.2实验主要试剂性质
1.3实验方法
在圆底烧瓶中称取9.5g无水甘油(约0.1mol),并加入1.8g(0.013mol)邻硝基苯酚,2.75g(0.05mol)邻氨基苯酚,使混合均匀。
然后缓慢加入4.5ml 浓硫酸(约8g)。
装上冷凝回流凝管,在电热套中加热,当溶液微沸时,立即移去火源。
反应大量放热,待作用缓和后,继续加热,保持反应物微沸1.5小时。
稍冷后,进行水蒸气蒸馏,除去未作用的邻硝基酚。
瓶内液体冷却后,加入6g氢氧化钠和6ml水的溶液。
再小心滴入饱和碳酸钠溶液,使呈中性。
再进行水蒸气蒸馏。
蒸出8-羟基喹啉(约收集馏液200ml)。
馏出液充分冷却后,抽滤收集析出物,洗涤干燥粗产品。
2 结果及分析
经蒸馏、冷却、抽滤后,得到淡黄色固体,称得实验产物湿重为4.16g。
实验理论值为:3.629g,产率为114.63%,产率偏大,可能由于产物未烘干且为进行重结晶,产品中有杂质等原因所致。
在本实验中,两次水蒸气蒸馏所处的PH不同,原因是第一次要除去杂质,而第二次要得到产物。
产物8-羟基喹啉既溶于酸又溶于碱。
成盐后不能被蒸出,所以第二次蒸馏前必须小心中和使PH在7~8之间,使产量最大。
另外,由于本实验的产物具有升华性质,而含有的固体杂质没有这个特征,故可以采用升华提纯,但升华时火不宜过大。
3 思考题
(1)为什么第一次水蒸汽蒸馏在酸性条件下进行,第二次又要在中性下进行。
答:两次水蒸气蒸馏所处的PH不同,第一次要除去杂质,在酸性条件下,8-羟基喹啉会变成盐,除去邻硝基苯酚。
而第二次要得到产物,因为8-羟基喹啉既溶于酸又溶于碱,成盐后不能被蒸出,所以第二次蒸馏前必须小心中和使PH在7~8之间,使产量最大。
(2)为什么在第二次水蒸汽蒸馏前,一定要很好的控制PH范围?碱性过强时有何不利?若已发现碱性过强时,如何补救。
答:因为8-羟基喹啉既溶于酸又溶于碱,成盐后不能被蒸出,所以第二次蒸馏前必须小心中和使PH在7~8之间,使产量最大。
碱性过强时,8-羟基喹啉会成盐,不能蒸馏出来。
若已发现碱性过强,可以适当加酸,以调整PH范围。
(3)具有什么条件的固体有机化合物,才能用升华法进行提纯?
答:实验想要得到的产物具有升华性质,而含有的固体杂质没有这个特征,可以采用升华提纯,但升华时火不宜过大。
(4)在进行升华操作时,为什么只能用小火缓缓加热?
答:适当控制火焰,可使升华速度放慢,以提高结晶纯度和产量。
若温度太高,会使产物发黄。
4参考文献
[1] 有机合成实验讲义
[2] 百度百科。
