(2020年7月整理)有机化学第十章习题醛酮课后习题答案.doc
有机化学第十章习题醛酮课后习题答案

有机化学第十章习题醛酮课后习题答案ationTechnologyCompany.2020YEAR习题1.用系统命名法命名下列化合物:2.写出下列化合物的结构:3•写出分子式为叽0,含有苯环的羰基化合物和名称。
4.写出2-甲基环戊酮与下列试剂反应的产物:1LiAlH 4⑶NHNH225(a)NHOH(b)HCl2⑺Zn-Hg/HCl ⑼HOCHCHOH ,干HCl225.理化性质比较:⑵NaBH4⑷CHNHNH652HMgBr,HO ⑻NaCN/HSO24(10)CHCOOOH31)比较下列各组化合物的沸点:A:①CHCHCHCH ②CHCHCHCHOH ③CHCHCHCHO3223322232HO2)比较下列化合物在水中的溶解度:第十章酮醌习题及答案①CH3CH 2CH 2CHO②CH 3CH 2CHO③O"CHOO(1)CH 3CH 2CCH(CH 3)2C H 3C H3(2)CH 3CH 2CHCH 2CHCH 2CHO(3)CH3CH 2CH 2CHOH3COCH 3(5)C 2H5ClCH3\CH 3CH 2CHCHO (6)(7)CH3OCH34-O-OO H_c —H_(1)2-甲基丙醛 ⑵乙烯酮 ⑶乙二醛缩甲醛 E )-3-苯基丙烯醛 (5)(R )-3-氯-2-丁酮⑹苯乙酮⑺5,6-二氯-2-环己烯-1, 4-二酮⑻环己酮缩氨脲⑼三聚乙醛⑽苯甲醛-2,4-二硝基苯腙B:①CHO ②HO(4)HO(8)(9)(10)(12)—CH=NHN —=N-OH(13)(14)Br3CHOCHO(3)比较下列化合物与HCN 加成反应的活性:①CH 3CHO ②C 6H 5COCH 3 比较下列化合物与NaHS03加成反应的活性: O 4) 5) ② 比较下列化合物的稳定性: O OH ①② 比较下列负离子的稳定性: o①O ② 7)比较下列化合物pka 的大小:①CH 3CHO ② 6.完成下列反应: CH 3COCH 3HCN CHCHCOCH 323OH - NaHSO.H 2OCH 3CoCH 3OIICH 3-C-CH 2CH 3⑷ Bi./Fe2③CH 3COCH 3 OIIC 6H 5CC 6H5O③O ③ O④OJ'<>CH 3③C 6H 5COCH 3OIIC 6H 5CC 6H5CH ?MgBjHRMgy ? 无水乙醚CH 3CHOH 2O/H+9 32—+CH 三CNaH 3O +3O IIC 6H 5CCH 3653NH 2OH・HCUCH 3(C 6H 5)3P =CHC H 32CH -C -C -CH33HQHAc-?【2H 3O +3+ nO+ CHCOCH 3IO II CH 3-C-CH 2CH 2Br CHONaBH 4 O II+CH 3-C-CH 3HCl 3)2NH HCl>NaOH,HOc2COOC 2H 5NaOC (CH 3)3・?Me 2CuLiHClAl C l 3-CuC 2l 2浓NaOH ?・■+?H 3O +OHOH干HClOII(CH 3CH 2-C )2OCH 3COOOHL ?干醚H 2O/H +CH 3CH 2-C -OK⑻⑼⑽(11)(12)闆(14)(15)(16)(⑺(18)(19)OII0-C-CH3(20)COCH3+? 1) CH3CHO(2)3)(CH3)2CHOH(4) (5) (CH3)2CHCHO(6)(7) CHCOCH653(8)7.下列化合物:能够发生碘仿反应的有?CH3CH2COCH2CH3C6H5CHO65—CHO能与亚硫酸氢钠反应的有?能与甲醛发生交叉Cannizzaro反应的有?能够与Tollens试剂反应的有?能够与Fehling试剂反应的有8.鉴别下列各组化合物:O H(1)A.CH3CH2CH2CHOB.CH3COCH2CH3C.CH3CHCH2CH3D.CH3CH2CH2CH2OH2)A.CHOB.COCH3C.CH=CH2D.C三CH(3)A.正戊醛B.苯甲醛C.2-戊酮D.3-戊酮E.2-戊醇F.3-戊醇O4) D.9.解释下列反应的机理:OII(1):H-C-CH2O(2):RR3(3):二苯基乙二酮在NaOH的作用下发生重排,生成二苯基羟乙酸钠,酸化后得到二苯基羟乙酸,如果用CH 30Na 代替NaOH ,贝V 可以得到二苯基羟乙酸甲酯。
《有机化学》章节习题答案.docx
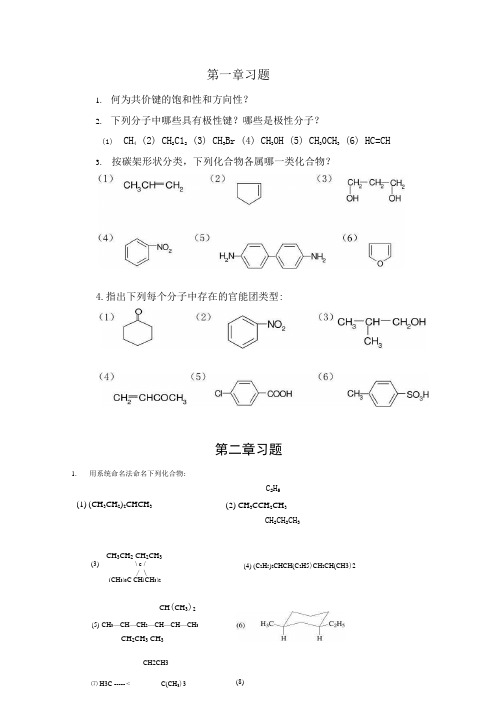
第一章习题1.何为共价键的饱和性和方向性?2.下列分子中哪些具有极性键?哪些是极性分子?(1)CH4 (2) CH2C12 (3) CH3Br (4) CH3OH (5) CH30CH3 (6) HC=CH3.按碳架形状分类,下列化合物各属哪一类化合物?第二章习题1.用系统命名法命名下列化合物:(1) (CH3CH2)2CHCH3C2H5 (2) CH3CCH2CH3CH2CH2CH3CH3CH2 CH2CH3(3)\ c // \(CH3)3C CH(CH3)2(4) (C2H5)2CHCH(C2H5)CH2CH(CH3)2CH(CH3)2(5)CH3—CH—CH2—CH—CH—CH3CH2CH3 CH3CH2CH34.指出下列每个分子中存在的官能团类型:⑺ H3C ----- < C(CH3)3 (8)2. 写出下列化合物的构造式:(1) 由一个叔丁基和异丙基组成的烷炷; (2) 含一侧链甲基,分子量为98的环烷炫(3) 分子量为114,同时含有1°、2°、3。
、4。
碳的烷炷。
3.写出下列化合物的结构式,如其名称与系统命名原则不符,请予以改正。
(1)3, 3-二甲基丁烷 (2)2, 3-二甲基-2-乙基丁烷 (3) 4 -异丙基庚烷(4) 3> 4-二甲基-3 -乙基戊烷(5)3, 4, 5-三甲基-4-正丙基庚烷 ⑹2 -叔丁基-4, 5 -二甲基己烷4. 相对分子质量为72的烷任进行高温氯化反应,根据氯化产物的不同,推测各种烷炷的结构式。
(1)只生成一种一氯代产物(2)可生成三种不同的一氯代产物(3) 生成四种不同的一氯代产物 (4)只生成二种二氯代产物 5.不查表将下列烷炷的沸点由高至低排列成序: (1)2, 3-二甲基戊烷 (2) 2-甲基己烷 (3)正庚烷 (4) 正戊烷(5)环戊烷6. 写出下列化合物的优势构象—( 「CH2CH3 (1) BrCH 2CH 2Cl (2) CH 3CH 2CH 2CH 2CH 3 (3) '、'、—/(4)反-1-甲基-4-叔丁基环己烷7. 写出1, 3-二甲基环已烷和1-甲基-4-异丙基环已烷的顺、反异构体优势构象,并比较每组中哪个稳定。
醛和酮习题及答案

醛和酮习题及答案醛和酮是有机化学中一类重要的化合物,它们含有羰基(C=O)。
醛的官能团是-CHO,而酮的官能团是-CO-。
下面我们通过一些习题来加深对醛和酮性质和反应的理解。
习题1:写出以下醛和酮的IUPAC名称。
- CH3CHO- CH3COCH3答案1:- CH3CHO的IUPAC名称是甲醛。
- CH3COCH3的IUPAC名称是丙酮。
习题2:醛和酮的羰基可以发生哪些类型的反应?- 醇的制备- 还原反应- 加成反应答案2:- 醛和酮可以通过还原反应转化为醇。
- 醛可以被还原剂如氢气或钠硼氢还原为醇,而酮通常需要更强的还原剂。
- 醛和酮的羰基可以与氢氰酸加成形成腈,或与格氏试剂等有机金属试剂加成。
习题3:醛和酮的红外光谱特征是什么?- 醛的羰基在红外光谱中通常出现在哪个波数范围?- 酮的羰基在红外光谱中通常出现在哪个波数范围?答案3:- 醛的羰基在红外光谱中通常出现在大约1720-1740 cm^-1的波数范围。
- 酮的羰基在红外光谱中通常出现在大约1705-1725 cm^-1的波数范围。
习题4:醛和酮的核磁共振氢谱特征是什么?- 醛的羰基氢在核磁共振氢谱中通常出现在哪个化学位移范围?- 酮的羰基氢在核磁共振氢谱中通常出现在哪个化学位移范围?答案4:- 醛的羰基氢在核磁共振氢谱中通常出现在9-10 ppm的化学位移范围。
- 酮的羰基氢在核磁共振氢谱中通常出现在2-3 ppm的化学位移范围。
习题5:以下化合物中哪些是醛,哪些是酮?- CH3CH2CHO- (CH3)2CO- CH3CH2COCH3答案5:- CH3CH2CHO是醛,因为它含有-CHO官能团。
- (CH3)2CO是酮,因为它含有-CO-官能团。
- CH3CH2COCH3是酮,因为它含有-CO-官能团。
习题6:醛和酮的氧化反应是什么?- 醛的氧化产物是什么?- 酮的氧化产物是什么?答案6:- 醛的氧化产物通常是羧酸。
- 酮的氧化产物通常是二羧酸,但酮通常不易被氧化。
高中化学(新人教版)选择性必修三课后习题:醛、酮(课后习题)【含答案及解析】

醛酮必备知识基础练1.下列反应中属于有机化合物被还原的是()A.乙醛发生银镜反应B.新制的Cu(OH)2与乙醛反应C.乙醛加氢制乙醇D.乙醛制乙酸、B、D项中均是由乙醛生成乙酸或乙酸盐,是在有机化合物分子中加入了氧原子,属于氧化反应。
C项中由乙醛生成乙醇,是在有机化合物分子中加入氢原子,属于还原反应。
2.(2020安徽淮南高二检测)下列各组物质中既不是同系物也不是同分异构体的是()A.甲醛、丁醛B.丙酮、丙醛C.乙醛、丙酮D.苯甲醛、对甲基苯甲醛项中两物质互为同系物;B项中两物质互为同分异构体;D项中两物质互为同系物;C项中两物质分子式不同,尽管相差一个CH2原子团,但是官能团不同,因此不属于同系物。
3.(2021吉林洮南高二期末)某有机化合物的化学式为C5H10O,能发生银镜反应和加成反应。
若将它与H2加成,所得产物结构简式可能是()A.(CH3)3COHB.(CH3CH2)2CHOHC.CH3(CH2)3CH2OHD.CH3CH2C(CH3)2OH,其可能的同分异构体有:CH3CH2CH2CH2—CHO、CH3CH(CH3)CH2CHO、CH3CH2CH(CH3)CHO、(CH3)3CCHO,醛跟H2的加成反应是发生在—CHO上,使之转化为—CH2OH,只有C项符合。
4.把有机化合物氧化为,所用的氧化剂最合理的是()A.O2B.酸性KMnO4溶液C.银氨溶液D.溴水,前者中的醛基变为后者中的羧基,而碳碳双键不被氧化,所以选择弱氧化剂银氨溶液或新制的氢氧化铜均可。
5.已知甲、乙、丙、丁四种有机化合物的转化关系如图。
其中甲、乙、丁均能发生银镜反应,则甲为()A.甲醇B.甲醛C.甲酸D.乙醛,可推知为醛类,甲、乙、丁均能发生银镜反应,推知甲只能为甲醛,B项正确。
6.下列有关有机化合物的判断正确的是()A.乙醛和丙烯醛()不是同系物,它们分别与足量氢气发生加成反应后的产物也不是同系物B.对甲基苯甲醛()可使酸性高锰酸钾溶液褪色,说明它含有醛基C.1 mol HCHO发生银镜反应最多生成2 mol AgD.苯酚发生还原反应后的产物在核磁共振氢谱中应该有5组吸收峰解析乙醛不含碳碳双键,丙烯醛含碳碳双键,二者不是同系物,它们分别与足量氢气发生加成反应后的产物分别为乙醇和1-丙醇,二者均为一元饱和醇,互为同系物,故A错误;中的甲基也能使酸性高锰酸钾溶液褪色,故B错误;1 mol HCHO发生银镜反应最多生成4 mol Ag,故C错误;苯酚发生还原反应后的产物为,有5种等效氢,所以其核磁共振氢谱中有5组吸收峰,故D正确。
10醛酮思考题、习题及答案

(8)
COCH3
O (9)
答案: 能发生碘仿反应的是:(1)(3)(5)(6)(8)
反应产物除 CHI3 外分别为:(1)CH3CH2COONa
(3)HCOONa (5)CH3CH2COONa
(6)CH2=CHCOONa (8) 能和饱和 NaHSO3 水溶液加成的是:(1)(2)(6)(7)(9)
COONa
OH CH3CCH2CH3 反应产物分别为:(1) SO3Na
OH (2) CH3CH2CH2CH SO3Na
8
CH2 (6)
OH CHCCH3
SO3Na
(7)
OH CH SO3Na
(9)
OH SO3Na
习题 10-9.下列化合物中,哪些能进行银镜反应? CH3CHCHO
(1)CH3COCH2CH3 H OH
1苯甲醇和苯甲醛2己醛和2己酮32己酮和3己酮4丙酮和苯乙酮52己醇和2己酮61苯基乙醇和2苯基乙醇7环己烯环己酮和环己醇82己醇3己酮和环己酮答案
10 醛酮 思考题、习题及答案
思考题 10-1. 利用什么波谱分析法可以区别化合物 PhCH=CHCH2OH 和 PhCH=CHCHO,简 述原因。
答案:可用红外光谱鉴别,原因:前者 OH 在 3200~3500cm-1 处有强而宽的吸收峰;后 者-CHO 的羰基在 1700 cm-1 处有一强吸收峰,在 2720 cm-1 处有两个弱而特征的吸收峰。
(ii)
CH(CH3)2
CH(CH3)2
CH3 O
O (iii) (CH3)3CCH=CHCC(CH3)3
O (iv)
HO
由 思考题 10-6.
O 合成
CH2OH
答案:
醛酮(习题与答案)

醛酮(习题与答案)一、命名:1. 2. 3.4. 5. 6.(CH3)2CH2CHO7、CH3COCH2CH2OH 8、CH3COCH(CH3)2 9、10、CH3COCH2COCH2CH311、12、13、14、OHCCH2CH2CH2CHO15、16、17、18、19、20、答案:1、苯乙酮2、邻羟基苯甲醛(水杨醛)3、4-氯-4-甲基-2-戊烯醛4、2-溴-4-硝基苯甲醛5、对甲基苯甲醛6、3-甲基丙醛7、4-羟基-2-丁酮8、3-甲基-2-丁酮9、1-环己基-1-丙酮10、2,4-己二酮11、3-甲基-6-庚炔醛12、3,3-二甲基环己基甲醛13、3-苯基-2-丙烯醛14、戊二醛15、4-甲基环己酮16、2-苯基丙醛17、对甲酰基苯乙酸18、α,β-萘二醛(1,2-萘二醛)19、1-苯基-2-丙酮(甲基苄基酮) 20、4-戊烯-2-酮二、完成反应:1.CHO240%NaOH+答:2.250%KOH+ Cl CHO答:3.答: 4.答: 5.答:6.CHO+加热CH3O CH3COCH3NaOH 答:7.答:8.答: 9.答: 10.答: 11.答:+COOH CH2OHCH3CH312.答:13.+CH3COCH2CH3I2NaOH++答:14.答:15.答:16.答:17.答:三、回答下列问题:1.下列化合物能发生碘仿反应得就是( )。
a、CH3CH2COCH3b、c、d、(CH3)2CHOH答:a、d2.下列化合物能发生碘仿反应得就是( )。
a、2-甲基丁醛b、异丙醇c、2-戊酮d、丙醇答:b、c3.下列化合物能发生碘仿反应得就是( )。
a、(CH3)2CHCHOb、CH3CH2OHc、C6H5CHOd、CH3COCH2CH3答:b、d4.下列化合物能发生碘仿反应得就是( )。
a、CH3CH2CH2OHb、CH3CH2CHOc、CH3CH2CHOHCH3d、C6H5COCH3答:c、d5.下列化合物与NaHSO3加成反应活性次序为( )。
有机化学(北大版)第10章习题解答
HCN
CH3
OH CH3OH C CN H2SO4 CH3
CH2=CCOOCH3 CH3
(5)
2CH3CHO
10%NaOH
CH3CH=CHCHO O CHCH2CH2CH3 O
CH2OH CH2OH 干HCl H3O+
O CHCH=CHCH3 O
H2 Pd
CH3CH2CH2CHO
(6)
CH3CH2CHO
第 10 章 习题解答
1. 命名下列化合物:
(1) (CH3)2CHCHO
(4) CH3O
(2) H3C
CHO (5) O
CHO
O CH3
(3) (CH3) 2CHCOCH(CH3)2
(6) O C
O ( 7) CH3CH2 C CH=CH2
答:(1) 2-甲基丙醛 (4)对甲氧基苯甲醛 (7)1-戊烯-3-酮
答:
缩酮
半缩酮
半缩醛
半缩醛
10.某化合物分子式为 C5H12O(A),氧化后得分子式为 C5H10O 的化合物(B)。B 能和 2,4二硝基苯肼反应得黄色结晶,并能发生碘仿反应。(A)和浓硫酸共热后经酸性高锰酸钾氧化 得到丙酮和乙酸。试推出 A 的构造式,并用反应式表明推导过程。
C H 3 C H C H (C H 3 ) 2 OH A [O ] C H 3 C O C H (C H 3 ) 2 B
答:
11.某化合物 C8H14O(A),可以很快地使溴水褪色,可以和苯肼发生反应,氧化后得到一分 子丙酮及另一化合物(B)。B 具有酸性,和次碘酸钠反应生产碘仿和一分子羧酸,其结构 是 HOOCCH2CH2COOH。写出(A)、(B)的结构式。
答:A B
有机化学(第二版)课后答案
有机化学(第二版)课后习题参考答案第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
)键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol 气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
、(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
高教第二版(徐寿昌)有机化学课后习题集规范标准答案第10章
第十章 醇和醚一、将下列化合物按伯仲叔醇分类,并用系统命名法命名。
1.2.CH 3CH 3CH 3C OH 3.OH4.OH 5.OH6.HOCH 2CH 2CH 2OH7.OHOH8.9.OHOH仲醇,异丙醇仲醇,1-苯基乙醇 仲醇,2-壬烯-5-醇二、 预测下列化合物与卢卡斯试剂反应速度的顺序。
1.正丙醇 2.2-甲基-2-戊醇 3.二乙基甲醇 解:与卢卡斯试剂反应速度顺序如下:2-甲基-2-戊醇>二乙基甲醇>正丙醇 三、 比较下列化合物在水中的溶解度,并说明理由。
1.CH 3CH 2CH 2OH2.HOCH 2CH 2CH 2OH3.CH 3OCH 2CH 34.CH 2OHCHOHCH 2OH5.CH 3CH 2CH 342135>>>>理由:羟基与水形成分子间氢键,羟基越多在水中溶解度越大,醚可与水形成氢键,而丙烷不能。
四、 区别下列化合物。
1.CH 2=CHCH 2OH 2.CH 3CH 2CH 2OH3.CH 3CH 2CH 2Cl解:烯丙醇 丙醇 1-氯丙烷2.CH 3CH 2CHOHCH 3CH 3CH 2CH 2CH 2OH (CH 3)3COH解: 2-丁醇 1-丁醇 2-甲基-2-丙醇3.α-苯乙醇 β-苯乙醇解:与卢卡斯试剂反应,α-苯乙醇立即变浑, β-苯乙醇加热才变浑。
五、顺-2-苯基-2-丁烯和2-甲基-1-戊烯经硼氢化-氧化反应后,生成何种产物? 解:CH 3C=CCH 3HC 6H 5B 2H 6NaOH,H 2O 2C 6H 5CHCHOH3CH 3CH 3CH 2=C CH 2CH 2CH 3B 2H 6NaOH,H 2O 2CH 3HOCH 22CH 2CH 3六、 写出下列化合物的脱水产物。
1.CH 3CH 2C(CH 3)2OHCH 3CH=C(CH 3)22.(CH 3)2CCH 2CH 2OHH 2SO 41moleH 2O(CH 3)2C=CHCH 2OH3.CH 2CHCH 3H +CH=CHCH 34.CH 2CHCH(CH 3)2+CH=CHCH(CH 3)25.CH 3CH=C CH 3CH 2C(CH 3)C(CH 3)CH 2CH 3CH 3C CH 3=CHCH 3OHOH七、 比较下列各组醇和溴化氢反应的相对速度。
有机化学第二版第十章习题答案
第10章 醛、酮、醌10-1 命名下列化合物。
(1)3-甲基-1-苯基-1-戊酮; (2)2,4,4-三甲基戊醛; (3)1-(1-环已烯基)丁酮; (4)(E )-苯基丙基酮肟; (5)3-丁酮缩乙二醇; (6)2-环已烯酮; (7)三氯乙醛缩二甲醇; (8)2-戊酮苯腙; (9)2,6-萘醌; (10)2,4-已二酮; (11)((E )-间甲基苯甲醛肟。
10-2 写出下列反应的主要产物。
PhCHOHCOONa +浓NaOHHCHO2OH+(Cannizzaro 反应)OZn-Hg / HClHCNH 3OOH COOHO(Clemmensen 还原)H 3CC CH 3O Mg C 6H 6H 3OH 2SO 4△(CH 3)2C C(CH 3)2OH OH(H 3C)3CC CH 3O(pinacol 重排)(1)(2)(3)(4)+HCHO(Mannich 反应)+HCl(5)(6)ON HCH 2CH 2NOCH 3OCH3CH 3OH(黄鸣龙还原)CO 3Cl+CO 2HCl+(Baeyer-Villiger reaction)ONH 2+PCl 5H NO(Beckmann 重排)O(1) HSCH 2CH 2SH2O3OHO(卤仿反应)(7)(8)(9)(10)CHCl 3+(Wittig reaction)CH 3MgBr+Ph 33(13)(12)(11)O+O(1,4-加成产物)OCHCH 2CH 3O OOHHONCOO(双烯合成反应)10-3 比较下列化合物的亲核加成反应活性。
(2)(1)C OCH 3H 3C C CH 3OH 3CC HOCOCH 3H 3C(3)(4)(3)>(1)>(2)>(4)10-4 将下列化合物按烯醇式的含量多少排列成序。
CH 3COCHCOCH 3CH 3COCH 2CH 3(2)(1)PhC H 2C O(3)(4)COCH 3CH 3COCH 2COCH 3C CH 3O(1)>(4)>(3)>(2)10-5 指出下列化合物中,哪些能发生碘仿反应?哪些能与饱和NaHSO 3反应?(2)(1)O(3)(4)(5)ICH 2CHOCH 3CH 2CHOC 6H 5COCH 3CH 3CHOCH 3CH 2CH 2OHCH 3CH 2CCH 2CH 3CH 3CH 2CHCH 3OH(7)(6)(8)O能与饱和NaHSO 3反应的有(1)、(2)、(5)、(8)[脂肪族甲基酮、大多数醛和8个碳以下的脂肪酮能进行此反应]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1第十章 醛酮醌习题及答案习题1.用系统命名法命名下列化合物: CH 3CH 2CCH(CH 3)2O(1)(2)(3)CH 3CH 2CHCH 2CHCH 2CHOCH 3CH 3CH 3HHCH 2CH 2CHO(4)(5)CH 3C 2H 5COCH 3HCH 3CH 2Cl(6)OCH 3CH 3(7)CHOOHOCH 3(11)(8)(9)(10)CO CO CO C HOH OO(12)(13)(14)(15)CH=NHN=N-OHOOOOCH 32.写出下列化合物的结构:⑴2-甲基丙醛 ⑵乙烯酮 ⑶乙二醛缩甲醛 ⑷(E )-3-苯基丙烯醛 ⑸(R )-3-氯-2-丁酮 ⑹苯乙酮 ⑺5,6-二氯-2-环己烯-1,4-二酮 ⑻环己酮缩氨脲⑼三聚乙醛 ⑽苯甲醛-2,4-二硝基苯腙 3.写出分子式为C 8H 8O ,含有苯环的羰基化合物和名称。
4.写出2-甲基环戊酮与下列试剂反应的产物:⑴LiAlH 4 ⑵NaBH 4 ⑶NH 2NH 2 ⑷C 6H 5NHNH 2 ⑸(a)NH 2OH (b)HCl ⑹C 2H 5MgBr,H 2O ⑺Zn-Hg/HCl ⑻NaCN/H 2SO 4 ⑼HOCH 2CH 2OH ,干HCl ⑽CH 3COOOH 5.理化性质比较:(1)比较下列各组化合物的沸点:A:①CH 3CH 2CH 2CH 3 ②CH 3CH 2CH 2CH 2OH ③CH 3CH 2CHCHOOH③①CHO②CHOHOCHOHOCHO④B:(2)比较下列化合物在水中的溶解度:2① CH 3CH 2CH 2CHO ② CH 3CH 2CHOCHO③(3)比较下列化合物与HCN 加成反应的活性:③①②④CH 3CHOC 6H 5COCH 3CH 3COCH 3C 6H 5CC 6H 5O(4)比较下列化合物与NaHSO 3加成反应的活性:HOOO③①②(5)比较下列化合物的稳定性:③①②④OHOOO(6)比较下列负离子的稳定性:③①②OOOOOCH 3(7)比较下列化合物pka 的大小:③①②④CH 3CHOC 6H 5COCH 3CH 3COCH 3C 6H 5CC 6H 5O6.完成下列反应:⑴-CH 3CH 2COCH 324?⑵OH -?NaHSO 3?CH 3COCH 3H 2O⑶CH 3-C-CH 2CH 3OCH 3MgBr H 2O?,⑷CH 3CHOBr 2 / FeH 2O / H +?Mg ??⑸O+CHCNaH 3O +??⑹NH 2OHHCl??C 6H 53O3?OCH 3(C 6H 5)3P=CHCH 3⑺+?⑻H 2O,HAcO(1mol) Br 2C CH 3CH 3C-CH 3I 2⑼CH 3OH 3O +?CH 3O ?⑽NaBH 4COONaOH,H 2OCH 3-C-CH 3⑾?+CH 3OCO H O⑿(CH 3)2NHHCl?O +HCHO+⒀?OCHOClCH 2COOC 2H 5NaOC(CH 3)3⒁+?OMe 2CuLi?+O⒂⒃322?CH 3++CO HCl浓NaOH?+?⒄CH 3ICH 3COOOHH 3O +??N⒅CH 32CH 2BrOOH OH2+Mg ?O ?⒆+(CH 3CH 22OO?OCHOO4⒇COCH 3+?O-C-CH 3O OH7.下列化合物:(1)CH 3CHO (2)CH 3CH 2COCH 2CH 3(3)(CH 3)2CHOH (4)O(5) (CH 3)2CHCHO (6) C 6H 5CHO (7) C 6H 5COCH 3(8)CHO能够发生碘仿反应的有?能与亚硫酸氢钠反应的有?能与甲醛发生交叉Cannizzaro 反应的有? 能够与Tollens 试剂反应的有? 能够与Fehling 试剂反应的有? 8.鉴别下列各组化合物:(1)CH 3COCH 2CH 3A.CH 3CH 2CH 2CHO B. C.CH 3CHCH 2CH 3OHD.CH 3CH 2CH 2CH 2OH(2)A.CHO COCH 3B.C.CH=CH 2 D.C CH(3)A.正戊醛 B.苯甲醛 C.2-戊酮 D.3-戊酮 E.2-戊醇 F.3-戊醇(4) A.B.OHOHC.CHOD.O9.解释下列反应的机理:(1):2CH 2CH 2-CH-C-HOO CH 3-3CHO(2):OHORRH 3O +RR(3):二苯基乙二酮在NaOH 的作用下发生重排,生成二苯基羟乙酸钠,酸化后得到二苯5基羟乙酸,如果用CH 3ONa 代替NaOH ,则可以得到二苯基羟乙酸甲酯。
C CC 6H 5C 6H 5OO NaOH 2CH 3ONa 3CCOONaOH2H +OH23OH2试用反应机理说明重排过程。
(4):O +ClCH 2COOEt(CH 3)3COKCOOEtO10.(1)用苯和≦2碳的有机化合物合成C 6H 5C (CH 3)2OH(2)CH 2=CHCH 2OH CH-CH-CHO OH OH由合成(3)由合成CH 33O(CH 3)3CCH 2COOH11.化合物A (C 12H 18O 2),不与苯肼作用。
将A 用稀酸处理得到B (C 10H 12O ),B 与苯肼作用生成黄色沉淀。
B 用I 2/NaOH 处理,酸化后得C (C 9H 10O 2)和CHI 3。
B 用Zn/ HCl 处理得D (C 10H 14)。
A 、B 、C 、D 用KMnO 4氧化都得到邻苯二甲酸。
试推测A ~D 可能的结构。
12.化合物A (C 6H 14O ),1HNMR 如下:δ0.9(9H ,单峰),1.10(3H ,单峰),3.40(1H ,四重峰),4.40(1H ,单峰),A 与酸共热生成B (C 6H 12)B 经臭氧化和还原水解生成C (C 3H 6O ),C 的1HNMR 只有一个信号:δ=2.1,单峰。
请推断A 、B 、C 的结构。
13.化合物A 的分子式为C 6H 12O 3,IR 谱在1710cm -1处有强吸收峰,用碘的氢氧化钠溶液处理A 时,得到黄色沉淀,但不能与Tollens 试剂生成银镜,然而A 先用稀硫酸处理后,再与Tollens 试剂作用,有银镜生成。
A 的1HNMR 谱数据如下:δ2.1(3H ,单峰),δ2.6(2H ,多重峰),δ3.2(6H ,单峰),δ4.7(1H ,三重峰) 试推测A 的结构。
答案:1.(1)2-甲基-3-戊酮;(2)3,5-二甲基庚醛;(3)(E )-4-己烯醛;(4)(R )-3-甲基-2-戊酮;(5)2-氯丁醛(α-氯丁醛);(6)3,5-二甲基环己酮;(7)4-羟基-3-甲氧基苯甲醛;(8)二苯基乙二酮;(9)1,2-二苯基-2-羟基乙酮;(10)二环[2,2,2]-2-辛酮;(11)螺[4,5]-8-癸酮;(12)苯甲醛苯腙;(13)环己酮肟;(14)4-溴-1,2-苯醌;(15)2-甲基-1,4-苯醌2.(CH 3)2CHCHO (1)(2)(3)CH 2=C=OH 2COO(4)CHO phH H6(5)COCH 33Cl H(6)(7)CCH 3OOO ClCl(8)(9)(10)NNH C ONH 2O OO CH 3CH 3CH 3CH=NHNNO 2NO 23.CHOCH 3CHOCH 3CH 3CHO(2-甲基苯甲醛)(3-甲基苯甲醛)(4-甲基苯甲醛)CH 2CHOCOCH 3(苯乙醛)(苯乙酮)4.CH 3(1)(2)(3)(4)OHCH 3OHCH 3N-NH 2CH 3N-NH 2(5)(6)(7)CH 3N-OHN-H O CH 3CH 3OH C 2H 5CH 3(8)(9)(10)CH 3CH 3OH CNOOO O CH 35.(1)A:②﹥③﹥①,B:②﹥③﹥④﹥① (2) ②﹥①﹥③ (3) ①﹥③﹥②﹥④ (4) ①﹥②﹥③ (5) ①﹥④﹥③﹥② (6) ②﹥③﹥① (7) ④﹥③﹥②﹥①6.⑴CCH 3CH 2CH 3CNC CH 3CH 2CH 3OHCOOH ,CH 3COCH 3CCH 3CH 3SO 3Na,⑵7C CH 3CH 3C 2H 5⑶,Br 2MgBr,HC CH 3⑷⑸NaO CCHOH CCH,C 6H 5⑹CH 3N OH,CH 36H 5O贝克曼重排⑺CH-CH 3CH 3 维蒂希反应Br ⑻OCHI 3⑼C CH3CH 3COOH CH 3+CH 3O⑽COOHCH=CH-C-CH 3⑾CH 3OO克莱森-施密特缩合CH 3CH 3⑿ONCH Cl曼尼希反应OH⒀OO O安息香缩合⒁OCHCOOC 2H 5 达尔森反应⒂CH 3α,β不饱和酮的1,4加成(类迈克尔反应)8⒃CH 3CHO加特曼-科赫反应,+CH 3COO -CH 3CH 2OH坎尼扎罗反应,CH 3⒄N烯胺加成反应,OCH 3烯胺水解,CH 3OO拜叶耳-维利格氧化(重排),⒅CH 3-C-CH 2CH 2Br O O CH 3-C-CH 2CH 2MgBr O O CH 3-C-CH 2CH 2CH 2CH 2OHO ,3⒆OCH=C-COOH 柏琴反应⒇COCH 3OH福瑞斯重排7.能够发生碘仿反应的有?(1)(3)(7)能与亚硫酸氢钠反应的有?(1)(4)(5)(6)(8) 能与甲醛发生交叉Cannizzaro 反应的有?(6) 能够与Tollens 试剂反应的有?(1)(5)(6)(8) 能够与Fehling 试剂反应的有?(1)(5)(8) 8.(1):CH 3COCH2CH 3A.CH3CH 2CH 2CHOB.C.CH 3CHCH 2CH 3OH D.CH 3CH 2CH 2CH 2OHTollens 试剂(+)(- )Ag (- )(- )(+)(+)(- )CHI 3CHI 3Lucas 试剂(- )浑浊9(2):A.B.C.D.(+)Ag (- )(- )(+)(+)(- )(+)Cu(NH 3)2+(- )砖红色沉淀(3):A.B.C.D.Tollens 试剂2(+)(- )CHI 3E.F.(+)(+)(- )(- )(- )Ag AgFehling 试剂Cu 2O (红色)(+)(- )(- )(+)(+)(- )(+)(- )I2/NaOH CHI 3(4):A.B.C.D.Tollens 试剂Lucas 试剂(- )(+)浑浊FeCl 3溶液(+)(- )(- )(- )紫色(+)(- )(- )Ag9.(1)H-C-CH 2CH 2CH 2-CH-C-H O O3OH-22-CHOOCH 3C-H CH 3CHO CH 3CHOOH(2)ORRH +OH +RR R R OH R ROHOHRRR 迁移- H +OHRR10CC 6H 5O CCC 6H 5OC 6H 5OH (3)二芳羟基乙酸重排CO -C 6H 5C 6H 5C OOHC OH C 6H 56H 5C OO -H 2OC OH C 6H 5C 6H 5C OOHCC 6H 5OCCC 6H 5OC 6H 5OCH 3 C C C 6H 5O -OCH 3C 6H 5O CH 3OHC C C 6H 5OH OCH 3C 6H 5O(4)ClCHCOOEt33COOEt O-Cl10.CH 3COCl 3CH 3MgBrC-CH 3OC-CH 3OMgBrCH 3(1)+2C-CH 3OHCH 3(2)CH 2=CHCH 2OHCrO 3-吡啶CH 2=CHCH 2OH OH OCOCH 2=CH HCH-CH-CHO 4OC OCH 2-CH H H +11(3)CH 33OBa(OH)2CH 3-C=CH-C-CH 3CH 3O(CH 3)2CuLi 3-C-CH 23CH 3CH 3OI 2/NaOHC-CH 2-C-ONaCH 3CH 3CH 3OH+C-CH 2-C-OH 3CH 3CH 3O11.ACH 3CH 2-C OCH 3OCH 3CH 3或CH 2CH 3COCH 3OCH 3CH 3BCH 3CH 2-C CH 3或CH 2CH 3C CH 3CCH 3CH 2-C OHC OH 或CH 2CH 3DCH 2CH 2CH 3CH 2-CH 3CH 3或CH 2CH 312.AB C(CH 3)33OH(CH 3)3CCH=CH 2CH 3-C CH 313.ACH 32CHOCH 3OCH 3O。
