有机化学官能团高效记忆表格
高中有机化学官能团识别汇总(大全)

高中有机化学官能团识别汇总(大全)
本文档旨在提供一个有机化学官能团识别的汇总,供高中学生
研究和参考。
以下是一些常见的有机化学官能团及其识别方法。
1. 羟基官能团 (-OH)
- 有机化合物中的羟基官能团通常能够形成氢键。
- 官能团测试方法:
- 用溴水进行溴素试验,当溴水变色或沉淀形成时,可能存在
羟基官能团。
- 使用酚酞试剂,当溶液变红时,可能存在羟基官能团。
2. 羰基官能团 (C=O)
- 羰基官能团有醛、酮和羧酸三种常见类型。
- 官能团测试方法:
- 使用银镜试剂,当溶液变镜面反射时,可能存在醛或酮官能团。
- 使用红石酸钠试剂,当溶液变紫色时,可能存在羧酸官能团。
3. 氨基官能团 (-NH2)
- 氨基官能团能与酸或酰氯反应生成相应的衍生物。
- 官能团测试方法:
- 使用叔胺试剂,当产生气泡或沉淀时,可能存在氨基官能团。
4. 卤素官能团
- 卤素官能团指有机化合物中的氯、溴或碘原子。
- 官能团测试方法:
- 使用银盐试剂,当产生白色、黄色或棕色沉淀时,可能存在
卤素官能团。
5. 双键官能团
- 双键官能团指有机化合物中的烯烃或芳香烃结构。
- 官能团测试方法:
- 使用溴水进行溴添加试验,当溴水变色或消失时,可能存在
双键官能团。
以上是一些常见的有机化学官能团及其识别方法的简要介绍。
希望对您的研究有所帮助。
更多有机化学官能团的识别方法可进一
步参考相关教材和资料。
请注意,本文档中的内容仅供参考,具体识别方法可能需要根据实际情况进行进一步确认。
有机化学的官能团总结

甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
CH4→C+2H2(条件为高温高压,催化剂)甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HClCH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HClCHCl3+Cl2→CCl4+HCl (条件都为光照。
)实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br乙烯和水CH2=CH2+H20→CH3CH2OH (条件为催化剂)乙烯和氯化氢CH2=CH2+HCl→CH3-CH2Cl乙烯和氢气CH2=CH2+H2→CH3-CH3 (条件为催化剂)乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃)乙炔和溴水C2H2+2Br2→C2H2Br4乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2乙炔和氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6 (条件为催化剂)实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。
CaCO3 === CaO + CO2 2CaO+5C===2CaC2+CO2CaC2+2H2O→C2H2+Ca(OH)2C+H2O===CO+H2-----高温C2H2+H2→C2H4 ----乙炔加成生成乙烯C2H4可聚合苯燃烧2C6H6+15O2→12CO2+6H2O (条件为点燃)苯和液溴的取代C6H6+Br2→C6H5Br+HBr苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)苯和氢气C6H6+3H2→C6H12 (条件为催化剂)乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃)乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)乙醇发生消去反应的方程式CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸 170摄氏度)两分子乙醇发生分子间脱水2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸 140摄氏度)乙醇和乙酸发生酯化反应的方程式CH3COOH+C2H5OH→CH3COOC2H5+H2O乙酸和镁Mg+2CH3COOH→(CH3COO)2Mg+H2乙酸和氧化钙2CH3COOH+CaO→(CH3CH2)2Ca+H2O乙酸和氢氧化钠CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH乙酸和碳酸钠Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑甲醛和新制的氢氧化铜HCHO+4Cu(OH)2→2Cu2O+CO2↑+5H2O乙醛和新制的氢氧化铜CH3CHO+2Cu→Cu2O(沉淀)+CH3COOH+2H2O乙醛氧化为乙酸2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)烯烃是指含有C=C键的碳氢化合物。
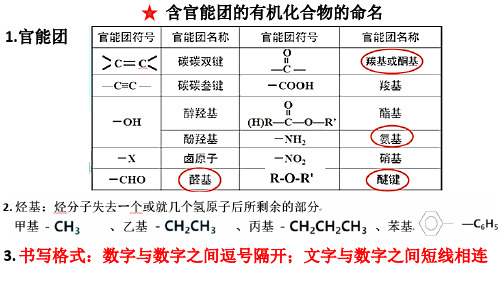
高中化学含官能团的有机化合物的命名
2-硝基苯胺 3-甲氧基苯甲酸
(2)链状
乙二酸
1,3-丙二醇 1,2-丙二醇
HOOC(CH2)4COOH
己二酸
3.酯的命名 命名格式:某酸某(醇)酯
乙二酸二乙酯
二乙酸乙二酯
4.环状化合物的命名 命名格式:环+某+类 某:碳原子数(天干地支)
类:类别
环己烷
环V己烯 1,3-环己官能团的有机化合物的命名
2.
3. 书写格式:数字与数字之间逗号隔开;文字与数字之间短线相连
1.单官能团化合物 关键:最长碳链含官能团;支链在前,主链在后;
标明官能团位置(醛基,羧基不用标,一定在端位)
4-甲基-1-戊炔 4-甲基戊醛
2-甲基-2-戊醇
2-甲基-2-氯丙烷
3-甲基丁酸
以苯环作母体 关键记住顺序:
以苯作取代基
-NO2、-X<-OR(烃氧基) <烷烃基<苯基 <-CH=CH2、-C≡CH<-NH2<-OH<-CHO<-COOH 前者为取代基,后者为母体。
苯的二元取代物 苯的三元取代物
2.双官能团
(1)含苯环
邻苯二甲酸
间苯二甲醛
对苯二酚
2-硝基甲苯 2-硝基苯酚 2-硝基苯甲醇 2-羟基苯甲酸 2-氯苯乙烯
如何快速记忆官能团

【一】:药物化学官能团记忆技巧【二】:有机化学官能团高效记忆(表格)高中常见有机化合物结构与性质总结其中1、能使KMnO4褪色的有机物烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂 2、能使Br2水褪色的有机物烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂3、能与Na反应产生H2的有机物醇、酚、羧酸、氨基酸、葡萄糖4、具有酸性(能与NaOH、Na2CO3反应)的有机物酚、羧酸、氨基酸5、能发生银镜反应或与新制Cu(OH)2反应的有机物醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖6、既有氧化性,又有还原性的有机物醛、烯烃、炔烃 7[O如何快速记忆官能团。
OOHCH22H2OCH2CH2OO【三】:九种方法快速记忆化学知识很多同学都觉得化学很难,其实化学很简单,但是需要记忆的很多,并且这些知识很多容易混淆,所以还需要理解内涵掌握本质。
不管怎么说,记忆对于学习无疑是至关重要的前提。
本文就化学知识的一些记忆方法,简单的阐述几点,希望对同学们有所启发。
一、口诀记忆由于知识点多,记忆量大,在化学学习中往往会出现一些很容易记住的口诀,老师要求我们去记忆它。
首先,要告诉自己这是一种学习的捷径,然后在深刻的理解它的内涵,最后记住了,就会成为你学习化学的利器。
如“升失氧,降得还”、“见量化摩,求啥先求摩”、“有弱才水解,都强不水解。
谁弱谁水解,谁强显谁性。
越热越水解,越弱越水解”。
二、归类记忆如何快速记忆官能团。
对所学知识进行系统分类,抓住特征,在以此类推。
如电解质判断的时候,把所学的化合物归类,再把强电解质弱、电解质的包含的类别记住,对于我们掌握本质就很有帮助;再如在掌握了各个主族、周期的相似性和递变性规律后,对于具体的元素单质、化合物的性质就容易多了。
三、理解记忆对所学知识进行分析、综合、比较、归纳总结,找出内在联系及规律,然后记忆这些带有规律性的知识。
如在记忆氧化还原反应、离子反应、化学平衡、电离平衡等概念,必须在理解的意义前提下去记忆。
(完整版)高中化学有机重点——官能团知识汇总

①引入-入-OH的方法:烯加水,醛、酮加氢,醛的氧化、酯的水解、卤代烃的水解、糖分解为乙醇和CO2
③引入C=C的方法:醇、卤代烃的消去,炔的不完全加成,*醇氧化引入C=O
2.消除官能团
①消除双键方法:加成反应
②消除羟基方法:消去、氧化、酯化
高中化学有机重点——官能团知识汇总
有机物官能团与性质
[知识归纳]
其中:
1.能使KMnO4褪色的有机物:烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂
2.能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂
3.能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖
4.具有酸性(能与NaOH、Na2CO3反应)的有机物:酚、羧酸、氨基酸
5.能发生银镜反应或与新制Cu(OH)2反应的有机物:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖
6.既有氧化性,又有还原性的有机物:醛、烯烃、炔烃
7.能发生颜色(显色)反应的有机物:苯酚遇FeCl3显紫色、淀粉遇I2变蓝、蛋白质遇浓硝酸变黄、葡萄糖遇Cu(OH)2显绛蓝
[有机物间的相互转化关系]
[有机合成的常规方法]
③消除醛基方法:还原和氧化
3.有机反应类型
常见的有机反应类型有取代(包括酯化、水解)、加成、加聚、消去、氧化、还原等。能够发生各种反应类型的常见物质如下:
高二化学选修五有机化学官能团识别整理特全

高二化学选修五有机化学官能团识别整理
特全
本文档包含了高二化学选修五中有机化学官能团的识别整理特全。
一、烃类官能团识别
1. 烷基(Alkane):只具有碳-碳单键;
2. 烯基(Alkene):具有一个碳-碳双键;
3. 炔基(Alkyne):具有一个碳-碳三键;
4. 芳基(Aryl):芳香环上的碳原子。
二、卤素化合物官能团识别
1. 氯代烷基(Alkyl halide):烷基中有一个或多个氯原子;
2. 锂代烷基(Alkyl lithium):烷基中有一个或多个锂原子;
3. 溴代烷基(Alkyl bromide):烷基中有一个或多个溴原子;
4. 碘代烷基(Alkyl iodide):烷基中有一个或多个碘原子。
三、醇类官能团识别
1. 醇基(Alcohol):一个或多个羟基(-OH);
2. 苯酚基(Phenol):苯环上一个羟基(-OH)。
四、醛类官能团识别
1. 醛基(Aldehyde):碳链中的一个羰基(C=O)。
五、酮类官能团识别
1. 酮基(Ketone):碳链中的一个羰基(C=O)。
六、羧酸类官能团识别
1. 羧基(Carboxyl):一个羧基(-COOH)。
七、酯类官能团识别
1. 酯基(Ester):羧酸酯基(-COO-)。
以上是高二化学选修五中常见的有机化学官能团的识别整理。
请根据需要查阅该文档,以帮助你更好地理解和识别有机化合物中的官能团。
有机化学中的官能团

有机化学中的官能团官能团是决定有机化合物性质的原子或原子团,有机化学反应主要发生在官能团上,官能团很大程度上决定了有机物的反应方向。
一.常见的有机化合物官能团有以下几种:6.羧基(-COOH);酸性,与NaOH反应生成水(中和反应),与NaHCO3、Na2CO3反应生成二氧化碳,与醇发生酯化反应二.表格如下:10药学三班温林文- 汉语汉字编辑词条文,wen,从玄从爻。
天地万物的信息产生出来的现象、纹路、轨迹,描绘出了阴阳二气在事物中的运行轨迹和原理。
故文即为符。
上古之时,符文一体。
古者伏羲氏之王天下也,始画八卦,造书契,以代结绳(爻)之政,由是文籍生焉。
--《尚书序》依类象形,故谓之文。
其后形声相益,即谓之字。
--《说文》序》仓颉造书,形立谓之文,声具谓之字。
--《古今通论》(1) 象形。
甲骨文此字象纹理纵横交错形。
"文"是汉字的一个部首。
本义:花纹;纹理。
(2) 同本义[figure;veins]文,英语念为:text、article等,从字面意思上就可以理解为文章、文字,与古今中外的各个文学著作中出现的各种文字字形密不可分。
古有甲骨文、金文、小篆等,今有宋体、楷体等,都在这一方面突出了"文"的重要性。
古今中外,人们对于"文"都有自己不同的认知,从大的方面来讲,它可以用于表示一个民族的文化历史,从小的方面来说它可用于用于表示单独的一个"文"字,可用于表示一段话,也可用于人物的姓氏。
折叠编辑本段基本字义1.事物错综所造成的纹理或形象:灿若~锦。
2.刺画花纹:~身。
3.记录语言的符号:~字。
~盲。
以~害辞。
4.用文字记下来以及与之有关的:~凭。
~艺。
~体。
~典。
~苑。
~献(指有历史价值和参考价值的图书资料)。
~采(a.文辞、文艺方面的才华;b.错杂艳丽的色彩)。
5.人类劳动成果的总结:~化。
~物。
6.自然界的某些现象:天~。
有机化学官能团高效记忆表格

物质类别
特征结构(官能团)
断键位置
反应类型
试剂条件
反应产物
烷烃
取代
X2,光照
烯烃
加成
X2的CCl4溶液
HX
H2O,催化剂
加成,还原
H2,催化剂
加聚
一定条件
—-
氧化
酸性KMnO4溶液
酸性KMnO4溶液褪色
炔烃
或
加成
X2的CCl4溶液
或
HX,催化剂,加热
或
加成,还原
H2,催化剂
或
—-
氧化
酸性KMnO4溶液
酸性KMnO4溶液褪色
芳香烃
取代
X2,FeX3
HNO3,浓H2SO4,加热
加成3H2
H2,Ni,加热
取代
HNO3,浓H2SO4,加热
氧化
酸性KMnO4溶液
卤代烃
—X
取代
NaOH水溶液(催),加热
消去
NaOH乙醇溶液(催),
加热
醇
—OH
取代、置换
Na
取代、酯化
羧酸—COOH,浓H2SO4,加热
[有机物间的相互转化关系]
图1:
Na
中和
NaOH溶液
取代、酯化
醇,浓H2SO4,加热
酯
取代、水解
稀H2SO4,加热
(或NaOH溶液,加热)
其中:
1、能使KMnO4褪色的有机物:
烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂
2、能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂
3、能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中常见有机化合物结构与性质总结
其中:
1、能使KMnO4褪色的有机物:
烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂
2、能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂
3、能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖
4、具有酸性(能与NaOH、Na2CO3反应)的有机物:酚、羧酸、氨基酸
5、能发生银镜反应或与新制Cu(OH)2反应的有机物:
醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖
6、既有氧化性,又有还原性的有机物:醛、烯烃、炔烃
7、能发生颜色(显色)反应的有机物:
苯酚遇FeCl3显紫色、淀粉遇I2变蓝、蛋白质遇浓硝酸变黄、葡萄糖遇Cu(OH)2显绛蓝[有机物间的相互转化关系]
图1:。
