李军川:乳腺导管内增生性病变(宁夏)
生存素与血管内皮生长因子在乳腺浸润性导管癌及导管内增生性病变

的准 确性 [ 2 ] , 早期 诊 断 、 早期 干预 对乳腺 癌预 后有
者年 龄 2 2 ~7 7岁 , 中位 5 1 . 2 4岁 ; 4 6例 肿 瘤 最 大 径小于 2 . 0 c m, 6 3例 2 . 0~ 5 . 0 c m、 1 9 例 大 于 5 . 0 c m; 组 织学 工级 2 2例 , Ⅱ级 7 4例 , Ⅲ级 3 2例 ; 4 5例无 腋 窝 淋 巴结 转 移 , 5 1例 1 ~3个 淋 巴结 转 移, 3 2 例 超 过 3个 淋 巴结 转 移 ; 3 7例 远 处 脏 器 转 移 。按 照 国际 抗 癌 联 盟 TNM 的 分 期 标 准 , 工期
2 3例 , Ⅱ期 4 4例 , Ⅲ期 2 2例 , Ⅳ期 3 9 例。
1 . 2 免 疫 组 织 化 学 方 法 及 结 果 判 读 本组 所用 S u r v i v i n和 VE GF试 剂 均 购 自福 州
乳腺导管原位癌的病理诊断
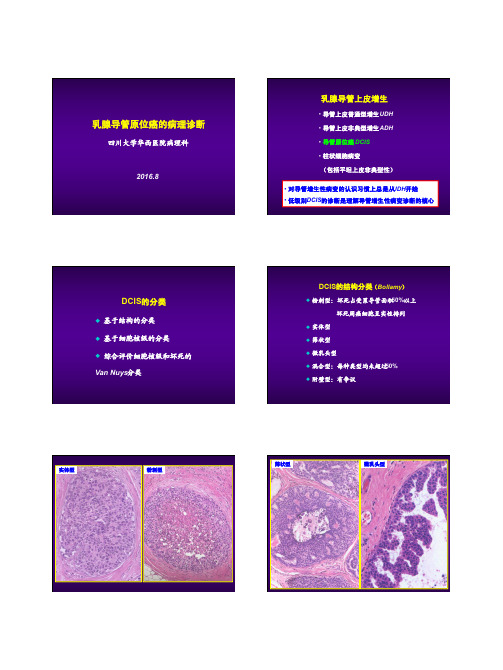
乳腺导管原位癌的病理诊断四川大学华西医院病理科2016.8乳腺导管上皮增生•导管上皮普通型增生UDH•导管上皮非典型增生ADH•导管原位癌DCIS•柱状细胞病变(包括平坦上皮非典型性)•对导管增生性病变的认识习惯上总是从UDH开始•低级别DCIS 的诊断是理解导管增生性病变诊断的核心DCIS的分类u 基于结构的分类u 基于细胞核级的分类u 综合评价细胞核级和坏死的Van Nuys 分类DCIS的结构分类(Bollamy)u粉刺型:坏死占受累导管面积50%以上坏死周癌细胞呈实性排列u实体型u筛状型u微乳头型u混合型:每种类型均未超过50%u 附壁型:有争议实体型粉刺型筛状型微乳头型所谓的“附壁型”2012 WHO:只有那些伴有高级别核改变的病变才能诊断为DCIS导管原位癌核级(低、中、高)Schnitt低级别DCIS的简要诊断标准u增生细胞纯化(特别是细胞核)u细胞分布较均匀u特征性的结构模式u病变往往累及多支导管低级别DCIS的结构模式u结构特点:1 筛状结构:细胞群内出现“冲凿”样圆形或椭圆形的腔隙,腔缘光滑、有张力、均匀分布2 微乳头:纺锤状(基底细,体部膨大)、量多体积大3 僵直的细胞搭桥、有张力的拱形结构4 实体结构:依赖对细胞形态的判断Tavassoli筛状结构有张力、均匀分布WHO纯化;细胞分布均匀WHO微乳头状结构WHO细胞纯化细胞纯化纺锤状Tavassoli僵直的细胞搭桥有张力的拱形结构WHO低级别DCIS诊断的量化标准u至少有两个导管完全受累(Page)u受累导管合计>2mm(Tavassoli )中等级别DCISu显示低核级,但部分导管含有坏死u 显示中等核级,坏死可有或无导管原位癌核级(低、中、高)Schnitt高级别DCISu核明显多形、极向紊乱、分布不均,核形不规则,染色质粗糙,核仁明显u核分裂常见,但不是诊断必需u呈单层、微乳头、筛状或实性u坏死常呈粉刺样,但并非必需u即使一个导管有典型形态学特点也足够诊断高级别核大汗腺型DCIS少见亚型u大汗腺型u梭形细胞型u印戒细胞型u透明细胞型u小细胞型u二态型u黏液型u鳞状细胞型u 囊性高分泌型梭形细胞型印戒细胞型透明细胞型二态型小细胞型p63黏液型囊性高分泌型鳞状细胞型如何报告“导管原位癌”• 核级(低、中、高)、坏死、钙化、组织学模式• 导管原位癌(高核级伴坏死、钙化,筛状、微乳头状结构)鉴别诊断UDH的简要诊断标准u 增生细胞间腔隙不规则,分布不均匀,多位于周边u 细胞核分布不均匀、有重叠(合体状)u 细胞形态多样,非纯化(杂)结构–细胞间腔隙WHO旺炽性增生florid hyperplasiaSchnitt 结构–细胞间腔隙结构 - 细胞间腔隙细胞 - 合体状Rosen细胞重叠、分界不清、合体状Schnitt细胞呈梭形,合体状Schnitt细胞呈梭形,流水状细胞形态多样,非纯化WHO 微乳头结构Schnitt细胞搭桥Schnitt TDLU内的UDHRosenUDH 伴有粉刺样坏死SchnittUDH 伴有坏死UDH 中有无肌上皮细胞成分?SMA calponinp63u 仅根据SMA 等肌上皮标记在导管增生性病灶中呈阴性表达就否定UDH 可能会导致误诊u UDH 偶尔表达p63Boecker ,J Pathol 2002绿色:SMA 红色:Ck8/18/19Note that the myoepithelial cells are not acomponent of the intraductal cell proliferation普通型增生Boecker :5 种细胞,即定向干细胞、腺中间细胞、腺上皮终端细胞、肌上皮中间细胞和肌上皮终端细胞仅表达高分子量CK ,如CK5/6仅表达CK8/18/19仅表达SMA 等表达CK5/6、CK8/18/19表达CK5/6、SMACK5/6UDH的增生细胞群确实含有多种成分,包括定向干细胞、腺中间细胞和腺终端细胞,但未发现具有肌上皮特点的细胞参与其中UDH ADHCK5/6DCIS DCISER染色UDH DCISWHO UDH DCIS UDHDCISADH 的传统诊断标准u 增生病灶出现低级别DCIS 的部分(不是全部)特征即可诊断ADH (不满足DCIS 定性标准)u 如果增生病灶具有低级别DCIS 的全部特征(包括细胞学和结构),只要不超过两个导管或大小不超过2mm ,也诊断ADH (不满足DCIS 定量标准)u 当诊断DCIS 有迟疑时则诊断ADHTavassoli :具有低级别DCIS 细胞学和结构特征的病变仅部分累及单个或多个导管非典型增生增生导管部分区域出现低核级DCIS 的特征Schnitt SchnittSchnitt• 变迁中的定量标准(ADH )- 1985 Page: < than 2 separate spaces (i.e., 1 space) - 1990 Tavassoli + Norris: < or = 2mm - 1998 Jensen and Page: 2-3mm - 2003 Page <4-5mm(2012 WHO :低级别DCIS 发生浸润性癌的时间间隔平均超过15年)• 多数情况下,是在TDLU受累以后使用• 仅测量形成充分的病灶• 病变导管呈纵切面时,不使用此标准SchnittSchnitt Koerner中等核级DCIS SchnittWHOADH是否存在分度(程度划分)?•完全受累(具有低核级DCIS特征),但范围小 - 重度•部分区域具有低核级DCIS特征,多病灶 - 中/重度•部分区域具有低核级DCIS特征,单病灶 - 轻/中度•导管内少数细胞具有纯化特征 - 轻度•如:borderline atypical d uctal hyperplasia / low-gradeductal carcinoma in situmarked ADH / severe ADH / extensive ADHfocal ADHRosen’ breast pathologySchnitt’ breast pathology2012 WHO易被误诊为浸润性癌的DCIS改变u DCIS的小叶癌化(lobular cancerization)u DCIS假浸润:纤维化导致DCIS形态不规则炎细胞浸润背景u DCIS出芽改变u DCIS累及腺病(硬化性、小管型、大汗腺型)和RS等u人工现象:如穿刺导致DCIS 细胞移位小叶癌化小叶癌化炎细胞浸润DCIS出芽改变貌似浸润癌的DCISHER2 DCIS假浸润DCIS假浸润DCIS假浸润DCIS累及腺病DCIS假浸润DCIS累及腺病穿刺导致DCIS细胞移位腺泡型浸润性小叶癌貌似DCIS 的癌栓特殊病例来自张祥盛老师女 38岁 左乳3cm肿物p63Calponin左腋窝淋巴结20/23、左侧锁骨下11/11有转移呈扩张性侵袭 / 膨胀性浸润的癌Bhargava, Dabbs缺乏肌上皮层的“DCIS”p63SMMHC病例p63ER ERPRPR病理诊断送检组织中查见癌,癌组织呈DCIS 形态,但部分肿瘤导管周围缺乏肌上皮层,不能排除其为呈膨胀性生长的浸润癌小 结• 乳腺DCIS 的病理诊断有章可循,但无绝对标准;诊断的主观性客观存在• 量化标准的运用• 基底型CK 的诊断价值• 真假浸润(包括DCIS 缺失肌上皮)致 谢u 华西医院病理科各位老师、同事!u 吴蕴 M.D. Anderson Cancer Center, USAu唐平 University of Rochester Medical Center, USA。
中国乳腺导管原位癌病理诊断共识(2022版)

中国乳腺导管原位癌病理诊断共识(2022版)摘要乳腺导管原位癌具有独特的临床特征、组织形态学和分子特征。
本共识全面阐述了导管原位癌相关生物标志物的临床意义,旨在提高导管原位癌标本取材、病理评估以及相关检测的准确性和可重复性,从而促进导管原位癌病理报告内容的规范化,为临床治疗和预后评估提供可靠依据。
正文乳腺导管原位癌(ductaIcareinomainsitu,DCIS)是一种乳腺非浸润性上皮细胞恶性肿瘤,局限于导管-小叶系统,显示不同程度的结构异常和细胞核级。
在临床、影像、组织形态及基因改变上均具有异质性,有进展为浸润性癌的风险,但并非必然。
随着乳腺影像学检查的普及,DC1.S检出率明显增加,占所有新发乳腺癌的20%~25%°由于DC1.S生物学行为不一,给临床治疗带来挑战。
正确诊断DC1.S对于临床治疗方案的确定和患者预后的评估至关重要。
2016年中国乳腺原位癌诊疗共识专家组制定了《乳腺原位癌诊疗专家共识》,但目前还缺乏相应的中国乳腺DCIS病理诊断规范。
本共识由中华医学会病理学分会乳腺疾病学组、中国抗癌协会肿瘤病理专业委员会乳腺肿瘤学组和中国临床肿瘤学会肿瘤病理专家委员会组织编写,由病理医师和临床医师共同制定,涵盖DCIS标本取材、肿瘤生物标志物检测及病理诊断报告内容等各环节规范化操作要点,旨在使DC1.S的病理诊断更精准,为相关临床诊疗提供依据。
一、乳腺DCIS取材及切缘评估1.瘤床取材:手术科室应提供详细的临床病史和病理信息,包括病变解剖部位(左右侧及象限)、影像学检查结果、有无术前穿刺活检及病理诊断、有无乳腺癌病史和家族史等。
对于乳腺广泛切除或区段切除标本,外科医师应用缝合线或其他标志物作解剖学定位(如上、下、内、外侧)。
病理取材医师应涂染料标记切缘,并结合临床标记和影像学检查进行肿物定位,间隔5~10mm将整个标本平行切开,作好标记。
有条件的单位可对标本进行X线照相。
若病变区域的直径<5cm,建议全部取材;若病变区域的直径25cm,需间隔1Cm至少取材一块组织,有条件的单位尽可能更多取材。
乳腺硬化性腺病冰冻病理诊断分析

乳腺硬化性腺病冰冻病理诊断分析乳腺硬化性腺病(Mammographic Sclerosing Adenosis,简称SA)是一种常见的乳腺疾病,也是乳腺透视的常见异常表现之一。
本文主要目的是通过冰冻病理诊断分析乳腺硬化性腺病的特点和诊断要点。
乳腺硬化性腺病是一种特征性的乳腺病理改变,主要由于乳腺管、管腔周围的腺体被大批成簇的纤维组织包围,并且出现较为明显的纤维化和增生。
该病变常见于乳腺导管周围的终末管腺体,特别是在乳腺的一侧或两侧中央部位。
乳腺硬化性腺病的临床特点主要有:乳房肿块、皮肤增厚、纤维性导管扩张及导管内白色或乳白色分泌物等。
乳腺硬化性腺病的冰冻病理诊断主要依靠镜下观察硬化性腺病的典型组织学特点。
一般情况下,冰冻切片的处理程序和方法与常规病理切片相似。
取得切除标本后,将其快速冷冻,制备成为薄片,并在显微镜下进行观察和分析。
而纤维化在冰冻切片中是易于辨认的,通常呈现出纤维组织的增生和包围导管的特点。
硬化性腺病的冰冻切片还可观察到管腔非典型增生的现象,其中大约三分之一的病例,其炎性因素也可能伴随其间。
乳腺硬化性腺病与乳腺纤维瘤在冰冻切片中有时很难鉴别。
不过,乳腺纤维瘤与硬化性腺病有明显的区别,主要体现在纤维瘤的纤维组织周围不包围导管。
乳腺硬化性腺病通常表现出更明显的纤维组织过度增生,而乳腺纤维瘤的纤维组织增生则较为轻微。
在冰冻切片的鉴别诊断过程中,我们应该结合患者的临床情况,全面分析病变,以获得准确的诊断结果。
乳腺硬化性腺病的冰冻病理诊断分析可以帮助我们了解该病变的组织学特点和临床意义,以便进一步指导临床治疗的选择和预后的评估。
通过冰冻病理诊断分析可以发现该病变与其他乳腺病变的区别和联系,提高对乳腺疾病的鉴别诊断能力,为临床工作提供更多的参考依据。
丁华野

导管扩张期
• • • • • • • 乳头后方可触及增粗变硬的乳管 乳头可挤压出“奶酪”样物质 乳头溢液也可带有血迹 乳晕下输乳管及大导管高度扩张 腔内充满粘稠物 管壁纤维性增厚 管周不同程度的炎细胞浸润
H9
H117
肿块期
• • • • • • 皮肤红肿、扪及肿块,可与皮肤粘连 乳头回缩等,腋下淋巴结可增大 大-中等导管扩展,腔内充有积聚物 导管壁的炎细胞浸润和纤维组织增生 导管破坏,内容物进入周围间质 炎症反应,组织坏死,病变融合成肿块
肉芽肿性小叶性乳腺炎
• • • • • • • • 认识不足,缺乏重视 缺乏公认的诊治标准与方法 临床表现及影像学与癌相似 病理常不能明确诊断 临床得不到及时針对性治疗 通常切开引流,抗生素冶疗 反复发作,迁延不愈,十分痛苦 正确的诊断治疗需要多学科协作
• 乳腺癌与肉芽肿性小叶性乳腺炎
• 乳腺红肿、疼痛 • 按一般炎症切开引流
冰806
冰
冰
冰
冰
发病机制
• • • • • • • • 病因不清,多数学者支持自身免疫 高泌乳素血症 口服避孕药 抗精神病类药物 垂体腺瘤 未哺乳 外伤 血IgG4升高
治疗及预后
• 首选治疗方式观点不一 • 手术切除彻底,不易复发 • 手术、激素、姑息治疗 • 抗生素无效 • 盲目切开引流,难愈合,形成窦道 • 治疗不当不及时,易复发,迁延不愈
• 肉芽肿性小叶性乳腺炎手术前后
有兴趣可参考下列文献
• 乳腺某些少见炎症性病变的诊断及鉴别诊断。乳腺 病理诊断及鉴别诊断,人民卫生出版社,2014.5 • 肉芽肿性小叶性乳腺炎的临床病理观察。中华病理 学杂志,2010,39(10):678 • 肉芽肿性小叶性乳腺炎伴导管扩张症临床病理观察 。中华病理学杂志,2013,42(10):678 • 肉芽肿性小叶性乳腺炎与抗精神病药物的相关性探 讨。诊断病理学杂志,2014,21(7):448 • 肉芽肿性小叶性乳腺炎伴发乳腺导管扩张症及结节 性红斑4例临床病理分析。诊断病理学杂志, 2014,21(8):488
乳腺非典型导管上皮增生的病理学分类与随访观察策略

乳腺非典型导管上皮增生的病理学分类与随访观察策略引言乳腺非典型导管上皮增生是一种常见的乳腺疾病,它在女性中的发生率较高。
该疾病是乳腺癌的前期病变之一,因此对其进行及时的诊断与随访观察具有重要意义。
本文旨在详细介绍乳腺非典型导管上皮增生的病理学分类和随访观察策略。
乳腺非典型导管上皮增生的病理学分类乳腺非典型导管上皮增生是一种异形增生,其病理学分类主要包括以下几种类型:1. 非典型导管上皮增生非典型导管上皮增生是乳腺非典型增生的一种常见形式,它主要表现为导管内上皮的异型增生。
病理学上,非典型导管上皮增生的细胞形态与正常上皮相比较为异常,细胞核呈现出异型性和增生特征。
2. 非典型导管内乳头状瘤非典型导管内乳头状瘤是一种相对罕见但具有较高恶性潜能的乳腺非典型增生。
它主要表现为导管内乳头状结构的异常增生,并且伴有细胞核异型性和增生。
该病理类型的患者需要特别密切的随访观察。
3. 非典型导管泡瘤状增生非典型导管泡瘤状增生是一种与浸润性导管癌密切相关的乳腺非典型增生类型。
它主要表现为导管内乳头状结构的扩张和囊变,并且伴有导管细胞核的异型性和增生。
该类型病理学改变的存在提示了潜在的恶性转化风险。
乳腺非典型导管上皮增生的随访观察策略乳腺非典型导管上皮增生的随访观察策略主要包括以下几个方面:1. 临床随访观察对乳腺非典型导管上皮增生确诊患者需要定期进行临床随访观察,以及乳腺自我检查。
随访观察的频率根据患者的具体情况而定,通常建议每6个月进行一次随访。
2. 影像学检查建议对乳腺非典型导管上皮增生患者进行乳腺超声检查或乳腺MRI检查,以及每年进行一次乳腺X线摄影检查。
这些影像学检查有助于评估病变病理学特征的变化,并对病变是否恶变进行进一步的判断。
3. 组织学评估定期进行组织学评估是乳腺非典型导管上皮增生患者随访观察的重要环节。
通过穿刺活检或手术活检获取组织标本,进行细胞学或病理学检查,以了解病变的进展情况。
4. 个体化治疗策略根据每个乳腺非典型导管上皮增生患者的具体情况,制定个体化的治疗策略,包括手术切除、药物治疗等。
p63、角蛋白及肌动蛋白在乳腺导管增生性病变中的表达及应用价值

在乳 腺 腺 管 这 种 表 达 方 式 支持 5个 细胞 假 说。 C 56 3 g 1 K / 、4 E 2在 A H 和 D I D CS中基 底 侧 、 巢 周 癌 呈 连续表 达 , 阳性 率分别 为 6 . 0 、4 3 %和 7 . 5 0 % 9 .0 5
表 3 4种 标 记 在 U H、 DH、 I 、B 增 生 腺 D A DC S I C 上 皮 细 胞 中 的表 达
C 8作 对 照 比较研 究 , 果显 示 ,K / 、 K 4 E 2 K 结 C 56 C 3  ̄ 1 和 C 8在 正 常乳腺 和 U H的 阳性 表达 率没 有 统计 K D 学差 异 , 但在 表达 部位 有所 不 同 , 两者 在腺 腔基底 前 侧 或腺腔 中灶 性表 达 , C 8在 腺腔 面 连续 或 弥漫 而 K
注: 与同组织类型其他指标比较, 00 P< .5
系或肌 上皮 细胞 系分 化 , 肿 瘤 的发生 常 是 单 克 隆 而 增 生 , 以 , 底 型角蛋 白在 乳腺增 生性 病变 鉴别诊 所 基
断 中有 意义 , 目前 已有 相 关 文献 报 道 。本 文 选 用基 底 型/ 分 子 角 蛋 白 C 5 6 和 3  ̄ 1 高 K/ 4 E 2及 腺 腔 型
35
山东 医药 2 1 第 5 0 2年 2卷第 3 3期
表2 4种标记在正 常乳腺 、 D D I A H、 C S基底膜侧
M E 的表 达 情 况 C
来 ; : 细胞 假说 , 近研究 表 明 , ③ 5个 新 还存 在 着 定 向
乳腺导管内肿瘤的病理分析

型导管内乳头状瘤12例,其中6例伴发于 导管内乳头状癌,表现为≥10%~<90% 的乳头覆盖上皮呈不典型增生改变。(3)导 管内乳头状原位癌20例,主要表现为乳头 区肌上皮层完全缺失、乳头覆盖上皮呈现 低级导管的原位癌型病变、或者2种病变 类型兼有。综上所述,EliVision法染色观 察肌上皮和导管腺上皮进行不同类型增 生性病变的诊断和鉴别还是很有价值。
【收稿日期】2012-02-19
160 中国卫生产业
1 资料与方法 1.1 一般资料
选取我院2009年1月至2011年3月病 理科诊治的乳腺导管内肿瘤患者60例作 为本次观察对象,年龄35~50岁,平均年 龄(41.5±10.0)岁,根据WHO分类(2003) 和Tavassoli等(1999、2003)有关标准,导 管内乳头状瘤28例,非典型导管内乳头状 瘤12例,导管内乳头状原位癌20例。 1.2 方法
medical laboratory sciences 医学检验
CHINA HEALTH INDUSTRY
乳腺导管内肿瘤的病理分析
曹敏 (白城中医院 吉林白城 137000)
Hale Waihona Puke 【摘要】目的 探讨乳腺导管内肿瘤的病理情况。方法 分析我院乳腺导管内肿瘤患者临床资料,通过察冷冻切片快速EliVision法
检测。结果 (1)导管内乳头状瘤28例,通过镜检可见到小管内有纤维-脉管轴心和扩张性导管的乳头状瘤,其是双层构型,主要包
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
组织病理学
Ø 低核级 DCIS:小的单一性细胞组成,拱形、微 乳头状、筛状或实性。可呈微腺泡状,菊形团样 。核大小一致,染色质均匀,核仁不明显,核分 裂像罕见。微钙化呈砂砾体型,坏死议 不常见。 会 Ø 中等核级 DCIS:细胞大小、形态和分 布轻到中 夏 宁 等程度改变,染色质粗细不均 ,核仁明显或不明 N P 分裂像,点状或粉刺 显。细胞极向不明显。见核 C 样坏死。见少许微钙 化 理 Ø 高核级 DCIS年 :病 高度非典型性的细胞,实性、筛 5 1 状或微乳头 状 。核明显多形性,极向差,染色质 0 2 粗大、块 状、形状及分布不规则,核仁明显,核 分裂像常见。粉刺样坏死特征,周围实性增生的 大而多形性瘤细胞。少数病例为管腔内只被覆单 层附壁样生长的高度非典型细胞,常见微钙化。 高细胞核级别 DCIS 大小通常>5mm。
议 会
平坦型上皮非典型增生
( Flat epithelial atypia,FEA )
议 Ø 发生于终末导管小叶单位(TDLU会 )的肿瘤性病变 夏 Ø 乳腺柱状上皮的病变的一种类 型 宁 N P C Ø 原有上皮细胞被单层或 多层低级别(形态单一) 理 的非典型性细胞所替代 。 病 年 5 Ø 同义词:伴 非典型性的柱状细胞改变, 伴非典型 1 0 2
(Atypical ductal hyperplasia,ADH )
议 Ø 累及终末导管小叶单位、分布均匀,单 一形态 会 上皮细胞增生 夏 宁 N Ø 一组同时具有特殊组织结构和细胞学形态的病 P C 变,发生乳腺癌的 危险性增加。 理 病 Ø 介于良恶性之 间,发生于终末导管小叶单位内 年
5 1 20
2
年 5 01
理 病
N P C
夏 宁
议 会
中级别,粉刺样坏死
性的柱状细胞增生
组织病理学
Ø 单层或多层上皮细胞,缺乏极向。核圆形,一致,核仁不 明显,与低级别DCIS细胞形态非常相似 Ø 立方形或柱状细胞,有顶浆分泌。见微小细胞簇或突起, 无明显的拱形、上皮桥和微乳头结构 Ø 腺泡不同程度扩张,结构尚规则,可含分泌物或絮状物, 常伴微小钙化。有些间质见淋巴细胞的浸润 Ø 病变与同时存在的小叶瘤变 、ADH 、低级别DCIS和低级 别浸润癌如小管癌等关系密切 。 Ø FEA 的ER阳性着色强而弥漫,但HER2无过表达 Ø 乳腺癌前驱病变或危险因素,FEA 有重要临床意义,低 级别乳腺肿瘤发生发展过程中的早期病变
议 会
柱状细胞病变和增生
( Columnar cell changes and hyperplasia ,H)
议 Ø 特殊上皮化生或增生性病变 会 夏 Ø 柱状细胞改变和柱状细胞增生是 发生于终末导管 宁 N 小叶单位(TDLU)的病变, 其特征是被覆柱状 P C 程度的扩张。 上皮细胞的腺泡增大 伴不同 理 病 Ø 同义词:盲管型腺病 ;小叶柱状上皮改变;柱状 年 5 1 上皮化生 ; 增生性小叶 扩张; 增生性小叶单位增 0 2 大;小叶增大伴柱状上皮改变
议 乳腺增生性病变 会 理 长江大学附属第一医院 病 年 荆州市第一人民医院 5 1 0 2 李军川
1
N P C
夏 宁
乳腺成分
乳腺实质:导管、小叶
20
乳腺间叶:脂肪、纤维、 年 15 血管、神经等
理 病
N P C
夏 宁
议 会
2
乳腺疾病
非肿瘤性病变: 发育异常 炎症 肿瘤:良性 夏 宁
议 会
2
年 增生性病变 5 1 0
2
年 5 01
理 病
N P C SMA标记导管外周存在连续
的肌上皮细胞
夏 宁
议 会
27
平坦型上皮非典型增生
Ø 在CCC或CCH的组织结构基础上,上皮 议 细胞显示非典型性。
宁 N Ø Tavassoli根据非典型性 P 程度可以分为轻 C 度、中-重度平坦型上皮非典型性 。轻度 理 病 :DIN1,重度 :DIN3 年 5 1 20
2
年 5 01
理 病
N P C
夏 宁
议 会
柱状细胞呈现复层 (>2层) 局部细胞核过染、 拥挤和重叠
2
年 5 01
理 病
N P C
夏 宁
议 会
柱状细胞可呈小丘状、簇状或微乳头状 细胞顶端常有明显的胞突 腺腔内亦常见有丰富的絮状分泌物和钙化
夏 宁 N 平坦型上皮非典型增生 CP 理 病 年 5 1 0 2
仅见1个导管上皮不典型性
2
年 5 01
理 病
N P C
夏 宁
议 会
累及相邻2个导管,细胞均 匀一致,显示不典型性
中心区较小单形性细胞增 生,似成熟现象
36
2
年 5 01
理 病
N P C
夏 宁
议 会
增生细胞形态单一,呈不 典型结构模式
ADH伴钙化
2
年 5 01
理 病
N P C
夏 宁
议 会
38
ADH伴不典型细胞,除外DCIS
柱状细胞变 (Columnar cell change,CCC)
2
年 5 01
理 病
N P C
夏 宁
议 会
柱状细胞衬覆在扩张的 终末导管单位,垂直于 基底膜,
2
年 5 01
理 病
N P C
相顶 对浆 规分 则泌 的泡 卵 圆 形 胞 核
夏 宁
议 会
柱状细胞增生 columnar cell hyperplasia,CCH
组织病理学
Ø 二级管腔或筛孔状结构。分布于周边,裂隙状,有些实性 增生,出现微乳头状结构 Ø 上皮分布紊乱,排列紧密,存在成熟现象 Ø 中央细胞流水样或合体样排列。排列不规则,界限不清, 核大小不一,见核沟及核内包涵体 Ø 上皮桥薄而伸展或弯曲,细胞核分布不均匀。围绕二级管 腔的上皮细胞核往往平行排列于管腔 Ø 常见上皮细胞、 肌上皮细胞甚至是化生的大汗腺细胞混杂 。见泡沫状细胞、钙化及罕见灶状坏死。偶见核分裂像 Ø 混合性免疫表型,CK5/6 和 CK34βE12等表达 。ER 在 UDH 中的染色不均匀
2
年 5 01
理 病
N P C
夏 宁
议 会
多个导管
2
年 5 01
理 病
N P C
夏 宁
议 会
细胞流水样排列
成熟现象
成分多样
5 1 20
病 年
边窗 理
CP 筛孔
周边见肌上皮 N
夏 宁
议 会
N 细胞结构无异型性 P 纤细细胞桥 C 2
夏 宁
议 会
年 5 01
理 病
14
夏 宁 柱状细胞病变和增生 N CP 理 病 年 5 1 0 2
Ø 分级的临床价值有待证实
会 夏
轻度不典型
2
年 5 01
理 病
N P C
夏 宁
议 会
5 1 20
病 年
中-重度不典型 理
N P C
夏 宁
议 会
免疫表型
u CCC和FEA细胞表达CK19,不表达34 BE-12 和 议 CK 5/6 会 u bcl-2 蛋白强表达。 u
u ER和PR强表达 。
u 5% -50% 的细胞 年 表达cyclin D1
2
年 5 01
理 病
N P C
夏 宁
议 会
扩张腺管衬立方上 皮,腔内有钙化物
FEA
导管周围见SMA标记肌上皮细 胞向腺上皮方向突起
上皮柱状,见顶泌突起,腔内有 絮状分泌物
2
年 5 01
理 病
N P C
夏 宁
议 会
25
5 1 20
病 年
N P FEA C 理
夏 宁
议 会
FEA
上皮2-3层,柱状,中度异型, 胞质顶泌突起,簇状乳头状突起
组织病理学
Ø 病变位于 TDLU Ø 细胞形态单一,分布均匀,缺乏流水样、 旋涡状 议 及细胞核重,核圆形、卵圆形,呈会 微乳头、丛状 夏 、叶状、拱形、桥状、实性、筛 状 宁 N Ø ADH 与低级别DCIS组织学形态 相似。旺炽型UDH P C 不应诊断为 ADH 理 Ø 低级别 DCIS常用 的量化标准是至少有两个导管完 病 年 全受累或受累 导管 合计>2mm 5 1 0 2 Ø 粗针穿刺活检的标本,ADH 和范围较小的低级别 DCIS 的鉴别诊断尤其要谨慎。可将其诊断为 ADH 或“非典型导管内增生性病变”
5 1 0 抗原不表达,其余的病例仅个别细 75% 的2 Ki-67
理 病
N P C
夏 宁
胞Ki-67阳性,表明细胞增殖率很低。
柱状细胞病变和平坦型上皮非典型增生诊断模式图
2
年 5 01
理 病
N P C
夏 宁
议 会
夏 宁 N 非典型导管增生 CP 理 病 年 5 1 0 2
议 会
非典型导管增生
16
病理特点
Ø 被覆柱状上皮细胞的腺泡增大伴扩张,顶浆分泌突 起 议 Ø 腺泡形态不规则,核卵圆形,垂直会 于基底膜排列 夏 Ø 管腔内常含有分泌物和/或微钙化灶 宁 N Ø 肌上皮可以很明显,特化的间质细胞成分 丰富 P C Ø 上皮细胞只有一层或 两层时为柱状细胞病变,超过 理 两层的分层或突起时 为柱状细胞增生 病 年 5 Ø 与其它良性病变 并存。与小叶肿瘤关系非常密切 1 0 Ø 强而弥漫2 的ER 阳性,无 HER2 的过表达 Ø 危险性很低
理 病
C
PN
恶性
3
乳腺增生性病变
导管增生 1. 普通型导管 增生 2. 柱状细胞改 变和增生 3. 平坦型上皮 非典型增生 4. 非典型导管 增生 5. 导管原位癌 小叶增生 上皮增 生 腺病 1.硬化性腺病 2.大汗腺腺病 3.小管型腺病 4.微腺性腺病 5.分泌性腺病 6.放射状硬化 性病变 1. 议 会 2. 3. 间叶成分 增生 假血管瘤 样间质增 生 脂肪坏死 手术后局 灶性纤维 化疤痕 结节性筋 膜炎 良性血管 病变
