酸胺缩合反应的经验总结
酸胺缩合反应机理

酸胺缩合反应机理酸胺缩合反应是有机合成中一种常见的反应类型,它可以用来合成酰胺化合物。
本文将详细介绍酸胺缩合反应的机理以及其应用。
一、酸胺缩合反应的机理酸胺缩合反应是通过酸催化下的胺与酸酐反应生成酰胺的过程。
该反应通常是在室温下进行,催化剂可以是无机酸(如硫酸、盐酸等)或有机酸(如甲酸、醋酸等)。
具体而言,酸胺缩合反应的机理可以分为以下几个步骤:1. 酸催化下的酸酐活化:首先,酸催化剂与酸酐发生反应,生成酸酐的活化物种。
这个步骤是酸胺缩合反应的关键,它使得酸酐具有进一步反应的活性。
2. 胺的亲核进攻:活化的酸酐与胺发生亲核进攻反应,胺中的氮原子攻击酸酐中的碳原子,形成酰胺中间体。
3. 脱水:酰胺中间体经过脱水反应,使得水分子从中间体中离去,生成最终的酰胺产物。
总的来说,酸胺缩合反应是通过酸催化下酸酐的活化、胺的亲核进攻和脱水三个步骤完成的。
这个反应机理在有机合成中得到了广泛的应用。
二、酸胺缩合反应的应用酸胺缩合反应在有机合成中有着重要的地位,它可以用来合成各种酰胺化合物。
酰胺是一类重要的有机化合物,具有广泛的应用价值。
1. 生物活性物质合成:酰胺是许多生物活性物质的结构基础,如药物、农药等。
通过酸胺缩合反应,可以合成具有特定生物活性的酰胺化合物,用于药物研究和开发。
2. 聚合物合成:酰胺是一类重要的聚合物单体,通过酸胺缩合反应,可以合成各种酰胺聚合物,如聚酰胺、聚酰胺酯等。
这些聚合物具有良好的力学性能和热稳定性,广泛应用于材料科学领域。
3. 有机合成:酸胺缩合反应可以用于合成具有特定结构和功能的有机分子,如含氮杂环化合物、天然产物等。
这些化合物在有机合成和药物研究中具有重要的意义。
酸胺缩合反应是一种常见的有机合成反应,它通过酸催化下的胺与酸酐反应生成酰胺。
该反应机理包括酸酐的活化、胺的亲核进攻和脱水三个步骤。
酸胺缩合反应在有机合成中具有广泛的应用,可以用于合成各种酰胺化合物,如药物、聚合物和有机分子等。
酸胺缩合反应经验总结
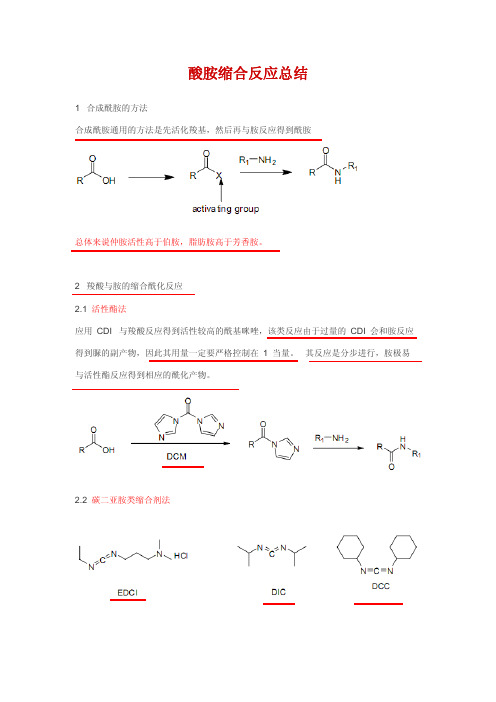
酸胺缩合反应总结1 合成酰胺的方法合成酰胺通用的方法是先活化羧基,然后再与胺反应得到酰胺总体来说仲胺活性高于伯胺,脂肪胺高于芳香胺。
2 羧酸与胺的缩合酰化反应2.1活性酯法应用 CDI 与羧酸反应得到活性较高的酰基咪唑,该类反应由于过量的 CDI 会和胺反应得到脲的副产物,因此其用量一定要严格控制在 1 当量。
其反应是分步进行,胺极易与活性酯反应得到相应的酰化产物。
2.2 碳二亚胺类缩合剂法使用该类缩合剂一般需要加入酰化催化剂或活化剂如,DMAP , HOBt ,等等,主要因为反应的第一阶段所生成的中间体不稳定,若不用酰化催化剂转化为相应得活性酯或活性酰胺,其自身易成脲。
EDCI HOBT,一般用的较多,搭配使用,有时酸的位阻较大或者连有吸电子基团反应或停留在活性酯这一步,一般加碱,2-3 当量的 DIEA,一般以二氯甲烷为溶剂,溶解性不好时也可用 DMF。
(有时加催化量的DMAP,针对有位阻的反应)。
这类缩合剂活性相对要差一些,一般需要和酸先活化 1 小时,再将胺加入。
2.3 鎓盐类的缩合剂法鎓盐类的缩合剂活性较高,从盐的种类分为两类一类是碳鎓盐,目前常用的 HATU,HBTU,等等。
另一类为鏻鎓盐,如 PyBOP。
HATU缩合效果较好但价格较贵, PyBOP 是我们常用的缩合剂中活性最高的,一般在其他方法不反应的条件下考虑。
3 常见副产物以及处理方法3.1 碳二亚胺类副产物以 EDCI 为例子,在没有 HOBT 存在的情况下,反应活性酯容易自身重排成脲:所以在反应中加入HOBT 以形成相对稳定的活性中间体:其反应后生成的脲水溶性很好,通常在反应干净的情况下,可以用稀酸洗掉,不须进一步纯化即可得到干净的产品。
在库反应中,此类缩合剂最常使用的是 EDCI,因其极性相对较大,在分离过程中不易与产物包裹在一起。
不过在产物极性大的情况下,分离过程中可能会带有 174 的杂MS。
3.2 鎓盐类副反应以 HATU 为例,在局部浓度不均匀的情况下,会产生以下副产物:所以在反应的时候,一般的加料顺序,应该是将酸,碱以及HATU 加到溶剂中,搅拌均匀再将胺加入,以避免此类副产物。
【亲测好评】酰胺缩合经验总结
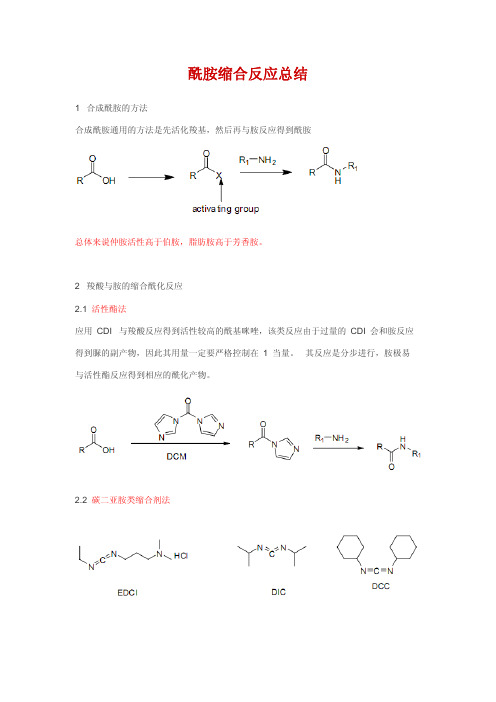
酰胺缩合反应总结1 合成酰胺的方法合成酰胺通用的方法是先活化羧基,然后再与胺反应得到酰胺总体来说仲胺活性高于伯胺,脂肪胺高于芳香胺。
2 羧酸与胺的缩合酰化反应2.1活性酯法应用 CDI 与羧酸反应得到活性较高的酰基咪唑,该类反应由于过量的 CDI 会和胺反应得到脲的副产物,因此其用量一定要严格控制在 1 当量。
其反应是分步进行,胺极易与活性酯反应得到相应的酰化产物。
2.2 碳二亚胺类缩合剂法使用该类缩合剂一般需要加入酰化催化剂或活化剂如,DMAP , HOBt ,等等,主要因为反应的第一阶段所生成的中间体不稳定,若不用酰化催化剂转化为相应得活性酯或活性酰胺,其自身易成脲。
EDCI HOBT,一般用的较多,搭配使用,有时酸的位阻较大或者连有吸电子基团反应或停留在活性酯这一步,一般加碱,2-3 当量的 DIEA,一般以二氯甲烷为溶剂,溶解性不好时也可用 DMF。
(有时加催化量的DMAP,针对有位阻的反应)。
这类缩合剂活性相对要差一些,一般需要和酸先活化 1 小时,再将胺加入。
2.3 鎓盐类的缩合剂法鎓盐类的缩合剂活性较高,从盐的种类分为两类一类是碳鎓盐,目前常用的 HATU,HBTU,等等。
另一类为鏻鎓盐,如 PyBOP。
HATU缩合效果较好但价格较贵, PyBOP 是我们常用的缩合剂中活性最高的,一般在其他方法不反应的条件下考虑。
3 常见副产物以及处理方法3.1 碳二亚胺类副产物以 EDCI 为例子,在没有 HOBT 存在的情况下,反应活性酯容易自身重排成脲:所以在反应中加入HOBT 以形成相对稳定的活性中间体:其反应后生成的脲水溶性很好,通常在反应干净的情况下,可以用稀酸洗掉,不须进一步纯化即可得到干净的产品。
在库反应中,此类缩合剂最常使用的是 EDCI,因其极性相对较大,在分离过程中不易与产物包裹在一起。
不过在产物极性大的情况下,分离过程中可能会带有 174 的杂MS。
3.2 鎓盐类副反应以 HATU 为例,在局部浓度不均匀的情况下,会产生以下副产物:所以在反应的时候,一般的加料顺序,应该是将酸,碱以及HATU 加到溶剂中,搅拌均匀再将胺加入,以避免此类副产物。
(整理)羧酸与胺的缩合酰化反应

羧酸与胺的缩合酰化反应王露化工与制药专业 1105班学号110150151指导教师刘雪凌老师摘要合成是制药的基本方法,也是很重要的方法,人类对药物的需求很大,要不断的创新、研发新药,合成是其中必不可少的方法,本文介绍了常见合成酰胺的方法,合成酰胺通用的方法是先活化羧基,然后再与胺反应得到酰胺。
其中羧酸与胺的反应是合成酰胺的重要方法【5】。
这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏【1】。
关键词:合成酰化活化前言药物对于我们任何一个人来说都不陌生,而且离不开。
现在药物的种类有很多,但还是有一些疾病无法治疗,所以我们需要不断的研发新药,而合成又是制药的基本领域和方法,所以我们需要学习、了解具体的合成方法【3】。
常见合成酰胺的方法➢羧酸与胺的缩合酰化反应➢氨或胺与酰卤的酰化反应➢氨或胺与酸酐的酰化反应➢其他缩合方法➢酯交换为酰胺➢氰基转化为酰胺羧酸与胺的缩合酰化反应1羧酸和胺的直接缩合反应羧酸与胺的反应是合成酰胺的重要方法: 这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏。
例如将a-羟基乙酸及苄胺于90℃共热,并蒸出生成的水及过量的苄胺,则生成a-羟基乙酰基苄胺【7】:90o C1.1混合酸酐法1.1.1混合酸酐法(一)氯甲酸酯法:主要应用羧酸与氯甲酸乙酯或异丁酯反应生成混合酸酐,而后再与胺反应得到相应的酰胺。
这一反应如果酸的a-位位阻大或者连有吸电子基团,有时会停留在混合酸酐这一步。
但加热可以促使其反应;这一反应也可用于无取代酰胺的合成。
ClCOOEt, NEt3 CHCl3, -20~5o C, 1.5h NH3 (gas) rt, 30min91%NMM, DMFr.t.33%1.1.2混合酸酐法 (二)羰基二咪唑:应用羰基二咪唑(CDI)与羧酸反应得到活性较高的酰基咪唑,许多酰基咪唑有一定的稳定性,有时可以分离出来。
有机化学基础知识胺的缩合反应和重排反应

有机化学基础知识胺的缩合反应和重排反应有机化学基础知识胺的缩合反应和重排反应胺是一类重要的有机化合物,具有含有氮原子的结构,广泛应用于制药、染料和农药等领域。
胺的化学性质非常活泼,可以经历多种反应,其中缩合反应和重排反应是常见的反应类型。
本文将重点介绍胺的缩合反应和重排反应的机理和应用。
一、胺的缩合反应胺的缩合反应是胺与其他化合物发生反应生成新的胺类化合物的过程。
常见的胺的缩合反应有亚胺化反应、胺酰胺化反应和脱水缩合反应。
1. 亚胺化反应亚胺化反应是胺与酮或醛反应生成亚胺的过程。
该反应在中性或弱碱性条件下进行,可以通过加热、溶剂或催化剂来加速反应速率。
亚胺化反应的机理是酮或醛与胺通过亲核加成生成中间体,然后中间体经过质子迁移、质子丢失和重排等步骤最终生成亚胺产物。
2. 胺酰胺化反应胺酰胺化反应是胺与酸酐反应生成胺酰胺的过程。
该反应在酸性条件下进行,可以通过加热或催化剂来促进反应。
胺酰胺化反应的机理是胺通过亲核加成进攻酸酐的羰基碳形成酰胺中间体,然后中间体经过质子迁移、质子丢失和重排等步骤最终生成胺酰胺产物。
3. 脱水缩合反应脱水缩合反应是胺与酸反应生成酰胺的过程。
该反应需要在脱水条件下进行,可以通过加热或加入脱水剂来促进反应。
脱水缩合反应的机理是胺通过亲核加成进攻酸的羰基碳形成酰胺中间体,然后中间体经过质子转移和脱水等步骤最终生成酰胺产物。
二、胺的重排反应胺的重排反应是胺分子内或胺与其他化合物之间的原子重排现象,产物是分子内或分子间的结构发生改变的新化合物。
常见的胺的重排反应有N-重排和C-重排。
1. N-重排N-重排是胺分子内氨基(氮原子)的重新排列和分子骨架的重构的反应。
该反应一般在高温和强酸或强碱催化下进行。
N-重排的机理是胺分子内的氨基通过质子化和质子迁移发生重排,最终生成新的分子结构。
2. C-重排C-重排是胺分子中碳原子的重新排列和分子骨架的重构的反应。
该反应一般在高温和催化剂存在的条件下进行。
羧酸与胺的缩合酰化反应.doc解析

常见合成酰胺的方法常见合成酰胺的方法羧酸与胺的缩合酰化反应氨或胺与酰卤的酰化反应氨或胺与酸酐的酰化反应其他缩合方法酯交换为酰胺氰基转化为酰胺第一部分:羧酸与胺的缩合酰化反应羧酸和胺的直接缩合反应羧酸与胺的反应是合成酰胺的重要方法:这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏。
例如将a-羟基乙酸及苄胺于90C共热,并蒸出生成的水及过量的苄胺,则生成a-羟基乙酰基苄胺:90o C HQCI-^COQH 十»HOCl^CONHCl-fePh混合酸酐法(一)氯甲酸酯法:主要应用羧酸与氯甲酸乙酯或异丁酯反应生成混合酸酐,而后再与胺反应得到相应的酰胺。
这一反应如果酸的a-位位阻大或者连有吸电子基团,有时会停留在混合酸酐这一步。
但加热可以促使其反应;这一反应也可用于无取代酰胺的合成。
CICOOEt, NEt 3CHCI3,-20〜5 o C, 1.5hCCHDH91%CICOOC 2H 5, TEA. THF, then NH 3(g)-20'C to it 65%混合酸酐法(二)羰基二咪唑:应用羰基二咪唑(CDI )与羧酸反应得到活性较高的酰基咪唑,许 多酰基咪唑有一定的稳定性,有时可以分离出来。
但一般来说其不用分离,反应液直接与胺一锅反应制备相应的酰胺;文献报道羰基二咪唑与三氟甲磺酸甲酯反 应得到的二甲基化的三氟甲磺酸盐(CBMIT )的缩合性能更好。
该类反应由于 CDI 或CBMIT 会和过量的胺反应得到脲的副产物,因此其用量一定要严格控制在 1最近有人发现应用CDI 合成Weinreb 酰胺是一个较好的方法。
混合酸酐法(三)磺酰氯:另一类常用的方法是羧酸和磺酰氯生成羧酸 -磺酸的混合酸酐,其NMM, DMFr.t.当量。
CONHa CH 3MeOTf (2 eq.)-OTf 2CH 3NO 2, 10°C与胺反应得到相应的酰胺。
酸胺缩合最理想方式:不用过柱子就可以拿到很纯的产物
酸胺缩合最理想方式:不用过柱子就可以拿到很纯的产物图片来源:J. Med. Chem.2016, 59, 4443−44582013年,来自英国伦敦大学学院的Tom D. Sheppard团队报道了一种新型Lewis酸B(OCH2CF3)3作为媒介的酸胺缩合反应,在绝大部分的合成例子中,最终产物都不需要柱纯化,通过商业可得的树脂经过简单的过滤即可得到纯品,不需要水层处理和柱层析。
该反应体系的底物范围非常之广,简单的酸到手性酸,苄胺与DMF的甲酰化反应等等都能顺利进行,以良好的产率和手性保持得到目标产物。
反应体系往往只需要固相操作就可以得到纯度较高的产物。
具体固相纯化方式见下图。
固相操作过程非常简单,具体如下所示:After the indicated time, the reaction mixture was diluted with CH2Cl2or EtOAc (3 mL) and water (0.5 mL). Amberlyst A-26(OH) (150 mg), Amberlyst 15 (150 mg) and Amberlite IRA743 (150 mg) were added to the reaction mixture, and it was stirred for 30 min. MgSO4 was added to the reaction mixture, which was thenfiltered, the solids were washed three times with CH2Cl2or EtOAc, and thefiltrate was concentrated in vacuo to yield the amide product.底物范围见下图:参与该反应的Lewis酸B(OCH2CF3)3也很容易制备,规模可达到50克级别,具体如下图所示。
酸胺缩合一:酰氯法
酸胺缩合一:酰氯法通过酰氯和胺反应制备酰胺,应用非常广泛。
优点•制备酰氯的试剂便宜,主要有以下几种氯代试剂,其中三氯氧磷用的相对较少。
直接购买Vilsmeier试剂价格贵,可以自制。
•酰氯活性高,应用范围广,反应快,可满足不同的胺,包括位阻大、活性低的胺。
缺点•如果酸的α-位置有手性中心,消旋风险高。
•酰氯活性高,一般需要滴加到胺的体系中,有的酰氯溶解性不好,难以实现。
芳香族甲酰氯一般是固体,活性低于脂肪族,可以采用一锅法加入。
•氯化亚砜和草酰氯用的多,制备酰氯时有氯化氢释放,对酸敏感的基团耐受性不好。
氯化亚砜法机理氯化亚砜法制备酰胺时,加入催化量DMF,会起到催化效果,经Vilsmeier盐,得到酰氯。
反应过程会释放二氧化硫和氯化氢。
优点便宜,容易去除。
缺点可能产生单质硫,不知道什么时候就会影响杂质谱;同时加DMF 催化会产生致突变杂质DMCC,所以原料药工艺能不加DMF,尽量避免添加,免得以后还需评估研究杂质。
常用条件制备酰氯阶段溶剂优选甲苯(可以带蒸去除残留的氯化氢、二氧化硫、以及氯化亚砜自身)。
其他溶剂包括:DCM、乙酸异丙酯、THF、乙腈等,THF最好少用。
当然,也可以直接用氯化亚砜作溶剂,后处理浓缩回收(不推荐)。
反应温度和底物相关。
制备酰胺阶段有机溶剂体系:一般加入有机碱做缚酸剂。
选择合适的溶剂和碱,让产生的有机胺盐酸盐溶解在溶剂中,析出产品,很完美。
例如三乙胺的盐酸盐难溶于乙腈或者二氯甲烷;DIPEA的盐酸盐溶于二氯甲烷或者乙腈。
两相体系:尽管酰氯活性高,可以和水反应,但仍可以根据胺的亲核性高于水,采用Schotten−Baumann条件,无机碱的水溶液和,与水不互溶的有机溶剂,进行两相反应。
放大案例一芳基甲酰氯,例如苯甲酰氯,因为共轭关系,活性低于脂肪族酰氯,有的以固体形式可以分离。
案例中化合物5和试剂氯化亚砜,在DMF催化下,以甲苯为溶剂,加热反应;反应完成后,以结晶形式析出,然后和化合物7(氨基酸,羧基没有保护)在碳酸氢钠、THF中一锅法加热制备酰胺8。
(整理)羧酸与胺的缩合酰化反应
羧酸与胺的缩合酰化反应王露化工与制药专业 1105班学号110150151指导教师刘雪凌老师摘要合成是制药的基本方法,也是很重要的方法,人类对药物的需求很大,要不断的创新、研发新药,合成是其中必不可少的方法,本文介绍了常见合成酰胺的方法,合成酰胺通用的方法是先活化羧基,然后再与胺反应得到酰胺。
其中羧酸与胺的反应是合成酰胺的重要方法【5】。
这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏【1】。
关键词:合成酰化活化前言药物对于我们任何一个人来说都不陌生,而且离不开。
现在药物的种类有很多,但还是有一些疾病无法治疗,所以我们需要不断的研发新药,而合成又是制药的基本领域和方法,所以我们需要学习、了解具体的合成方法【3】。
常见合成酰胺的方法➢羧酸与胺的缩合酰化反应➢氨或胺与酰卤的酰化反应➢氨或胺与酸酐的酰化反应➢其他缩合方法➢酯交换为酰胺➢氰基转化为酰胺羧酸与胺的缩合酰化反应1羧酸和胺的直接缩合反应羧酸与胺的反应是合成酰胺的重要方法: 这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏。
例如将a-羟基乙酸及苄胺于90℃共热,并蒸出生成的水及过量的苄胺,则生成a-羟基乙酰基苄胺【7】:90o C1.1混合酸酐法1.1.1混合酸酐法(一)氯甲酸酯法:主要应用羧酸与氯甲酸乙酯或异丁酯反应生成混合酸酐,而后再与胺反应得到相应的酰胺。
这一反应如果酸的a-位位阻大或者连有吸电子基团,有时会停留在混合酸酐这一步。
但加热可以促使其反应;这一反应也可用于无取代酰胺的合成。
ClCOOEt, NEt3 CHCl3, -20~5o C, 1.5h NH3 (gas) rt, 30min91%NMM, DMFr.t.33%1.1.2混合酸酐法 (二)羰基二咪唑:应用羰基二咪唑(CDI)与羧酸反应得到活性较高的酰基咪唑,许多酰基咪唑有一定的稳定性,有时可以分离出来。
酸胺缩合反应的经验总结
酸胺缩合反应的经验总结1.反应物的选择首先要选择合适的酸和胺反应物。
通常情况下,酸反应物一般选择羧酸,胺反应物一般选择胺或氨的衍生物。
此外,还需要考虑酸胺反应物的亲核性和亲电性,以确定反应机理和条件。
2.反应溶剂的选择3.反应条件的控制4.缩合剂的选择在酸胺缩合反应中,常用的缩合剂有DCC(二异氰酸酯)、EDCI(硝基三氯化磷)、HATU(1-羟基-7-硝基-硫代氨基三氟甲烷磺酰吡咯烷)等。
这些缩合剂能够促进酸和胺之间的缩合反应,并且在反应结束后容易除去。
5.pH值控制在酸胺缩合反应中,pH的控制十分重要。
通常情况下,酸和胺的碱性越大,反应速率越快。
因此,在反应过程中可以适当调整反应体系的pH值,以加速反应进程。
6.水的防止由于酸胺缩合反应中存在缩合剂的生成,水的存在会影响反应的进行。
因此,在反应过程中需要尽量避免水的加入,可以使用一些水分子筛或干燥剂吸附水分。
7.高纯度的反应物和溶剂为了保证酸胺缩合反应的有效进行,需要使用高纯度的反应物和溶剂。
杂质可能影响反应的选择性和产率,所以要进行适当的纯化和检测。
8.产物的分离和纯化在反应结束后,需要对产物进行分离和纯化。
常见的方法有结晶、萃取和柱层析等。
根据产物的性质和纯度要求,选择合适的纯化方法。
9.实验安全在进行酸胺缩合反应时,应严格遵守实验室安全规定,如佩戴适当的防护设备、操作正确的废物处理等。
总结起来,酸胺缩合反应是一种常用的有机合成反应,可以用于构建C-N或C-C键。
在进行反应时,需要选择合适的反应物、溶剂和缩合剂,并进行适当的pH控制和水的防止。
对产物的分离和纯化要进行合适的处理。
同时,实验中要注意安全操作。
以上的经验总结可以指导实验工作的开展和优化,提高反应的效率和产物的纯度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
酸胺缩合反应总结
1 合成酰胺的方法
合成酰胺通用的方法是先活化羧基,然后再与胺反应得到酰胺
总体来说仲胺活性高于伯胺,脂肪胺高于芳香胺。
2 羧酸与胺的缩合酰化反应
2.1活性酯法
应用 CDI 与羧酸反应得到活性较高的酰基咪唑,该类反应由于过量的 CDI 会和胺反应得到脲的副产物,因此其用量一定要严格控制在 1 当量。
其反应是分步进行,胺极易与活性酯反应得到相应的酰化产物。
2.2 碳二亚胺类缩合剂法
使用该类缩合剂一般需要加入酰化催化剂或活化剂如,DMAP , HOBt ,等等,主要因为反应的第一阶段所生成的中间体不稳定,若不用酰化催化剂转化为相应得活性酯或活性酰胺,其自身易成脲。
EDCI HOBT,一般用的较多,搭配使用,有时酸的位阻较大或者连有吸电子基团反应或停留在活性酯这一步,一般加碱,2-3 当量的 DIEA,一般以二氯甲烷为溶剂,溶解性不好时也可用 DMF。
(有时加催化量的DMAP,针对有位阻的反应)。
这类缩合剂活性相对要差一些,一般需要和酸先活化 1 小时,再将胺加入。
2.3 鎓盐类的缩合剂法
鎓盐类的缩合剂活性较高,从盐的种类分为两类一类是碳鎓盐,目前常用的 HATU,HBTU,等等。
另一类为鏻鎓盐,如 PyBOP。
HATU缩合效果较好但价格较贵, PyBOP 是我们常用的缩合剂中活性最高的,一般在其他方法不反应的条件下考虑。
3 常见副产物以及处理方法
3.1 碳二亚胺类副产物
以 EDCI 为例子,在没有 HOBT 存在的情况下,反应活性酯容易自身重排成脲:
所以在反应中加入HOBT 以形成相对稳定的活性中间体:
其反应后生成的脲水溶性很好,通常在反应干净的情况下,可以用稀酸洗掉,不须进一步纯化即可得到干净的产品。
在库反应中,此类缩合剂最常使用的是 EDCI,因其极性相对较大,在分离过程中
不易与产物包裹在一起。
不过在产物极性大的情况下,分离过程中可能会带有 174 的杂MS。
3.2 鎓盐类副反应
以 HATU 为例,在局部浓度不均匀的情况下,会产生以下副产物:
所以在反应的时候,一般的加料顺序,应该是将酸,碱以及HATU 加到溶剂中,搅
拌均匀再将胺加入,以避免此类副产物。
若产品极性较大的情况下,与 HATU代谢的产物包裹在一起,会产生 117 的杂 MS。
由于此副产物254 下没有紫外吸收,所以在产物极性较大,推荐选取机分。
3.3 TFA带来的副产物
若前一步反应为 DeBoc,成 TFA 盐的话,反应之前最好先游离一下,因为反应可
能会有三氟乙酰化的副产物。
此类副产物最常见于脂肪类小分子酸胺coupling的时候。
3.4 DMF带来的副产物
DMF对于许多化合物来说都是良溶剂,并且许多胺即使成盐,在 DMF中也有不错
的溶解度,所以许多缩合反应大家都会选取 DMF,但是在反应选取的碱比较强的情况下,会产生以下副产物:
在反应中如果遇到此类情况,可以用DMA来代替 DMF,会避免此副产物的出现。
4 碱的选取
一般情况下,TEA和 DIEA是酸胺缩合最常用的碱,不过在投库反应中,这两种碱
在机分的时候 MS 脱尾,可能会在产物中包裹 101/130 的杂 MS,导致 QC 无法通过,可以选用 NMM 来代替,目前为止,还没有发现 NMM 导致 QC不过的情况。
对于有手性反应来说,文献报道中显示,TEA可能会造成更多的消旋,相对来说DIEA要好很多,NMM 还没有看到相关的报道。
5 敏感基团
对于有苯酚类的酸胺缩合,有报道称选用无机碱会尽可能避免酯的生成,常用
K2CO3 等。
对于吲哚类,咪唑等含有氨基的酸胺缩合反应,如果选取HATU 的话,要注意量的控制,避免最终产物出现副反应,MS加 99。
6 综述
在反应过程中,如果胺的活性差的话,反应可能会留在活性酯阶段。
常用的溶剂为DCM、MeCN、DMF、DMSO,最常用的是DCM,若DCM不溶,则用DM F+TBTU效果比较好(个人认为)。
常用的缩合剂:
1) EDCI(1.2eq)+HOBT(1.2eq)+Et3N(2eq)
2) EDCI(1.2eq)+DMAP(1.2eq)+Et3N(2eq)
3) HATU(1.2eq)+DIPEA(2eq) or HATU(1.2eq)+Et3N(2eq)
4) TBTU(1.2eq)+DIPEA(2eq) or TBTU(1.2eq)+Et3N(2eq)
反应机理:
酸胺缩合反应的经验总结(补充)
第一、我们可以先分别试一下TBTU和HOBT,EDCI,若是反应结果不是令人满意,这种情况下我们一般再试HATU,BOP,虽然HATU和TBTU是一种类型的缩合剂,但是有时候HATU会得到很好的结果。
第二、若上面的条件得不到我们想要的结果,那么我们就可以用CDI来试验。
把酸溶解在二氯甲烷里,分批加入CDI,点板反应完毕后,转移到滴液漏斗中,滴加到胺的二氯甲烷溶液里,一般效果会很好。
第三、若是还不行,那就只有把酸做成酰氯了,然后在三乙胺的条件下和胺反应做成酰胺,这一般是最后的方法了。
第四、不过还有一种可以试验的条件,就是用羧酸盐,用羧酸盐与胺做缩合反应,这是没有办法的办法了,可以死马当活马医。
