膜片钳技术
膜片钳实验与技术

汇报人:XX
单击输入目录标题 膜片钳实验原理 膜片钳实验操作流程 膜片钳实验数据分析 膜片钳实验的应用实例
膜片钳实验的未来发展与挑战
添加章节标题
膜片钳实验原理
膜片钳技术的基本原理
膜片钳实验原理:通过玻璃微电极接触细胞膜,记录单一离子通道活动的 电位变化,从而研究细胞膜离子通道的特性。
膜片钳实验操作步骤
准备实验器材:包括膜片钳 放大器、微操纵器、微电极、
细胞夹持器等
添加标题
细胞贴片稳定:等待细胞贴 片稳定后,进行下一步操作
添加标题
开启膜片钳放大器:开启放 大器,调节放大器参数,确 保记录到有效的膜电流信号
数据记录:记录膜电流信号, 进行分析和处理
添加标题
添加标题
添加标题
添加标题
新型膜片钳技术的研发,提高实验效率和准确性 应用人工智能技术,实现自动化数据分析与处理 结合其他技术手段,拓展膜片钳技术的应用领域 持续优化膜片钳设备,降低实验成本,提高普及率
膜片钳实验在多学科交叉中的应用前景
神经科学领域:研究神经元电活动与行为之间的联系 生理学领域:研究生物体的生理功能和机制 药理学领域:研究药物对细胞膜通道的影响和作用机制 生物医学工程领域:开发新型膜片钳技术,提高实验的灵敏度和特异性
膜片钳技术的特点:高灵敏度、高分辨率和高时间分辨率,能够记录单个 离子通道的活动。
膜片钳技术的应用范围:研究细胞膜离子通道的生理功能、药理作用和药 物作用机制等。
膜片钳实验的影响因素:电极内液的成分、温度、细胞内外的离子浓度和 pH值等。
膜片钳实验的应用范围
神经科学:研究神经细胞的电生理特性 药理学:药物对膜通道的影响 生理学:研究生物膜的离子通道功能 病理学:研究疾病状态下膜通道的异常变化
膜片钳技术参数

膜片钳技术参数一、膜片钳放大器系统(1)膜片钳放大器*1. 双电极膜片钳放大器用于细胞内和细胞外记录、膜片钳记录(全细胞、巨膜片、游离膜片)、电流测定法/伏安法、离子选择电极的测量、人工脂双层记录2. 电压钳模式下提供4种反馈电阻(50 MΩ、500 MΩ、5 GΩ、50 GΩ),可以测定0.2 pA~200 nA范围的电流。
电流钳模式下提供3种反馈电阻(50 MΩ、500 MΩ、5 GΩ),可以测定2 nA~200 nA 范围的电流。
3. 膜片钳放大器具有两个相同且独立的探头,为计算机控制,多数功能可通过点击鼠标而自动完成。
4. 全细胞膜电容补偿范围:Rf=500M时,Cm 1-100pF/Rs 400k-1000M串联电阻补偿范围:带宽:0.32-16kHz;校正值:0.4-1000M(500M时)5. 输出增益范围:主输出:1,2,5,10,20,50,100,200, 500, 1000, 2000;主输出滤波频率范围:4-极Bessel低通滤波(Hz):2Hz-30kHz (2)数模转换器1转换器为即插即用型设备,能被Windows系统自动识别。
*2 为一台单独的仪器,不跟膜片钳放大器组合为一台仪器。
具有丰富数量的模拟/数字输入/输出端口,方便在软件中进行额外的附加控制。
3 16位高分辨率、低噪声转换器。
模拟信号输入通道数:8;模拟信号输出通道数:8;数字输出通道数:8。
4 采样速率:1 Hz - 500 kHz。
5 输入电阻: 1 MΩ;输入型号;TTL兼容制系统,方便外接其他刺激器,隔离器等。
输出电阻:< 0.5Ω6 输出电流:±4mA;数字化噪音< 1 mV7 系统自带消除噪音功能。
最大输入信号±10 V;消除最大噪音幅度20 V;噪音消除:线频率50Hz和谐波至10 kHz;取消相应时间< 1 s(3)记录和分析软件*1. 分析程序可对数据脱机处理,不需要使用密码锁2. 既包含采样程序又包含分析程序3. 膜测试功能在记录每条扫描线时可计算串联电阻Ra和膜电容4. 如果施加了漏减功能,则可同时自动记录下漏减前后的电流5. 在对每条扫描线进行记录时,可采用两个不同的采样频率进行6. 可以设置灵活的基础刺激和条件刺激方式用来不间断记录长时程增强效应和长时程抑制效应(LTP/LTD)。
膜片钳

㈢分析
1.事件检测方法——50%阈值检测法: 将阈值水平设在开放水平与关闭水平中间
2.单通道电流幅度和电导的分析 ➢目的:揭示通道的通透性机制;帮助区分通道的类 型、通道不同的亚单位组成以及突变等 ➢单通道电流的分析—— 幅度直方图 ➢单通道电导的计算 ⑴斜率电导:步阶电压(voltage step);斜坡电压 (voltage ramp) ⑵拟合电流幅度直方图:高斯拟合
Rs的影响:使膜电位对命令电压的反应时间延迟;产生 电压降,影响钳制电位的数值;与膜电容形成一个单极 RC滤波器,限制了摄取电流信号的频带宽。
膜电阻(Rm):指电流通过细胞膜时所遇到的阻力。 在静息状态下,Rm主要来自脂质双分子层的电阻。
3. 膜漏电流去除:
➢电容器(capacitor):
被绝缘体隔开的两个导体 的组合,其储存电荷的能 力用电容(capacitance) 表示。
㈡ Ag/AgCl电极
Ag + Cl-
电子从Ag/AgCl 电极流向浴液
AgCl +e电子从浴液流向Ag/AgCl电极
➢长时间导通电流,AgCl会消耗掉,要定期镀AgCl: 含Cl-的溶液,长度为1~1.5cm
➢玻璃微电极尾端烧灼,防止AgCl被刮掉
电极电阻
二、封接
测试脉冲(20mV) 产生的电极电流
原因:离子通道的开放导致膜电阻迅速降低,电流 和电压的关系偏离了欧姆定律。
分外向整流和内向整流
外向整流:指随膜电位的去极化,I-V曲线靠近y轴
内向整流:指随膜电位的去极化,I-V曲线靠近x轴
(2)离子通道的激活(activation) (3)离子通道的失活(inactivation) 衰减(decay):通道在激活因素持续存在条件下的 失活。用衰减的时间常数来表示 稳态失活(steady-state inactivaion):反映通道 失活数目的电压依赖性,可用失活曲线表示 (4)通道失活后的恢复 通道失活后,必须将激活因素去除并维持一定时间, 才能使通道脱离失活状态,再次给予激活因素时通道 才能恢复开放。维持时间即通道失活后的恢复时间。 (5)离子通道的去激活(deactivation) 指在激活因素结束时通道的关闭过程,所记录到的电 流称尾电流。有些离子通道的尾电流也具有电压依赖 性,关闭过程呈指数分布。
膜片钳技术概述

2)屏蔽罩:用铜丝网制成,防止周围环境 的杂散点场对膜片钳放大器的探头电路的干扰。 有的膜片钳实验所测试的细胞或某种物质是光 敏感的,或者膜片钳实验是与光学测量联合进 行测需要采取光屏蔽,则屏蔽罩的外壁用黑色 布遮盖或在暗室里操作以减少强光的干扰。
2、光学部分
倒置显微镜 优点: 具有较好的视觉效果 便于将玻璃微电极与细胞的顶部接处。 具有较好的机械稳定性。
荧光染料Fu ra-2 可被紫外光激发发射出 荧光, 它可选择性地结合钙离子, 而与钙离子 结合的Fu ra-2 越多, 以相同紫外光激发出的 荧光就越弱, 因此可根据荧光强度的变化计算 出单位体积中钙离子浓度的变化。具体过程为: 在做全细胞记录之前, 以孵育或经电极扩散的 方法使荧光染料Fu ra-2 进入细胞, 然后对该 细胞内荧光强度、细胞膜离子通道电流及细胞 膜电容等多种指标变化情况进行观测,并分析 这些变化间的相互关系。
电极电容Cp极小,只有几各pF,相应的 电路时间常数甚小,因而对于Cp瞬态补偿称为 快电容补偿,细胞膜电容的值约为1µF/cm2, 由于此时的充电电流需要流经串联电阻Rs(Rs 的值约为几个兆欧),时间常数较大,故Cm 的补偿称为慢电容补偿。此外,串联电阻Rs因 跨接在Cp和Cm之间,当有电流经过时,将产 生可观的压降,如当Rs=5MΩ ,I=2mA时, 可导致钳制电位误差达10mV;消除这种误差的
3、电子部件:包括膜片钳放大器、刺激器、示
波器及记录系统。 膜片钳放大器:
是膜片钳实验中一个核心仪器,通过它 把生物电信号放大。从原理来说,膜片钳放大 器的探头电路即I-V变换器有两种基本结构形 式,即电阻反馈式和电容反馈式,前者是一种 典型的结构,但是相比较而言,后者降低了噪 声,所以特别适用超低噪声的单通道记录。
膜片钳技术及其应用

膜片钳技术可以用于研究细胞信号转导过程中离子通道和受体的变 化,了解信号转导的机制。
细胞功能调控的研究
膜片钳技术可以用于研究细胞功能调控的机制,例如细胞兴奋性的 调节和细胞内离子浓度的变化。
04 膜片钳技术的优势与局限 性
膜片钳技术的优势
高灵敏度
细胞无损
膜片钳技术具有高灵敏度,能够检测单 个离子通道的活动,从而提供关于细胞 膜电位和离子通道功能的重要信息。
膜片钳技术可以在保持细胞完整性的 情况下进行实验,不会对细胞造成严 重损伤或干扰细胞的正常功能。
实时监测
膜片钳技术可以对细胞膜电位进行实时 监测,从而了解离子通道的动态变化, 有助于深入理解细胞生理和病理过程。
膜片钳技术的局限性
1 2 3
实验条件要求高
膜片钳技术需要高精度的实验设备和条件,包括 低温、低噪声和低阻抗等,这增加了实验的难度 和成本。
03
04
05
膜片钳放大器
微操纵器
细胞培养皿或显 微镜载玻片
电极溶液
细胞内和细胞外 灌流液
用于放大细胞膜电信号, 提高信号的检测灵敏度。
用于精确控制电极的移动 ,以便在细胞膜上定位和 进行膜片钳实验。
用于培养和固定细胞,以 便进行膜片钳实验。
用于填充电极,以保持电 极的湿润和导电性。
用于维持细胞内外环境的 稳定,并排除干扰实验的 物质。
03
在单细胞水平上研究细胞信号转导和离子通道功能,深入了 解细胞生理和病理过程。
膜片钳技术与其他技术的联合应用
结合光学成像技术,利用膜片钳技术对神经元电生理特性进行同时监测和成像,实现多参数的同时测 量。
与基因编辑技术结合,利用膜片钳技术对特定基因表达的离子通道进行功能研究,深入了解基因与离子 通道的关系。
膜片钳技术原理

膜片钳技术原理膜片钳技术是一种常见的实验技术,广泛应用于生物学、药理学、细胞生物学等领域。
它是利用一种特殊的仪器,通过对细胞膜的控制和操作,实现对细胞内外环境的调控和研究。
膜片钳技术的原理主要涉及到膜片形成、膜片钳的构造和工作原理等方面,下面将对这些内容进行详细介绍。
首先,膜片的形成是膜片钳技术的基础。
膜片是由玻璃或石英毛细管制成的,其内外涂有一层导电性金属。
在形成膜片的过程中,需要将毛细管和细胞膜接触,利用毛细管的吸附作用将细胞膜抽附到毛细管上,形成一个微小的膜片。
这一步骤的关键是要保持膜片的完整性和稳定性,以确保后续实验的准确性和可靠性。
其次,膜片钳的构造是实现膜片钳技术的重要工具。
膜片钳通常由微操作系统、压力控制系统、电压控制系统等组成。
微操作系统用于控制膜片的形成和定位,压力控制系统用于控制膜片与细胞膜的接触压力,电压控制系统用于记录和调节膜片与细胞膜之间的电压变化。
这些系统的协同工作,使得膜片钳能够对细胞膜进行高度精准的操作和控制。
最后,膜片钳技术的工作原理是通过对膜片与细胞膜之间的接触和电学特性的测量,实现对细胞内外环境的调控和研究。
在实验中,可以通过改变膜片与细胞膜的接触压力和电压,观察细胞膜的电学特性和通透性的变化,从而研究细胞的离子通道、受体通道等功能。
同时,也可以利用膜片钳技术对细胞内外环境的离子浓度、pH值等进行精准调控,以研究细胞的生理和病理过程。
总之,膜片钳技术是一种重要的细胞生物学实验技术,其原理涉及膜片的形成、膜片钳的构造和工作原理等方面。
通过对这些原理的深入理解和掌握,可以更好地应用膜片钳技术进行细胞内外环境的调控和研究,为生物学、药理学等领域的研究工作提供重要的技术支持。
膜片钳技术及应用

制备玻璃微电极
拉制微电极 材料:硼硅酸盐毛细玻璃管。 要求:玻璃毛胚外径1.3~1.7㎜,内径1.0~1.2
㎜,壁的厚度在0.2㎜以上。管壁越厚,拉 制出的电极尖端管壁也越厚,电极的跨壁 电容就越小,噪声也就越低。
玻璃微电极及膜片的几何形状
电极拉制仪
拉制方法:两步拉制法。
第一步:使玻璃软化,并拉开一个距离,形 成一个细管,即拉制电极的颈部;
高阻封接形成的电流图
膜片钳技术四种基本记录模式
细胞吸附膜片(cell-attached patch) 将两次拉制后经加热抛光的微管电极置于
清洁的细胞膜表面上,形成高阻封接,在细 胞膜表面隔离出一小片膜,既而通过微管电 极对膜片进行电压钳制,高分辨测量膜电流, 称为细胞贴附膜片。由于不破坏细胞的完整 性,
膜片钳技术
向细胞内注射恒定或变化的电流刺激, 纪录由此引起的膜电位的变化,这叫做电流 钳技术。在具体实验中,可通过给予细胞一 系列电流脉冲刺激,诱发细胞产生动作电位。
电压钳技术是通过向细胞内注射一定的
电流,抵消离子通道开放时所产生的离子流, 从而将细胞膜电位固定在某一数值。由于注 射电流的大小与离子流的大小相等、方向相 反。因此它可以反映离子流的大小和方向。
电极液的充灌
对于尖端较细的玻璃微电极,膜片钳实 验中常用的方法是:在微电极尾部施加负压 使尖端充灌电极内液,然后用注射器在微电 极尾部充灌电极内液,最后轻弹微电极杆步 使其内的气泡排出。
充灌长度为电极的1/3。
制备细胞标本
从理论上来讲,膜片钳实验用的细胞标 本可来自体内各种组织细胞,只要细胞表面 光滑,能与微电极尖端形成高阻封接即可。 但在标本制备上,不同组织细胞间联接牢固 程度不同,采用的分离方法也不完全相同。 大体上包括冲洗、酶解消化或机械分离以及 清洗等步骤。
膜片钳技术
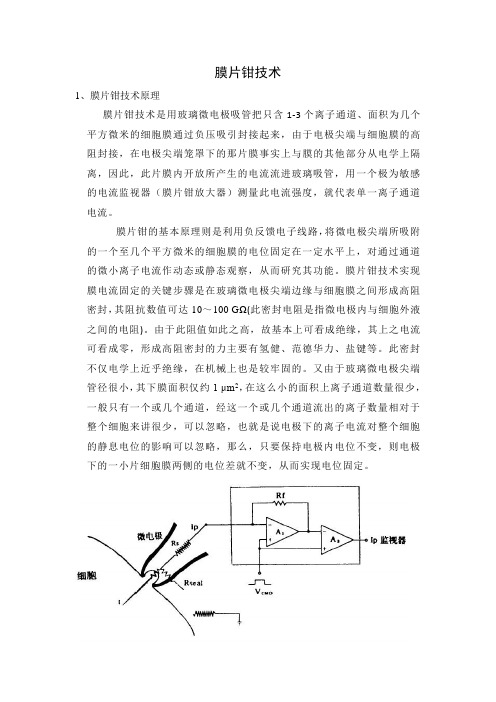
膜片钳技术1、膜片钳技术原理膜片钳技术是用玻璃微电极吸管把只含1-3个离子通道、面积为几个平方微米的细胞膜通过负压吸引封接起来,由于电极尖端与细胞膜的高阻封接,在电极尖端笼罩下的那片膜事实上与膜的其他部分从电学上隔离,因此,此片膜内开放所产生的电流流进玻璃吸管,用一个极为敏感的电流监视器(膜片钳放大器)测量此电流强度,就代表单一离子通道电流。
膜片钳的基本原理则是利用负反馈电子线路,将微电极尖端所吸附的一个至几个平方微米的细胞膜的电位固定在一定水平上,对通过通道的微小离子电流作动态或静态观察,从而研究其功能。
膜片钳技术实现膜电流固定的关键步骤是在玻璃微电极尖端边缘与细胞膜之间形成高阻密封,其阻抗数值可达10~100 GΩ(此密封电阻是指微电极内与细胞外液之间的电阻)。
由于此阻值如此之高,故基本上可看成绝缘,其上之电流可看成零,形成高阻密封的力主要有氢健、范德华力、盐键等。
此密封不仅电学上近乎绝缘,在机械上也是较牢固的。
又由于玻璃微电极尖端管径很小,其下膜面积仅约1 μm2,在这么小的面积上离子通道数量很少,一般只有一个或几个通道,经这一个或几个通道流出的离子数量相对于整个细胞来讲很少,可以忽略,也就是说电极下的离子电流对整个细胞的静息电位的影响可以忽略,那么,只要保持电极内电位不变,则电极下的一小片细胞膜两侧的电位差就不变,从而实现电位固定。
膜片钳技术的原理图[51]Rs是与膜片抗阻串联的局部串联电阻(或称入路阻抗),Rseal是封接阻抗。
RS通常为1~5MΩ,如果Rseal高达10GΩ以上是成为Ip/I=Rseal/(Rs+Rseal)-1。
此Ip可作为I~V转换器(点线)内的高阻抗负反馈电阻(Rf)的电压下降而被检测出。
实际上这是场效应管运算放大器(A1)的输出中包括着膜电阻成分,这部分将在通过第二级场效应管运算放大器(A2)时被减掉。
本实验采用的是全细胞记录模式。
全细胞记录构型(whole-cell recording)高阻封接形成后,继续以负压抽吸使电极管内细胞膜破裂,电极胞内液直接相通,而与浴槽液绝缘,这种形式称为“全细胞”记录。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
测试题:
1. 膜片钳的主要记录方式有哪几种,各
有何优缺点? 2. 什么叫整流,产生整流的原因是什么?
膜的被动反应
离子通道开放 膜的主动反应
外向整流
随膜电位的去极化,I-V曲线明显向Y轴(电流轴)靠 近。如IK电流。
内向整流
随膜电位的去极化,I-V曲线明显向X轴(电压轴)靠 近。如烟碱电流。
去极化方向
去极化方向
IK电流的外向整流
烟碱电流的内向整流
尾电流(Tail current)
指通道在激活因素结束时的关闭过程中,所记录
6. 基本概念及参数设置
输入漏电流(Input leakage current)
理论上讲,不施加外部命令时,通过放大 器探头的电流应该为0,如果由于放大器本 身的原因产生了电流,这就是漏电流。由于 放大器控制电流漂移的质量很高,一般漏电 流都很小。
封接电流(Seal current)
由于封接质量不高(没有形成良好的高 阻封接),从封接处产生的电流。成为噪 声。
第三部分
全细胞记录结果举例
+80mV
+40mV
0mV
-40mV
-80mV 200ms
Iso Hypo
Current Density (pA/pF)
-40
60
30
0 -80 0 -30 40 80
Voltage (mV)
-60
Iso 4 Iso 2 Hypo Hypo
Current (nA)
0
倒 置 相 差 显 微 镜
EPC-7膜片钳放大器(德国)
4. 膜片钳的记录方式及基本操作
细胞吸附式(Cell-attached
mode 或 on cell mode)
内膜向外式(Inside-out mode)
外膜向外式(Outside-out mode)
全细胞记录方式(Whole-cell
C-FAST和τ-FAST按钮 “Fast”钮补偿快电容,主要是电极电 容。大部分的电容瞬变值可用“Fast”控 制钮进行补偿。
五.缓慢电容补偿(slow capacitative compensation) “C-Slow”钮补偿慢电容,即电极尖端与 大地之间的电容,主要是膜片电容。
在全细胞记录模式,缓慢电容补偿的值 即为该细胞的电容值。
内向电流(Inward current) 从细胞外进入细胞内的正离子(如Na+)电
流或从细胞内流向细胞外的负离子(如Cl-) 电流。
外向电流(Outward current)
从细胞内流向细胞外的正离子(如K+ )电
流或从细胞外流向细胞内的负离子(如Cl-)
电流。
Electrode与pipette的区别
Electrode
指金属电极,即Ag/AgCl电极。
Pipette
指拉制出的玻璃电极,它不是真正意 义上的电极,而是真正电极的依托。
命令电压(Command
voltage, Vcmp)
通过放大器或计算机发出的指令电压, 用于钳制细胞膜电位。
钳制电位(Holding
potential, Vh)
人为地将细胞膜内外的电压差固定在某 一数值,这一数值即为钳制电压或称钳制 电位。实施这一行为的技术为电压钳技术 (Voltage clamp)。
由于有细胞膜内折(Infolding)的存在,
实际的Cm要比计算的大1.5-3倍。
一般情况下,生物膜的电容大体都是
1μF/cm2。
• 电极电容(Pipette capacitance, C )
p
电极电容包括跨壁电容( Ct )、电极非浸 液部分与邻近地表形成的漂浮电容(Cs)。
跨壁电容(Transmural capacitance, Ct) 电极浸液部分的内外液之间形成的电容, 跨壁电容的介质为玻璃电极壁。 在膜片钳实验中其值可能很大,一般电极 浸液深1mm会产生1pF或更大一些的电容。
到的电流称为尾电流(Tail current)。
-40mV Vh=-100mV -70mV
2nA 5ms
电流的Rundown现象 指随着记录时间的延续,通道电流逐渐
降低的现象。许多种类细胞的钙电流都具有 Rundown现象。
Rundown现象形成的原因
全细胞记录模式形成以后,由于电极内 液与细胞内液之间的相互透析,造成细胞内 大分子物质稀释或丢失;同时,细胞内ATP 也因稀释而严重不足,而钙离子在外排时耗 能较大,从而导致Rundown现象的发生。
-2
-4
0
500
1000
1500
Time (s)
附录1. 推荐书目
王绍, 徐涛. 电生理学方法. 韩济生主编. 神经 科学原理. 第二版. pp55-65. 北京:北京医科 大学中国协和医科大学联合出版社,1999. 张均田主编. 现代药理学实验方法. 北京:北 京医科大学中国协和医科大学联合出版社, 1997. 陈军. 膜片钳实验技术. 北京: 科学出版社, 2001. 刘振伟. 脑片膜片钳技术及其研究概况. 张均 田主编. 神经药理学研究进展. pp137-150. 北 京:人民卫生出版社,2002.
Patch clamp 镜下观
Patch clamp 镜下观
2. 膜片钳的工作原理
3. 膜片钳记录的常用设备
1) 电极拉制器
2) 倒置相差显微镜
3) EPC-10膜片钳放大器 4) 三维微操纵仪 5) CED 1401数-模/模-数转换器 6) CED EPC 软件包
电极拉制器: 二步法拉制
减小跨壁电容的方法: 1. 加厚电极管壁:采用厚壁玻璃毛坯 拉制电极,或在电极浸液部分外部涂以硅 胶树脂等疏水性物质。
2. 减小电极浸液深度:浸液部分越大, Ct越大。 3. 补偿电路:采用膜片钳放大器内置 的电容补偿电路进行补偿。
慢电容(Slow capacitance, Cslow)与 快电容(Fast capacitance, Cfast)
一、串联电阻(Series resistance, Rs)补偿 Rs是指流过电极尖端的电流所遇到的所有
电阻。
当将电极放入浴液中或在形成高阻封接时,
Rs主要是电极电阻;
全细胞记录模式形成后, Rs包括电极电阻 、
破裂膜的残余膜片电阻、细胞内部电阻。
Rs引起的误差有如下二方面: 1. 串联电阻产生电压降,严重影响膜钳制 电压的数值;
2. 膜电位对步阶命令电压的反应时间延迟。 补偿方法:调节“%-COMP”按钮
二. 液界(接)电位及其补偿 主要成分: 1. 液体--金属:AgCl电极与电极内液;
2. 电极内液--细胞外液;
3. 电极内液--细胞内液(破膜后,等待一
定时间即可消除)。
范围:可达几百mV 补偿方法:电极入水按“Search”,“Offset”
电流钳模式: 固定电流, 记录电压
全细胞记录的操作步骤
1. 制作细胞涂片 2. 拉制玻璃电极 3. 灌注电极液,安装电极 4. 在显微镜下找到微电极,移动三维操 纵仪,使电极尖端接触细胞 5. 用负压轻轻抽吸,钳紧细胞,形成全 细胞记录模式 6. 给予一定的钳制电压并观察电流
全 细 胞 记 录 的 形 成 过 程
recording)
微电极的拉制
材料:硼硅酸盐毛细玻璃管
拉制方法:二步法 要求:尽可能使头颈部短些( Rs) 拉制好的微电极涂硅酮树酯、热刨光
电极液的充灌: 无气泡 充灌玻璃电极长度的1/3
微电极的安装
记录(测量)电极和参考电极:
材料是Ag,表面镀成AgCl
减少接触电位
5. 全细胞记录
电压钳模式: 固定电压, 记录电流
第二部分
电压门控性离子通道 基本知识
•电流密度( Current density)
单位细胞膜面积的电流大小。在进行 全细胞记录时,由于细胞直径大小的不同, 离子通道数目也不相同,因此为便于不同 细胞间的比较,采用电流密度这一概念。
由于膜电容的大小与细胞大小成正比,故 电流密度 = Im/Cm (pA/pF)
整流(Rectification) 整流是指电流易向一个方向流动,而不易 向反方向流动。内向性整流是指正离子易从 膜外向膜内流动,而不易从膜内流向膜外。
原因:离子通道的开放导致膜电阻发生了
变化。 表现:电流和电压的关系不满足欧姆定律 的直线关系。
无整流
有整流
V=IRc
V=IRv
离子通道不开放
三. 膜片钳系统中的电容 膜电容(Membrane capacitance, Cm) 细胞膜的脂质双分子层是电的不良导体, 因而由细胞外液-脂质双分子层-细胞内液就 构成了细胞膜电容。 Cm的大小与细胞膜表面积(包括内陷折 叠部分)成正比,与脂质双分子层的厚度成 反比。
对于一个球形细胞,膜电容的计算公式为: Cm=πd2 / 100 (pF) d为细胞直径(μm)
1. 膜片钳的发展历史
1976年德国马普生物物理化学研究所 Neher和Sakmann首次在青蛙肌细胞上记 录到Ach激活的单通道离子电流,从而产 生了膜片钳技术。 1980年Sigworth等获得10-100GΩ的高阻 封接(Giga-seal)。 1981年Hamill和Neher等对该技术进行了 改进,引进了全细胞记录技术。
膜片钳技术讲座
2006年12月
第一部分第三部分
全细胞记录结果举例分析
第一部分
膜片钳技术的基本概念
学习内容
1. 膜片钳的发展历史
2. 膜片钳的工作原理
3. 膜片钳记录常用的设备
4. 膜片钳记录的方式及基本操作
5. 全细胞记录的步骤 6. 基本概念和参数的设置
