健胃消食片检验方法确认方案
高效液相色谱法测定健胃消食片中橙皮苷的含量

高效液相色谱法测定健胃消食片中橙皮苷的含量摘要】目的:采用高效液相色谱法测定健胃消食片中橙皮苷的含量。
方法:采用高效液相色谱方法,色谱柱:VP-ODS柱(4.6mm*250mm,5um),柱温30摄氏度,流动相:甲醇:0.5%冰醋酸溶液(40:60),检测波长:285nm,流速1.0ml/min,进样量20ul。
结果:当进样量为0.05~12微克时,进样量与峰面积有良好的线性关系,仪器具有良好精密度时RSD=1.26%,平均加样回收率为98.54%。
结论:高效液相色谱法测定健胃消食片中橙皮苷含量不仅对加强中药质量控制方面起重要作用,而且对药品中其他成分的含量测定有了深刻的启发。
【关键词】高效液相色谱法;橙皮苷;健胃消食片【中图分类号】R286.0 【文献标识码】A 【文章编号】2095-1752(2017)33-0042-02Determination of Hesperidin in Jianwei Xiaoshi Tablets by High Performance Liquid ChromatographyYu Jie.Suining City Maternal and Child Health Care Family Planning Service Center Pharmacy,Suining 629000,China【Abstract】Objective To determine the content of hesperidin in Jianwei Xiaoshi Tablets by high performance liquid chromatography (HPLC). Methods The chromatographic column: VP-ODS column (4.6mm * 250mm, 5um), column temperature 30℃, mobile phase: methanol: 0.5% glacial acetic acid solution (40:60), detection wavelength: 285nm, Flow rate 1.0ml / min, injection volume 20ul. Results When the injection volume was 0.05 ~12 μg, the injection volume had a good linear relationship with the peak area. RSD = 1.26% and the average recovery was 98.54% when the instrument had good precision. Conclusion The determination of hesperidinin Jianwei Xiaoshi tablet by high performance liquid chromatography is not only an important role in strengthening the quality control of traditional Chinese medicine, but also has a profound inspiration for the determination of other components in medicine.【Key words】HPLC; Hesperidin; Jianwei Xiaoshi tablet健胃消食片是由山楂、陈皮、麦芽、太子参、山药组成的中成药,可采用高效液相色谱法(HPLC法)测定健胃消食片中黄岑苷含量和橙皮苷含量[1]。
健胃消食片中山楂及山药的薄层色谱鉴别

!--.:附录 /01+
!制剂与炮制!
对中药砂炒盐水浸渍炮制方法的讨论
王$ 辉’ ,范冬霞’ ,付志荣!
(’+ 湖北省黄石普仁医院,湖北 黄石$ 53.--!;$ !+ 湖北省黄石市中心医院$ 53.---)
摘要:目的 鉴别穿山甲、鳖甲、鸡内金等砂烫类中药的正品与伪品。方法 对穿山甲、鳖甲、鸡内金等砂烫类中药进行钠
&" %# 山楂的鉴别 取本品 *- C,研细,加水 *- 4D,再加入 * 4ED 3 % 同法制成阴性对照品溶液。另取山药对照药材粉末 + C,同法制 盐酸 27 - 4D,超声处理 ,2 456,加入醋酸乙酯 -2 4D,超声处理 ,2 成对照药材溶液。照薄层色谱法[*]实验,吸取上述供试品溶液、
%# 实验材料
试品色谱中,在与对照药材色谱相应的位置上,显相同的深蓝颜
对照药材:山楂( 中国药品生物制品检定所)、山药( 购于上 色斑点,而阴性对照无干扰。见图 *。
海康桥中药饮片有限公司,经鉴定为薯蓣科植物薯蓣 "#$%&$’() &" &# 山药的鉴别 取本品 *- C,研细,加水洗涤 , 次,*22 4D 3 次。
摘要:目的 建立健胃消食片的薄层色谱鉴别方法。方法 采用薄层色谱鉴别了处方中的山楂、山药。结果 山楂的薄层
色谱鉴别较药典方法样品用量少,操作简单,专属性强;山药的薄层色谱鉴别操作简单,专属性强。结论 结合《 中国药 典》中对太子参的薄层色谱鉴别,可以全面控制该品种的质量;为含山楂、山药的制剂提供了新的薄层色谱鉴别方法。
$ &#山楂药材$ $ $ $ $ $ $ $ $ $ $ &#山药药材$ $ $ $ $ $ $ $ $ [ ’ ]$ 国家药 典 委 员 会+ 中 国 药 典,! 部[ ,]+ 北 京:化 学 工 业 出 版 社,
健胃消食片治疗小儿消化不良临床疗效分析

健胃消食片治疗小儿消化不良临床疗效分析摘要】目的:分析研究健胃消食片对小儿消化不良的治疗效果。
方法:选取2013年3月至2015年3月到我院就诊的消化不良的小儿患者202例,随机分为两组,观察组和对照组各101例。
观察组采取健胃消食片治疗法,对照组采取多潘立酮治疗法,两周后对比两组的疗效。
结果:观察组总有效率为93.14%,明显高于对照组的总有效率(68.32%)(P<0.05)。
结论:健胃消食片对于小儿消化不良有较好的治疗效果,临床效果好、安全性高且适口性好,可作为治疗小儿消化不良的首选药。
【关键词】健胃消食片;消化不良;小儿;临床疗效消化不良是一种常见的消化系统疾病,常发生于小儿,其发病原因多为胃动力不足或胃肠功能紊乱,临床症状为腹胀、腹泻、食欲减退、呕吐等,上腹部多有不适感,若治疗不及时极有可能影响小儿以后的生长发育。
消化不良从中医上来讲起因为脾虚,而健胃消食片由中药制成,具有消食化积、健胃理气的功效。
本研究选取2013年3月至2015年3月的202例消化不良的小儿患者进行了分析研究,观察组使用健胃消食片进行治疗,并与使用西药治疗的对照组进行对比,取得了很好的疗效,现将详细结果报道如下。
1.资料与方法1.1临床资料研究资料共计202例,均来自2013年3月至2015年3月到我院就诊的消化不良的小儿患者。
根据治疗时选用的药物不同将这些资料均分为两组,采用健胃消食片治疗的为观察组,共计101例患儿;采用多潘立酮治疗的为对照组,共计101例患儿。
观察组中有男孩儿56例,女孩儿45例,年龄在2岁到13岁之间,体重在7千克到30千克之间,平均体重(14.01±6.98)kg;对照组中有男孩儿55例,女孩儿46例,年龄在2岁到14岁之间,体重在7千克到32千克之间,平均体重(15.78±6.59)kg。
病例选择标准为:年龄小于15岁;符合小儿消化不良的临床诊断标准;无其他影响疗效评价的疾病;患儿及其家属知情同意并签署知情同意书。
反相液相色谱法测定健胃消食片中薯蓣皂苷元的含量

反相液相色谱法测定健胃消食片中薯蓣皂苷元的含量罗晓燕;蔡力创;欧阳克氙;刘建平【摘要】采用两相溶剂水解法提取健胃消食片中山药所含薯蓣皂苷元,用反相高效液相色谱法检测其含量,由薯蓣皂苷元的量来确定健胃消食片中山药的含量,建立健胃消食片中山药的液相色谱分离测定方法.薯蓣皂苷元在6.24~62.40 μg/mL内与峰面积呈良好的线性关系,回归方程为Y=34.4815X-18.1383,R=0.9999;平均回收率为96.4%,RSD为1.62%.该方法简便,结果准确,重复性好,可作为健胃消食片的质量控制方法.【期刊名称】《南昌大学学报(理科版)》【年(卷),期】2010(034)005【总页数】3页(P480-482)【关键词】健胃消食片;反相高效液相色谱法;山药;薯蓣皂苷元【作者】罗晓燕;蔡力创;欧阳克氙;刘建平【作者单位】江西省科学院生物资源研究所,江西,南昌,330029;江西省科学院生物资源研究所,江西,南昌,330029;江西省科学院生物资源研究所,江西,南昌,330029;江西省科学院生物资源研究所,江西,南昌,330029【正文语种】中文【中图分类】O657健胃消食片为山楂、陈皮、山药、麦芽、太子参等经加工制成的片剂,具有健胃消食的功能,用于脾胃虚弱,消化不良。
而山药具有补脾养胃,生津益肺,补肾涩精的功效,是本品的有效成分。
目前,健胃消食片主要通过橙皮苷、太子参和山楂的含量测定,作为健胃消食片质量控制和考察工艺的稳定性的指标[1],未见以山药所含薯蓣皂苷元含量作为指标。
为更好地控制产品质量,保证产品的疗效,选用以反相高效液相色谱法(RP-HPLC)对制剂中山药所含薯蓣皂苷元含量进行了测定,从而有效地控制产品质量。
1.1 仪器与试剂Agilent1100高效液相色谱仪系列(GB79ADEGASSER;GB14A-QUATPUMP;G1314-VWD); SartoriorsBs210s电子天平;XTerraRP18(150mm× 3.9mm,5um)色谱柱;SG2200H型超声波清洗器; KDM型可调恒温水浴锅。
HPLC测定健胃消食片中橙皮苷的含量
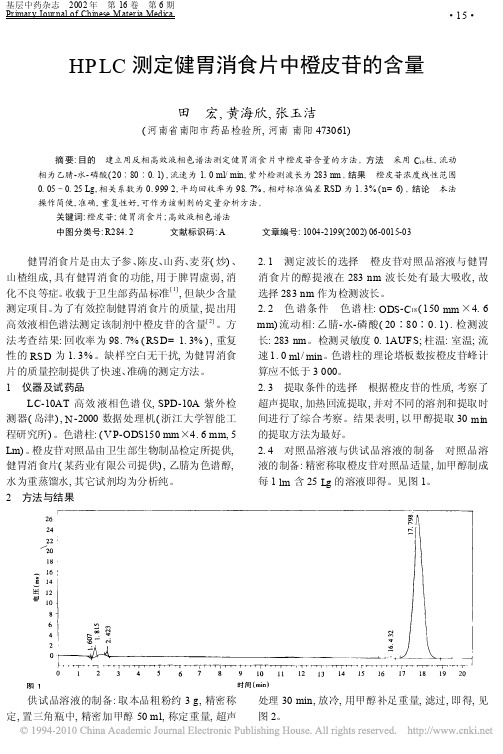
HPLC测定健胃消食片中橙皮苷的含量田 宏,黄海欣,张玉洁(河南省南阳市药品检验所,河南南阳473061) 摘要:目的 建立用反相高效液相色谱法测定健胃消食片中橙皮苷含量的方法。
方法 采用C18柱,流动相为乙腈-水-磷酸(20∶80∶0.1),流速为1.0ml/min,紫外检测波长为283nm。
结果 橙皮苷浓度线性范围0.05~0.25L g,相关系数为0.9992,平均回收率为98.7%,相对标准偏差RSD为1.3%(n=6)。
结论 本法操作简便,准确,重复性好,可作为该制剂的定量分析方法。
关键词:橙皮苷;健胃消食片;高效液相色谱法 中图分类号:R284.2 文献标识码:A 文章编号:1004-2199(2002)06-0015-03 健胃消食片是由太子参、陈皮、山药、麦芽(炒)、山楂组成,具有健胃消食的功能,用于脾胃虚弱,消化不良等症。
收载于卫生部药品标准[1],但缺少含量测定项目。
为了有效控制健胃消食片的质量,提出用高效液相色谱法测定该制剂中橙皮苷的含量[2]。
方法考查结果:回收率为98.7%(RSD=1.3%),重复性的RSD为1.3%。
缺样空白无干扰,为健胃消食片的质量控制提供了快速、准确的测定方法。
1 仪器及试药品LC-10AT高效液相色谱仪,SPD-10A紫外检测器(岛津),N-2000数据处理机(浙江大学智能工程研究所)。
色谱柱:(V P-ODS150mm×4.6mm,5 L m)。
橙皮苷对照品由卫生部生物制品检定所提供,健胃消食片(某药业有限公司提供),乙腈为色谱醇,水为重蒸馏水,其它试剂均为分析纯。
2 方法与结果2.1 测定波长的选择 橙皮苷对照品溶液与健胃消食片的醇提液在283nm波长处有最大吸收,故选择283nm作为检测波长。
2.2 色谱条件 色谱柱:ODS-C18(150mm×4.6 mm)流动相:乙腈-水-磷酸(20∶80∶0.1).检测波长:283nm。
健胃消食片试验资料

3、样品批号:100302、100303、100304
4、包 装:口服固体药用高密度聚乙烯瓶包装
三、考察项目及方法
将上述三批样品按市售包装要求,采用口服固体药用高密度聚乙烯瓶包装。根据
药瓶包装材料与药物相容性试验指导原则中所列片剂稳定性重点考察项目进行,
具体考察项目为性状、崩解时限、含量。以上项目均根据健胃消食片质量标准进
18 24 36 0 3 6 9 100304
衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后 显淡棕黄 色;气香, 味微甜、酸 本品为薄膜 衣片,除去 薄膜衣片后
2、方法 2、1 菌液制备:接种金黄色葡萄球菌、大肠埃希菌、枯草杆菌新鲜培养物至营 养肉汤培养基中,在 30~35℃下培养 18~24 小时;接种白色念珠菌、黑曲霉的新 鲜培养物至改良马丁培养基或改良马丁琼脂培养基中,在 23~27℃下培养 24~120 小时,上述培养物用 0.9%无菌氯化钠溶液制成每 1ml 含菌数为 50~100CFU 的菌 悬液,备用。
批号
改良马丁琼脂培养基 改良马丁培养基 营养肉汤培养基
101210 101125 100628
营养琼脂培养基
101108
胆盐乳糖培养基
100609
PH7.0 氯化钠-蛋白胨缓 100424 冲液
健胃消食片质量标准的研究
HEI LONGJ ANG M E CI I DI NE AND H ARM AC Au . 0 7 Vo. 0No 4 P Y g 2 0 , 13 .
・1 ・ 7
健 胃消食 片质量 标 准 的研 究
李桂 红 苏德 龙。张金 飞。刘 洪伟。 , , ,
1 材 料 与 试 药
醇 1 使溶解 , mL 作为 供 试 品溶 液 。 取 山楂对 照药 材2 加 水 另 g, 10 0mL, 煮 1 , 过 , 液 浓 缩 至 2mL, 稀 盐 酸 调 节 p 煎 h滤 滤 0 用 H 值 至 I 2 用 乙 酸 溶 ~ , 同 液 。取 缺 山楂 的 样 品 , 供 试 品溶 液 制 备方 法 制 成 阴 性 对 照 按
2 3 陈 皮 的鉴 别 . 取 本 品 3 O片 , 去 包 衣 , 细 , 锥 形 瓶 中 , 甲 醇 除 研 置 加 10 0mL, 声 提 取 3 mi, 过 , 液 蒸 干 , 渣 加 甲醇 2 超 0 n滤 滤 残 mL 使 溶 解 , 为 供 试 品溶 液 。另 取 橙 皮 苷 对 照 品 , 甲醇 制 成 每 1 作 加 毫升含 47 .mg的溶 液 , 为 对 照 品 溶 液 。再 取 陈 皮 对 照药 材 作 0 7 , 甲 醇 1 mL, 声 提 取 3 mi , 过 , 液 浓 缩 至 2 .g加 0 超 0 n滤 滤 mL, 作 为 对 照 药 材 溶 液 。取 缺 陈 皮 的 样 品 , 供 试 品 溶 液 制 备 方 按
2 1 太 子 参 的 鉴 别 .
取本品3 O片 , 去 包 衣 , 细 , 甲 醇 5 mL, 热 回 流 除 研 加 0 加 3 mi, 过 , 液 蒸 干 , 渣 加 水 2 mL使 溶 解 , 过 AB 0 n滤 滤 残 0 通 8型 大孔 树 脂 柱 ( 径 1 2m , 高 1c , 水 3 0 内 Ic 柱 m)用 5 0 mL洗 脱 , 去 弃 水 洗液 , 用 7 乙醇 2 0 脱 , 集 乙 醇 洗 脱 液 , 干 , 再 O 0 ml洗 收 蒸 残 渣加 甲醇 】 溶 解 , 为 供 试 品 溶 液 。另 取 太 子 参 对 照 ml使 作 药 材 5 , 水 煎 煮 2 , 心 , 上 清 液 , 过 AB 型 大孔 树 脂 g用 h离 取 通 8 柱 , 法 制 成 对 照 药 材 溶 液 。 缺 太 子 参 的样 品 , 供 试 品 溶 同 取 按 液 制 备方 法 制 成 阴性 对 照 样 品溶 液 。 薄 层 色 谱 法 (中 国 药 照 《 典 )0 5年 版 一部 附 录 VI ) 验 , 取 上 述 3种 溶 液 各 7 L, 20 试 B 吸 , u 分别 点 于 同一 硅 胶 G 薄 层 板 上 , 以环 己 烷 一醋 酸 乙 酯 一 甲 酸 ( 0: 0: ) 2 2 1 为展 开 剂 , 开 , 出 , 干 , 以 1 香 草 醛 硫 展 取 晾 喷 酸溶液 , 15 于 O ℃加 热 至 斑 点 显 色清 晰 。供 试 品 色 谱 中 , 与 在 对 照药 材 色 谱 相 应 的 位 置 上 . 相 同 的 颜 色 斑 点 。 阴性 对 照 显 样 品在 其 相 应 的 位 置 上 , 显 相 同 颜 色 的 斑 点 。结 果 见 图 1 不 。
健胃消食片中熊果酸的含量测定
HL P C法测定健 胃消食片 中熊果酸的含量 , 灵敏 度高 、 准确 、 快速 、 属性强 、 专 重现性好 。可用于健 胃消食
片 中熊果 酸 的含 量 测片 ; P C; 熊果酸
D t mia o f sl c i w i i si a l LU W WU Y— og G a gh uC eli h r ee n t no o cA i i Ja eXa h be r i Ur i dn n o T t / e. ihn . u nzo hni P a— z j
a on w s .3 0 3 g 1 vrg eoe a 9 .4 ,R D 0 8 % ( m u t a 0 0 2— . 2 ,1 eaeaercvr w s 9 7 % 1 y S . 4 n:6 . o cui T e ) C nls n o h
meh d i i l ,fs n c u ae I c n b s d frt e q ai o t l fJa w i a s i a lt to ssmp e a t d a c rt . t a e u e o u l y c n r in eXio h be . a h t oo t
当提高温度 一方 面有 利 于 蔗糖 的水 解 , 利 于脱 水 有 反应 的进 行 , 应 温 度 低 , 解 速 度 慢 , 水 不 完 反 水 脱 全, 收率低 。但温 度 过 高 , 然 水 解 完全 , 可能 发 虽 但 生产 物深度 裂解 , 化 , 合 , 反应 物 粘 稠 , 黑 , 氧 聚 使 焦
h o a ewa . / n T ee t a ee gh w s2 0 n Re u t T e f w r t s1 0 ml mi . e d t cie w v ln t a 1 m. s l T el e rr n e o roi cd l h v s h i a a g f s l a i n u c
健胃消食片中熊果酸的含量测定
健胃消食片中熊果酸的含量测定刘炜 吴义忠摘要 目的 建立健胃消食片中熊果酸的含量测定方法。
方法 采用HPLC法测定熊果酸含量,ODS为色谱柱,流动相为乙腈-0 2%磷酸(90:10),检测波长210n m,流速1m l/m i n。
结果 熊果酸进样量在0 032~0 32 g范围内线性关系良好,平均回收率99 74%,RSD为0 84%(n=6)。
结论HPLC法测定健胃消食片中熊果酸的含量,灵敏度高、准确、快速、专属性强、重现性好。
可用于健胃消食片中熊果酸的含量测定。
关键词 HPLC;健胃消食片;熊果酸Determ i nation ofU rsolic Aci d i n Jianwei X iaoshi Tabl et L IU Wei,WU Yi-zhong.Guangzhou Chenliji Phar-m aceutica Fact ory.Guangzhou510130,ChinaAbstract Objective To establi sh a m et hod for deter m i n i ng ursoli c aci d i n Ji an w ei X i aosh i tab l e.t M ethods HPLC m ethod w as used.Themob ile phasew as aceton itrile-0 2%phosphori c acid sol ution(90:10). The fl ow rate was1 0m l/m i n.The detecti ve w avelength w as210n m.R esults The li near range of ursolic acid a m ount was0 032~0 32 g,The average recovery w as99 74%,RSD0 84%(n=6).Conclusi on The m ethod i s sm i p l e,fast and accurate.It can be used for the qualit y control of Jian w ei X iaos h i table.t K ey words Jianwei X iaos h i Tab l e;t H PLC;U rsolicA ci d健胃消食片有健胃消食的功能,临床多用于脾胃虚弱所致的食积之症,处方由太子参、陈皮、山药、炒麦芽、山楂组成。
高效液相色谱法测定消食健胃片中绿原酸的含量
高效液相色谱法测定消食健胃片中绿原酸的含量发表时间:2015-10-30T15:56:46.677Z 来源:《医药前沿》2015年第26期供稿作者:成霄朱佳茜[导读] 湖州市食品药品检验研究院浙江湖州消食健胃片是一种常见的胃肠道消化药,有山楂、麦芽、六神曲、槟榔组成,一直以来都未对其含量进行控制。
成霄朱佳茜(湖州市食品药品检验研究院浙江湖州 313000)【摘要】目的:建立消食健胃片中绿原酸含量测定的方法。
方法:采用高效液相色谱法,以ZORBAX SB-C18(4.6mm×150mm,5μ)为色谱柱,流动相为乙腈-0.4%磷酸(13:87),流速1.0 mL?min-1,检测波长为327nm。
结果绿原酸在0.0050mg?mL-1~0.0500 mg? mL-1范围内线性关系良好(r=1.0000),平均回收率为99.59%,RSD=0.94%。
结论:该方法准确、可靠、重复性好、专一性强,可用于消食健胃片中绿原酸的含量测定。
【关键词】消食健胃片;绿原酸;高效液相色谱【中图分类号】R927.2 【文献标识码】A 【文章编号】2095-1752(2015)26-0372-02 Quantitative Determination of Chlorogenic acid In Xiao Shi Jian Wei Pian by HPLC Cheng Xiao,Zhu Jiaxi. Huzhou Institutes for Food and Drug Control,Huzhou,313000,China 【Abstract】Objective To study and establish the reversed phased high performance liquid chromatography method for determination of Chlorogenic acid in Xiao Shi Jian Wei Pian. Method The chromatographic conditions were as follows: Agilent ZORBAX SB-C18(4.6×150mm,5μ),column was used as stationary phase,the mobile phase was composed of Acetonitrile and 0.4% phosphoric acid solution (13:87),the flow rate was 1.0 mL?min-1;the UV absorbance detection wavelength was set at 327nm. Results The Chlorogenic acid curve was linear within the range of 0.0050-0.0500 mg?mL-1(r=1.0000);The average recovery of Chlorogenic acid was 99.59%. Conclusion The result showed that this method was convenient、rapid 、sensitive、reproducible and accurate. It can be used in determination of Chlorogenic acid in Xiao Shi Jian Wei Pian.【Key words】Chlorogenic acid; Xiao Shi Jian Wei Pian ; HPLC 消食健胃片是一种常见的胃肠道消化药,有山楂、麦芽、六神曲、槟榔组成,一直以来都未对其含量进行控制。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
健胃消食片检验方法确认文件编号:贵州省科晖制药厂健胃消食片检验方法确认方案起草人_____________ 部门____________ 日期___________ 审核人_____________ 部门____________ 日期___________ 审核人_____________ 部门____________ 日期___________ 批准人_____________ 日期__________ _目录一、确认方案1.概述2.确认的原则和目的3.确认的项目和范围4.组织及职责4.1确认方案和报告的起草、审核、批准4.2确认方案的培训4.3组织实施过程中的变更和偏差4.4实施组织人员5.样品和标准品信息6.分析仪器7. 实施检验人员信息8. 确认方法8.1鉴别检验方法确认8.2含量测定确认9.结论报告二、确认报告三、确认证书1、概述健胃消食片收载于《中国药典》2010年版一部,本公司生产的规格为0.5g/片,其检测主要内容为:【性状】本品为浅棕黄色的片;气微香,味微甜、酸。
【鉴别】(1)取本品48片,研细,加甲醇50ml,加热回流30分钟,滤过,滤液蒸干,残渣加水20ml使溶解,通过D101型大孔吸附树脂柱(内径为1.2cm,柱高为15cm),用水200ml洗脱,弃去水洗液,再用乙醇100ml洗脱,收集乙醇洗脱液,蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取太子参对照药材5g,加水煎煮2小时,离心,取上清液,通过D101型大孔吸附树脂柱,同法制成对照药材溶液。
照薄层色谱法(中国药典2010年版一部附录VI B)试验,吸取上述两种溶液各20μl,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯(4︰1)为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,于105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。
(2)取本品48片,研细,加甲醇50ml,加热回流30分钟,滤过,滤液蒸干,残渣加水20ml使溶解,用乙酸乙酯振摇提取2次,每次20ml,合并乙酸乙酯液,蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取山楂对照药材2g,加水100ml,煎煮1小时,滤过,滤液浓缩至20ml,用稀盐酸调pH值至1~2,用乙酸乙酯振摇提取两次,同法制成对照药材溶液。
照薄层色谱法(《中国药典》2010年版一部附录VI B)试验,吸取上述两种溶液各20μl,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-甲酸(20:20:1)为展开剂,展开,取出,晾干,喷以2%三氯化铁乙醇溶液,在105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的主斑点。
【检查】重量差异按《中国药典》2010年版一部附录项下[重量差异] 检查法依法检查,应符合规定。
崩解时限按《中国药典》2010年版一部附录崩解时限检查法依法检查,应符合规定。
【含量测定】照高效液相色谱法(中国药典2010年版一部附录VI D)测定。
本品每片含陈皮以橙皮苷(C28H34O15)计,不得少于0.12mg。
色谱条件与系统适用性实验以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.5%冰醋酸溶液(40:60)为流动相;检测波长283nm。
理论塔板数按橙皮苷峰计算应不低于2000。
对照品溶液的制备取橙皮苷对照品约12.5mg,精密称定,置100ml量瓶中,加甲醇使溶解并稀释至刻度,摇匀,精密量取3ml,置25ml量瓶中,加50%甲醇稀释至刻度,摇匀,即得(每1ml中含橙皮苷15ug)。
供试品溶液制备取重量差异项下的本品,研细,取约2g,精密称定,精密加入甲醇20ml,称定重量,置水浴上加热回流1小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置10ml量瓶中,加水稀释至刻度,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。
2、确认的原则和目的建立健胃消食片测定方法的确认方案,在实验过程中需严格按照标准操作,确保试验结果真实可信,以确认健胃消食片按《中国药典》2010年版一部检验方法在本化验室的可靠性。
3、确认的项目和范围为了解其检验方法的可靠性,我们对其主要项目:三项鉴别和含量测定进行方法确认。
其余常规检查项目则不必确认,微生物限度的验证另行进行验证。
4.组织及职责4.1确认方案和报告的起草、审核、批准该检验方法确认方案由化验室负责起草,方案经化验室、验证委员会、质量部等部门审核,最终由验证委员会主任批准。
确认过程实施完成后,确认过程由方案起草人负责汇总,并经化验室、验证委员会、质量部部门主管审核,最终由验证委员会主任批准报告及合格证书。
4.2确认方案的培训确认方案起草人在方案经验证委员会批准后及确认方案实施前,对本次确认实施的相关人员组织培训工作,由化验室主管领导人负责该次验证方案的培训工作,并将该次的培训记录交至人力资源部归档。
4.3组织实施过程中的变更和偏差该次确认工作组织实施由化验室、验证委员会主管领导负责,质量部负责对验证过程中的变更和偏差进行确认。
4.4实施组织人员部门姓名验证分工化验室负责确认工作的安排。
确保验证工作按方案进行。
负责起草验证方案、验证报告,负责对相关人员进行培训。
负责按照方案的要求执行,并记录检验原始记录,负责将检查结果填写在本方案的附件记录表中。
质量部确认方案适用法令规章、标准、产品质量标准;偏差管理(如果需要)。
负责验证过程的监督工作安排。
负责对验证中出现的问题提出指导意见负责审核批准偏差。
验证委员会协助起草验证方案,为验证过程提供技术支持,并负责保存所有验证相关资料以备查。
协调验证的正常进行,为验证过程提供技术支持。
总验证委员会主任负责验证方案及报告的审核与批准,提供资源,颁发验证证书。
5.样品和标准品信息在验证前应确认供试品信息;确认所使用的标准品信息及对照品溶液应在有效期内。
确认信息见附表1。
6. 分析仪器在验证前应确认所使用的电子天平、高效液相色谱仪、鼓风干燥箱可正常使用,计量合格证在效期内,确认信息见附表2。
7. 实施检验人员信息检验人员信息见附表38. 确认方法由两名检验人员,分别按以下的检验方法采用不同检验仪器(如有)分别测定同一批次健胃消食片供试品,对两人的检验结果进行比较确认,比较结果应符合各项目的可接受标准。
8. 1鉴别检验方法确认操作方法:(1)取本品48片,研细,加甲醇50ml,加热回流30分钟,滤过,滤液蒸干,残渣加水20ml使溶解,通过D101型大孔吸附树脂柱(内径为1.2cm,柱高为15cm),用水200ml洗脱,弃去水洗液,再用乙醇100ml洗脱,收集乙醇洗脱液,蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取太子参对照药材5g,加水煎煮2小时,离心,取上清液,通过D101型大孔吸附树脂柱,同法制成对照药材溶液。
照薄层色谱法(中国药典2010年版一部附录VI B)试验,吸取上述两种溶液各20μl,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯(4︰1)为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,于105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。
(2)取本品48片,研细,加甲醇50ml,加热回流30分钟,滤过,滤液蒸干,残渣加水20ml使溶解,用乙酸乙酯振摇提取2次,每次20ml,合并乙酸乙酯液,蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取山楂对照药材2g,加水100ml,煎煮1小时,滤过,滤液浓缩至20ml,用稀盐酸调pH值至1~2,用乙酸乙酯振摇提取两次,同法制成对照药材溶液。
照薄层色谱法(《中国药典》2010年版一部附录VI B)试验,吸取上述两种溶液各20μl,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-甲酸(20:20:1)为展开剂,展开,取出,晾干,喷以2%三氯化铁乙醇溶液,在105℃加热至斑点显色清晰。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的主斑点。
可接受标准:两个试验人员,采用不同检验仪器(如有)分别测定同一批次的供试品,两人的测试均应显相同且符合规定的结果。
记录见附表4。
8. 2含量测定确认操作方法:色谱条件与系统适用性实验以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.5%冰醋酸溶液(40:60)为流动相;检测波长283nm。
理论塔板数按橙皮苷峰计算应不低于2000。
对照品溶液的制备取橙皮苷对照品约12.5mg,精密称定,置100ml量瓶中,加甲醇使溶解并稀释至刻度,摇匀,精密量取3ml,置25ml量瓶中,加50%甲醇稀释至刻度,摇匀,即得(每1ml中含橙皮苷15ug)。
供试品溶液制备取重量差异项下的本品,研细,取约2g,精密称定,精密加入甲醇20ml,称定重量,置水浴上加热回流1小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置10ml量瓶中,加水稀释至刻度,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。
可接爱标准:两个试验人员,采用不同检验仪器分别测定同一批次的供试品,两人测试结果的相对偏差应≤2.0%。
记录见附表5。
9. 结论报告根据实验结果,起草相关的结论报告。
健胃消食片检验方法确认报告1.概述:1.2. 验证概述:设备验证小组根据该产品的验证方案(方案号: )于年月日至年月日用批号:健胃消食片供试品,对该品种的主要检验项目薄层鉴别、含量测定的检验方法进行了确认。
1.3鉴别检验方法确认年月日至年月日对健胃消食片的鉴别检验方法进行了确认,两名检验员的结果均符合相关要求。
具体记录见附表4。
1.4 含量测定检验方法确认:年月日至年月日对健胃消食片的含量测定方法进行了确认,两名检验员的结果偏差,结果均符合相关要求。
具体记录见附表5。
2.评价与建议确认实验由经培训合格的检验员进行实验,所使用的仪器均有计量合格证且在效期内,实验结果均符合要求,确认的检验方法可用于健胃消食片的检测。
3. 验证结论:检验方法经确认符合要求,可用于该品种的检验方法操作。
姓名工作部门日期备注起草人化验室会审人化验室验证委员会质量部批准人验证委员会主任附表1 供试品及对照品信息项目 供试品 标准品 品名 健胃消食片含量测定用橙皮苷对照品 鉴别用太子参对照药材 鉴别用山楂 对照药材批号 浓度 有效期至 确认人附表2 检验仪器信息分析天平 高效液相色谱仪鼓风干燥箱设备编号运行状态 计量合格证 确认人附表3 实验人员信息编号 姓名 所属部门A B附表4 鉴别检验方法确认 检验人员检验结果可接受标准鉴别(1)鉴别(2)两个试验人员,采用不同检验仪器(如有)分别测定同一批次的供试品,两人的测试均应显相同且符合规定的结果。
