第四章 核磁共振波谱
有机波谱分析 第四章 核磁共振波谱

4-1-5 核磁共振与核自旋能级跃迁
E
−
0 无磁场
γhH0 ∆Ε = 2π
γhH0 1 (m = − ) 4π 2
γhH0 1 + (m = + ) 4π 2
γ:磁旋比 h: Plank常数 Ho: 磁场强度 m: 磁量子数
(Ho)
由能级分裂现象说明,高场强仪器比低场强仪器测得的核磁共振信号清晰。 由能级分裂现象说明,高场强仪器比低场强仪器测得的核磁共振信号清晰。
µ
r
只有当I 只有当 > O时,才能发生共振吸收,产生 时 才能发生共振吸收, 共振信号。 共振信号。
原子核自旋时,会产生一个磁场, 原子核自旋时,会产生一个磁场,两磁极间的 磁偶极的大小称为核磁矩µ 核磁矩是一个矢量, 磁偶极的大小称为核磁矩µ。核磁矩是一个矢量,方 的方向重合。 成正比: 向与自旋角动量P的方向重合 其大小与P成正比 向与自旋角动量 的方向重合。其大小与 成正比: γP γ为磁旋比,代表原子核的特性) µ = γ (γ为磁旋比,代表原子核的特性
H0
黄石理工学院医学院药学系
自旋的质子
4-1-2原子核的自旋与核磁距 原子核的自旋与核磁距
大多数原子核可围绕某个轴作自身 旋转运动,可用自旋角动量P来描述 来描述, 旋转运动,可用自旋角动量 来描述, 其方向与旋转轴重合, 其方向与旋转轴重合,其值由下式 决定: 决定: h
P=
2π
I (I +1)
黄石理工学院医学院药学系
小结: 小结:共振条件
(1) 核有自旋 磁性核 核有自旋(磁性核 磁性核) (2)外磁场,能级裂分; 外磁场,能级裂分 外磁场 (3)照射频率与外磁场的比值ν0 / H0 = γ / (2π ) 照射频率与外磁场的比值 π
第四章 核磁共振波谱法-氢谱 第四节

↓ ↓ 1/4
氢核相邻三个H原子,H核裂分为四重峰。强度比为1 ︰3 ︰3 ︰1
(4)裂分峰之间的峰面积或峰强度之比符合二项展开式 各项系数比的规律。(a+b)n n为相邻氢核数
n=1 (a+b)1
1︰1
n=2 (a+b)2
1︰2 ︰1
n=3 (a+b)3
1︰3︰3 ︰1
(5)氢核邻近有两组偶合程度不等的H 核时,其 中一组有n个,另一组有n’个,则这组H 核受两 组 H 核自旋偶合作用,谱线裂分成(n+1)(n’+1) 重峰。偶合程度相同时,谱线裂分成(n+n’+1)。
(4)两组氢核相互偶合的J值必然相等,即:Jab=Jba (5)氢核相互偶合的值变化很大,为1-50 。 通过双
数键偶合的为负值,用2J, 4J…表示,使用时用绝对 值;通过单键偶合的J为正值,用1J, 3J…表示。
(6)H 与H 的偶合常数可分为同碳偶合常数 、 邻碳 偶合常数 、 运程偶合常数 、 芳香族及杂原子化合 物偶合常数等(参考书上内容,P.120-P.128)。
若 X 核的自旋量子数 I =1/2,在外磁场 B0中 X 核有 两种不同取向 m = +1/2 和 m = -1/2,它们分别产生两个
强度相同( B ),方向相反的小磁场,其中一个与外磁场 方向 B0相同,另一个与 B0相反。这时 A 核实际受到的磁 场强度不再是 B0(1-),而是[B0(1-)+ B ]和[B0 (1-)-B],因此 A 核的共振频率应为:
(1)J 值的大小与B0无关。影响J值大小的主要因素是原子 核的磁性和分子结构及构象。因此,偶合常数是化合物分子
结构的属性。
(2)简单自旋偶合体系J值等于多重峰的间距,复杂自旋偶
波谱分析第四章5自旋偶合与自旋裂分

22
(1)丙烯型偶合
通过三个单键和一个双键的偶合(H-C =C-C-H); J 为负值(0~-3Hz); 大小与双面夹角有关,θ为90°时偶合最强,θ为0°和 180°时偶合最小。
H
CH3
CC
13CH2F2
A 2M 2X
H
Cl
H
A A 'B B '
11
三、相互偶合的一般规则
1.一组相同的磁核,所具有裂分峰的数目: 由邻近的磁核数目(n)决定的 裂分峰数目 = 2In+1 当有不同的邻近时(n、n’) 裂分峰数目=( n+1)(n’+1)
C l C l Hc C l C C C Hc
Ha Hb Hc
X Hb
C从OHH锯O、、齿HH型65 远JJ程均均偶约约合00..6,4HHz判z 断-OH 与–NO2形成氢键
26
1,1,2-三氯丙烷 Hb 与Ha和Hc的偶合 (Jab ≠ Jac) Hb =( n+1)(n’+1)= (1+1)(3+1)=8
2. 裂分峰强度比相当于二项式(a+b)n展开式的系数比
n=2 1:2:1;
n=3 1:3:3:1 ;
n=4 1:4:6:4:1
3.裂分峰以该质子化学位移为中心,峰形左右对称。
、Y、Z… (δ位于低场);K、L △ν/J< 6用相差较近的字母表示
、M…(δ位于中场);
AX、AMX、AB、ABC…等系统
(3)每一种磁全同的核的个数写在大写字母右下角。
(4)I=1/2的非氢核(13C、15N、19F
波谱分析-第四章_核磁共振-3

1、饱和现象
对于氢核(1H),由于外磁场作用造成能级 分裂的∆E 比电子能级、振动能级差小4~ 8个数量级,室温下比值仅为1.0000099, 即每一百万个氢核中低能级氢核比高能级 的多10个左右。 当n+= n-时,就观察不到 NMR 信号, 这种现象称为“饱和”。
2、驰豫
自发辐射的几率与能级差成正比 。
两种取向不完全 与外磁场平行, =54˚24′ 和 -125˚36 ′
当一个原子核的核磁矩处于磁场B0中,由 于核自身的旋转,而外磁场又力求它取向 于磁场方向,在这两种力的作用下,核会 在自旋的同时绕外磁场的方向进行回旋, 这种运动方式称为进动或拉莫进动。
若进动频率 回, 则拉莫方程式:
2 p 回 = B0
§4.2 核磁共振基本原理
一、原子核的自旋
原子=原子核+电子
原子核=质子+中子(=质量数)
原子核是带正电荷的粒子
若原子核存在自旋, 产生自旋角动量( P ):
2015-5-21
9
自旋角动量是一个矢量, 是空间方向量子化的。
P = h I(I + 1) 2p
h:普朗克常数; I:自旋量子数,与核的质量 数和所带电荷数有关;
类似于红外或紫外吸收光谱,是吸收光谱 的另一种形式。
附:核磁共振与紫外光谱、红外光谱比较
紫外-可见 红外 红外光 800nm~ 1000m 核磁共振 无线电波1~100m, 波长最长,能量最小, 不能发生电子振动、 转动能级跃迁
吸收 能量
紫外可见光 200~800nm
跃迁 类型
价电子能级 跃迁
振动及转动 能级跃迁
13
二、 自旋核在磁场中的行为——回旋和核磁共振 自旋量子数 I为半整数的原子核(1H、 13C等),可当作电荷均匀分布的球 体,绕自旋轴转动时,产生磁场,类 似一个小磁铁。
第四章核磁共振HNMR ppt课件

两种自旋取向能级差与外磁 场B0的关系
2020/11/13
19
现在从另一角度来讨论核磁共振现象。
在B0中,原子核绕其自旋轴旋转(自旋 轴与核磁矩μ方向一致),而自旋轴又与静磁 场B0保持某一夹角θ,而绕B0进动,称为 Larmor进动(如图所示)
2020/11/13
I=1/2的核的Larmor进动
尽管共振频率各有差异,但差异不大,仅为百万 分之十左右,对其绝对值的测量难以达到所需要 的精度。
2020/11/13
32
故实际工作中是采用测定相对值来表示,即 以某标准物质的共振峰为原点,测定样品中 各共振峰与原点的相对距离,这种相对距离 就称为化学位移(Chemical shift)。
2020/11/13
26
4.1.4 驰豫过程 1.弛豫过程
当大量的原子核在外磁场中取向并达到平衡,高低能 级的分布可利用Boltzman定律来描述。即低能级的数目 略多于高能级的数目,且ΔE极小。当用射频电磁波照射外 磁场中原子核时,低能级的核吸收能量跃迁至高能级,产 生核磁共振信号。由于ΔE极小,高能级粒子通过自发辐射 回到低能级的几率几乎为零。因此若要在一定时间间隔内 持续检测到NMR信号,必须有某种过程存在,它使高能级 的原子核回到低能级,以保持低能级的粒子数始终略大于 高能级的粒子数。这个过程就是弛豫过程。
ωL=ω=2πν=γB0
ν共振= γB0/2π
参见下面的示意图
2020/11/13
22
核磁能量吸收和跃迁过程
2020/11/13
23
下面对核磁共振方程进行讨论
( ν共振= γB0/2π )
①对于同一核,如I=1/2的1H核,发生共振时,
ν照射与B0的关系
波谱解析 第四章 碳谱作业参考答案
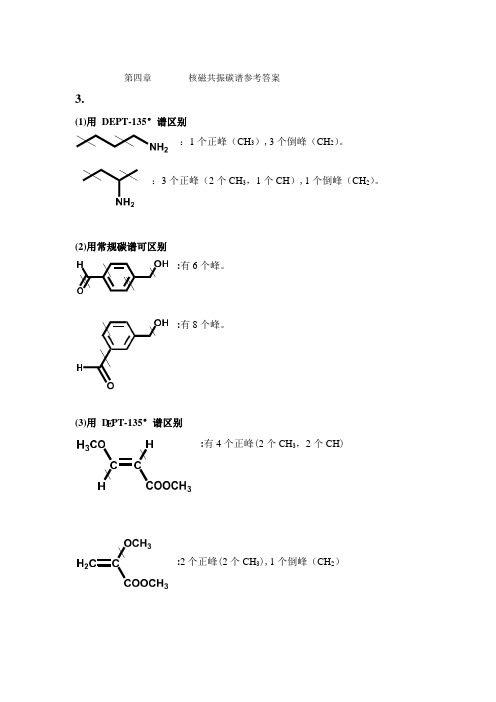
E : (3)用 D PT-135°谱区别 第四章 核磁共振碳谱参考答案3.(1)用 DEPT-135°谱区别:1 个正峰(CH 3),3 个倒峰(CH 2)。
:3 个正峰(2 个 CH 3,1 个CH ),1 个倒峰(CH 2)。
(2)用常规碳谱可区别:有 6 个峰。
有 8 个峰。
:有 4 个正峰(2 个 CH 3,2 个 CH ):2 个正峰(2 个 CH 3),1 个倒峰(CH 2)6.1)由分子式C5H9O2Br 计算不饱和度Ω=1,结构中可能含一个双键或一个环。
2)1H NMR 解析:1.25(t):CH x-CH2- ;2.85(t): 弱吸电子基团-CH y-CH2- ;3.55(t): 弱吸电子基团-CH z-CH2- ;4.20(q): -CO2-CH m-CH3(该基团CH m必定与吸电子基团相连。
根据化学位移和分子式可初步判断是与酯基氧原子相连) 3)13C NMR 解析:共有五条峰,与结构式中碳数一致,说明分子中不含对称元素。
178.2(s): 羧酸或其衍生物的C=O;60.8(t): -CH2-,与氧原子相连37.8(s): -CH2-,可能与弱吸电子原子相连26.5(t): -CH2-,可能与弱吸电子原子相连14.2(q): -CH34)推断过程:碳谱表明分子中有1 个羰基,3 个亚甲基和1 个甲基,因此氢谱中4.20ppm 处必定为亚甲基,所以分子中含CO2CH2CH3片段,再结合氢谱,该片段中CH3出峰应该在1.25ppm 处。
这样一来,可以进一步推断2.85 和3.55ppm 处的信号必然是剩余两个亚甲基,由于都为t 峰,这两个亚甲基必定相连,所以推测出分子含有片段CH2CH2,且两端都连有弱吸电子基团。
至此,分子中含有如下片段:一个B(r(端基),因此该化合物的结构为:端基),一个CH2CH2,一个CO2CH2CH38.1)由分子式C8H5NO2可算出不饱和度Ω=7,结构中可能含有苯环。
第四章 核磁共振-氢谱

4.1.3 核的回旋和核的共振
当一个原子核的核磁矩处于磁场HO中,由于核自身的旋 转,而外磁场又力求它取向于磁场方向,在这两种力的作用 下,核会在自旋的同时绕外磁场的方向进行回旋,这种运动称 为Larmor进动。
自旋量子数( I ) 1/2 没有外磁场时,其自旋磁距取向是混乱的 在外磁场H0中,它的取向分为两种(2I+1=2) 一种和磁场方向相反,能量较高 (E=μH0) 一种和磁场方向平行,能量较低 ( E= 0)
前言 过去50年,波谱学已全然改变了化学家、生物学家和生 物医学家的日常工作,波谱技术成为探究大自然中分子内部 秘密的最可靠、最有效的手段。NMR是其中应用最广泛研 究分子性质的最通用的技术:从分子的三维结构到分子动力 学、化学平衡、化学反应性和超分子集体、有机化学的各个 领域。 1945年 Purcell(哈佛大学) 和 Bloch(斯坦福大学) 发现核磁共振现象,他们获得1952年Nobel物理奖。 1951年 Arnold 发现乙醇的NMR信号,及与结构的关 系。 1953年 美国Varian公司试制了第一台NMR仪器。
4.2.4 核磁共振图谱
CHCl3
低场
向左
(δ 增大)
磁场强度
向右
(δ 减小)
高场
图3-5 乙醚的氢核磁共振谱
4.3. 氢的化学位移
4.3.1 化学位移
在一固定外加磁场(H0)中,有机物的1H核磁共 振谱应该只有一个峰,即在:
= E / h = · ( 1/2)· H0
分子中各种质子(原子核)由于所处的化学环 境不同,而在不同的共振磁场下显示吸收峰的 现象,称为化学位移,表示:δ/ppm。
核磁共振的条件:
ΔE = h v迴= h v射= hH0/2π 或 v射= v迴= H0/2π
核磁共振波谱法-氢谱

级E1向高能级E2跃迁,所需能量为: △E=E2-E1= B0 -(-B0) = 2 B0 △E与核磁矩及外磁场强度成正比,外加磁场 B0越大,能级分裂越大,△E越大。
无磁场 (简并) m= -1/2 E2= +B0 △E=2 B0 m= +1/2 E1= - B0
由式 E = -B0及图可知1H核在磁场 中,由低能
= 0.99999
处于低能级的核数比高能态核数多十万分之一, 而NMR信号就是靠这极弱过量的低能态核产生的
若以合适的射频照射处于磁场的核,核吸收能量 后,由低能态跃迁到高能态,其净效应是吸收能 量,产生共振信号。 若高能态核不能通过有效途径释放能量回到低能 态,低能态的核数越来越少,一定时间后, N(-1/2)=N(+1/2),这时不再吸收,核磁共振信号消失, 这种现象为“饱和”。 必须通过核自旋弛豫来保持低能态的核的数目占 微弱多数。 据波尔兹曼定律,提高外磁场强度,降低工作温 度,可减少 N(-1/2) / N(+1/2)值,,提高观察NMR信号 的灵敏度。
仪器组成:
1、永久磁铁:提供外磁场, 要求稳定性好,均匀,不均匀 性小于六千万分之一。 2、射频振荡器:线圈垂直于 外磁场,发射一定频率的电磁 辐射信号。60MHz至600MHz或 更高。 3、射频信号接受器(检测 器):当质子的进动频率与辐 射频率相匹配时,发生能级跃 迁,吸收能量,在感应线圈中 产生毫伏级信号。
26.75 6.73 -2.71 25.18 10.84
核自旋能级分布和驰豫:
(一)核自旋能级分布
1H核在磁场作用下,被分裂为m=+1/2和
m=-1/2两个能级,处在低能态核和处于高能态 核的分布服从波尔兹曼分布定律:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• 裂分峰的相对强度,可用二项式(a+b)n展开的系数表示(n 为等位H的个数),各裂分蜂之间的间距相等。 如:相邻等位H个数 1 峰数 2 强度 1:1
2
3
3
4
1:2:1
1:3:3:1
6.4 积分曲线与质子的数目
核磁共振谱中吸收峰的面积(强度)的 大小与产生该峰的等位氢原子数目成正比。
6.5
是原子核的基本属性之一,γ越大,核磁共振中
越容易检测到。
1H 13C
=26.752×107 T-1· S-1 =6.728×107 T-1· S-1
(T特斯拉,磁场强度的单位,S秒);
(二)核磁共振(跃迁)的条件
ν =
实现核磁共振的方式:
γ Ho 2π
保持外磁场强度不变, 改变电磁辐射频率------扫频
• 1960年左右出现脉冲傅里叶变换核磁共振方法
和谱仪——化学领域中的应用取得革命性进步。
6.1 核磁共振的基本原理
(一)原子核的自旋与自旋取向
Ha Hb
H原子核 无磁场
Ho
外磁场中,磁性原子核的两种自旋取向造成两 种不同能级。
E
↓ 自旋磁矩与外磁场相反
ΔE
↑ 自旋磁矩与外磁场相同 H0
• 原子核的磁旋比
与O (醇、醚、酯)相连:
与N相连:
R2NCH
2.2~3.2
与C=O(酮、酸、酯、醛)相连:CHC=O 2~3
6.3 自旋-自旋耦合
硝基丙烷的核磁共振氢谱 自旋-自旋耦合:相邻磁核之间的相互干挠现象; 自旋裂分:由自旋-自旋耦合而引起的多重谱线现象
(1) 耦合作用的一般原理
Ha核, 不考虑邻近核时: H实 = H0 – H感 Ha核邻近有一个Hb核: Hb的自旋状态↑ :H1实 = H0 – H感 + H’
共振中出现不同共振信号的现象。
6.2 1H-NMR 的化学位移
(一)屏蔽效应
H 实=H 0 H 感
为使氢核发生共振,须 提高外磁场强度以抵消 诱导磁场 由此产生了化学位移
化学位移
化学位移:由于化学环境的差异而引起的同类磁核在核磁 共振中出现不同共振信号的现象。
有机分子中,与不同基团相连的氢原子核周围的电子云 密度不一样,它们的信号就在不同的位置出现。
1种
2种
3种
(4) 耦合作用的一般规则:
• n+1规律:一个(组)等位H与相邻碳上的n个等位H偶合,将
产生n+1重峰。
如:CH3CH2OH(2+1;3+1;1)
• 裂分峰组的中心是该组磁核的化学位移值。相邻两峰之间 的裂距是耦合常数J 的大小(Hz)。 • 非邻位碳上的氢,通常不发生自旋裂分。 • • 等位H核相互之间没有谱线裂分现象。 活泼氢与其它氢核之间没有裂分现象
化学位移δ减小。
—烯氢质子位于去屏蔽区。δ= 5~6 — 醛基上的氢除位于双键的负屏蔽区,还受 相连氧原子强烈电负性的影响,使其共振 峰移向更低场,δ= 9.0~10.0。
苯环的各向异性效应
苯环上的6个π电子产生 比烯氢更强的诱导磁场。 δ在更低场,大于烯氢, 约为6.0~9.0
叁键的各向异性效应
低场
高场
(二)化学位移的表示方法
• 屏蔽作用引起的共振频率差别很小。 100 MHz仪器中,不同化学环境的1H的共振频率差别
在0~1500Hz范围内,难以测量。
以一标准物质作为基准,测定样品和标准
物质的共振频率之差。
化学位移的表示:
1,2,2-三氯丙烷的1H NMR谱
CH3CClCH2Cl
甲基:
保持电磁波辐射频率不变, 改变外磁场强度------扫场
(三)核磁共振仪
样 品 管
ν =
γ Ho 2π
1HNMR工作原理
核磁共振谱示意图:
吸 收 能 量 强 度
信号
γ Ho 2π
ν =
低场
H0
高场
H
磁场强度(频率υ0)
ν =
γ Ho 2π
几种常见核磁共振谱图: 核磁共振氢谱:1H NMR 核磁共振碳谱:
亚甲基:
基准物质的选择: 四甲基硅烷
CH3
(tetramethylsilane,简称TMS)
优点是:
CH3 Si CH3 CH3
• 化学性质不活泼,四个甲基有相同的化学环境,在谱图 中都只有一个吸收峰。 • 核受屏蔽作用强,一般化合物的峰在其左边(比其低的 磁场共振)。产生的信号不会干扰样品信号。
向右
( 减小)
高场
(三)影响化学位移的因素
化学位移原因:由电子云屏蔽作用引起的
凡影响电子云密度的因素都将影响化学位移。 其中影响最大的是:诱导效应和各向异性效应.
(1) 相连原子的电负性(诱导效应) • 化学位移随着相邻电负性基团的电负性的增大而增大
H H C H X
(2) 磁的各向异性效应
述
核磁共振波谱:外磁场中的原子核吸收电磁波
后发生自旋能级跃迁而产生的分子吸收光谱。
检测电磁波被吸收的情况就可得到核磁共
振波谱。根据波谱图上吸收峰的位置、强度和精
细结构可以研究分子结构。
发展历史
• 1946年观察到核磁共振信号——1952年诺贝尔 物理奖。 • 1950年前后发现化学位移及自旋-自旋耦合现 象——应用到化学领域。
炔氢正好位于正屏蔽 区,故共振峰出现在较 高场,δ较小,小于烯氢, 一般2~3
•
(3) 氢键的影响
• 两个电负性基团分别通过共价键和氢键产生吸电子诱导作 用,使共振发生在低场。
(五)各类1H的化学位移
1~2:与饱和碳相连的饱和碳上的氢(CCHn) 2~4.5:相邻有电负性基团(如:羰基、氧、硫、氮、Cl、Br等)
υ2 υ3 ( υ0)
υ1
以此类推,当相邻有三个完全相同的Hb核时, Ha裂分为四重峰,各峰的强度比为1:3:3:1
当相邻有多个相同或不同类型的Hb核时,
Ha裂分较复杂,称为多重峰。
(2) 耦合常数 J
• J的计算:两裂分峰之间的距离。
• 表示耦合的磁核之间相互干扰程度的大小,以赫兹
Hz为单位。
13C
NMR
核磁共振氟谱:19F NMR
核磁共振磷谱:31P NMR
根据核磁共振基本原理,分子中所有的氢原子都具有 相同的共振信号。
如,H0=1.4092T时,
1H
的共振频率为60 MHz
实际情况并非如此!!! 例如:乙醇的氢谱中有三个共振吸收峰。
乙醇的核磁共振氢谱
化学位移:由于化学环境的差异而引起的同类磁核在核磁
Hb 的自旋状态↓ : H2实 = H0 – H感 – H’
Jab
υ1
υ0
υ2
两个Hb核产生的局部磁场
H1实 = H0 + H感 + 2H'
H0
H2实 = H0 + H感 + H' - H' = H0 + H感 H3实 = H0 + H感 - 2H'
a
Jab
Jab
相邻两个相同核产生的局部磁场 引起的峰裂分
• 根据每一个峰组的化学位移、质子数目以及裂分峰
组情况推测对应的结构单元及相邻碳上H
• 根据化学位移和耦合关系连接结构单元
例1. 某化合物分子式为C2H6O,其1H NMR谱图如下图所示:
c CH3CH2OH a
b
试推断该化合物的结构。
例2.分子式为C3H6O的化合物的1H NMR如下,试确定其结构。
•
在1H和13C谱中规定:TMS的化学位移值=0,位于图谱
的右边。在它的左边 为正值,在它的右边 为负值,绝大 部分有机物中的氢核的 是正值。
1H
= 0~20
• 由于化学位移是一个相对值,因此,在不同外磁场的感应 强度下发生共振时,某个氢核的化学位移是不会变的。
低场
向左
( 增大)
磁场强度
O CH3CCH3
1H-NMR
的谱图解析
CH3CH2CONH2
低场
高场
1)峰的化学位移值(δ值)——各类型H所处的化学环境;
2) 峰的裂分数目或偶合常数——相邻H核的数目;
3)峰的面积——等位H的相对数目。
根据1H NMR推断未知化合物的结构
解析步骤
• 计算不饱和度f • 测量积分曲线的高度,确定各峰组对应的质子数目
•大小与化学键的性质以及立体化学等因素有关,与外 加磁场无关, 是核磁共振提供的重要参数之一。
(3) 等位质子(等位H)及吸收峰组数
化学环境、化学结构、立体结构相同的氢原子称
为等位氢原子。每一种等位H显示一组吸收峰。 一个有机化合物有几种不同类型的等位H,就会有
几组吸收峰。
判断以下化合物有几种等位H?
第六章 核磁共振波谱
( Nuclear Magnetic Resonance Spectroscopy,NMR)
有机化合物的结构确定
红外光谱
揭示分子中官能团种类、确定化合物类型。
核磁共振 提供分子中各种氢原子、碳原子等的数目及原子
所处的化学环境。
• 分子内部的运动与波谱: —— 外层价电子的运动(UV)
或苯环相连的饱和碳上的氢 (XCHn,苄位氢)
炔氢:2~3 烯氢:4.5~8
芳氢及杂环上的氢13
活泼氢化学位移不固定
质子类型
δ 值
2.2~3
1.7~2.0 3~4 2.5~4 3.4~4.5
苄基氢
烯丙型 与卤素相连
ArC-H
C=C-C-H Cl-CH Br-CH
—— 原子核间的相对振动(IR)—— 振动能级 —— 原子核自旋运动 (NMR)
