工业盐酸中铁含量的测定
分光光度法测定铁含量的方法汇总

标,绘制吸光度-显色剂用量曲线,确定显色剂的用量。 4.溶液适宜酸度范围的确定 在 9 只 50 mL 容量瓶中各加入 2.0 mL10-3
mol·L-1。铁标准溶液和 1.0 mL 100 mol·L-1 盐酸羟胺溶液,摇匀后放置 2 min。 各加 2 mL 1.5 g·L-1 邻二氮菲溶液,然后从滴定管中分别加入 0,2.00,5.00, 8.00,10.00,20.00,25.00,30.00,40.00 mL 0.1 mol·L-1NaOH 溶液摇匀,以 水稀释至刻度,摇匀。用精密 pH 试纸或酸度计测量各溶液的 pH。
3、试剂 1) 氢氧化钠溶液(300g/L) 2) 硝酸溶液(1+3) 3) 30%过氧化氢(密度为 1.11g/L) 4) 硫氰酸钠溶液(250g/L) 5) 铁标准溶液(此溶液 1ml 中含有 0.1mg 铁) 4、分析步骤
称取 0.0500g 试料于 250mL 锥形瓶中,加 5mL 氢氧化纳溶液,低温加热溶解后,加 20mL 硝酸溶液,煮沸约 20s,冷却。加 60mL 水、一滴过氧化氢、10mL 硫氰酸钠溶液, 放置 6min, 以空白夜做参比,1cm 比色皿,于 500nm 处,测定吸光度。同时做空白试验。 5、标准曲线的绘制
7.铁含量的测定试样溶液按步骤 1 显色后,在相同条件下测量吸光度, 由标准曲线计算试样中微量铁的质量浓度。
方案六 邻二氮菲分光光度法测定微量铁
一、实验目的
⒈学习确定实验条件的方法,Fra bibliotek握邻二氮菲分光光度法测定微量铁 的方法原理;
⒉掌握 721 型分光光度计的使用方法,并了解此仪器的主要构造。
二、实验原理
2.吸收曲线的绘制 在分光光度计上,用 1 cm 吸收池,以试剂空白溶液(1 号)为参比,在 440~560 nm 之间,每隔 10 nm 测定一次待测溶液(5 号)的吸光度 A,以波长为横坐标,吸光度为纵坐标,绘制吸收曲线,从而选择测定铁的最 大吸收波长。
电感耦合等离子体原子发射光谱法在工业用合成盐酸中铁元素测定中的应用

第16期2021年6月No.16June ,2021电感耦合等离子体原子发射光谱法在工业用合成盐酸中铁元素测定中的应用摘要:文章建立了电感耦合等离子体原子发射光谱法测定工业用合成盐酸中铁元素的分析方法,选择238.204nm 的分析谱线进行测定,方法的加标回收率为98.5%~100.2%,相对标准偏差(n =11)小于1.5%,检出限0.004mg/L 。
测定结果与国家标准方法测定值基本一致,可以适用于工业合成盐酸中铁元素的测定。
关键词:电感耦合等离子体原子发射光谱法;盐酸;铁中图分类号:O657.31文献标志码:A江苏科技信息Jiangsu Science &Technology Information汪洪涛,朱婕妤,洪华*(江苏省产品质量监督检验研究院,江苏南京210007)作者简介:汪洪涛(1985—),男,江苏盐城人,工程师,学士;研究方向:化学分析。
*通信作者:洪华(1979—),男,江苏南京人,高级工程师,博士;研究方向:化学分析。
引言盐酸是化学工业重要的基础原料,广泛应用于农业、石油化工、轻工、纺织、电力、冶金、国防军工、食品加工等国民经济各命脉部门。
铁作为工业用合成盐酸主要控制指标之一,其含量高低不仅关系自身产品质量,也影响下游产品的质量。
国家标准GB 320—2006《工业用合成盐酸》[1]中,铁含量采用1,10-菲啰啉分光光度法进行测定,该方法仪器普及性广,但是涉及酸碱调节及化学显色反应,实验操作干扰因素较多,耗时长。
本研究采用电感耦合等离子发射光谱法测定铁含量,实验表明,其具有简便快速、干扰少、重现性高的优点。
1实验部分1.1仪器及工作条件全谱直读型Agilent 5100电感耦合等离子发射光谱仪(安捷伦公司);玻璃同心雾化器(双通道旋流雾化室);垂直火炬双向观测;吹扫型中阶梯光栅分光系统;VistaChipII CCD 密封检测器;光谱范围167~785nm ;分辨率0.0075nm ;输出功率0.7~1.7kW 可调。
GB320-2006工业用合成盐酸

工业用合成盐酸1 范围本标准规定了工业用合成盐酸的要求、采样、试验方法、检验规则及标志、包装、运输和贮存、安全。
本标准适用于有氯气和氢气合成的氯化氢气体,用水吸收制得的工业用合成盐酸。
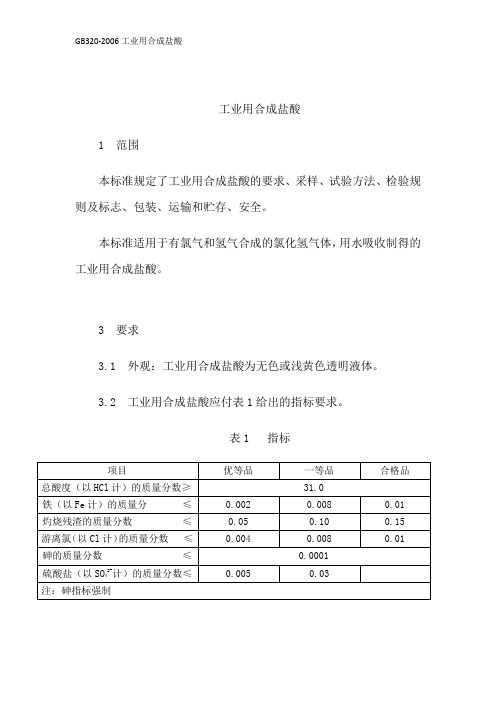
3 要求3.1 外观:工业用合成盐酸为无色或浅黄色透明液体。
3.2 工业用合成盐酸应付表1给出的指标要求。
表1 指标4 采样4.1 产品按批检验。
生产企业以每一成品槽或每一生产周期生产的工业用合成盐酸为一批。
用户以每次收到的同一批次的工业用合成盐酸为一批。
4.2 工业用合成盐酸从槽车或贮槽中采样时,宜用GB/T6680中规定的适宜的耐酸采样器自上、中、下三处采取等量的有代表性样品。
生产企业可将槽车或贮槽内的工业用合成盐酸混匀后于采样口采取有代表性样品,进行检测。
4.3 工业用合成盐酸从塑料桶或陶瓷坛中采样时,按GB/T6678中规定的采样单元数随机抽样,拆开包装,宜采用GB/T6680中规定的适宜耐酸采样器自上、中、下三处采取等量的有代表性样品。
4.4 将采取的样品混匀,装于清洁、干燥的塑料瓶或具磨口塞的玻璃瓶中,密封。
样品量不少于500mL。
样品瓶上应贴上标签并注明:生产企业名称、产品名称、批号或生产日期、采样日期及采样人。
5 试验方法除非另有说明,在分析中仅使用确认为分析纯试剂和GB/T6682中规定的三级水或相当纯度的水。
试验中所需标准溶液、制剂及制品,在没有其他规定时,均按GB/T601、GB/T602、GB/T603规定制备。
5.1 外观目视观察5.2 总酸度的测定 滴定法 5.2.1 原理试料溶液以溴甲酚绿为指示液,用氢氧化钠标准滴定溶液滴定至溶液由黄色变为蓝色为终点。
反应式如下:H ++OH -→H 2O5.2.2 试剂5.2.2.1 氢氧化钠标准滴定溶液:c (NaOH )=1mol/L 5.2.2.2 溴甲酚绿指示液:1g/L 。
5.2.3 仪器一般的实验室仪器和以下仪器。
5.2.3.1 锥形瓶,100mL (具磨口塞)。
分光光度法测铁含量

分光光度计测定工业盐酸中的铁含量周次:双周二一、实验目的1.掌握一种测定溶液中铁含量的实验方法。
2.掌握分光光度计的测试原理和使用方法。
3.学习如何选择吸光度分析的实验条件。
二、实验原理分光光度法测量的理论依据是伯郎—比耳定律:当容液中的物质在光的照射和激发下,产生了对光吸收的效应。
但物质对光的吸收是有选择性的,各种不同的物质都有其各自的吸收光谱。
所以根据定律当一束单色光通过一定浓度范围的稀有色溶液时,溶液对光的吸收程度A与溶液的浓度c(g/l)或液层厚度b(cm)成正比。
其定律表达式:A=abc(a是比例系数)。
当c的单位为mol/l时,比例系数用ε表示,则A=εbc称为摩尔吸光系数。
其单位为L·mol-1·cm-1它是有色物质在一定波长下的特征常数。
邻二氮菲可测定试样中铁的总量的条件和依据:邻二氮菲亦称邻菲咯啉(简写phen),是光度法测定铁的优良试剂。
在pH=2~9的范围内,邻二氮菲与二价铁生成稳定的桔红色配合物((Fe(phen)3)2+)。
此配合物的lgK稳= 21.3,摩尔吸光系数ε510= 1.1×104 L·mol-1·cm-1,而Fe3+能与邻二氮菲生成3∶1配合物,呈淡蓝色,lgK稳=14.1。
所以在加入显色剂之前,应用盐酸羟胺(NH2OH·HCl)将Fe3+还原为Fe2+,其反应式如下:2 Fe3+ + 2 NH2OH·HCl →2Fe2+ + N2 + H2O + 4H+ + 2Cl-测定时控制溶液的酸度为pH≈5较为适宜,用邻二氮菲可测定试样中铁的总量。
三、仪器与药品752型分光光度计1台;容量瓶(50mL)7只;量筒(100mL)1个;烧杯(100mL)4只;胖肚移液管(25 mL)2支;刻度移液管(10 mL)2支;洗耳球1只。
100μg·mL-1铁标准溶液;0.15% 邻二氮菲水溶液;10%盐酸羟胺溶液;1mol·L-1乙酸钠溶液;1 mol·L-1 NaOH溶液;6 mol·L-1 HCl(工业盐酸试样)。
GB320-2006工业用合成盐酸
工业用合成盐酸1 范围本标准规定了工业用合成盐酸的要求、采样、试验方法、检验规则及标志、包装、运输和贮存、安全。
本标准适用于有氯气和氢气合成的氯化氢气体,用水吸收制得的工业用合成盐酸。
3 要求3.1 外观:工业用合成盐酸为无色或浅黄色透明液体。
3.2 工业用合成盐酸应付表1给出的指标要求。
表1 指标4 采样4.1 产品按批检验。
生产企业以每一成品槽或每一生产周期生产的工业用合成盐酸为一批。
用户以每次收到的同一批次的工业用合成盐酸为一批。
4.2 工业用合成盐酸从槽车或贮槽xx采样时,宜用GB/T6680xx规定的适宜的耐酸采样器自上、xx、下三处采取等量的有代表性样品。
生产企业可将槽车或贮槽内的工业用合成盐酸混匀后于采样口采取有代表性样品,进行检测。
4.3 工业用合成盐酸从塑料桶或陶瓷坛xx采样时,按GB/T6678xx规定的采样单元数随机抽样,拆开包装,宜采用GB/T6680xx规定的适宜耐酸采样器自上、xx、下三处采取等量的有代表性样品。
4.4 将采取的样品混匀,装于清洁、干燥的塑料瓶或具磨口塞的玻璃瓶中,xx。
样品量不少于500mL。
样品瓶上应贴上标签并注明:生产企业名称、产品名称、批号或生产日期、采样日期及采样人。
5 试验方法除非另有说明,在分析xx仅使用确认为分析纯试剂和GB/T6682xx规定的三级水或相当纯度的水。
试验中所需标准溶液、制剂及制品,在没有其他规定时,均按GB/T601、GB/T602、GB/T603规定制备。
5.1 外观目视观察5.2 总酸度的测定滴定法5.2.1 原理试料溶液以溴甲酚绿为指示液,用氢氧化钠标准滴定溶液滴定至溶液由黄色变为蓝色为终点。
反应式如下:H++OH-→H2O5.2.2 试剂5.2.2.1 氢氧化钠标准滴定溶液:c(NaOH)=1mol/L5.2.2.2 溴甲酚绿指示液:1g/L。
5.2.3 仪器一般的实验室仪器和以下仪器。
5.2.3.1 锥形瓶,100mL(具磨口塞)。
GB320_2006工业用合成盐酸
工业用合成盐酸1 范围本标准规定了工业用合成盐酸的要求、采样、试验方法、检验规则及标志、包装、运输和贮存、安全。
本标准适用于有氯气和氢气合成的氯化氢气体,用水吸收制得的工业用合成盐酸。
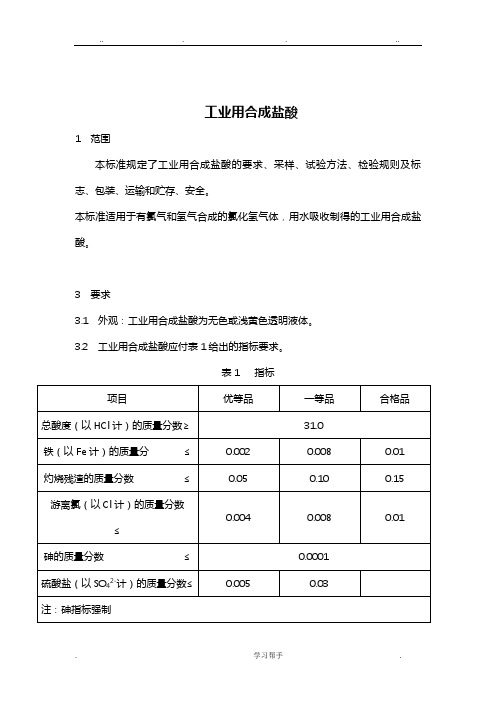
3 要求3.1 外观:工业用合成盐酸为无色或浅黄色透明液体。
3.2 工业用合成盐酸应付表1给出的指标要求。
表1 指标4 采样4.1 产品按批检验。
生产企业以每一成品槽或每一生产周期生产的工业用合成盐酸为一批。
用户以每次收到的同一批次的工业用合成盐酸为一批。
4.2 工业用合成盐酸从槽车或贮槽中采样时,宜用GB/T6680中规定的适宜的耐酸采样器自上、中、下三处采取等量的有代表性样品。
生产企业可将槽车或贮槽内的工业用合成盐酸混匀后于采样口采取有代表性样品,进行检测。
4.3 工业用合成盐酸从塑料桶或陶瓷坛中采样时,按GB/T6678中规定的采样单元数随机抽样,拆开包装,宜采用GB/T6680中规定的适宜耐酸采样器自上、中、下三处采取等量的有代表性样品。
4.4 将采取的样品混匀,装于清洁、干燥的塑料瓶或具磨口塞的玻璃瓶中,密封。
样品量不少于500mL。
样品瓶上应贴上标签并注明:生产企业名称、产品名称、批号或生产日期、采样日期及采样人。
5 试验方法除非另有说明,在分析中仅使用确认为分析纯试剂和GB/T6682中规定的三级水或相当纯度的水。
试验中所需标准溶液、制剂及制品,在没有其他规定时,均按GB/T601、GB/T602、GB/T603规定制备。
5.1 外观目视观察5.2 总酸度的测定滴定法5.2.1 原理试料溶液以溴甲酚绿为指示液,用氢氧化钠标准滴定溶液滴定至溶液由黄色变为蓝色为终点。
反应式如下:H++OH-→H2O5.2.2 试剂5.2.2.1 氢氧化钠标准滴定溶液:c(NaOH)=1mol/L5.2.2.2 溴甲酚绿指示液:1g/L。
5.2.3 仪器一般的实验室仪器和以下仪器。
5.2.3.1 锥形瓶,100mL(具磨口塞)。
工业盐酸中铁含量的测定

工业盐酸中铁含量的测定1、实验目的(1)了解并掌握1,10-菲啰啉分光光度法测盐酸中铁含量的方法及操作(2)进一步掌握分光光度计的使用方法(3)熟练比色皿的清洗,装样等操作(4)加强对一般溶液的配制操作练习2、实验原理(1)分光光度计的工作原理就是基于物质对光的吸收具有选择性,不同的物质都有各自的吸收光谱,即有不同的吸光度。
(2)盐酸羟胺能将三价铁还原为二价铁。
(3)在pH为4、5的缓冲溶液体系下,二价铁能与1,10-菲啰啉发生反应,生成橙红色的配合物。
3、实验仪器分析天平、紫外-可见分光光度计、洗瓶、胶头滴管、烧杯、比色皿、玻璃棒、移液管、洗耳球、pH试纸、滤纸、容量瓶、量筒。
4、实验药品工业盐酸、浓氨水、浓盐酸、氢氧化钠、盐酸羟胺、乙酸——乙酸钠缓冲溶液、铁标夜(硫酸亚铁按)、1,10-菲啰啉试剂。
6、实验步骤(1)所需溶液的配置①配制50mL的0、01g/L的铁标准溶液:量取5、0mL的0、1g/L的铁标液于烧杯中,用去离子水将其稀释,用50mL的容量瓶定容,备用(邱文静)②配制250mL的(1+10)盐酸溶液:用量筒量取浓度为12mol/L的浓盐酸22、7mL于烧杯中,再用量筒量取227、3mL的去离子水将其稀释,用250mL的容量瓶将其定容,搅拌均匀,贴上标签,以待备用(严翠平)③配制100mL的(1+1)氨水溶液(第二次用的就是氢氧化钠):用量筒量取浓氨水50mL于烧杯中再用量筒量取50mL去离子水将其稀释,搅拌均匀,贴上标签,备用(任云杰)④配制100mL的盐酸羟胺溶液:准确称取10、0g的盐酸羟胺试剂于烧杯中,再用适宜量的去离子水将其溶解,搅拌均匀,用100mL的容量瓶将其定容,贴上标签,备用(蒋滟耀)⑤配制100mL的1,10-菲啰啉溶液:准确称取0、2g的1,10-菲啰啉试剂于烧杯中,再用适宜量的去离子水将其溶解,搅拌均匀,用100mL的容量瓶将其定容,贴上标签,以待备用(邱文静)⑥配制100mLHAc--NaAc缓冲溶液(pH=4、5):准确称取11、8908g的乙酸钠,再用量筒量取40mL的冰醋酸于烧杯中,用去离子水稀释,用100mL容量瓶定容贴上标签,以待备用(严翠平)⑦配制200mL的试样溶液:称取早已洗净烘干的空具塞锥形瓶的质量为m mL,在量取70mL的工业盐酸于瓶中,再次称量,在置于内装100mL去离子水的200mL容量瓶中,再用水定容,备用(任云杰)(2)标准曲线绘制——测定铁标液的吸光度②向每个容量瓶中加入10mL的(1+1)的盐酸溶液,加水至20mL处,用氨水溶液调至pH 为2~3,再加入1mL盐酸羟胺溶液,5mLHAc--NaAc缓冲溶液与2mL1,10—菲啰啉溶液,再用水稀释至刻度,摇匀,静置15min。
盐酸质量标准及检验操作规程

盐酸质量标准及检验操作规程一、引言盐酸(化学式HCl)是一种常见的无机化合物,在工业生产和实验室中经常使用。
为确保盐酸的质量,需要制定相应的质量标准和检验操作规程。
本文将介绍盐酸的质量标准及检验操作规程,以保障盐酸的生产和使用过程中的安全性和可靠性。
二、盐酸质量标准1. 外观与性状盐酸应为无色透明液体,不得有悬浮物或沉淀物。
2. 盐酸含量盐酸的含量应符合国家相关标准要求,通常为36%~38%。
含量低于36%或高于38%的盐酸不得使用。
3. 游离氯离子盐酸中游离氯离子的含量应保持在合理范围内,国家标准通常要求不得超过0.01%。
4. 铁含量盐酸中铁含量的限制值通常为0.002%,不得超过此限制。
5. 重金属含量盐酸中的重金属含量应符合国家相关标准要求,通常各重金属的限制值均不得超过规定限值。
三、盐酸的检验操作规程1. 外观与性状检验取适量盐酸样品置于透明玻璃瓶中,观察其色泽和透明度。
不得有异物、悬浮物或沉淀物。
2. 盐酸含量测定采用滴定法(常用的是酸碱滴定法),以红井钠溶液作为指示剂,取适量盐酸样品滴定至试液颜色转变为橙红色,记录所需的滴定液体积,计算盐酸含量。
3. 游离氯离子含量检验采用离子选择电极法进行检验,按照仪器使用说明进行操作。
记录测得的游离氯离子含量。
4. 铁含量测定采用比色法进行测定,将盐酸样品与显色剂混合,经一定时间后测定吸光度,按照标准曲线计算并记录铁含量。
5. 重金属含量检验采用原子吸收分光光度法等对盐酸中的各重金属进行检验。
按照实验室标准操作规程进行操作,记录检验结果。
四、结论通过对盐酸的质量标准及检验操作规程的介绍,可以确保盐酸在生产和使用过程中的质量稳定、合规和安全。
工作人员在操作过程中应严格按照检验操作规程进行,确保检测结果准确可靠。
同时,也需要定期对仪器设备进行校准与维护,以确保检验装置的正常运行。
盐酸的质量标准和检验操作规程是保证盐酸质量的重要基础。
只有遵循这些规程,才能有效地控制盐酸的质量,降低生产和使用过程中的风险,保障工作安全和产品质量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
工业盐酸中铁含量的测定
1、实验目的
(1)了解并掌握1,10-菲啰啉分光光度法测盐酸中铁含量的方法及操作
(2)进一步掌握分光光度计的使用方法
(3)熟练比色皿的清洗,装样等操作
(4)加强对一般溶液的配制操作练习
2、实验原理
(1)分光光度计的工作原理是基于物质对光的吸收具有选择性,不同的物质都有各自的吸收光谱,即有不同的吸光度。
(2)盐酸羟胺能将三价铁还原为二价铁。
(3)在pH为的缓冲溶液体系下,二价铁能与1,10-菲啰啉发生反应,生成橙红色的配合物。
3、实验仪器
分析天平、紫外-可见分光光度计、洗瓶、胶头滴管、烧杯、比色皿、玻璃棒、移液管、洗耳球、pH试纸、滤纸、容量瓶、量筒。
4、实验药品
工业盐酸、浓氨水、浓盐酸、氢氧化钠、盐酸羟胺、乙酸——乙酸钠缓冲溶液、铁标夜(硫酸亚铁按)、1,10-菲啰啉试剂。
5、药品配置表
6、实验步骤
(1)所需溶液的配置
①配制50mL的L的铁标准溶液:量取的L的铁标液于烧杯中,用去离子水将其稀释,用50mL的容量瓶定容,备用(邱文静)
②配制250mL的(1+10)盐酸溶液:用量筒量取浓度为12mol/L的浓盐酸于烧杯中,再用量筒量取的去离子水将其稀释,用250mL的容量瓶将其定容,搅拌均匀,贴上标签,以待备用(严翠平)
③配制100mL的(1+1)氨水溶液(第二次用的是氢氧化钠):用量筒量取浓氨水50mL 于烧杯中再用量筒量取50mL去离子水将其稀释,搅拌均匀,贴上标签,备用(任云杰)
④配制100mL的盐酸羟胺溶液:准确称取的盐酸羟胺试剂于烧杯中,再用适宜量的去离子水将其溶解,搅拌均匀,用100mL的容量瓶将其定容,贴上标签,备用(蒋滟耀)
⑤配制100mL的1,10-菲啰啉溶液:准确称取的1,10-菲啰啉试剂于烧杯中,再用适宜量的去离子水将其溶解,搅拌均匀,用100mL的容量瓶将其定容,贴上标签,以待备用(邱文静)
⑥配制100mLHAc--NaAc缓冲溶液(pH=):准确称取的乙酸钠,再用量筒量取40mL的冰醋酸于烧杯中,用去离子水稀释,用100mL容量瓶定容贴上标签,以待备用(严翠平)
⑦配制200mL的试样溶液:称取早已洗净烘干的空具塞锥形瓶的质量为m mL,在量取70mL的工业盐酸于瓶中,再次称量,在置于内装100mL去离子水的200mL容量瓶中,再用水定容,备用(任云杰)
(2)标准曲线绘制——测定铁标液的吸光度
①按照下列表格量取贴标溶液分别置于6个50mL的容量瓶中
(蒋滟耀)
②向每个容量瓶中加入10mL的(1+1)的盐酸溶液,加水至20mL处,用氨水溶液调至pH为2~3,再加入1mL盐酸羟胺溶液,5mLHAc--NaAc缓冲溶液和2mL1,10—菲啰啉溶液,再用水稀释至刻度,摇匀,静置15min。
(邱文静)
③制作空白样:用一个空的容量瓶依次加入第二步中的试剂(不加铁标样)再用其润洗玻璃比色皿后装样,在波长510nm处,调整分光光度计零点(严翠平)
④用适宜的比色皿装以上六个容量瓶的溶液,在波长为510nm处测得相应的吸光度
(任云杰)
⑤以铁含量(ug)为横坐标,与其相应的吸光度为纵坐标绘制标准曲线(蒋滟耀)(3)测定工业盐酸中铁的含量
①配制试料:量取的试样溶液置于50mL的容量瓶中(蒋滟耀)
②测定准备:向试料中加水至20mL处,用氨水溶液调至pH值为2~3,再加入1mL 盐酸羟胺溶液,5mLHAc----NaAc缓冲溶液和2mL1,10—菲啰啉溶液再用水稀释至刻度处,摇匀,静置15分钟。
(邱文静)
③空白试验:向一个未加试料的50mL的容量瓶中加入10mL(1+1)盐酸溶液,再加入相同的与试料溶液中的其他试剂,再用其润洗玻璃比色皿在装样,在波长510nm处,调整风光光度计零点。
(严翠平)
④用试料溶液润洗玻璃比色皿,再装样,在波长为510nm处测定其吸光度,平行三组。
(任云杰)
八、测定结果
(1)计算标准曲线的线性回归方程。
对于无基体干扰或能消除基体干扰的浓度波动较大的大批样品的测试,我们通常选择的方法是分光光度法中最经典的方法——标准曲线法。
这种方法也是实际工作中使用最多的一
种定量方法。
其特点是:对仪器要求不高,是分光光度法中简便易行的方法。
工作曲线的绘制方法是:配制4个以上的浓度不同的待测组分的标准溶液,以空白溶液为参比溶液,在选定的波长下,分别测定各标准溶液的吸光度。
以标准溶液浓度为横坐标,吸光度为纵坐标,在坐标纸上绘制曲线。
同时,在相同条件相对待测物试样进行显色反应,并测定其吸光度A 。
再从标准曲线上查找待测组分的浓度C 。
标准曲线可通过计算机绘制,也可以用回归分析法进行拟合。
计算公式:
y=ax+b
其中:()()()
∑∑-=---=
n
i n
i x x y y x x a 1
2
1
x a y b -=
(2)在测得试料溶液的吸光度与标准曲线相对比,找到试料溶液中相对铁的含量为m 铁含量以铁的质量分数
ω计算:
1
32210m m -⨯=
ϖ
1m ——式样质量的数值,单位为克(g )
; 2m ——由标准曲线查得的试料中铁含量的数值,单位为微克(ug )。
(3)允许差
平行测定结果之差的绝对值不大于%。
取平行测定结果的算术平均值为报告结果。
九、注意事项
1、菲啰啉溶液配制好后应避光保存,防止分解
2、在使用比色皿时,注意保护光学面
3、在实验过程中,盐酸具有腐蚀性,防止溅到皮肤,伤害皮肤组织
4、在量取盐酸,浓氨水等有刺激性试剂时,请勿大口吸气,且操作尽量减少时间 十、实验讨论
1、邻菲啰啉比比色测定铁的原理是什么用该法测出的铁含量是否是式样中亚铁含量
2、绘制标准曲线和测定试样为什么要在相同条件下进行这里主要指哪些条件。
