第七章 氧化还原反应电化学基础
第七章-氧化还原反应与电化学基础

§7.2 电化学电池
5. 正负极
• 电子的流出极叫负极:Zn极 • 电子的流入极叫正极:Cu极
6. 阴阳极
• 阳极(Positive Electrode): 凡是进行氧化反应的电极叫阳极。
• 阴极(Negative Electrode): 凡是进行还原反应的电极叫阴极。
第七章 氧化还原反应与电化学基础
在超氧化物中(KO2),氧的氧化数 为 1 ;
2
在氧的氟化物(OF2,O2F2)中,氧的 氧化数分别为+2和+1。
❖ 在所有的氟化物中氟的氧化数为-1。
第七章 氧化还原反应与电化学基础
§7.1 基本概念
例:
SiO2: Si的氧化数为+4; Cr2O72-:Cr的氧化数为+6; Fe3O4: Fe的氧化数为 8 ;
Mz+(aq)+ze-
–
离子电极
2OH-(aq) Pt | O2(p)|OH-(c)
金属-难 溶盐电极
AgCl(s) +e-
Ag(s) +Cl-(aq) Ag|AgCl|Cl-
§7.3 电极电势
(Electrode Potential)
7.3.1 电极电势的产生 7.3.2 电极电势的意义 7.3.3 电池电动势 7.3.4 标准电极电势 7.3.5 标准电极电势表 7.3.6 Nernst方程式 7.3.7 Nernst 方程式的应用
MgCl2(s)
第七章 氧化还原反应与电化学基础
§7.1 基本概念
2. 失去电子的过程叫氧化,得到电子的
过程叫还原
Zn(s) Zn2+(aq)+2eCu2+(aq)+2e- Cu(s) 局限性:形成共价分子的氧化过程不
大学无机化学-第七章-氧化还原反应-电化学基础-课件

种元素的原子总数各自相等且电荷数相等 ④ 确定两半反应方程式得、失电子数目的最小公倍
数。将两个半反应方程式中各项分别乘以相应的 系数,使得、失电子数目相同。然后,将两者合 并,就得到了配平的氧化还原反应的离子方程式。 有时根据需要可将其改为分子方程式。
3Cl2 (g) + 6OH- = 5Cl- + ClO3- + 3H2O 3Cl2 (g) + 6NaOH = 5NaCl + NaClO3 + 3H2O
无机化学
§7.1 氧化还原反应的基本概念
例 4 配平方程式
Cr(OH)3 (s) + Br2 (l) + KOH
K2CrO4 + KBr
Cr(OH)3 (s) + Br2 (l)
电极组成:Pt , Cl2(p) | Cl- (a)
电极反应: Cl2 + 2e
2Cl-
无机化学
§7.2 电化学电池
3. 金属-金属难溶盐-阴离子电极
将金属表面涂有其金属难溶盐的固体,然后浸 入与该盐具有相同阴离子的溶液中构成的电极
电极组成:Ag ,AgCl(s)| Cl- (a) 电极反应:AgCl + e Ag + Cl电极组成:Hg ,Hg2Cl2(s)| Cl- (a) 电极反应:Hg2Cl2+2e 2Hg +2Cl-
无机化学
§7.1 氧化还原反应的基本概念
2-2 半反应法(离子—电子法) 配平原则 (1)反应过程中氧化剂得到的电子数等于还
原剂失去的电子数 (2)反应前后各元素的原子总数相等
氧化还原反应和电化学基础

8
⑷ 离子型化合物中,元素的氧化数等于该 ⑸ 离共子价所型带化的合电物荷中数,,共如用:电N子aC对I。偏向于电负性大 的原子 ,两原子的形式电荷数即为它们的氧化数, 如:HCI。 ⑹ 中性分子中,各元素原子氧化数的代数和为9 零。
S4O62- 4x+(-2)×6=-2 x=2.5 H5IO6 I:+7 ; S2O32- S:+2 例:求MnO4-中Mn的氧化值
2×3
0
+5
Zn+ HNO3
+2
+2
Zn(NO3)2+ NO + H2O
3 ×2
56
配系数
先配变价元素,再用观察法配平其 它元素原子的系数。
15
用氧化数表示氧化还原的状态 对于离子化合物的氧化还原反应来说,电 子是完全失去或完全得到的。但是,对于共价化 合物来说,在氧化还原反应中,有电子的偏移, 但还没有完全的失去或得到,因此用氧化数来表 示就更为合理。
16
例如:
H2+Cl2=2HCl 这个反应的生成物是共价化合物,氢原子的电子 没有完全失去,氯原子也没有完全得到电子,只是形成 的电子对偏离氢,偏向氯罢了。用氧化数的升降来表示 就是氯从0到-1,氢从0到+1。这样,氧化数的升高就是 氧化,氧化数的降低就是还原。在氧化还原反应里,一 种元素氧化数升高的数值总是跟另一种元素氧化数降低 的数值相等的。
11
一、氧化值的定义
在氧化还原反应中,电子转移引起某些原子的价 电子层结构发生变化,从而改变了这些原子的带电状 态。为了描述原子带电状态的改变,表明元素被氧化 的程度,提出了氧化态的概念。表示元素氧化态的的 数值称为元素的氧化值,又称氧化数。
氧化还原反应 电础

(6)在所有的氟化物中,氟的氧化值为-1。
(7)碱金属和碱土金属的化合物中的氧化值分别为+1和+2。
(8)在中性分子中,各元素氧化值的代数和为零。在多原子离子中,各元素氧化值的代数和等于离子所带电荷数。例如:K 2 Cr 2 O 7 中Cr 为+6,Fe 3 O 4 中,Fe 为+8/3,Na 2 S 2 O 3 中,S 为+2。
元素氧化值的改变与反应中得失电子相关联。元素氧化值升高、失去电子的物质是还原剂,还原剂是电子的给予体,它失去电子后本身被氧化。元素氧化值降低、得到电子的物质是氧化剂,氧化剂是电子的接受体,它得到电子后本身被还原。无机反应中常见的氧化剂一般是活泼的非金属单质(如 等)和高氧化数的化合物(如 、 ;还原剂一般是活泼的金属(如Na,K,Ca,Mg,Zn等)和低氧化数的化合物(如KI,FeSO4,SnCl2等)。
原电池中与电解质溶液相连的导体称为电极。在电极上发生的氧化或还原反应则称为电极反应或半电池反应。两个半电池反应合并构成原电池总反应称为电池反应。
每个半电池可由同一元素的两种不同状态组成。
氧化值与化合价的区别是:化合价只能是整数,而且共价数没有正负之别,氧化数可以是正、负整数或分数,甚至可以大于元素的价电子数。
任何氧化还原反应都是有两个“半反应”组成,如:
Cu2+ + Fe=Cu+Fe2 +
是由下列两个“半反应”组成:
还原反应:Cu2+ + 2e=Cu
氧化反应:Fe-2e= Fe2 +
工学氧化还原反应电化学基础

7-1 氧化还原反应的基本概念 7-2 电化学电池 7-3 电极电势 7-4 电极电势的应用
知识回顾: 四大平衡
酸碱 氧化还 沉淀溶 络合反 平衡 原平衡 解平衡 应平衡
思考:
对于氧化还原反应:
7-1 氧化还原反应的基本概念
7.1.1 氧化值 Def:
属1。的氢化物(如NaH、CaH2、LiAlH4)中,氢的氧化值为★ 通常,在化合物中氧的氧化值为-2;但在过氧化物(如
HO22OF22中,,Na氧2O的2,氧B化aO值2)分中别氧为的+氧2和化+值1为。-1;而在OF2和 ★ 在所有氟化物中,氟的氧化值为-1。 ★ 碱金属和碱土金属在化合物中的氧化值分别为+1和+2。 ★ 在中性分子中,各元素氧化值的代数和为零。在多原
氧化值法 离子—电子半反应法(适用于有介质参与的复
杂反应)
配平氧化还原反应方程式的基本原则:
电荷守恒 质量守恒
下面分别用酸性溶液和碱性溶液中的氧 化还原反应为例介绍离子-电子法的配平步骤。
配平酸性溶液中的反应:
KMnO4 K2SO3 H MnSO4 K2SO4
e-
7-2 电化学电池
伏特(Alessandro Volta 1745~ 1827)。意大利物理学家。 1800年3月20日宣布发明伏打 电堆,这是最早的直流电源。 从此,人类对电的研究从静 电发展到流动电(电流)。为纪 念他,人们将电动势单位取 名伏特。
7.2.1 原电池的构造
原电池: 将化学能转化为电能的装置
MnO4 8H Mn2 4H 2O SO32 H2O SO42 2H
口诀:少氧的一边加H2O,多氧的一边加H+。
第7章 氧化还原反应 电化学基础

第7章氧化还原反应电化学基础一、单选题1. 下列电对中,Eθ值最小的是:A: Ag+/Ag;B: AgCl/Ag;C: AgBr/Ag;D: AgI/Ag2. Eθ(Cu2+/Cu+)=0.158V,Eθ(Cu+/Cu)=0.522V,则反应2 Cu+Cu2+ + Cu的Kθ为:A: 6.93×10-7;B: 1.98×1012;C: 1.4×106; D: 4.8×10-133. 已知Eθ(Cl2/ Cl-)= +1.36V,在下列电极反应中标准电极电势为+1.36V 的电极反应是:A: Cl2+2e- = 2Cl- B: 2 Cl- - 2e- = Cl2C: 1/2 Cl2+e- = Cl- D: 都是4. 下列都是常见的氧化剂,其中氧化能力与溶液pH 值的大小无关的是:A: K2Cr2O7 B: PbO2C: O2 D: FeCl35. 下列电极反应中,有关离子浓度减小时,电极电势增大的是:A: Sn4+ + 2e- = Sn2+B: Cl2+2e- = 2Cl-C: Fe - 2e- = Fe2+ D: 2H+ + 2e- = H26. 为防止配制的SnCl2 溶液中Sn2+被完全氧化,最好的方法是:A: 加入Sn 粒B:. 加Fe 屑C: 通入H2D: 均可7. 反应Zn (s) + 2H+→ Zn 2++ H2 (g)的平衡常数是多少?A: 2×10-33 B: 1×10-13 C: 7×10-12 D: 5×10 26二、是非题(判断下列各项叙述是否正确,对的在括号中填“√”,错的填“×”)1. 在氧化还原反应中,如果两个电对的电极电势相差越大,反应就进行得越快2.由于Eθ(Cu+/Cu)= +0.52V , Eθ(I2/ I-)= +0.536V , 故Cu+ 和I2不能发生氧化还原反应。
第7章-电化学基础
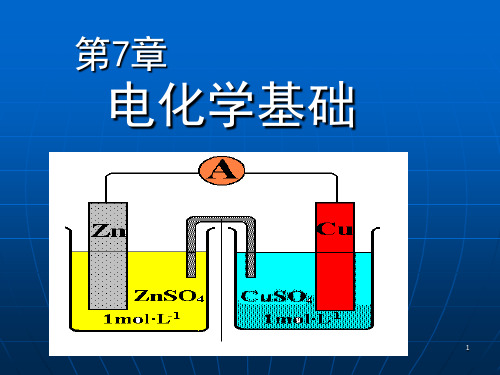
标准电极电势的测定
例5 简述测定Pt | Fe3+(1.0), Fe2+(1.0)的标准电极电势的方法及结果。 解 将Pt | Fe3+(1.0), Fe2+(1.0)与标准氢电极组成电池。从实验电流的方向确定此待测电极为正极,标准氢电极为负极。 测得电动势为0.771V,则 EΘ= E+Θ - E- Θ = EΘFe3+ /Fe2+ - EΘH+/H2
2.电极反应
任何氧化还原反应都可拆分为两个氧化还原电对的半反应(半电池反应,电极反应): Fe3+ + e → Fe2+ Sn2+ → Sn4+ + 2e 氧化-还原反应的实质: 两个共轭电对之间的电子转移反应。
3.电对拆分:
2MnO4-+5H2C2O4 + 6H+ → 2Mn2+ + 10CO2 + 8H2O MnO4- + 8H+ + 5e → Mn2+ + 4H2O ① H2C2O4 → 2CO2 + 2H+ + 2e ② MnO4- / Mn2+; CO2 /H2C2O4
例1 用离子-电子法配平下列氧化还原反应: K2Cr2O7 + KI + H2SO4 →K2SO4 + Cr2(SO4)3+I2+H2O 解:先写成离子反应式: Cr2O72- + I- + H+→ Cr3+ + I2 + H2O 将离子反应式分成两个半反应: I- → I2(电对:I2 /I- ) Cr2O72- + H+ → Cr3+ + H2O(电对:Cr2O72- /Cr3+) 分别配平两个半反应: 2I- = I2 + 2e Cr2O72- + 14 H+ + 6e = 2Cr3+ +7 H2O
9氧化还原反应
第七章:氧化还原反应 电化学基础主要内容:氧化还原反应的概念原电池 电极电势电极电势的应用重点难点:氧化还原方程式的配平。
原电池的电动势及电极电势。
Nernst 方程式及其有关的简单计算,根据Nernst 方程式分析浓度对电极电势的影响。
浓差电池原理。
元素电势图及其应用,判断氧化剂或还愿剂的相对强弱,判断氧化还原反应进行的方向,计算标准平衡常数。
教学目的:熟悉氧化还原反应的基本概念,能熟练地配平氧化还原反应方程式。
了解原电池及其电动势的概念。
掌握电极电势的概念及其影响因素,Nernst 方程式及其有关的简单计算,电极电势的应用。
掌握元素电势图及其应用。
§7.1 氧化还原反应的基本概念应中,得到电子的物质是氧化剂,失去电子的物质是还原剂。
还原剂失去电子被氧化,氧化剂得到电子被还原。
7.1.1 氧化值在氧化还原反应中,由于发生了电子转移,导致某些元素带电状态发生变化。
为了描述元素原子带电状态的不同,人们提出了氧化值的概念。
氧化值也叫做氧化数。
氧化:氧化数增加的过程;还原:氧化数降低的过程1970年,国际纯粹与应用化学联合会(IUPAC)对氧化值的定义是:氧化值是某元素一个原子的荷电数,这个荷电数是假设把每个化学键的电子指定给电负性更大的原子而求得的。
例如,在NaCl中,钠的氧化值为+1,氯的氧化值为-1。
在SO2中,硫的氧化值为+4,氧的氧化值为-2。
由此可见,氧化值是元素在化合状态时人为规定的形式电荷数。
确定氧化值的规则:★在单质中,元素的氧化值为零。
★在单原子离子中,元素的氧化值等于离子所带的电荷数。
★在大多数化合物中,氢的氧化值为+1,只有在活泼金属的氢化物(如NaH,CaH2)中,氢的氧化值为-1。
★通常,在化合物中氧的氧化值为-2;但在过氧化物(如H2O2,Na2O2,BaO2)中氧的氧化值为-1;而在OF2和O2F2中,氧的氧化值分别为+2和+1。
★在所有氟化物中,氟的氧化值为-1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章氧化还原反应电化学基础一、教学基本要求1、掌握氧化值,氧化,还原,氧化还原反应,原电池,标准电极电势,标准氢电极,甘汞电极,元素电势图等基本概念。
2、掌握氧化—还原方程式的配平方法。
3、熟练掌握能斯特方程的相关计算,能运用其讨论离子浓度对电极电势的影响。
4、熟练掌握电极电势的应用。
5、掌握元素电势图及其应用。
二、内容要点本章以原电池作为讨论氧化还原反应的物理模型,重点讨论标准电极电势的概念以及影响电极电势的因素。
同时将氧化还原反应与原电池电动势联系起来,判断反应进行的方向和限度。
(一)、氧化还原反应的基本概念。
氧化还原反应是一类有电子转移(或得失)的反应。
1、氧化值(1)氧化值是某元素的一个原子的荷电数。
该荷电数是假定把每一化学键的电子指定给电负性更大的原子而求得的。
在化合物分子中,氧化值是元素的电荷数或形式电荷数。
(2)氧化值的确定规则:A 在单质中,元素的氧化值为零。
B 在单原子离子中,等于离子所带的电荷数。
C 大多数化合物中,氢的氧化值为+1:只有在金属氢化物(NaOH,CaH2)中,氢的氧化值为—1。
D 通常,氧的氧化值为—2,但是在H2O2,NaO2,BaO2等过氧化物中,其氧化值为—1,在氧的氟化物中,如OF2和O2F2中,氧的氧化值分别为+2,+1。
E 所有氟化物中,氟的氧化值为—1。
F 碱金属和碱土金属在化合物中的氧化值为+1和+2。
G 在中性分子中,各元素氧化值的代数和为零。
在多原子离子中,各元素氧化值的代数和等于离子所带电荷数。
2.还原剂和氧化剂:在氧化还原反应中,失电子的物质是还原剂,即电子给予体。
其本身被氧化,其元素氧化值升高;得电子的物质是氧化剂,即电子接受体,其本身被还原,其元素氧化值降低。
3.电对:氧化还原反应是由还原剂被氧化和氧化剂被还原这两个“半反应”组成。
在“半反应”中同一元素高氧化值的物种被称为氧化型,低氧化值的物种被称为还原型,氧化型与还原型组成“电对”,“电对”与“半反应”是相互对应的。
4.氧化还原反应方程式的配平。
配平原则①方程式两边各种元素的原子总数必须各自相等,各物种的电荷数之代数和必须相等。
②反应中氧化剂和还原剂的得失电子数相等。
配平方法:1.氧化值(数)法2.离子—电子法配平步骤:①写出主要反应物和生成物的离子式。
②分别写出两个半反应。
③根据介质的酸碱性配平两个半反应。
先使等号两边各种元素的原子数各自相等,再用加电子数的方法使方程式两边电荷数相等。
表7—1 离子—电子法配平经验规则介质条件反应方程式左边O原子数加入物质右边生成物酸性多 H+少 H2OH2OH+碱性多 H2O少 OH-OH-H2O中性多 H2O少 H2OOH-H+④将两个半反应分别乘以相应的系数后相加,即得到配平的离子反应方程式。
(二).电化学基础1.原电池:借助氧化—还原反应而产生电流,使化学能转化为电能的装置。
原电池由两个“半电池”(正极和负极)组成。
在正极上氧化剂得电子被还原,在负极上还原剂失去电子被氧化。
分别在两个半电池中发生的氧化或还原反应,叫做半电池反应或电极反应。
氧化和还原的总反应称为电池反应。
两个“半反应”之间通过导线和盐桥等连接起来,才能产生电流。
注意:书写电极反应和电池反应时,必须满足物质的量及电荷平衡。
同时应标明离子或电解质溶液的浓度,气体的压力,纯液体或纯固体的相态。
2.电池符号(电池图示)原电池装置可用简单的电池符号来表示。
书写要求:例:Zn(s)∣Zn2+(aq,c1)‖H+(aq,c2) ∣H2(g,pΘ) ∣Pt①把组成电池的各种物质从左到右,排成一排,负极写左边,正极写右边。
②以化学式表示各种物质,并注明相态,压力,浓度(活度),温度。
若p,T不注明,表示θp,25o C.③用“∣”表示相接界,用“‖”表示盐桥。
同一相中两物种的离子式或分子式以“,”分开。
④对于没有电子导体的电极,如H2(气体电极),需配上零价的惰性金属,但该惰性金属不参加电极反应,表示时加上一括号。
(三).电极电势原电池中电流的产生是由于两个电极的电极电势不同所致1.原电池的电动势:原电池的电动势是构成原电池的两个电极间的最大电势差,即正极的电极电势E (+)减去负极的电极电势E (-)等于电池的电动势。
E MF=E (+)+E (-) (7—1)2.标准电极电势:标准氢电极(SHE):a.构成:将镀有铂黑的铂片(镀铂黑的目的是增加电极的表面积,促进对气体的吸附,以有利于与溶液达到平衡)浸入含有氢离子的酸溶液中,c(H+)=1.0mol·L -1,并不断通入纯净的氢气使氢气冲打在铂片上。
同时使溶液被氢气所饱和,氢气泡围绕铂片浮出液面。
b.氢电极的图示可表示为:P t |H2(g)|H+(aq)或H+(aq)|H2(g)|Pt2H+(aq)+2e- H2(g)规定标准氢电极的还原电极电势为零,即EΘ(H+/H2)=0c .氢电极的电极电势随温度变化改变得很小,但携带不便,而使用条件却要求十分严格。
甘汞电极(SCE)a.构成:金属—难溶盐电极。
由两个玻璃管组成,内套管下部有一多孔素瓷塞并盛有汞和甘汞Hg2Cl2混合的糊状物,在其间插有作为导体的铂丝。
在其外管中盛有铂和KCl溶液和少量KCl晶体(以保证KCl溶液处于饱和状态);外玻璃细管的最底部也有一多孔素瓷塞。
b.甘汞电极的图示Hg(l)|Hg2Cl2(s)Cl-或Cl-|Hg2Cl2(s)|Hg(l)电极反应 Hg2Cl2(s)+2e- 2Hg(l)+2Cl-(aq)c.以标准氢电极的电极电势为基准,饱和甘汞电极的标准电极电势EΘ(Hg2Cl2/Hg)=0.2415V标准电极电势:标准电极电势可以通过实验测得。
使待测半电池中各物种均处于标准态下,将其与标准氢电极相连接组成原电池,以数字电压表测定电池的电动势并确定其正极和负极,进而可推算出待测半电池(电极或电对)的标准电极电势。
一般电极电势高的电对为正极;电极电势低的电对为负极;两电极的标准电极电势之差等于原电池的标准电动势。
即EΘMF=EΘ(+)-EΘ (-) (7—2)注意:(1)教材中所用标准电极电势是标准还原电极电势,所对应的电极反应必须是还原反应。
对同一电对而言,还原电势与氧化电势其绝对值相等,符号相反。
(2)电极电势无加合性。
(3)影响电极电势的因素内因:电对本性外因:反应温度,氧化型物质和还原性物质的浓度,压力。
能斯特(Nernst)方程对于一般的电极反应:氧化型+z e- 还原型E(T)= EΘ(T)-[()/]ln[()/]mnRT c czF c cθθ氧化型还原型(7—3)298K下,可简化为:E(298K)= EΘ(298K)-()()[c/] 0.0592lg[c/]mnc z cθθ氧化型还原型注意:1、式中的幂指数m,n,x,y与电极反应中相应物种化学式的系数一致。
2、溶液中的离子,分子物种,以c表示;气体参与电极反应时,以p表示;纯固体,纯液体不表示。
3、式中的氧化型和还原型分别是电极反应中等号左侧和右侧的各物种。
当c(氧化型)或p(氧化型)增大,电极电势增大;c (还原型)或P(还原型)增大,电极电势减小。
4、如果电极反应中氧化型或还原型物种形成难溶电解质、配合物,弱酸或弱碱时,都能使电极电势改变。
5、如果电对的氧化型生成难溶化合物,使c(氧化型)变小,则电极电势变小。
如果电对的还原型生成难溶化合物,使c(还原型)变小,则电极电势变大。
当氧化型和还原型同时生成沉淀时,若KΘSP(氧化型)< KΘSP(还原型)则电极电势变小;反之,则变大。
6、如果电对的氧化型生成配合物,使c(氧化型)变小,则电极电势变小。
如果电对的还原型生成配合物,使c(还原型)变小,则电极电势变大。
当氧化型和还原型同时生成配合物时,若KΘf(氧化型)> KΘf(还原型)则电极电势变小;反之,则变大。
7、含氧酸及其盐、氧化物的氧化能力随介质酸性的增强而增大。
(四).电极电势的应用(1)判断氧化剂和还原剂的相对强弱EΘ大,该电对的氧化型物质得电子能力强,是相对强的氧化剂(其还原型是相对弱的还原剂)EΘ小,该电对的还原态物质失电子能力强,是相对强的还原剂(其氧化型是相对弱的氧化剂)例:根据标准电极电势,判断Ag+,Zn2+,Ag,Zn中哪种物质氧化性较强,哪种还原性较强?EΘ (Zn2+∕Zn) =-0.7621VEΘ(Ag+/Ag) =0.7991VEΘ(Zn2+∕Zn)< EΘ(Ag+/Ag)故Ag+氧化性较强,Zn还原性较强(2)判断氧化还原反应进行的方向自发的氧化还原反应总是在得电子能力强的氧化剂与失电子能力强的还原剂之间发生。
即:强还原剂(1)+强氧化剂(2)→弱氧化剂(1)+弱还原剂(2)E MF=E (氧)- E (还)= E (+)-E (-)>0即:氧化剂对应的电对电势大于还原剂对应的电对电势。
经验判断:E MFΘ >0.2V 反应正向进行-0.2 V < E MFΘ< 0.2V 要根据浓度具体计算E MFΘ<-0.2V 反应逆向进行(3)判断原电池的正、负极、计算原电池的电动势正极——E较大的电极负极——E较小的电极E MF=E (+)-E (-)(4)确定氧化还原反应进行的限度计算标准平衡常数KΘln kΘ(T)=()zFE TRT(7—4)298.15Klg k Θ= MF (298.15k)0.0592vzE θ (7—5)注意: z —电池反应的电子得失数EΘMF —原电池的标准电动势(5)元素电势图①元素电势图:将同一元素不同氧化值的物种组成的各电对的标准电极电势以图的形式(从左到右,氧化值由高而低)表示出来,即为元素电势图。
E 1Θ E 2Θ E 3ΘA B C D(z 1) (z 2) (z 3)E ΘX(z X )②元素电势图的应用: A 、判断歧化反应:判断某中间氧化值物种能否歧化,若E Θ右>E Θ左该物种能发生歧化反应。
B 、计算标准电极电势:E ΘX = θθθ112233z E z E z E zX++ (7—6)z X = z 1+z 2+z 3。
