高中化学知识的结构体系(word版)
高中化学知识结构体系

高中化学知识结构体系一、化学的基本概念和原理1. 化学的定义和研究对象化学是研究物质的组成、性质、结构、变化规律以及与能量的关系的科学。
它主要研究物质的构成、性质和变化,包括物质的分子结构、化学键以及化学反应等。
2. 原子与元素原子是构成物质的最基本单位,由原子核和电子组成。
元素是由具有相同原子序数的原子组成的物质,元素可以通过化学反应进行组合和分解。
3. 分子与化合物分子是由两个或多个原子通过化学键连接而成的粒子,是化合物的最小单位。
化合物是由两种或更多种元素组成的纯物质,具有固定的化学组成。
4. 化学键与键能化学键是原子之间的相互作用力,是原子间电子的共享或转移所形成的力。
化学键的强弱可以通过键能来衡量,键能越大,化学键越稳定。
5. 化学反应与反应速率化学反应是物质发生变化的过程,包括物质的转化、生成和消失等。
反应速率是指单位时间内反应物消耗或生成的物质量。
二、物质的性质和分类1. 物质的性质物质的性质包括物理性质和化学性质。
物理性质是指物质在不改变其化学组成的情况下所表现出的性质,如颜色、形状、密度等。
化学性质是指物质在与其他物质发生反应时所表现出的性质,如燃烧性、与酸碱反应等。
2. 物质的分类物质可以分为纯物质和混合物。
纯物质是由同一种物质组成的,如元素和化合物。
混合物是由两种或多种不同物质混合在一起而形成的,如溶液、悬浊液和气体混合物等。
三、化学反应与化学方程式1. 化学反应的基本概念化学反应是指物质在一定条件下发生物质的转化、生成和消失等过程。
化学反应可以通过化学方程式来描述,化学方程式由反应物、生成物和反应条件组成。
2. 化学方程式的平衡与配平化学方程式需要满足质量守恒和电荷守恒的原则。
通过调整系数可以使化学方程式平衡,即反应物和生成物的物质量之比满足化学方程式的配平要求。
四、化学元素与周期表1. 化学元素的周期表化学元素是由具有相同原子序数的原子组成的物质,元素可以通过周期表来进行分类和研究。
(完整word版)高中化学必修二第一章知识点和习题(含答案),推荐文档

第一章物质结构元素周期律一、原子结构质子(Z个)原子核注意:中子(N个)质量数(A)=质子数(Z)+中子数(N)1.原子)原子序数=核电荷数=质子数=原子的核外电子数核外电子(Z个)★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层:一(能量最低)二三四五六七对应表示符号: K L M N O P Q3.元素、核素、同位素元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。
(对于原子来说)二、元素周期表1.编排原则:①按原子序数递增的顺序从左到右排列②将电子层数相同......的各元素从左到右排成一横行..。
(周期序数=原子的电子层数)③把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行..。
主族序数=原子最外层电子数2.结构特点:核外电子层数元素种类第一周期 1 2种元素短周期第二周期 2 8种元素周期第三周期 3 8种元素元(7个横行)第四周期 4 18种元素素(7个周期)第五周期 5 18种元素周长周期第六周期 6 32种元素期第七周期 7 未填满(已有26种元素)表主族:ⅠA~ⅦA共7个主族族副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族(18个纵行)第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间(16个族)零族:稀有气体三、元素周期律1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。
元素性质的周期性变化实质是元素原子核外电..........子排布的周期性变化.........的必然结果。
高中化学必修2思维导图(Word版)
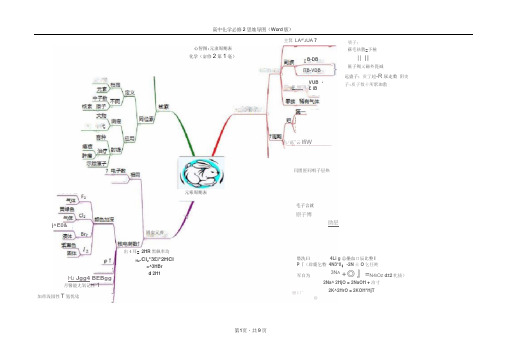
j^E0&主箕LA^'J UA 7心智图:元隶周期表化学(宓修2第1毫)B-DBITB-VDB却_畑飞之VUB ・£I B元寒周期表園实元養H J Jgg4 BEBgg月醫能尢氧记性1出4耳= 2HR黑飙率均Hz.Cl z*3£i*2HCl=^3HBrd 2H1加帝浅园性T氢忧唸占/菇"云lfiW* -----------JL-L -------------------------- 1--------------------------------------------嘖子;蘇毛祛敷=予極II II匾子羯乂磁外毘减远蛊子;贡亍超-R尿走数阴吏子:质子数十所駅珈敷闫匱匪同唱子层热毛子言就原子博助层塔洗曰4Li g总壘血口辰比整IP『(辟鹿乞特4N3*0;-2N士O乞任盹3N A+◎』=N4I O Z d±2牝拔)2Na^ 2HjO = 2NaOH + 泊寸2K^2HrO = 2KOH*HjT军白为屉卜厂◎H 原子子站斎武核电荷參堵勺打同誨牟宣走文元拱 元青哥朝潼叱学强心皆暨;元袞周期律化学锂化学(必悸2第1童)隔吉寿于乍毛力丑□r 贸性原子克:”空王咗托丄,屋_裁勻同N 「鳏论伽皐牛旳 fflMa 力酋WHHS 胡転占步輕理性质焉响舷性广莊匪辜議羸物廣寻找启发 fc ---- « J -------- 1 備/_■ : 兀魁隹凰不意圏宣口同匱或广—-电子昨叭 西石策子捋嵩!匚二—.它三玄塔二一 尉卜聽亍竝司"L]同主察桓同吾丢性晅子字效1一 E助层里孑救WL內吾+ ]r 4化台•'介医匪敷斗_原于半径暑13个V 电子敷 r ~《葩.塀呈苣之鱼寻梅心音圍:代学反应与能星 化宝(必修2第2章】•佶能与捣詬rs乏卫奉r wr 化学反应与蕃量学能与邑聽原电池丈A連□決:毛子不下取;禹子不上岸 爾垃匣©謹:如正还 禅池B 進謹:色過艺虽大割吏良应複门f *・严 「・r ・严厂 -----------------------------------'.叱円頁衣豈尺矽淞亶『圭豌牛1甘厂 —’ L -------- 卑检吁间 」H_U 便垦删浏严nnoi/(L-5) .袤云mol/CL-min ;j^B8y ― ----- --------il-t > Q 晅护•反应AH -Q L - Q /------------- ------------二” < D 京註乏二2)^册舷匝T 辭「 疋反帆_—TTA RB3®C T亦Yu 原电乜电輕罢甞近正視2屮f -H :T対E Zn ■ 2e- -Zn^ 靱云 rn ^ZH 1 -Zn 1- + HrT住期殺:Cu'- +Je- =Cu卿:2HK>-4e =O ;t*4H^总豈・M : ^Cu-^^H^O =£M ^Cu-0s r-H4H- 平衡丽珈師:直更标衣①¥丘-唾 g ■各柜琳室聞不娈 闻按耗:◎::总合住翌、总£3糕、总需底的垦科SB?阎的适毒恋 更②互处師空度或平垢相灯舒质星不墮冇间适而迪* 卷台休的廉色不輔时问应莊而逝 言瘻蘇任何时聞戒立:叵捷标志墓孤住趣恵呵竇⑥融侪电I® 达平斬也就是.交星不更砖池巨二二乂若乜冋更屋池裝餐老能-化我云皿二吨子兰垢tuSG-高中化学必修2思维导图(Word 版)心智囹:眉简单的有机物-甲烷昨(必想2第3韋)C-C 柜唾fe5a P=fl.717j/L j正匸荀W 空可希 同茎X 崔海唇■;…*时取1换代r ~\^TSC.H. + 心 愈” 0 4- 3H E O 匸丸事XiSM 不同强分辰茗体优■曲同分毛同廿予式 CH 4+CI J ^ fH^Cb 十 Cb CHClj + CL 庄整nci-bCHzCi 伺部麻那那卫斗Hd + CH^LCW 机君判】 t 呈邑nci 十匚HCM 氮访]制聞) -^£>HCI * <XL (四氣化瑕・灭火剂「有机海册Ik 上亦确皤申不竝 最简单的有WMir 甲烷 砂二样 冒英粗區 碍同元索 H-C -HH具一烷ZT 端 (T 烷两科同分吳梅樹 道式匚“甩“沁nn c;比曲+』$lq 逑+3丰1)円Q 前離点T兰一股一直T遇性俸取亡卜卯工+dj[垂诸中不证M :曰C^HiiJ^^CiHis-CiH^儘行子氏毎H 可以裂代谀朗4 乎6CO j + 3H;a火皓明亮「有、:T黒奉色代亦岫取代壽---------------------------------------―—1 + HO-NO;■| J(m^M)加.成PJ不迂奎KMnQ.逗化雅0+HO-SOjH-20住旳一^0 环己做加5皈劇平輕SOsH+H:OKMnOi 逐鱼80.代躍海蜒鱼KMnO*JH亦于萼 6 竝-nCO2 +伯幻垃威22磁c=c乙値来自石油和煤的两种基本化工嗣屁辱杓疾I 石fruk'MX低行于一壹分子■* -C-C-加虑反应一―.至使一皿CjFL + 3Oj 磁.JCOj + 2HjO(>d® 瞻・SSJ®CH;・ CH; * HCI - CHjCH^I (制気乙境CHi-CHj:+Br:- <H:BrChr8r f涙水歸iM = £H= + KQ +詈姿_■• *3山T戲乙對胃嗓加庄水平SMK丁 CHj=CH7+ HZ Ni> CHjCHi汽,Cl-I;-}? (MSJE®心智閏:来自石油和淇的两种基車化工恵料化学(魁修2第』章)nCHi = CHi乙晞聊匸或反应和肚聚豆应驴主KWrO-tISfigj CHjOII,——CHjY — H -H —O — I M 5 :—- 乙蒔 一—严军葢牛甘H 俎 右H 艇换□II-匚Hi —C —C^Czhii +HjO乙薛己塞拡取弋堆汩£连世疑中HCHXOOHOCHjCHrOH + SOj最基—COOH乙辱I 匯基—CHOI 赵—NO : r-la<Ot * 2CI~liCOO H=2C HjCOONa + CO :1 + HQ 霁鞍幡称Ch J €OOH>H ;CO=■■工盏穗、竺唾吵釉[L17贰沸蛊才吏虹炬石笈旦醴可 口M — 廿 _— _ ir^ja_»_^jL-rr~n g5i llCH J C-OHP<HjO *握址哥 亡u 或Aq 眈理性■鱼ZCHjCHfQH + Qj —— iCHsCHC+ZHjO 朋弓吃渦盡 门忙、"552 HH 7CHX>H+2lMa — JtHjCHiONa^MjT -舅ii 发 平屢IN 可质应 心宵團:生活中两种常见前有阴化学(凶02第垣)生活中两种常见的右翊滋H£6匪奩X.墓怛恫右智團;基本营养物庾此学(必修2第月章)I Q097僚蛋兰更麦芽请疥砖唐聲芝C<脂册憨BTF竝存在q脣9S IT(SkoCUh 亠riH£坐炮淀粉{或肝進襄)变黄疑雋打毛唳廉克蛊曲旨肪竝■c=cW匪匚计七Qx + H卫涅赫吏莓曲^±/—出薜歸病基本营舷质在■輛飪sq + GHq苇萄睹寻雀nQHizOt野華密比淒S+E<TX M作用内匪阳H退里議窘丈.... ............. <...... 1SS柞用]「加1u tt——忒.圣丁盘W*・,3*™ ■-=--———S ____有參二::匚热m髯杏活洩全寻-冒环令壬■聯戟术込4毎方旬裁禺伍廿4------- J潯水缺膏理幵再匚利用翠全原矿沏的幵勵」用右冒聞;开发^用金廣矿物和画水熒再化学(必惶2 S4M)毎水j籃利巨區海水如這源的开发利用、沖口列益臺csra , ■I~^^41薊鬭垦金黒览驾金畧資通.—盍于沁愛TS 咖査成本海水水誑浪利用m LixlOfl37%«ffi球环星>妁&_飞金寓飾?HgO 5^; 2Hg * C J F酣肿4Ag + Oil■- gF^Of * 3C0 2F* -H 3C0;(髙啡轶}阻J6*氛I臺墨2宅+ Al工id答心彬:?fuiS + Oz=^r Xu 亠50二叹1 去聞]Fe 十Cu 5(□二=FeSO^ +MgCL =Sfi= Mg Yb f 2A I7O54AI + 5O3t JNaCi 2Na + CIJ熔融塢融冬“u煖融g 蛊監需零f H WOWQH1°瞬也匪QMi 屮^\Tjfc±7心曾團:资砖合利用 环境懈护化字滋修2第4章)気上三■亟一%左碇酸兮裂化羊ct 合成“m 匕的单之CH ; =匚缶 拒节一£衬YH :I - ■“ ’fflW星盘聚化煤石油去愿吒资源煤合利用 环境探护:变忧隧戎屋二意贾遇士主乙殊8密气汽化盲工东二右-M 璽严曲■ 一生成物血垦._ 100旺丿CwHji 豐专z ■* C S H U +C I M H 血瞰血压* *T/Ure^=wt —I*三三n 犀合磴歆目生产甲磐不同洗点各锻廿乱冃台老気黃桝气。
(完整word版)高考化学物质结构与性质

高考化学物质结构与性质前言:高中化学120个关键知识,为高中理科生整理,请同学们收藏学习,为了资源的共享,请把此资料转载分享、或发表在博客、论坛上,以便分享给更多的同学一. 学习内容:分子结构与晶体结构二. 学习目标了解化学键的含义,理解并掌握共价键的主要类型及特点,共价键、离子键及金属键的主要区别及对物质性质的影响。
能根据杂化轨道理论和价层电子对互斥模型判断简单分子或离子的空间构型,了解等电子体的含义。
了解原子晶体、分子晶体和金属晶体的结构特征,掌握不同晶体的构成微粒及微粒间的相互作用力,掌握影响晶体熔沸点、溶解性的因素。
三. 学习重点、难点分子结构与晶体结构的特点,影响物质熔沸点和溶解性、酸性的因素四. 学习过程(一)化学键与分子结构:1、化学键:相邻的两个或多个原子之间强烈的相互作用,通常叫做化学键。
三种化学键的比较:离子键共价键金属键形成过程阴阳离子间的静电作用原子间通过共用电子对所形成的相互作用金属阳离子与自由电子间的相互作用构成元素典型金属(含NH4+)和典型非金属、含氧酸根非金属金属实例离子化合物,如典型金属氧化物、强碱、大多数盐多原子非金属单质、气态氢化物、非金属氧化物、酸等金属配位键:配位键属于共价键,它是由一方提供孤对电子,另一方提供空轨道所形成的共价键,例如:NH4+的形成在NH4+中,虽然有一个N-H键形成过程与其它3个N-H键形成过程不同,但是一旦形成之后,4个共价键就完全相同。
共价键的三概念意义共价键按成键形式可分为σ键和π键两种,σ键主要存在于单键中,π键主要存在于双键、叁键以及环状化合物中。
σ键较稳定,而π键一般较不稳定。
共价键具有饱和性和方向性两大特征。
2、分子结构:价层电子对互斥理论:把分子分成两大类:一类是中心原子上的价电子都用于形成共价键。
如CO2、CH2O、CH4等分子中的C原子。
它们的立体结构另一类是中心原子上有孤对电子(未用于形成共价键的电子对)的分子。
高中化学知识架构图

高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)源-于-网-络-收-集源-于-网-络-收-集第四部分:有机化学有机抓住官能团的性质烃烃的衍生物糖链烃(脂肪烃)环烃饱和链烃烷烃:C n H 2n+2(n ≥1)R —CH 3 不饱和链烃 烯烃:C n H 2n (n ≥2) R —CH=CH 2二烯烃:C n H 2n-2(n ≥4)R —CH=CH —CH=CH 2 炔烃:C n H 2n-2(n ≥2) R —C ≡CH环烷烃C n H 2n (n ≥3)芳香烃(苯和苯的同系物)C n H 2n-6(n ≥6)R卤代烃(官能团:—X ):饱和一卤代烃C n H 2n+1X(n ≥1)R —X 醇 (官能团:—OH ):饱和一元醇C n H 2n+1OH(n ≥1)R —OH 醚 C n H 2n+2O (n ≥2)R —O —R 酚(苯酚)(官能团:—OH )C n H 2n-6O (n ≥2)OH羧酸 (官能团:—COOH ):饱和一元羧酸 C n H 2n+1O 2 (n ≥1)R —COOH醛 (官能团:—CHO )C n H 2n O (n ≥1)R —CHO 酮 (官能团:—CO —)C n H 2n O (n ≥3)R —CO —R ’酯 (官能团:—COO —R ):饱和一元羧酸和饱和一元醇形成的酯 C n H 2n O 2 (n ≥2)R —COOR ’ 硝基化合物(官能团—NO 2)R —NO 2 胺(官能团—NH 2)R —NH 2单糖:葡萄糖、果糖C 6H 12O 6(互为同分异构) 二糖:蔗糖、麦芽糖C 12H 22O 11(互为同分异构)有机化合物源-于-网-络-收-集。
高中化学word知识点总结

高中化学word知识点总结一、原子与分子1. 原子结构:原子由原子核和核外电子组成。
原子核包含质子和中子,质子带正电,中子不带电,电子带负电。
2. 原子序数:原子序数等于核内质子数,也等于核外电子数,决定了元素的化学性质。
3. 电子排布:电子按能级排布,每个能级有其最大容纳电子数,排布遵循泡利不相容原理和洪特规则。
4. 分子:由两个或多个原子通过化学键结合而成的稳定粒子。
5. 化学键:原子间相互作用力,包括离子键、共价键和金属键。
二、元素周期表1. 周期表结构:元素按原子序数排列,分为7个周期和18个族。
2. 主族元素:1A至8A族,最外层电子数与族数相同。
3. 过渡元素:8B族至7B族,具有不完全填充的d轨道。
4. 镧系和锕系元素:位于周期表下方,具有特殊的电子排布。
三、化学反应1. 反应类型:包括合成反应、分解反应、置换反应和还原-氧化反应等。
2. 化学方程式:用化学符号表示反应物和生成物的关系,通常伴随质量守恒。
3. 反应速率:受反应物浓度、温度、催化剂等因素影响。
4. 化学平衡:可逆反应达到动态平衡状态,反应物和生成物浓度保持不变。
5. 酸碱反应:酸与碱反应生成水和盐,pH值用于表示溶液的酸碱性。
四、溶液与溶解1. 溶液:一种物质或几种物质分散在另一种物质中形成的均相混合物。
2. 溶解度:在一定温度下,某种物质在溶剂中的最大溶解量。
3. 饱和溶液:溶解物质达到最大溶解度的溶液。
4. 溶解平衡:溶解和结晶达到动态平衡的状态。
五、氧化还原反应1. 氧化:物质失去电子的过程。
2. 还原:物质获得电子的过程。
3. 氧化剂:使其他物质氧化的物质,本身被还原。
4. 还原剂:使其他物质还原的物质,本身被氧化。
5. 电化学系列:金属按照还原能力排列的序列。
六、化学能与热能1. 化学能:化学反应中储存或释放的能量。
2. 热能:物质内部粒子运动产生的能量。
3. 反应热:化学反应过程中吸收或释放的热量。
4. 燃烧:可燃物质与氧气反应,迅速释放大量热和光的过程。
(完整word版)高中化学知识点总结
化学知识点总结一基本概念:1、化学变化:生成了其它物质的变2、物理变化:没有生成其它物质的变化3、物理性质:不需要发生化学变化就表现出来的性质(如:颜色、状态、密度、气味、熔点、沸点、硬度、水溶性等)4、化学性质:物质在化学变化中表现出来的性质(如:可燃性、助燃性、氧化性、还原性、酸碱性、稳定性等)5、纯净物:由一种物质组成6、混合物:由两种或两种以上纯净物组成,各物质都保持原来的性质7、元素:具有相同核电荷数(即质子数)的一类原子的总称8、原子:是在化学变化中的最小粒子,在化学变化中不可再分9、分子:是保持物质化学性质的最小粒子,在化学变化中可以再分10、单质:由同种元素组成的纯净物11、化合物:由不同种元素组成的纯净物12、氧化物:由两种元素组成的化合物中,其中有一种元素是氧元素13、化学式:用元素符号来表示物质组成的式子14、相对原子质量:以一种碳原子的质量的1/12作为标准,其它原子的质量跟它比较所得的值某原子的相对原子质量=相对原子质量≈ 质子数+ 中子数(因为原子的质量主要集中在原子核)15、相对分子质量:化学式中各原子的相对原子质量的总和16、离子:带有电荷的原子或原子团17、原子的结构:原子、离子的关系:注:在离子里,核电荷数= 质子数≠ 核外电子数19、还原反应:在反应中,含氧化合物的氧被夺去的反应(不属于化学的基本反应类型)氧化反应:物质跟氧发生的化学反应(不属于化学的基本反应类型)缓慢氧化:进行得很慢的,甚至不容易察觉的氧化反应自燃:由缓慢氧化而引起的自发燃烧20、催化剂:在化学变化里能改变其它物质的化学反应速率,而本身的质量和化学性在化学变化前后都没有变化的物质(注:2H2O2 === 2H2O + O2 ↑ 此反应MnO2是催化剂)21、质量守恒定律:参加化学反应的各物质的质量总和,等于反应后生成物质的质量总和。
(反应的前后,原子的数目、种类、质量都不变;元素的种类也不变)22、溶液:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物溶液的组成:溶剂和溶质。
(完整word版)高中化学《《选修3物质结构与性质》》教材分析
高中化学vv选修3物质结构与性质>>教材分析
物质结构理论是现代化学的重要组成部分,也是医学、生命科学,材料科学、环境科学、能源科学、信息科学的重要基础。
它揭示了物质构成的奥秘。
物质结构与性质的关系,有助于人们理解物质变化的本质,预测物质的性质,为分子设计提供科学依据
在本课程模块中,我们将从原子、分子水平上认识物质构成的规律,以微粒之间不同的作用力为线索,侧重研究不同类型物质的有关性质,帮助高中学生进一步丰富物质结构的知识,提高分析问题和解决问题的能力。
一、模块的功能
高中化学选修3是在在必修课程基础上为满足学生的不同需要而设置的。
我省理工方向的学生必须选修本模块,它是学业水平考试和高考的内容。
本模块选修课程旨在让学生了解人类探索物质结构的重要意义和基本方法,研究物质构成的奥秘,认识物质结构与性质之间的关系,提高分析问题和解决问题的能力。
二、模块的课程目标
通过本课程模块的学习,学生应主要在以下几个方面得到发展:
1从科学家探索物质构成奥秘的史实中体会科学探究的过程和方法,增强学习化学的兴趣;
2•进一步形成有关物质结构的基本观念,初步认识物质的结构与性质之间的关系;
3 •能从物质结构决定性质的视角解释一些化学现象,预测物质的有关性质;
4•在理论分析和实验探究过程中学习辩证唯物主义的方法论,逐步形成科学的价值观。
三、模块的内容标准及学习要求
学习要求分为基本要求和发展要求:
基本要求:全体学生应在本节学习时掌握。
发展要求:有条件的学生可在选修3结束时掌握。
第二章分子结构与性质
第三章晶体结构与性质
节。
高中化学知识点总结word
高中化学知识点总结word一、基本概念与原理1. 物质的组成与分类- 物质由元素组成,分为纯净物和混合物。
- 纯净物包括单质和化合物,单质是由同种元素构成,化合物由不同元素以固定比例结合。
2. 原子结构- 原子由原子核和核外电子组成。
- 原子核包含质子和中子,核外电子围绕原子核运动。
- 电子排布遵循奥布定律,分为s、p、d、f轨道。
3. 化学式与化学方程式- 化学式表示物质的组成和分子的结构。
- 化学方程式表示化学反应的过程,包括反应物、生成物和反应条件。
4. 化学反应类型- 合成反应、分解反应、置换反应、还原-氧化反应等。
5. 化学计量- 质量守恒定律:化学反应前后物质总质量不变。
- 摩尔概念:物质的量的单位,用于化学反应的定量计算。
二、元素与化合物1. 元素周期表- 元素按照原子序数排列的表格,分为周期和族。
- 元素周期表反映了元素的周期律和族律。
2. 主族元素- 包括碱金属、碱土金属、硼族、碳族、氮族、氧族、卤素、稀有气体。
- 各主族元素具有相似的化学性质。
3. 过渡金属- 包括第3至12族的金属元素。
- 过渡金属通常具有多种氧化态。
4. 化合物的性质- 酸碱性、氧化还原性、溶解性、热稳定性等。
5. 重要的无机化合物- 氧化物、酸、碱、盐。
- 常见无机化合物的性质和用途。
三、化学反应原理1. 化学平衡- 可逆反应达到动态平衡,反应速率相等。
- 勒沙特列原理:系统自动减弱外界条件变化的影响。
2. 酸碱理论- 阿伦尼乌斯酸碱理论、布朗斯特-劳里酸碱理论。
- pH值:表示溶液酸碱性的量度。
3. 氧化还原反应- 氧化还原反应中,电子的转移是核心。
- 氧化剂和还原剂的概念。
- 电化学系列和标准电极电势。
4. 配位化学- 配体与中心离子的配位键合。
- 配位化合物的命名和性质。
四、有机化学基础1. 有机化合物的定义- 含有碳元素的化合物,除了碳酸盐、碳酸、简单的碳酸衍生物。
2. 有机化合物的结构- 碳的四面体结构、异构现象。
《化学教案》word版
《化学教案》word版一、教案简介本教案主要针对高中化学课程,涵盖了基本概念、原理、实验和应用等内容。
通过系统的讲解和练习,使学生掌握化学基础知识,培养学生的实验技能和科学思维能力。
二、教学目标1. 了解并掌握化学基本概念、原理和方法。
2. 能够运用化学知识解释和解决实际问题。
3. 培养学生的实验操作能力和科学探究能力。
4. 提高学生的科学思维能力和创新意识。
三、教学内容第一章:化学基本概念1.1 物质的组成和分类1.2 原子和分子1.3 离子和化合价1.4 化学方程式第二章:元素周期律2.1 元素周期表2.2 元素周期律的应用2.3 金属与非金属元素2.4 过渡元素第三章:化学反应3.1 化学反应类型3.2 化学平衡3.3 氧化还原反应3.4 酸碱反应第四章:实验技能4.1 实验基本操作4.2 常见仪器的使用4.3 实验安全与事故处理4.4 化学实验方案的设计与评价第五章:化学与生活5.1 生活中的化学现象5.2 化学与健康5.3 化学与环境5.4 化学在高新技术领域的应用四、教学方法1. 采用讲授法,系统讲解化学基本概念、原理和方法。
2. 利用实验法,培养学生的实验操作能力和科学探究能力。
3. 采用案例分析法,引导学生运用化学知识解决实际问题。
4. 利用讨论法,培养学生的科学思维能力和创新意识。
五、教学评价1. 平时成绩:包括课堂表现、作业完成情况、实验报告等。
2. 期中考试:测试学生对化学基本概念、原理和方法的掌握程度。
3. 期末考试:全面考察学生的化学知识运用能力和实验技能。
4. 学生自我评价:反思学习过程中的收获和不足,提高自主学习能力。
六、教学资源1. 教材:高中化学教材2. 课件:PPT课件,辅助讲解和展示化学知识3. 实验器材:实验室设备和学生实验套装4. 网络资源:相关化学知识和实验视频、论文等5. 练习题库:针对不同知识点设计的练习题和模拟试题七、教学进度安排本章内容预计授课时间为2周,具体安排如下:第一天:1.1 物质的组成和分类第二天:1.2 原子和分子第三天:1.3 离子和化合价第四天:1.4 化学方程式第五天:复习并进行章节测试八、教学活动设计1. 课堂讲解:教师通过PPT课件,生动形象地讲解化学基本概念、原理和方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学知识的结构体系
★在高考考试大纲中,对高考化学科考试范围分为“必考内容”和“选考内容”两部分。
总计51个知识点,167个考点。
1、必考内容:涵盖必修模块“化学1”、“化学2”和选修模块“化学反应原理”的内容。
2、选考内容:涵盖选修模块“化学与生活”、“化学与技术”、“物质结构与性质”、“有机化学基础”的内容,在高考中考
生从中任选一个模块考试。
必考内容,必修一:19个知识点,56个考点。
必考内容,必修二:10个知识点,32个考点。
必考内容,选修四:5个知识点,21个考点。
选考内容,选修一二三:10个知识点,33个考点。
选考内容,选修五六:7个知识点,25个考点。
(必考)必修1——人教版高一上学期
第一章从实验学化学
•本章特点内容比较简单,但是从第二节物质的量开始很多学生学不明白。
•本章是高一学生开始化学退步的开始,甚至是高三理科生的死结。
•应对办法:真正的理解知识,配合少量的习题。
•高考命题:计算题或者阿伏伽德罗常数的选择题,属于高考热点。
第二章化学物质及其变化
•本章内容主要是氧化还原和离子反应。
•本章很多同学存在的困难是氧化还原配平。
•应对办法:学习配平技巧。
•高考命题:离子共存、离子方程正误的选择题,属于高考热点、常考点。
氧化还原易出计算类选择或者计算题,也可能出判断类选择。
第三章金属及其化合物
•本章重点内容是金属钠、过氧化钠、金属铁的两种变价、铝的两性。
是会考重点。
•本章方程式增多,学生困惑在方程式的记忆。
但本章学生自己感觉难度不大。
•应对办法:学习归纳法的技巧,系统学习。
•高考命题:推断题,实验题,选择题。
第四章非金属及其化合物
•本章重点内容是氨气、氯气、碳和硅。
是会考重点。
尤其是氯气和氨气的制取是会考必考点。
•本章方程式增多,学生困惑在方程式的记忆。
但本章学生自己感觉难度不大。
•应对办法:学些归纳法之类的技巧,系统学习。
(必考)必修2——人教版高一下学期
第一章物质结构元素周期律
•本章重点为元素周期律的五大规律。
•本章学的时候较容易,但是周期表不易记忆。
会考必考点
1.应对办法:将周期表的主族元素反复熟悉,反复分析,形成高中化学的记忆桩。
2.高考命题:无机推断、选择题和实验题。
第二章化学反应与能量
•重点内容为原电池、吸放热反应判断和反应速率计算。
会考每一个点命制一道选择题。
•《选修四》半册将继续深入学习。
•应对办法:化繁为简。
第三章有机化合物
•重点是甲烷、乙烯、乙醇、乙酸乙酯。
会考会出现填空题,难度不大。
•《选修四》半册将继续深入学习,但是内容并不重复!
•应对办法:理解为主,结构决定性质。
第四章化学与可持续发展
•重点为金属冶炼。
•应对办法:通过金属性非金属性串联金属与非金属的实际应用。
学习化学与可持续发展的连接点•高考命题:选择题和实验题。
(必考)选修4——人教版高二上/下学期
第一章化学反应与能量
•本章是高考热点、重难点。
•重要内容为:燃烧热、中和热和盖斯定律。
近年比较流行在大题中考察热化学方程的书写。
•应对办法:首先知识一定要理解,其次平时学习一定要拓展难度,多见新题和难题。
第二章化学反应速率和化学平衡
•高考热点、重难点。
一般以选择题和大题形式考查。
•重点内容:化学反应速率、平衡标志、转化率、平衡移动。
•应对办法:学习技巧、分类通关。
第三章水溶液中的离子平衡
•高考热点、重难点。
一般以选择题形式考查。
•重点内容:电离/水解平衡的移动、离子浓度比较、KSP。
•应对办法:理解知识、掌握技巧、反复学习、多加练习。
第四章电化学基础
•高考热点、重难点。
一般以选择题或大题形式考查。
•重点内容:燃料电池、钢铁腐蚀、电镀、精炼铜、蓄电池。
•应对办法:学习技巧、分类通关。
(选考)选修5——人教版高二上/下学期
第一章认识有机化合物
•学习重点为同分异构体、有机物命名、原子共平面问题。
•本章难度最大,核磁共振和红外光谱属于新加内容,高考易命题。
第二章烃和卤代烃
•主要内容为有机物的化学性质和特性。
第三章烃的含氧衍生物
•主要内容为有机物的化学性质和特性
第五章进入合成高分子化合物的时代
•主要考察高分子合成,一般推断最后一步。
•有机高考命题为一道有机推断题,主要考察整个化学学科的综合能力。
(选考)选修1——人教版高二上/下学期
第一章关注营养平衡
第二章促进身心健康
第三章探索生活材料
第四章保护生存环境
知识点多,考察细碎,会考高考经常从中取材。
(选考)选修6——人教版高二上/下学期
第一单元从实验走进化学
第二单元物质的获取
第三单元物质的检测
第四单元研究型实验
•高考会命制一道19分左右的实验题,但是该部分内容一般会在《必修一》第三、四章或者高三总复习中详细讲解,一般不会细讲本册书。
化学变化
物质结构
时间内容学习目标
高一暑预习必修一学业水平考试要求
高一秋必修一同步提高高考中档题要求,无机大题初探高一寒预习必修二学业水平考试要求
高一春必修二同步提高周期律达到高考要求
高二暑预习选修四化学反应原理学业水平考试要求
高二秋选修四同步提高高考难题要求
高二寒预习选修五有机化学学业水平考试要求
高二春选修五有机化学高考中难题目要求
高三暑一轮复习基本概念,元素化合物一轮复习高考领先
高三秋一轮复习基本理论,有机化学一轮复习高考领先
高三寒二轮复习化学实验二轮复习总结规律
高三春三轮复习高考分类汇编认清高考,收心备战。
