第6章精馏2
化工原理蒸馏精馏知识要点

三、操作线方程
1. 精馏段操作线方程
对如图划定范围作物料衡算 V=L+D 对易挥发组分衡算 Vyn+1=Lxn + DxD V, yn+1
D,xD
第n板
L, xn
Dx D L y n 1 x V V 令回流比 R=L/D xD R y n1 xn R1 R1
2. 恒摩尔溢流
精馏段内,每层塔板下降的溢流摩尔流量相等。 提馏段内,每层塔板下降的溢流摩尔流量相等
L1=L2=…=Ln=定值 (精馏段) L 1=L2=…=Ln=另一定值 (提馏段) 一定注意: 精馏段和提馏段下降的溢流分别不相等。 精馏段和提馏段上升的蒸汽分别不相等。 因为加料板加入原料液后使两段汽液两相流量发 生变化。 当各组分摩尔汽化焓相等,汽液接触良好且可忽 略显热(与汽化热比较),保温良好且塔的热损失 可忽略时,恒摩尔流假定基本上成立。
露点
泡点
x或 y
0 P p A pB p 0 x p A A B (1 x A )
xA
0 P pB 0 p0 p A B
y A p0 A xA / P
对某一温度和总压,由这几式可求出xA,yA。 得出一系列的值后便可作出如前图所示的图来。 对于非理想溶液,计算很复杂。一般由实验得 出平衡数据。实验得出的平衡数据也是计算的 基础。
2. 相对挥发度(relative volatility)
溶液中两组分挥发度之比称相对挥发度,。通 常用易挥发组分挥发度作分子。
vA pA / x A vB pB / x B
武汉大学-《化学工程基础》第6章精馏-2

提馏塔段的计算公式
q q
q
y
x
x
q q q
q q q
➢ 由提馏段第二层塔板下降的液体组成x’2与 y’2符合相平衡关系, 由相平衡方程可以解出 x’2, 依此类推, 当x’m≤xw为止。提馏段的理 论塔板数为m-1, 而精馏塔所有的塔板数为 (m+n-1)
➢ 由此可以求出理论塔板数。 ➢ 这种方法计算的结果较准确。
§7传质设备
• 7-1评价传质设备的指标 • 传质设备主要有填料塔和板式塔. 评价
指标为: • 1.分离效果 • 分离效果是指每层塔板或单位高度的填
料所能分离的程度, 它取决于物料的性 质与操作状态。 • 2.生产能力 • 是指单位时间单位塔截面上处理的物料 的量.它与空塔速度有关. •
• 3.压力降
yn1 yn1
一块实际板汽相浓度的变化 一块理论板汽相浓度的变化
yn* — —与xn成平衡的气相组成。
• (2)液相莫弗里板效率(EML)
EML
xn1 xn1
xn xn*
一块实际板液相浓度的变化 一块理论板液相浓度的变化
xn* — —与yn成平衡的液相组成。
2.总板效率
N ET N
N N
• 精馏原料的进料状态有以下5种: • (1)温度低于泡点的冷液体,δ>1; • (2)处于泡点的液体,δ=1; • (3)温度介于泡点与露点之间的气液混合
物,0<δ<1; • (4)温度处于露点的饱和蒸汽,δ=0; • (5)温度高于露点的过热蒸汽,δ<0. • 表现在图上是提馏线向左移动.
五种进料对δ线的影响
• 2.根据xf和xd,1计算最小回流比Rmin
• 最小回流比Rmin为:
化工原理 第六章 蒸馏

相同时进行多次部分冷凝和部分汽
化。 精馏条件:塔顶的液体回流和塔 釜的产生的蒸汽回流。
29
t P=定值 t1
t P=定值 t1 t2 t3 1 2 3
xW x1
xF
y1
yF
x(y)
x1
x2 xF x3 y1
y2 y3 x(y)
图6-10 一次部分气化的图
图6-11 多次部分气化和冷凝的示意图
30
V HF 加料板F L’ hF V’ H F+1
L' L q F
L L q F
'
F L V ' V L'
V ' V (q 1)F
41
V F L V F L V (1-q)F F qF L L’ 汽液混合进料
V =V (1 q)F
V’
V’
L’ 冷液进料
p p xA p
0 A 0 B
0 A
0 B
0 B
0 P pB xA 0 0 p A pB
xB 1 x A
——泡点方程
若平衡的气相为理想气体,可用道尔顿分压定律:
0 pA pA yA x P P
yB 1 y A
——汽液两相平衡组成间的关系
0 0 0 pA pA p pB f A (t ) p f B (t ) —露点方程 yA xA 0 0 p p pA pB p f A (t ) f B (t )
3
传质过程或分离操作:物质在相间的转移过程。
蒸馏:将液体混合物部分气化,利用各组分的挥发 度不同的性质以实现分离目的的操作。
易挥发组分(轻组份):沸点低的组分 难挥发组分(重组份):沸点高的组分
中山大学化工原理课件 第6章-精馏

0 0 pA P pB yA 0 0 P p A pB
上式为一定总压下汽相组成与温度的关系式。该温度又称为露点 (dew-point),上式又称为露点方程。
严格地说没有完全理想的物系。对那些性质相近、结构相似的组分 所组成的溶液,如苯-甲苯,甲醇-乙醇等,可视为理想溶液;若汽相 压力不太高,可视为理想气体,则物系可视为理想物系。 对非理想物系不能简单地使用上述定律。汽液相平衡数据更多地依靠 实验测定。
塔顶产品 yA 加热器 原料液
减压阀
闪 蒸 罐 xA
Q
塔底产品
三、精馏原理与流程 1. 精馏操作流程 精馏塔 精馏段 提馏段 塔顶冷凝器 塔釜再沸器 塔顶冷凝液 馏出液 回流液 塔釜产品 – 釜液 进料液 – 原料液 进料板
精 馏 段
提 馏 段
2. 精馏原理
T y2 o2 x2 x1 b 0 o1 y1
第四节 物料衡算和操作线方程
V
一. 全塔物料衡算 总:
D, xD
F D W
轻:
F, xF
FxF DxD WxW
W, xW
应用1: 确定产量及组成之间的关系
应用2: ① 确定馏出液采出率
F, xF
V
L
D, xD
D xF xW F xD xW
② 确定xD,max或 Dmax
露点
气相区
t/C
两相区
露点线
泡点 泡点线
液相区
0
xA
xf x(y)
yA
. 1.0
当温度达到该溶液的露点,溶液全部汽化成为组成为 yA= xf 的气相, 最后一滴液相的组成为 xA。
第六章 蒸馏

第六章蒸馏第一节概述一、蒸馏分离依据---利用液体混合物中各组分具有不同的挥发度而进行分离的操作;----即利用在相同温度下各组分的蒸汽压不同。
易挥发组分(轻组分)A难挥发组分(重组分)B例如:酒精(A)与水(B)溶液,沸腾部分汽化,y A>x A同理,蒸汽部分冷凝,x B>y B∴蒸馏----使液体混合物部分汽化,利用其挥发度差异实现初步分离的一种传质操作精馏---利用多次部分汽化,多次部分冷凝,使汽相得到较纯的轻组分,液相得到较纯的重组分的操作二、蒸馏操作分类简单蒸馏(微分蒸馏)与平衡蒸馏(闪蒸)常压蒸馏、加压蒸馏与减压蒸馏连续蒸馏与间歇蒸馏普通蒸馏与特殊蒸馏三、蒸馏分离推动力与分离极限蒸馏是汽液两相间的传质过程蒸馏分离推动力——两相浓度偏离平衡的程度蒸馏分离极限——汽液两相达到相平衡(动态平衡)第二节 双组分溶液的汽液相平衡一、相组成表示法1.质量分率 iAA G G a ∑=该相的总质量一相中某组分质量可见:a <1, a A +a B …+ a N =1 2.摩尔分率 x A ,x B , y A ,y B 3.两者关系 )/(/)/(/i i AA i i A A i A A M a M a M G M G n n x ∑=∑=∑=对两元溶液:B B A A AA A M a M a M a x ///+=BB A A AA A M x M x M x a +=二、溶液的蒸汽压与Raoult 定律1.蒸汽压:汽液相平衡是一种动态平衡纯溶液----在达到汽液动态平衡时,逸出的A 分子数=回到液相的A 分子数,此时汽相中A 的压强=该温度下A 的饱和蒸汽压0A P混合液(A 、B 互溶)----在达到平衡时,由于A 、B 分子间相互作用,使B p <0B P , p A <0A P溶液存在三种分子间的作用力:AA f ,BB f ,AB f (1) 理想溶液:AB BB AA f f f ==显示无容积效应,无热效应如:苯-甲苯,甲醇-乙醇,烃类同系物溶液 (2)非理想溶液(实际溶液);AB BB AA f f f ≠≠2.Roult 定律:实验证明,在一定温度下,理想溶液的汽相中,任一组分的分压等于:A A A P x p =, 00)1(B A B B B P x P x p -==00000)()1(B B A A B A A A B A P P P x P x P x p p P +-=-+=+=00BA B A P P P P x --=∴ 非理想溶液不符合Roult 定律,汽液平衡关系主要靠实验数据。
化工原理-6章蒸馏

y x 1 ( 1)x
——相平衡方程
当 α为已知时,可用相对挥发度表示了气液相平衡关系。
当 1 当 1
y=x, 即相平衡时气相的组成与液相的组成相同, 不能用蒸馏方法分离。
则y>x,α愈大,y比x大的愈多,组分A和B愈易分离。
三、双组分理想溶液的气液平衡相图
双组分理想溶液的汽液平衡关系用相图表示比较直观、 清晰,而且影响蒸馏的因素可在相图上直接反映出来。蒸馏 中常用的相图为恒压下的温度-组成( t-x-y )图和气相-液 相组成( x-y )图。
当生产任务要求将一定数量和组成的原料分离成指定组成 的产品时,精馏塔计算的内容有:出液和塔釜残液的流量、塔 板数、进料口位置、塔高、塔径等。
6.4.1 全塔物料衡算
1.全塔物料衡算
单位时间为基准
总物料衡算: qn,F=qn,D+qn,W 易挥发组分物料衡算:
qn,FxF=qn,DxD+qn,WxW qn,F、qn,D、qn,W——流量,kmol/h
二、蒸馏的分类
1、按蒸馏方法:简单蒸馏、平衡蒸馏(闪蒸)、精馏、特殊精馏。 2、按操作压力:常压;减压;加压。 3、按原料液组分数:双组分蒸馏和多组分蒸馏 4、按操作方式:间歇蒸馏和连续蒸馏。
三、蒸馏操作的特点
优点:* 适用面广,液体混合物和气体混合物均可 * 操作流程较简单,无需其他外加介质
缺点:* 能耗大
一、利用饱和蒸气压计算气液平衡关系
法国物理学家拉乌尔在1887年研究含有非挥发性溶质的 稀溶液的行为时发现的,可表述为:“在某一温度下,稀溶 液的蒸气压等于纯溶剂的蒸气压乘以溶剂的摩尔分数”。
PA PA0 xA ——拉乌尔定律
pA0——纯组分A在溶液温度下的饱和蒸气压,Pa; xA——溶液中组分A的摩尔分数;
第六章 精馏

6.4.1 计算的前提
为了计算简化,假设进料中各组分的摩尔气化热
相等,同时定如下:
引入塔中的进料预热至泡点,温度与进料板温度接近; 塔身绝热,没有热损失 各层塔板上气化和冷凝的物质的量相等 回流采用全凝操作,回流组成与产品组成相同; 精馏段各层的回流量都相等; 提馏段各层的回流量都相等; 提馏段回流量等于精馏段回流量与进液量之和。
求全回流下的最小理论塔板数 求出最小回流比,确定实际回流比 由以上两结果求得理论板数
全回流下的最小理论板数:
相对挥发度定义式6-3: yA/yB=αxA/xB 对第1块板:yA1/yB1=α yA2/ /xB1 对第2块板:yA2/yB2=αxA2/xB2 同时,全回流操作相当于操作线为对角线y=x, 则yA2=xA1;yB2=xB1 故, yA1/yB1=α2xA2/xB2 类推得到 yA1/yB1=αNxAN/xBN
6-2.1 平衡蒸馏的计算
过程描述:
将原料加热到超过进料的泡点,当此 气液混合相进入闪蒸塔的瞬间,蒸汽 和残液处于平衡。从而达到分离目的。
特点:
在较低温度下得到较高的馏出率 多用在高温易分解的物质的蒸馏
气化率和液化率
f=V/F q=W/F=1-f 平衡蒸馏的计算 xD=(f-1)xw/f+xf/f 或 xD=qxw/(q-1)-xf/(q-1)
图解求算的原理
第1块板上:y1和x1满足平衡方程, 即点( y1,x1)在平衡线上; 第2块板上升的蒸气y2与第一块板 下降的回流液满足操作线方程, 即点( y2,x2)在操作线上。 则从y1 到y2需要一块理论板。 依此类推。
精馏1传质过程概述1传质过程的定义传质过程的定义
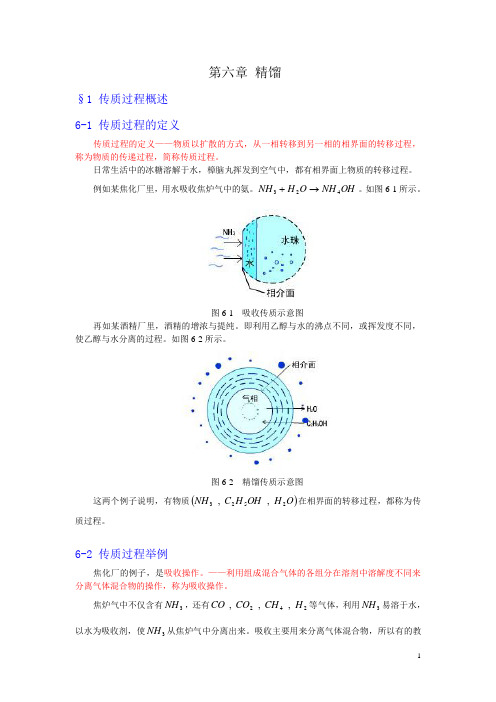
第六章 精馏§1 传质过程概述 6-1 传质过程的定义传质过程的定义——物质以扩散的方式,从一相转移到另一相的相界面的转移过程,称为物质的传递过程,简称传质过程。
日常生活中的冰糖溶解于水,樟脑丸挥发到空气中,都有相界面上物质的转移过程。
例如某焦化厂里,用水吸收焦炉气中的氨。
OH NH O H NH 423→+。
如图6-1所示。
图6-1 吸收传质示意图再如某酒精厂里,酒精的增浓与提纯。
即利用乙醇与水的沸点不同,或挥发度不同,使乙醇与水分离的过程。
如图6-2所示。
图6-2 精馏传质示意图这两个例子说明,有物质()O H OH H C NH 2523 , , 在相界面的转移过程,都称为传质过程。
6-2 传质过程举例焦化厂的例子,是吸收操作。
——利用组成混合气体的各组分在溶剂中溶解度不同来分离气体混合物的操作,称为吸收操作。
焦炉气中不仅含有3NH ,还有242 , , , H CH CO CO 等气体,利用3NH 易溶于水,以水为吸收剂,使3NH 从焦炉气中分离出来。
吸收主要用来分离气体混合物,所以有的教材称吸收为气体吸收。
如图6-3所示。
图6-3 吸收局部示意图水称为溶剂,3NH 称为溶质,炉气中其他气体称为惰性组分。
用水吸收氯化氢气体)(HCl ,制备盐酸,也是一种吸收操作。
酒精厂的例子,是精馏操作。
——利用液体混合物各组分沸点(或挥发度)的不同,将物质多次部分汽化与部分冷凝,从而使液体混合物分离与提纯的过程,称为精馏操作。
精馏主要用来分离液体混合物,所以有的教材称精馏为液体精馏。
传质过程还有,萃取——利用混合物各组分对某溶剂具有不同的溶解度,从而使混合物各组分得到分离与提纯的操作过程。
例如用醋酸乙酯萃取醋酸水溶液中的醋酸。
如图6-4所示。
图6-4 萃取示意图此例中醋酸乙酯称为萃取剂)(S ,醋酸称为溶质)(A ,水称为稀释剂)(B 。
萃取操作能够进行的必要条件是:溶质在萃取剂中有较大的溶解度,萃取剂与稀释剂要有密度差。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
全回流和芬斯克方程
• 全回流——当xd→0时,则R→∞,此时 称为全回流。这时精馏段与提馏段操作 线方程均与对角线(y=x)重合,此时理 论板数最少(Nm)。
• 全回流时,最少理论板数的计算式
芬斯克公式推导
• 全回流时,qn,D=O, R=qn,L/qn, D=∞,最少理论板数的计算式
• 最小回流比
xd R1
即连 的直线 b0,Rxd1与axd,xd
➢ ③作进料线,y x xF
1 1
过 exF,xF点,作 1的 斜直 率 A于 线 C d 为交 ➢ ④作提馏段操作线
y2 / q n ,L q n ,L q n ,F q n ,F q n ,W x 1 / q n ,L q q n n ,W ,F q n ,W x W
即连 cxW,xW与 d 所得直线即是。
➢ ⑤从a点开始,在平衡线与操作线之间作直角梯 级,直到超过O点。有多少直角梯级,就有多少 块理论板数。跨越d点的阶梯为加料板。
4-2 回流比的影响及选择
• 稳定回流是维持定常连续精馏过程的必要条件,应用回 流与上升蒸汽是精馏过程的基本条件。所以,回流比的 大小是影响精馏操作最重要的因素。
• 对于组成一定的料液和分离要求,增加回流比,精馏段 操作线的斜率R/R+1增大,精馏段和提馏段操作线均向对 交线方向移动,它们与平衡线之间的距离增大,表示塔 内气、液两相离开平衡状态的距离增大,两相间的推动 力增加。结果,分离所需要的理论塔板数减少。
• 显然,R越大,所需理论塔板数越少。当R增到 无穷大时,其实质上是馏出液量为零,即上升 蒸汽在冷凝器中冷凝后全部回流,故称为全回 流,这是增大回流比的极限。因此,此时分离 所需的理论塔板数为最小理论塔板数。
• 最小回流比——当R减小时,R/(R+1)↓, 当R减至两操作线交点逼近平衡线时, 此时N→∞,此时R称为最小回流比Rmin。
• 适宜回流比的确定
• (1)回流比R对理论板数的影响。如图 所示。
R,xD ,操作线靠近平衡N线, R1
反之,R,xD ,操作线远离平衡N线, R1
即 N正比于1 R
➢ 由此可以求出理论塔板数。 ➢ 这种方法计算的结果较准确。
4-2 图解法
通常采用直角梯级图解法。其实质仍然是
以平衡关系与操作关系为依据,将两者绘在x-y
图上,便可图解得出达到指定分离任务所需的
理论塔板数及加料板位置。
图解步骤如下:
➢ ①作平衡线(x-y)与对角线
➢
②作精馏段操作的影响
qn,V qn,L qn,D R 1 qn,D
R , qn,V , 塔 直径 ,冷凝 器,蒸 馏釜 设备费
R , N , 塔高下降,设备费 R , qn,V , 冷 却水量 ,加热蒸 汽量,
操作费
• 1线为“设备费~R”的关系式 • 2线为“操作费~R”的关系式 • 3线为“总费用~R”的关系式。 • 取总费用为最少的3线中的低点,一般取
五种进料对δ线的影响
进料状况 A,冷凝体
δ值 斜率δ/(δ-1) 进料线位 置
>1
+
B,泡点液
=1
∞
体
C,汽-液混 0~1
-
合物
D,露点蒸
=0
0
汽
E,过热蒸
<0
+
汽
4-5简捷法求理论塔板数
➢吉利兰图法求理论板数 ➢1.由作图法或解析法求出Rmin,并确
定适宜的回流比R。 ➢2.由芬斯克方程求出Nmin。
提馏塔段的计算公式
y2 / q n ,L q n ,L q n ,F q n ,F q n ,W x 1 / q n ,L q q n n ,W ,F q n ,W x W
➢ 由提馏段第二层塔板下降的液体组成x’2与y’2符 合相平衡关系,由相平衡方程可以解出x’2,依 此类推,当x’m≤xw为止。提馏段的理论塔板数 为m-1,而精馏塔所有的塔板数为(m+n-1)
逐板计算法:
• 逐板计算法是利用进料的气液相平衡关系和操 作线方程去计算每一块理论塔板的气液相浓度。
• 其依据是:进入每块塔板的气液相在塔板上充 分接触,最大限度地实现热量、质量传递,由 不平衡达到平衡。
从塔最上层上升的蒸汽y1,在塔顶冷凝器 中被全部冷凝后,得到的塔顶馏出液组成、塔
顶回流液的组成xd与第一层塔板上升的蒸汽组 成y1相同,即y1=xd。
➢ 因是理论塔板,由塔顶第一板下降的回流液组成x1 与该板上升蒸汽的组成y1符合气、液平衡方程。
y1
x1 1(1)x1
➢ 第二层塔板的组成符合精馏段操作方程
y2 RR1x1Rx d1
依此类推,算到第n板的液相组成xn与加料板的组成 xf近似为止,即xn≤xf, 表明第n层为加料板;可做 为提馏板的第一层,故精馏段的理论板数为n-1, 以后再逐级向下计算。
➢3.计算(R-Rmin)/(R+1),在吉利兰图上查出 对应的(N-Nmin)/(N+1),然后算出理论板 数N。
➢ 【例3-4】某二元理想混合液其平均相对挥 发度为 m 1.3。若进料组成 xF 0.5
➢ ,要求馏出液组成为 xD 0.9
➢ ,釜液组成 xW 0.1 ,泡点进料,回流比 R取为8.0。试求所需理论板数。
§4 理论塔板数的计算
在精馏塔设计中引入理论塔板的概念,是为了 简化计算。通常是先求出理论板数,然后根据塔板 效率予以修正,求出实际的塔板数。
对于填料塔,用相当于一块理论塔板分离效率 的填料层高度代表塔板,称为填料的等板高度,只 要求出理论板数即可以求出填料塔的填料层高度。
4-1 逐板计算法
• 假设离开该板(第n块板)的上升蒸汽Yn组成 和板上(第n块板)下流液体Xn组成互成平衡, 该板称之为理论板。
最小回流比的1.1-2倍。即R=(1.1-2) Rmin
4-4进料热状况的影响
• 精馏原料的进料状态有以下5种: • (1)温度低于泡点的冷液体,δ>1; • (2)处于泡点的液体,δ=1; • (3)温度介于泡点与露点之间的气液混合
物,0<δ<1; • (4)温度处于露点的饱和蒸汽,δ=0; • (5)温度高于露点的过热蒸汽,δ<0. • 表现在图上是提馏线向左移动.
• 【例3-5】欲用一连续精馏塔分离含苯为 44%(摩尔分数)的苯-甲苯二元混合物 液,现用泡点进料,操作回流比R=3,相 对挥发度a=2.41,要求塔顶产品含苯 xD=95.5%,塔底残液含苯xw=5.85%.试用 逐板计算法、图解法和简捷算法求取该
