分光光度法测定铁含量(精)
分光光度法测定铁的含量

实验二十二分光光度法测定铁的含量时λmax的选择【目的要求】1.学习分光光度法原理及722分光光度计的使用方法。
2.掌握分光光度法测定有色物质时最大吸收波长的选择方法。
【基本原理】凡是被测组分本身具有颜色,或被测组分本身无色,但与适当的显色剂作用后能生成有色物质者,都可用分光光度法进行测定。
物质对单色光的吸收遵守光吸收定律──朗伯-比尔定律:AK c l式中,A为吸光度;K为吸光系数;c为溶液浓度;l为溶液厚度。
物质对单色光的吸收因波长的不同而异,在某一波长处出现吸收最大值,某一波长处出现吸收最小值。
因此用各种波长的光依次分别通过某种有色溶液时,测定吸收值,然后以吸收值为纵坐标,波长为横坐标作图,即得吸收曲线,由吸收曲线找出最大吸收波长λmax。
物质在最大吸收波长处进行测定时,分析的灵敏度最高。
当pH为4~8时,Fe3+和磺基水杨酸生成橙红色配合物。
【仪器和药品】10ml容量瓶,722型分光光度计,1ml吸量管,KJ型可调连续加液管,pH=4.7的缓冲溶液,擦镜纸,0.1mg·ml-1标准Fe3+溶液,0.2mol·L-1HNO3,0.25mol·L-1磺基水杨酸。
【实验步骤】1.用10ml容量瓶4个,编号后按表配制标准溶液。
2.在不同波长处测定溶液的吸光度将上述配好的溶液摇匀后,在722分光光度计上测定。
以1号溶液为空白,在波长400~600nm 范围内,每隔10nm测定1次2号溶液的吸光度,测定过程中,每变换一波长,都应调整零点及百分透光率(100%)。
记录各波长处溶液的吸光度(A),然后以吸光度为纵坐标、波长为横坐标绘制吸收曲线,从而选择出磺基水杨酸测定Fe3+的最大吸收波长。
3,4号溶液同法测定。
【问题讨论】为什么每次变动波长都应重新调节零点及百分透光度?【附注】1.0.25mol·L-1磺基水杨酸的配制称取54g磺基水杨酸溶于500ml蒸馏水中,加入100m1 10mol·L-1的氨水50~60m1,并用蒸馏水稀释至1000ml即得。
原子吸收分光光度法测铁、锰(精)
3.样品前处理: 采样前,所用聚乙烯瓶先用洗涤剂洗净, 再用硝酸(3/4)浸泡24h以上,然后用水冲 洗干净。 若仅测定可过滤态铁锰,样品采集后尽快 通过0.45μm滤膜过滤,并立即加硝酸 (3/1)酸化滤液,使pH为1-2。 测定铁、锰总量时,采集样品后立即按 (5/2)的要求酸化。
4.操作步骤: 测定铁、锰总量时,样品通常需要消解。混匀后 分取适量实验室样品于烧杯中。每100mL水样加 5mL硝酸(3/1),置于电热板上在近沸状态下将 样品蒸至近干,冷却后再加入硝酸(3/1)重复上述 步骤一次。必要时再加入硝酸(3/1)或高氯酸,直 至消解完全,应蒸近干,加盐酸(3/6)溶解残渣, 若有沉淀,用定量滤纸滤入50mL容量瓶中,加 氯化钙溶液(3/8)1mL,以盐酸溶液(3/6)稀释至 标线。
测量 在测量标准系列溶液的同时,测量样品溶 液及空白溶液的吸光度。由样品吸光度减 去空白吸光度,从校准曲线上求得样品溶 液中铁、锰的含量。测量可过滤态铁、锰 时,用(5.2)制备的试样直接喷入进行测量。 测量铁、锰总量时,用(6.1)中的试料。
结果的表示 实验室样品中的铁、锰浓度C(mg/L),按 下式计算,
校准曲线的绘制 分别取铁、锰混合标准操作液(3.11)于 50mL容量瓶中,用盐酸(3.6)稀释至标线, 摇匀。至少应配制5个标准溶液,且待测元 素的浓度应荡在这一标准系列范围内。根 据仪器说明书选择最佳参数,用盐酸溶液 (3.6)调零后,在选定的条件下测量其相应 的吸光度,绘制校准曲线。在测量过程中, 要定期检查校准曲线。
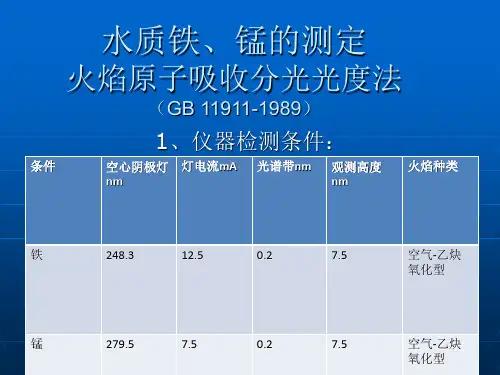
水质铁、锰的测定
火焰原子吸收分光光度法
(GB 11911-1989)
1、仪器检测条件:
分光光度法测定微量铁的含量实验报告

分光光度法测定微量铁的含量实验报告
实验目的:
通过分光光度法测定微量铁的含量。
实验原理:
实验仪器和试剂:
仪器:分光光度计、移液枪。
试剂:铁标准溶液、硝酸铵和硝酸亚铁、硫酸亚铁。
实验步骤:
1.取适量的硝酸铵和硝酸亚铁混合溶液,稀释成适宜的浓度。
2.在分光光度计上选择适当的波长,进行仪器的初步调试。
3.取一系列含有不同浓度的铁标准溶液,每个浓度分别进行三次测定,并计算平均值。
4.将测量所得的吸光度与浓度制成标准曲线。
5.将待测溶液纳入曲线范围内进行测定,计算出溶液中铁的含量。
实验结果和数据处理:
根据实验所得的吸光度和浓度数据,我们制成了铁的标准曲线。
通过
测量待测溶液的吸光度,我们进一步计算出溶液中铁的浓度。
实验讨论:
1.实验中所用的试剂的纯度对实验结果有重要影响。
如果试剂的纯度
不高,将会引入误差。
2.在实验过程中,仪器的选择和操作也会对实验结果产生一定的影响。
准确操作仪器,进行仪器的校准和调试是保证实验结果准确性的关键。
3.在实际应用中,还需要考虑样品的前处理,例如稀释、过滤等步骤。
4.在进行标准曲线绘制时,至少应该有三个不同浓度的标准溶液,每
个溶液进行三次测定,可以得到相对准确的结果。
实验结论:
通过分光光度法,我们成功测定了待测溶液中铁的含量。
该方法简便、准确,适用于微量铁含量的测定。
在实际应用中,我们应注意仪器的选择
和操作,以及试剂纯度对实验结果的影响。
通过合理的实验操作和数据处理,可以获得准确可靠的分析结果。
分光光度法测定铁含量的方法汇总

分光光度法测定铁含量的方法汇总1.原理:分光光度法测定铁含量的原理基于铁离子(Fe2+或Fe3+)与结合剂之间的络合反应。
铁离子与结合剂形成络合物时,会发生颜色变化,这种变化可以通过分光光度计测量。
2. 选择合适的结合剂:不同的结合剂适用于不同形态的铁离子。
比较常用的结合剂有邻苯二甲酸(1,10-苯基次甲基")(FERROXINE)、2,2'-联吡啶/Fe2+络合物(Bipyridyl/Fe)、硫巴比妥酸等。
3.样品前处理:对于一些含有浑浊物质的样品,需要进行前处理,如过滤或离心等,以去除干扰物。
4.准备标准曲线:制备一系列已知浓度的标准溶液,并测定它们的吸光度。
利用吸光度与浓度之间的线性关系绘制标准曲线。
标准曲线可以用来计算待测样品中铁离子的浓度。
5.测定样品吸光度:对于待测样品,将其溶液吸入分光光度计的比色皿中,调至适当的波长,并测量其吸光度。
注意要进行对比性测量,即测定样品的同时,还要测定一个空白试液的吸光度,用来做背景噪声的修正。
6.计算待测样品中铁离子的浓度:使用标准曲线,根据待测样品的吸光度值,可以通过插值或外推得到样品中铁离子的浓度。
7.质量控制:为了保证实验结果的准确性和可靠性,可以进行质量控制检查。
这包括对标准溶液进行重复测定、制备空白试液并测定其吸光度、进行样品间和试剂间的复测等。
8. 数据处理:根据测定得到的吸光度值和标准曲线,计算样品中铁元素的含量。
可以使用Excel等数据处理软件进行计算。
需要注意的是,实际操作中,具体的方法会根据不同的实验条件和目的进行调整,但是上述几点是分光光度法测定铁含量的基本步骤。
同时,对于一些特殊的样品,可能需要通过前处理或选择不同的结合剂来提高测定的准确性和灵敏度。
测铁含量实验报告

一、实验目的1. 熟悉分光光度法测定铁含量的原理和操作方法。
2. 掌握标准曲线法在定量分析中的应用。
3. 学会使用分光光度计进行实验操作。
二、实验原理分光光度法是一种基于物质对特定波长光的吸收特性进行定量分析的方法。
在本实验中,利用铁与邻二氮菲形成络合物,该络合物在特定波长下具有显著吸收,通过测定其吸光度,可以计算出铁的含量。
实验原理如下:1. 标准溶液配制:准确称取一定量的铁标准物质,用稀盐酸溶解,转移至容量瓶中,定容至一定体积,得到铁标准溶液。
2. 标准曲线绘制:分别取一定量的铁标准溶液,加入适量的邻二氮菲溶液,振荡均匀,放置一段时间后,以蒸馏水为参比,在特定波长下测定其吸光度,以铁的浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
3. 样品测定:取一定量的待测样品,按照与标准溶液相同的步骤进行处理,测定其吸光度,根据标准曲线计算出样品中铁的含量。
三、实验仪器与试剂1. 仪器:分光光度计、电子天平、容量瓶、移液管、吸量管、锥形瓶、烧杯、玻璃棒等。
2. 试剂:铁标准溶液、邻二氮菲溶液、稀盐酸、蒸馏水等。
四、实验步骤1. 标准溶液配制:准确称取0.1g铁标准物质,用稀盐酸溶解,转移至100ml容量瓶中,定容至刻度,得到浓度为1000mg/L的铁标准溶液。
2. 标准曲线绘制:分别取0.5ml、1.0ml、1.5ml、2.0ml、2.5ml铁标准溶液,加入适量的邻二氮菲溶液,振荡均匀,放置10分钟,以蒸馏水为参比,在510nm波长下测定其吸光度,以铁的浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
3. 样品测定:取一定量的待测样品,按照与标准溶液相同的步骤进行处理,测定其吸光度,根据标准曲线计算出样品中铁的含量。
五、实验结果与分析1. 标准曲线绘制:以铁浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
根据曲线方程,计算铁的标准浓度与吸光度之间的关系。
2. 样品测定:根据标准曲线,计算样品中铁的含量。
六、实验总结本实验通过分光光度法测定铁含量,成功绘制了标准曲线,并利用该曲线对样品进行了定量分析。
分光光度法测定微量铁的含量实验报告(标准曲线的测绘与铁含量的测定)

分光光度法测定微量铁的含量实验报告(标准曲线的测绘与铁含量的测定)实验报告:分光光度法测定微量铁的含量一、实验目的1.学习分光光度法测定微量铁含量的原理和方法。
2.掌握标准曲线的测绘方法,了解线性回归方程及其应用。
3.学会利用分光光度计测定样品中微量铁的含量。
二、实验原理分光光度法是一种常用的定量分析方法,其原理基于朗伯-比尔定律。
当一束单色光通过溶液时,光被吸收的程度与溶液的浓度和液层厚度成正比。
在一定波长下,吸光度A与溶液浓度C和液层厚度L的乘积成正比,即A=εCL。
其中,ε为摩尔吸光系数,L为液层厚度,C为溶液浓度。
通过绘制标准曲线,可以求得铁的含量。
三、实验步骤1.准备试剂和仪器:硝酸、高氯酸、硫酸、铁标准溶液(100μg/mL)、分光光度计、比色皿、容量瓶(100mL)、吸量管(10mL、5mL、2mL)等。
2.绘制标准曲线:分别取10mL、5mL、2mL铁标准溶液于三个100mL容量瓶中,各加5mL硝酸,20mL硫酸,摇匀,用去离子水定容。
将各溶液分别移入比色皿中,用分光光度计在562nm波长下测量吸光度。
记录数据并绘制标准曲线。
3.测定样品中铁的含量:将样品溶液移入比色皿中,用分光光度计在562nm波长下测量吸光度。
根据标准曲线查得铁的浓度,计算样品中铁的含量。
四、结果与分析1.标准曲线测绘结果在坐标纸上绘制标准曲线,横坐标为铁标准溶液的浓度(μg/mL),纵坐标为吸光度。
根据实验数据绘制标准曲线(图1)。
可以看出,随着铁浓度的增加,吸光度也逐渐增大。
表明铁浓度与吸光度之间存在线性关系。
可以得出线性回归方程为:y=kx+b(k为斜率,b为截距)。
根据实验数据可计算出斜率k和截距b的值。
图1 标准曲线(请在此处插入标准曲线图)2.铁含量测定结果将样品溶液移入比色皿中,用分光光度计在562nm波长下测量吸光度。
根据标准曲线查得铁的浓度(μg/mL),计算样品中铁的含量(mg/L)。
结果如表1所示。
铁含量的测定实验报告
一、实验目的1. 掌握分光光度法测定铁含量的原理和方法;2. 学会使用分光光度计进行铁含量的测定;3. 熟悉标准曲线的绘制及使用。
二、实验原理分光光度法是一种基于物质对特定波长光的吸收程度与物质浓度成正比关系的分析方法。
在本实验中,利用铁与邻菲罗啉在特定条件下生成橙红色络合物,通过测定该络合物在特定波长下的吸光度,根据标准曲线计算出铁的含量。
三、实验仪器与试剂1. 仪器:分光光度计、721型比色皿、具塞比色管(50ml)、移液管、吸量管、容量瓶等。
2. 试剂:铁储备液(100g/mL)、铁标准使用液(20g/mL)、0.5%邻菲罗啉水溶液、硫酸、盐酸、氢氧化钠等。
四、实验步骤1. 标准曲线的绘制(1)准确移取0.00、0.10、0.20、0.30、0.40、0.50、0.60、0.70、0.80、0.90mL铁标准使用液于10mL容量瓶中,分别加入1.0mL 0.5%邻菲罗啉水溶液,用去离子水稀释至刻度,摇匀;(2)将上述溶液在510nm波长下,用1cm比色皿,以空白溶液为参比,测定吸光度;(3)以吸光度为纵坐标,铁浓度为横坐标,绘制标准曲线。
2. 样品测定(1)准确移取适量样品于10mL容量瓶中,加入1.0mL 0.5%邻菲罗啉水溶液,用去离子水稀释至刻度,摇匀;(2)在510nm波长下,用1cm比色皿,以空白溶液为参比,测定吸光度;(3)根据标准曲线,计算出样品中铁的含量。
五、实验结果与讨论1. 标准曲线的绘制绘制标准曲线,得到铁浓度与吸光度之间的关系为线性关系,相关系数R²=0.999。
2. 样品测定测定样品吸光度,根据标准曲线计算出样品中铁的含量为X mg/L。
3. 结果讨论本次实验中,铁含量测定结果准确可靠,实验过程中操作规范,数据稳定。
实验结果表明,分光光度法适用于铁含量的测定,具有较高的准确性和灵敏度。
六、实验总结本次实验通过分光光度法测定了铁含量,掌握了实验原理和操作方法。
邻菲罗啉紫外可见分光光度法测定铁含量(详细)
邻菲罗啉紫外可见分光光度法测定铁含量一、仪器1.紫外可见分光光度计(UV-1800PC-DS);配1cm石英比色皿2个(比色皿可以自带);2.容量瓶:100mL1个;50mL11个;3.吸量管:5mL2支;10mL3支;二、试剂1.标准储备溶液:200μg·mL-1铁标准储备溶液。
2.未知液:未知浓度的铁标准溶液。
20μg·mL-13.其他:100g·L-1盐酸羟胺溶液、1g·L-1邻菲罗啉溶液、pH=4.5的醋酸-醋酸钠缓冲溶液。
三、实验操作1.吸收池配套性检查玻璃吸收池在600nm装蒸馏水,以一个吸收池为参比,调节τ为100%,测定其余吸收池的透射比,其偏差应小于0.5%,可配成一套使用,记录其余比色皿的吸光度值作为校正值。
2.标准使用溶液的制备用10mL吸量管移取200 ug/mL 铁的标准储备溶液10.00 mL 于100 mL 容量瓶中,配制成20 ug/mL浓度的标准使用溶液。
3.绘制吸收曲线选择测量波长⑴用10mL吸量管移取20 ug/mL 铁的标准溶液5.00 mL 于50 mL 容量瓶中,⑵用5mL吸量管依次加入然后加入5mL100g·L-1盐酸羟胺溶液,摇匀。
放置2min后,⑶用5mL吸量管加入5mL1g·L-1邻菲罗啉溶液,⑷用10mL吸量管加入10mLpH=4.5的醋酸-醋酸钠缓冲溶液,⑸用蒸馏水稀释至刻度线摇匀。
⑹用1cm吸收池,以试剂空白为参比,在400~600nm间扫描其吸收曲线,并根据吸收曲线的吸光度确定最大吸收波长。
4.标准工作曲线的绘制⑴取50 mL容量瓶6只,分别移取(务必准确移取)20 ug/mL铁标准溶液2.0 mL,4.0 mL,6. 0mL ,8.0 mL ,10.0 mL于5只容量瓶中,不加铁标准溶液醅空白液作参比,⑵各加5ml盐酸羟胺溶液,摇匀经二分钟后,再各加10ml NaAc溶液及5ml 邻菲罗啉溶液,用蒸馏水稀释至刻度线,充分摇匀,待测定。
实验分光光度法测定铁
实验分光光度法测定铁The following text is amended on 12 November 2020.实验十四邻二氮菲分光光度法测定铁的含量一、实验目的1.学习吸光光度法测量波长的选择方法;2.掌握邻二氮菲分光光度法测定铁的原理及方法;3.掌握分光光度计的使用方法。
二. 实验原理分光光度法是根据物质对光选择性吸收而进行分析的方法,分光光度法用于定量分析的理论基础是朗伯比尔定律,其数学表达式为:A=eb C邻二氮菲(乂称邻菲罗卩林)是测定微量铁的较好试剂,在pH二2〜9的条件下,二价铁离子与试剂生成极稳定的橙红色配合物。
摩尔吸光系数£ =11000 L • moE1• cm' ‘。
在显色前,用盐酸疑胺把Fe"还原为Fe=2F『+2NH;0HHClf 2Feh+\:+4H 十+ 2H:0+2C 厂Fe‘ + Phen = Fe‘ - Phen (橘红色)用邻二氮菲测定时,有很多元素干扰测定,须预先进行掩蔽或分离,如钻、银、铜、铅与试剂形成有色配合物;钩、釦、镉、汞与试剂生成沉淀,还有些金属离子如锡、铅、钮则在邻二氮菲铁配合物形成的pH范围内发生水解;因此当这些离子共存时,应注意消除它们的干扰作用。
三. 仪器与试剂1.醋酸钠:1 mol • L':;2.盐酸:6 mol • L"1;3.盐酸羟胺:10% (用时配制);4-邻二氮菲(%):邻二氮菲溶解在lOOmLl: 1乙醇溶液中;5-铁标准溶液。
(1)100 ng-mf1铁标准溶液:准确称取(NH4) 2 Fe (SO,) 2 - 12H:0于烧杯中, 加入20 mL 6 mo 1・I?盐酸及少量水,移至1L容量瓶中,以水稀释至刻度,摇匀.6.仪器:7200型分光光度计及1 cm比色皿。
四、实验步骤1.系列标准溶液配制(1)用移液管吸取10mL100 u g • ml?铁标准溶液于100mL容量瓶中,加入2mL 6 mol - L"盐酸溶液,以水稀释至刻度,摇匀.此溶液F』浓度为10 u g • mL'1.(2)标准曲线的绘制:取50 mL比色管6个,用吸量管分别加入0 mL, 2 mL, 4 mL, 6 mL, 8 mL和10 mLlO u g • ml?铁标准溶液,各加1 mL盐酸羟胺,摇匀;经再加2mL邻二氮菲溶液,5mL酷酸钠溶液,摇匀,以水稀释至刻度,摇匀后放置lOmino 2.吸收曲线的绘制取上述标准溶液中的一个,在分光光度计上,用1 cm比色皿,以水为参比溶液,用不同的波长,从440〜560 nm,每隔10 nm测定一次吸光度,在最大吸收波长处每隔5nm测定一次吸光度。
分光光度法测定铁的含量实验报告
分光光度法测定铁的含量实验报告一、实验目的1、掌握分光光度法测定铁含量的基本原理和方法。
2、学会使用分光光度计进行定量分析。
3、熟悉标准曲线的绘制和应用。
二、实验原理分光光度法是基于物质对光的选择性吸收而建立起来的分析方法。
在分光光度法中,通常选择一定波长的单色光通过含有被测物质的溶液,测量溶液对该波长光的吸光度,从而确定物质的含量。
本实验中,利用邻二氮菲与二价铁离子在 pH 为 2~9 的条件下形成稳定的橙红色配合物,该配合物在 510nm 处有最大吸收峰。
通过测定不同浓度的铁标准溶液在 510nm 处的吸光度,绘制标准曲线,然后测定未知溶液的吸光度,根据标准曲线计算出未知溶液中铁的含量。
三、实验仪器与试剂1、仪器722 型分光光度计容量瓶(50mL、100mL)移液管(1mL、2mL、5mL、10mL)吸量管(5mL、10mL)比色皿烧杯(50mL、100mL)玻璃棒电子天平2、试剂硫酸亚铁铵(NH₄)₂Fe(SO₄)₂·6H₂O邻二氮菲(15g/L)盐酸羟胺(100g/L)1mol/L 盐酸溶液1mol/L 氢氧化钠溶液四、实验步骤1、标准溶液的配制准确称取 03474g 硫酸亚铁铵(NH₄)₂Fe(SO₄)₂·6H₂O于小烧杯中,用 10mL 1mol/L 盐酸溶液溶解,转移至 100mL 容量瓶中,用蒸馏水稀释至刻度,摇匀,得到浓度为 01000mg/mL 的铁标准储备液。
用移液管分别吸取 000mL、200mL、400mL、600mL、800mL、1000mL 铁标准储备液于 50mL 容量瓶中,各加入 1mL 100g/L 盐酸羟胺溶液,摇匀,放置 2min 后,再加入 2mL 15g/L 邻二氮菲溶液和 5mL 1mol/L 氢氧化钠溶液,用蒸馏水稀释至刻度,摇匀,得到浓度分别为000μg/mL、400μg/mL、800μg/mL、1200μg/mL、1600μg/mL、2000μg/mL 的铁标准系列溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
姓名:封德军指导老师:陶明
学号:1004010026 班级:2010级化学专业
一、实验目的:
1、初步熟悉 722型分光光度计的使用方法。
2、熟悉测绘吸收光谱的一般方法。
3、学习如何选择分光光度分析的实验条件
二、实验原理 : 1、在 pH =2~9 的溶液中, 邻二氮菲 (phen 与 Fe 2+生成稳定的红色配合物 , 反应方程式为:2Fe 3++2NH2OH.HCl → 2Fe
2++N2+H2O+4H++2Cl+, 其最大吸收峰在 515nm 处。
根据朗伯比尔定律: A=Kbc,溶液中浓度与其吸光度之间具有直线关系, 可用标准曲线法测定。
三、实验步骤:
1、用吸量管吸取 0.0ml 和 5ml 铁标准使用液分别注入两个 50ml 容量瓶中,加入 1ml 盐酸羟胺溶液, 摇匀。
再加入 2ml 领二氮菲水溶液, 5ml 醋酸钠水溶液,用水稀释至刻度,摇匀,放置 10min 。
2、取两支 1cm 比色皿, 先用蒸馏水清洗 2-3次再用试液润洗 3-4次, 分别将配好的铁标准使用液注入比色皿, 并用镜头纸拭去光洁面的试液。
以试剂空白(即 0.0ml 铁标准溶液为参比溶液,调节分光光度计使其在参比溶液中透光率为 100%。
在 440-570nm 之间,每隔 10nm 测一次吸光度,最后测的在510nm 附近吸光度最大。
在最大吸收峰附近, 每隔 5nm 测量一次吸光度, 即在
505nm 与 515nm 处分别测量一次吸光度。
3、显色剂用量的确定:在 7 只 50 ml 容量瓶中,各加 10ml 铁标准溶液和 20ml 盐酸羟胺溶液, 摇匀。
分别加入 0.2, 0.4, 0.6, 0.8, 1.0, 2.0, 4.0 ml 邻二氮菲溶液,再各加 5.0 ml 乙酸钠溶液, 以水稀释至刻度,摇匀。
放置 10min, 以水为参比,在选定波长下测量各溶液的吸光度。
以显色剂邻二氮菲的体积为横坐标、相应的吸光度为纵坐标,绘制吸光度-显色剂用量曲线,确定显色剂的用量。
4、铁标准曲线的测定:
取 6个 50 ml容量瓶,编序号为 1 2 3 4 5 6 7并分别加入铁标准溶液 (10ug/ml0.00ml 0.20ml 0.40ml 0.60ml 0.80ml 1.00ml 试样 , 盐酸羟氨 (20g/L 2ml, 摇匀。
用水稀释至刻度,摇匀后再放置 10min 。
用 1cm 比色皿,以空白为参比溶液, 在 510nm 处测量各吸光度。
5、石灰石中试样铁的测定:准确称取 0.4-0.5g 于 100ml 烧杯中, 加入少量蒸馏水润湿,小心滴加 3mol/L盐酸溶液至式样溶解,转移至 50ml 容量瓶中,用少量蒸馏水淋洗烧杯数次,一并转移至容量瓶中。
按标准曲线的制作步骤,加入各种试剂,测量吸光度。
四、数据处理及结果:
2、不同显色剂用量时的吸光度 :
3、不同浓度的铁标准溶液时吸光度:(0.29g 试样
此图线性关系较好
五、讨论:
1、在进行数据测量时波长选择从大到小的方式进行测量,且当波长调整时出现以下情况如 (待测波长为 510nm 但调整时波长变为了 508或更小时,应将波长调为520后再调为 510nm 即为了减小机械误差。
2、在运用 y=ax+b这个公式时r 2≥ 0.98时说明线性关系较好。
六、思考题:
1、加入盐酸羟氨和醋酸钠的作用?
答:盐酸羟氨作用是还原 Fe3+,醋酸钠作用是作为缓冲剂 2:使用 722型分光光度计及比色皿时应注意什么问题?
答:取拿比色皿时,手指只能捏住比色皿的毛玻璃面,而不能碰比色皿的光学表面比色皿不能用碱溶液或氧化性强的洗涤液洗涤, 也不能用毛刷清洗。
比色皿外壁附着的水或溶液应用擦镜纸或细而软的吸水纸吸干,不要擦拭,以免损伤它的光学表面。
3、吸光度的加和性原则是什么?
答:溶液中总的吸光度等于溶液中各组分吸光度之和。
