高三一轮复习专题一认识有机化合物教案

1. 有机化合物的分类及结构特点
1.1 有机化合物的分类
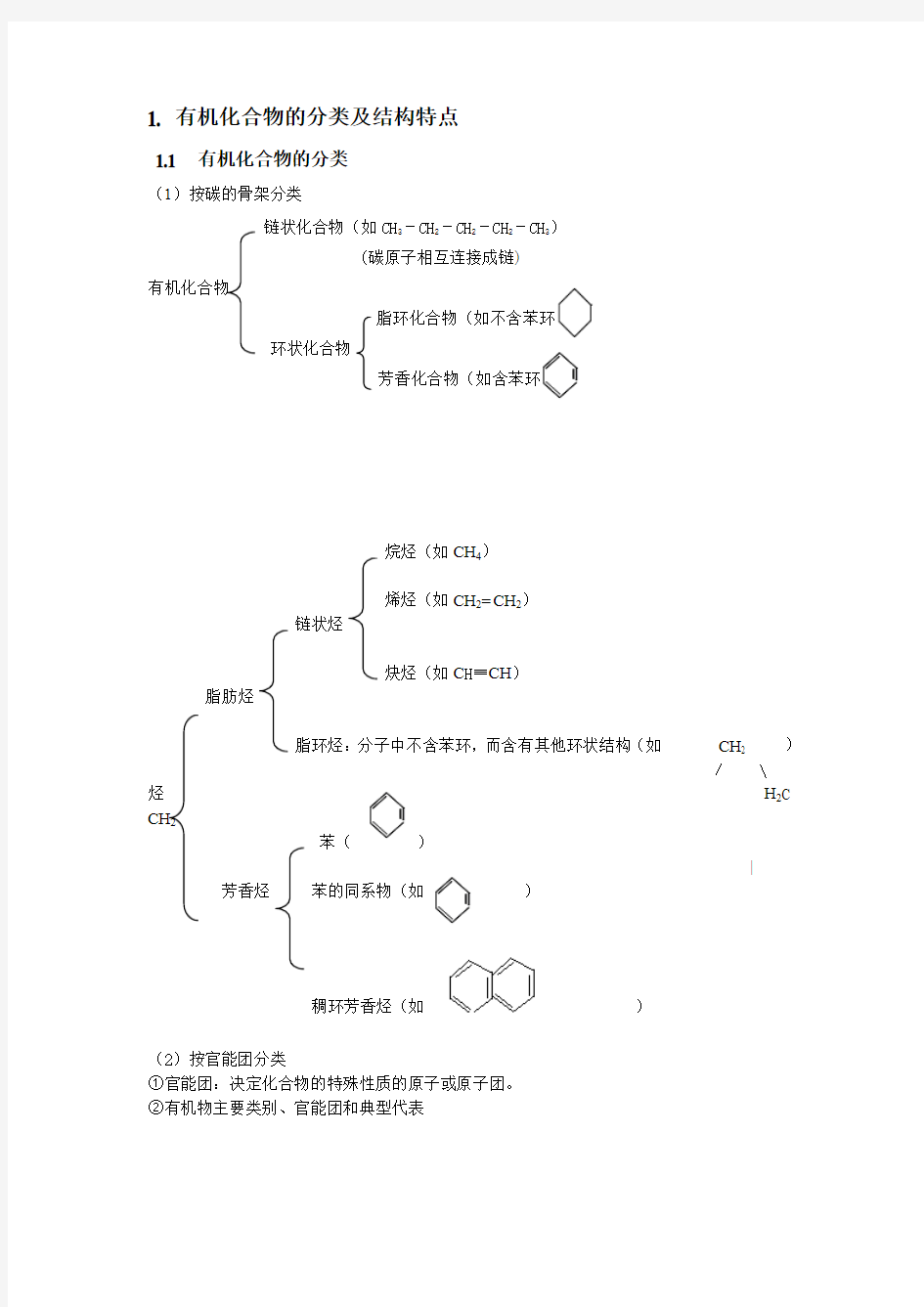
(1)按碳的骨架分类
链状化合物(如CH3-CH2-CH2-CH2-CH3)
(碳原子相互连接成链)
有机化合物
脂环化合物(如不含苯环
环状化合物
芳香化合物(如含苯环
烷烃(如CH4)
烯烃(如CH2=CH2)
链状烃
炔烃(如C H≡CH)
脂肪烃
脂环烃:分子中不含苯环,而含有其他环状结构(如CH2 )
∕ \
烃H
C
CH2
苯()
|
芳香烃苯的同系物(如)
稠环芳香烃(如)
(2)按官能团分类
①官能团:决定化合物的特殊性质的原子或原子团。
②有机物主要类别、官能团和典型代表
双键
醚键
醛基
羰基
酯
重点提示:一种有机物中可能同时含有多种官能团,从而使一种有机物可以同时有多方面的化学性质。
1.2 有机物的结构特点
(1)碳原子的成键特点
成键数目→每个碳原子形成四个共价键
∣
成键种类→单键、双键或三键
∣
连接方式→碳链或碳环
(2)有机物分子里原子共线、共面:
共线、共面其实是分子的构型问题,掌握并会画出以下分子的构型:
CH4正四面体,键角109о28′
C2H4平面型结构,键角120о,6个原子在同一平面上;
C2H2直线型结构,键角180о,4个原子在同一直线上
平面型结构,键角120о,12个原子在同一平面上
(3)同系物
结构相似,在分子组成上相关一个或若干CH2原子团的有机物互称为同系物。
(4) 同分异构体
①同分异构现象:化合物具有相同的分子式而结构是不同的现象
②同分异构现象的常见类型
异构方式形成途径示例
碳链异构碳链骨架不同CH3CH2 CH2CH3和CH3
∣
CH3---CH-----CH3
位置异构官能团位置不同HC≡C—CH2CH3和CH3—C≡C—C 官能团异构官能团种类不同CH3CH2OH和CH3—O—CH3
2、有机物的命名
2.1烷烃的命名
烷烃系统命名法命名步骤可归纳为:选主链,称某烷;编号位,定支链;取代基,写在前,
标位置,连短线;不同基,简到繁,相同基,合并算。可解释为:一长、一近、一多、一少,
即“一长”是主链要长,“一近”是编号起点离支链最近,“一多”是支链数目要多,“一少”
是支链位置编号之和要少。如
2,3---二甲基己烷
说明:(1)碳原子数在10以下的用甲乙丙丁戊己庚辛壬,碳原子数在10以上的用数字表
示;
(2)简单烷烃(碳原子数在6以下)可用习惯命名法,如C(CH3)4命名为“新戊烷”。
2.2烯烃和炔烃的命名
(1)将含有双键或三键的最长碳链作为主链,称为“某烯”或“某炔”;
(2)从距离双键或三键的近的一端给主链上的碳原子依次编号定位;
(3
2.3
苯的同系物的命名是以苯做母体。如
有两个取代基,则用“邻、间、对”表示取代基的位置,如
邻二甲苯间二甲苯对二甲苯
3、同分异构体的书写及判断
3.1同分异构体的书写规律
(1)烷烃
烷烃只存在于碳链异构,书写时应注意要全面而不重复,具体规则如下:成直连,一条线;摘一碳,挂中间,往边移,不到端;摘二碳,成乙基;二甲基,同、邻、间。如C5H12的同分异构体有:
CH3CH2CH2CH2CH3
(2)具有官能团的有机物,一般书写顺序:碳链异构→官能团位置异构→官能团类别异构。
如:C4H10O的同分异构体有:
①醇类
②醚类
(3)芳香族化合物:取代基在苯环上的相对位置具有邻、间、对3种。
如:C8H10苯的同系物有:
3.2同分异构体数目的判断方法
(1)基元法
①丙基(---C3H7)有两种结构,则丙醇、丁醛、丁酸都有两种结构。
②丁基(---C4H9)有四种结构,则丁醇、戊醛、戊酸都有四种结构。
③戊基(---C5H11)有八种结构,则戊醇、己醛、己酸都有八种结构
(2)替代法
例如,二氯苯(C6H4Cl2)有三种同分异构体,四氯苯也有三种(将H替代Cl);又如CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
(3)等效氢法
等效氢是判断同分异构体数目的重要方法,其规律有:a. 同一碳上的氢是等效的;b. 同一碳上所连的甲基上的氢是等效的;c. 处于镜面对称位置上的氢是等效的 3.3有机物的顺反异构
(1)顺反异构。如2-丁烯,若甲基在双键同一侧,称为顺式;甲基在双键两侧称为反式。
反式 顺式 (2)对映异构。如:乳酸,两种分子结构互为镜像。
三、典型例题
【例1】 下列说法中错误的是( )
①化学性质相似的有机物是同系物 ②分子组成相差一个或若干个CH2原子团的有机物是同系物 ③若烃中碳、氢元素的质量分数分别相同,它们必定是同系物 ④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似
A .①②③④
B .只有②③
C .只有③④
D .只有①②③ 例2.[2011·常州一模]下列有机分子中,所有的原子不可能处于同一平面的是( )
A .CH 2CHCN
B .CH 2CHCHCH 2
C .CHCH 2
D .CCH 2CH 3CHCH 2
例2.D 【解析】 乙烯和苯都是平面型分子,所有原子都在同一平面内,A 、B 、C 三种物质中分别可以看作乙烯分子中的一个氢原子分别被—CN 、—CH===CH 2、取代,所以所有原子仍有可能在同一平面内。而D 中物质可以认为是CH 4分子中的一个氢原子被CCH 2CHCH 2取代,故所有原子不可能处于同一平面内。 例3.[2011·高邮月考]有机物A 的分子式为C 11H 16 ,它不能因反应而使溴水褪色,但能使酸性KMnO 4溶液褪色,经测定数据表明,分子中除含苯环外不再含有其他环状结构,且苯环上只有一个侧链,符合此条件的烃的结构有( )
A .5种
B .6种
C .7种
D .8种
C 【解析】 由题给条件可确定该有机物A 属苯的同系物,且与苯环直接相连的碳原子上应含有氢原子。即该有机物A 有形如CH 2R 和CHRR 的结构。若为 CH 2R ,则—R 为—C 4H 9,因丁基有四种结构,则CH 2C 4H 9有四种结构;若为CHRR ,则R 1、R 2可同时为—C 2H 5,只有一种结构;R 1、R 2也可为—CH 3与—C 3H 7,因丙基有两种结构,故此时有机物A 也有两种结构。据此可以得出符合题设条件的有机物共有7种。
例4.聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好,不易老化、耐擦洗、色泽亮丽等优点。右边是聚丙烯酸酯的结构简式,它属于( )
①无机化合物 ②有机化合物 ③高分子化合物 ④离子化合物 ⑤共价化合物
A .①③④
B .①③⑤
C .②③⑤
D .②③④ 例5.下列物质不.
属于醇类的是:C A .
HO
CH 2OH
B .CH 3CHCH 2OH HO
C.CHO COOH
D.
CH2CH2OH
例6.进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是:D
A.(CH3)2CHCH2CH2CH3B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2D.(CH3)3CCH2CH3
例7.(2012·吉林期末)分子式为C7H16的烷烃中,含有3个甲基的同分异构体(不考虑立体异构)的数目是( )
A.2种 B.3种
C.4种 D.5种
【解析】B 根据同分异构体有3个甲基可知只能有一个取代基,若为甲基有两种结构,若为乙基只有一种结构,故选B。
【答案】C
例8.写出下列化合物的名称或结构简式:
(1)结构简式为此烃名称为。(2)结构简式为的烃可命名为。(3)2,5-二甲基-2,4-己二烯的结构简式:。
(4)结构简式为CH3CHCHCH2CH3
H3CCHCH3
CH3的烃可命名为:。
答案:
(1)3-甲基-2-丙基-1-戊烯(2)1-甲基-3-乙基苯(3) (4)2,4-二甲基-3-乙基戊烷
四、当堂练习
1.下列物质属于有机物的是(C )A.氰化钾(KCN)B.氰酸铵(NH4CNO)
C.乙炔(C2H2)D.碳化硅(SiC)
2.下列有机物是按照碳的骨架进行分类的是( C )A.烷烃B.烯烃C.芳香烃D.卤代烃
3.下列关于官能团的判断中说法错误的是(B )A.醇的官能团是羟基(-OH)B.羧酸的官能团是羟基(-OH)
C.酚的官能团是羟基(-OH)D.烯烃的官能团是双键
H3C CH2CH3
4.关于同分异构体的下列说法中正确的是( B )
A.结构不同,性质相异,化学式相同的物质互称同分异构体
B.同分异构体现象是导致有机物数目众多的重要原因之一
C.同分异构体现象只存在于有机化合物中
D.同分异构体现象只存在于无机化合物中
5.下列烷烃中可能存在同分异构体的是( D )
A.甲烷B.乙烷C.丙烷D.丁烷
6.同分异构体现象在有机化学中是非常普遍的,下列有机物互为同分异构体的是(AD )
①CH2=CHCH3 ②③CH3CH2CH3④HC CCH3⑤⑥
CH3CH=CHCH3
A.①和②B.①和③C.①和④D.⑤和⑥
7.下列哪个选项属于碳链异构(AB )A.CH3CH2 CH2CH3和CH3CH(CH3)2B.CH2=C(CH3)2和CH3CH=CHCH3
C.CH3CH2OH和CH3OCH3D.CH3CH2 CH2COOH 和CH3COOCH2 CH2 8.请同学们根据官能团的不同对下列有机物进行分类。
(1)芳香烃:;
(2)卤代烃:;
(3)醇:;
(4)酚:;
(5)醛:;
(6)酮:;
(7)羧酸:;
(8)酯:。
9.A、B、C、D、E、F、G四种有机物,其中B、C为不饱和烃,但是只有B能够使溴的四氯化碳溶液褪色;A能够在光照条件下与氯气发生取代反应,其二氯取代物是D,D
有两种同分异构体;B与溴的四氯化碳溶液可以发生加成反应,加成产物是E,且E只有一种同分异构体F;C在FeBr3在催化剂的作用下,可以与液溴发生取代反应,取代产物是G,G没有同分异构体。
试根据以上事实,推断A、B、C、D、E、F、G的结构简式。
A ;
B ;
C ;
D ;
E ;
F ;
G 。
10.同分异构体和同系物是不同的两个概念,观察下面列出的几种物质的化学式或者结构式,然后解题。
①CO(NH2)2②NH4CNO ③CH3CH2CH3④CH3CH2CH2CH3
其中,(1)互为同分异构体的是;
(2)互为同系物的是;
(3)实际上是同种物质的是。
答案:19.(1)⑨;(2)③⑥;(3)①;(4)⑤;(5)⑦;(6)②;(7)⑧⑩;(8)④。
22.A:CH3CH3;B:CH2=CH2;C:;D:CH3CHCl2(或者CH2ClCH2Cl);E:CH2BrCH2Br;
F:CH3CHBr2;G:
21.(1)①和②,④与⑦,⑤与⑥(或者⑧);
(2)③、④、⑤、⑥(或者⑧)、⑦;(3)⑥与⑧。
五、课后作业
1.(2012年襄阳模拟) 的正确名称是( )
A.2,5-二甲基-4-乙基己烷 B.2,5-二甲基-3-乙基己烷
C.3-异丙基-5-甲基己烷 D.2-甲基-4-异丙基己烷
【解析】对烷烃的命名关键是选好主链。主链最长且支链最多,然后从支链近的一端编号。
的名称为2,5-二甲基-3-乙基己烷。
【答案】B
2.分子式为C5H7Cl的有机物,其结构不.可能是( )
A.只含有1个双键的直链有机物
B.含2个双键的直链有机物
C.含1个双键的环状有机物
D.含一个三键的直链有机物
【答案】A
【解析】该有机物与饱和的有机物相比较少了四个氢原子,故不可能是只含有一个双键的链状有机物.
3.(2012·合肥模拟)下列化合物的分子中有三类氢原子的是( )
A.2,2,3,3-四甲基丁烷B.2,3,4-三甲基戊烷
C.3,4-二甲基己烷 D.2,5-二甲基己烷
4.某有机化合物结构如图,,关于该化合物的下列说法正确的是( )
A.由于含有氧元素故不是有机物
B.完全燃烧时只有二氧化碳和水两种产物
C.分子中含有羟基属于醇
D.不能使溴水褪色
【答案】B
【解析】是不是有机物与含有氧元素没有关系;由于只含有碳、氢、氧三种元素,所以燃烧产物只有二氧化碳和水;分子中的羟基与苯环直接相连,属于酚类;分子中含有碳碳双键,可以使溴水褪色.
5.某烯烃与H2加成后得到2,2-二甲基丁烷,该烯烃的名称是 ( )
A.2,2-二甲基-3-丁烯B.2,2-二甲基-2-丁烯
C.2,2-二甲基-1-丁烯D.3,3-二甲基-1-丁烯
【答案】D
【解析】2,2-二甲基丁烷去掉2个氢原子,只能得到一种烯烃:(CH3)3CCH===CH2,再命名为3,3-二甲基-1-丁烯.
6.下列有关微粒之间关系和特征描述正确的是
【答案】D
7.下列有机物命名正确的是
A .
CH 2CH 2
Br Br
二溴乙烷 B .
CH 2=CCH 3
C 2H 5
2-乙基-丙烯
C .
CH 3CHOH
CH 3
2-丙醇 D . 氯甲苯
【答案】C
8.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得。 D
OH HO
CH COOH
OH
+HC C O
O (乙醛酸)
(羟基扁桃酸)
下列有关说法正确的是学 A .苯酚和羟基扁桃酸互为同系物
B .常温下,1mol 羟基扁桃酸只能与1mol Br 2反应
C .乙醛酸的核磁共振氢谱中只有1个吸收峰
D .羟基扁桃酸分子中至少有12个原子共平面
9.下图是由4个碳原子构成的6种有机物(氢原子没有画出),试回答下列问题:
(1)互为同分异构体的是________; (2)e 中所含官能团的名称为_______;
(3)b 、c 、d 、e 中与氢气完全加成后所得产物与a 互为同分异构体的有_______; (4)a 、b 、c 、d 、e 五种物质中,4个碳原子一定处于同一个平面上的有_______。 (5)依据上图说明碳原子的成键方式有哪些_______。
【解析】a、b、c、d、e、f对应的物质分别是2-甲基丙烷、2-甲基1-丙烯、2-丁烯、1,3-丁二烯、1-丁炔、环丁烷。(1)b、c、f互为同分异构体,d和e互为同分异构体。
(3)b与氢气加成后的产物与a是同一种物质,而不是同分异构体。(4)d中双键碳原子之间通过单键相连,单键可以自由旋转,4个碳原子可能共平面,也可能不在一个平面上。
【答案】(1)b、c、f;d、e (2)碳碳三键
(3)c、d、e (4)b、c、e
(5)碳原子可以与碳原子或其他原子形成4个共价键,碳原子可以形成单键、双键、三键,碳原子可以形成碳链、碳环
10.下列是八种环状的烃类物质:
(1)互为同系物的有________和________(填名称).互为同分异构体的有________和________、________和________(填写名称,可以不填满,也可以再补充).
(2)正四面体烷的二氯取代产物有________种;立方烷的二氯取代产物有________种;金刚烷的一氯取代产物有________种.
(3)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例)并用系统命名法命名:________________________、__________________________.
【解析】 (1)同系物指结构相似,分子组成上相差一个或若干个CH2原子团的化合物,因此环己烷与环辛烷互为同系物;同分异构体指分子式相同,结构不同的化合物,因此苯与棱晶烷(分子式均为C6H6),环辛四烯与立方烷
(分子式均为C8H8)互为同分异构体.
(2)正四面体烷结构对称,只有一种氢原子,故二氯代物只有一种;立方烷分子中只有一种氢原子,但其二氯代
物有3种,分别为;金刚烷分子中有两种氢原子,其一氯代物
有2种.
(3)符合条件的可为,一氯代物分别为和
,也可为,一氯代物分别为,
【答案】 (1)环己烷环辛烷苯棱晶烷环辛四烯立方烷
(2)1 3 2
备战高考化学易错题专题训练-认识有机化合物练习题附答案
备战高考化学易错题专题训练-认识有机化合物练习题附答案 一、认识有机化合物练习题(含详细答案解析) 1.当1mol某气态烃与2mol Cl2发生加成反应时,分子中的不饱和碳原子全部转化为饱和碳原子,所得产物再与4mol Cl2进行取代反应后,生成只含C、Cl两种元素的化合物。则该气态烃是( ) A.乙炔B.乙烯C.丁二烯D.丙炔 【答案】D 【解析】 【分析】 【详解】 1mol该气态烃与2molCl2发生加成反应时,分子中的不饱和碳原子全部转化为饱和碳原子,说明分子中含有2个C=C或1个C≡C键;所得产物再与Cl2发生取代反应时,若将氢原子全部取代,需要4mol Cl2,根据取代反应原理可知,该烃分子中加成产物含有4个H,即原烃中含有H原子为4,只有丙炔符合,故答案为D。 2.由环已烷、乙醇、乙醚组成的混和物,经测定其中碳的质量分数为72%,则氧的质量分数为 A.14.2% B.16% C.17.8% D.19.4% 【答案】A 【解析】 【分析】 环己烷的分子式为C6H12可以改写成(CH2)6,乙醇的分子式为C2H6O可以改写成 (CH2)2·H2O,乙醚的分子式为C4H10O,可以改写成(CH2)4·H2O,所以该混合物可以看成CH2与H2O构成的。 【详解】 由于该混合物中C的质量分数为72%,所以CH2的质量分数为: 12 72%=84% 14 ÷,那么 H2O的质量分数为:1-84%=16%,O元素的质量分数为: 16 16%14.2% 18 ?≈,A项正 确; 答案选A。 3.下列有关物质结构或性质的说法不正确的是() A.三联苯与四联苯互为同系物 B.可用燃烧法鉴别环乙烷、苯、CCl4 C.分子式为C5H10的烃存在顺反异构体
第一章 认识有机化合物(全章教案)
第一章认识有机化合物 第一节有机化合物的分类 一、教学目标 【知识与技能】 1、了解有机化合物的分类方法,认识一些重要的官能团。 2、掌握有机化合物的分类依据和原则。 【过程与方法】 根据生活中常见的分类方法,认识有机化合物分类的必要性。利用投影、动画、多媒体等教学手段,演示有机化合物的结构简式和分子模型,掌握有机化合物结构的相似性。 【情感、态度与价值观】 通过对有机化合物分类的学习,体会分类思想在科学研究中的重要意义。 二、教学重点 认识常见的官能团;有机化合物的分类方法 三、教学难点 认识常见的官能团,按官能团对有机化合物进行分类 四、教学过程 【引入】师:通过高一的学习,我们知道有机物就是有机化合物的简称,最初有机物是指有生机的物质,如油脂、糖类和蛋白质等,它们是从动、植物体中得到的,直到1828年,德国科学家维勒偶然发现由典型的无机化合物氰酸铵通过加热可以直接转变为动植物排泄物——尿素的实验事实,从而使有机物的概念受到了冲击,引出了现代有机物的概念——世界上绝大多数含碳的化合物。有机物自身有着特定的化学组成和结构,导致了其在物理性质和化学性质上的特殊性。研究有机物的组成、结构、性质、制备方法与应用的科学叫有机化学。 我们先来了解有机物的分类。 【板书】第一章认识有机化合物 第一节有机化合物的分类 师:有机物从结构上有两种分类方法:一是按照构成有机物分子的碳的骨架来分类;二是按反映有机物特性的特定原子团来分类。 【板书】一、按碳的骨架分类
链状化合物(如CH3-CH2-CH2-CH2-CH3) 有机化合物 脂环化合物(如) 环状化合物 芳香化合物(如) 【板书】二、按官能团分类 表1-1 有机物的主要类别、官能团和典型代表物 双键 醚键 醛基 羰基 羧基 酯基 【随堂练习】按官能团的不同可以对有机物进行分类,你能指出下列有机物的类别吗?
高三数学第一轮教案简易逻辑
简易逻辑 二.教学目标:了解命题的概念和命题的构成;理解逻辑联结词“或”“且”“非”的含义;理解四 种命题及其互相关系;反证法在证明过程中的应用. 三.教学重点:复合命题的构成及其真假的判断,四种命题的关系. 四.教学过程: (一)主要知识: 1.理解由“或”“且”“非”将简单命题构成的复合命题; 2.由真值表判断复合命题的真假; 3.四种命题间的关系. (二)主要方法: 1.逻辑联结词“或”“且”“非”与集合中的并集、交集、补集有着密切的关系,解题时注意类比; 2.通常复合命题“p 或q ”的否定为“p ?且q ?”、“p 且q ”的否定为“p ?或q ?”、“全为”的否定是“不全为”、“都是”的否定为“不都是”等等; 3.有时一个命题的叙述方式比较的简略,此时应先分清条件和结论,该写成“若p ,则q ”的形式; 4.反证法中出现怎样的矛盾,要在解题的过程中随时审视推出的结论是否与题设、定义、定理、公理、公式、法则等矛盾,甚至自相矛盾. (三)例题分析: 例1.指出下列命题的构成形式及构成它的简单命题,并判断复合命题的真假: (1)菱形对角线相互垂直平分. (2)“23≤” 解:(1)这个命题是“p 且q ”形式,:p 菱形的对角线相互垂直;:q 菱形的对角线相互平分, ∵p 为真命题,q 也是真命题 ∴p 且q 为真命题. (2)这个命题是“p 或q ”形式,:p 23<;:q 23=, ∵p 为真命题,q 是假命题 ∴p 或q 为真命题. 注:判断复合命题的真假首先应看清该复合命题的构成形式,然后判断构成它的简单命题的真假,再由真值表判断复合命题的真假. 例2.分别写出命题“若220x y +=,则,x y 全为零”的逆命题、否命题和逆否命题. 解:否命题为:若220x y +≠,则,x y 不全为零 逆命题:若,x y 全为零,则220x y += 逆否命题:若,x y 不全为零,则220x y +≠ 注:写四种命题时应先分清题设和结论. 例3.命题“若0m >,则20x x m +-=有实根”的逆否命题是真命题吗?证明你的结论. 解:方法一:原命题是真命题, ∵0m >,∴140m ?=+>, 因而方程20x x m +-=有实根,故原命题“若0m >,则20x x m +-=有实根”是真命题; 又因原命题与它的逆否命题是等价的,故命题“若0m >,则20x x m +-=有实根”的逆否命题是真命题. 方法二:原命题“若0m >,则20x x m +-=有实根”的逆否命题是“若2 0x x m +-=无实根,则0m ≤”.∵20x x m +-=无实根 ∴140m ?=+<即104 m <- ≤,故原命题的逆否命题是真命题. 例4.(考点6智能训练14题)已知命题p :方程210x mx ++=有两个不相等的实负根,命题q :
高三物理一轮复习导学案
2014届高三物理一轮复习导学案 第七章、恒定电流(1) 【课题】电流、电阻、电功及电功率 【目标】 1、理解电流、电阻概念,掌握欧姆定律和电阻定律; 2、了解电功及电功率的概念并会进行有关计算。 【导入】 一.电流、电阻、电阻定律 1、电流形成原因:电荷的定向移动形成电流. 2、电流强度:通过导体横截面的跟通过这些电量所用的的比值叫电流强度.I= 。由此可推出电流强度的微观表达式,即I=__________________。 3、电阻:导体对电流的阻碍作用叫电阻.电阻的定义式:__________________。 4、电阻定律:在温度不变的情况下导体的电阻跟它的长度成正比,跟它的横截面积成反比.电阻定律表达式__________________。【导疑】电阻率,由导体的导电性决定,电阻率与温度有关,纯金属的电阻率随温度的升高而增大;当温度降低到绝对零度附近时,某些材料的电阻率突然减小到零,这种现象叫超导现象.导电性能介于导体和绝缘体之间的称为半导体。 二.欧姆定律 1、部分电路欧姆定律:导体中的电流跟它两端的电压成正比,跟
它的电阻成反比.表达式:____________________________ 2、部分欧姆定律适用范围:电阻和电解液(纯电阻电路).非纯电阻电路不适用。 三、电功及电功率 1、电功:电路中电场力对定向移动的电荷所做的功,简称电功;W=qU=IUt。这就是电路中电场力做功即电功的表达式。(适用于任何电路) 2、电功率:单位时间内电流所做的功;表达式:P=W/t=UI(对任何电路都适用) 3、焦耳定律:内容:电流通过导体产生的热量,跟电流强度的平方、导体电阻和通电时间成正比。表达式:Q=I2Rt 【说明】(1)对纯电阻电路(只含白炽灯、电炉等电热器的电路)中电流做功完全用于产生热,电能转化为内能,故电功W等于电热Q;这时W= Q=UIt=I2Rt 4、热功率:单位时间内的发热量。即P=Q/t=I2R ④ 【注意】②和④都是电流的功率的表达式,但物理意义不同。②对所有的电路都适用,而④式只适用于纯电阻电路,对非纯电阻电路(含有电动机、电解槽的电路)不适用。 关于非纯电阻电路中的能量转化,电能除了转化为内能外,还转化为机械能、化学能等。这时W》Q。即W=Q+E其它或P =P热+ P其 它、UI = I2R + P其它 【导研】 [例1]一根粗线均匀的金属导线,两端加上恒定电压U时,通过金属导线的电流强度为I,金属导线中自由电子定向移动的平均速率为v,若将金属导线均匀拉长,使其长度变为原来的2倍,仍给它两端加上恒定电压U,则此时() A、通过金属导线的电流为I/2 B、通过金属导线的电流为I/4 C、自由电子定向移动的平均速率为v/2 D、自由电子定向移动
高中化学专题1认识有机化合物第1单元有机化学的发展与应用学案苏教版
第一单元有机化学的发展与应用 1.了解有机化学的发展史。 2.了解有机化学在生产、生活、科技与能源方面的重大作用。 教材整理1 有机化学的发展 1.19世纪初,瑞典化学家贝采利乌斯提出有机化学的概念。有机化学即研究有机化合
物的组成、结构、性质、制备方法与应用的科学。 2.19世纪中叶以前,科学家提出“生命力论”,认为有机物只能由动物或植物产生,不可能通过人工的方法将无机物转变为有机物。 3.1828年,德国化学家维勒用无机盐氰酸铵(NH4CNO)合成了尿素[CO(NH2)2],这是人类历史上第一次由无机化合物合成有机物,尿素的人工合成开启了有机合成的大门,动摇了“生命力论”的基础。此后,其他化学家又以无机物为原料合成了醋酸、苹果酸、甲烷、乙炔等有机化合物,使人们彻底摈弃了“生命力论”。 4.1965年,中国科学院生物化学研究所、有机化学研究所和北京大学化学系三个单位协作,第一次用人工方法合成了具有生物活性的蛋白质结晶牛胰岛素。 (1)含碳元素的化合物都是有机物。( ) (2)NH4CNO与CO(NH2)2互为同分异构体。( ) (3)有机物只能由动、植物产生,不能通过人工合成。( ) (4)醋酸、苹果酸、甲烷、CO、HCN均为有机物。( ) 【答案】(1)×(2)√(3)×(4)× 教材整理2 有机化学的应用 1.在人类衣食住行所需的物品中,有许多来源于天然有机物,如糖类、油脂、蛋白质、石油、天然气、天然橡胶等。塑料、合成纤维、合成橡胶、合成药物等合成有机物广泛应用于生活的方方面面。 2.有机物在维持生命活动的过程中发挥着重要的作用。例如,依靠酶的催化作用,人体将食物消化,并将一些简单分子合成生命活动所需的生物分子。 3.药物化学已经成为化学的一个重要领域,世界上每天都会合成出的备选药物大多数是有机化合物。
第一章认识有机化合物知识点复习
第一章认识有机化合物知识点复习 考点1:有机物的特点 1.无机化合物和有机化合物的划分 无机化合物(简称无机物)通常指不含碳元素的化合物,无机物包括酸、碱、盐、氧化物等,另外,单质也属于无机物。有机化合物(简称有机物)是一类含有碳元素的化合物,比如烃及其各种衍生物就是我们常见的有机物。 无机物和有机物的划分不是绝对的,少数含碳化合物性质更像无机物,所以将它们划分为无机物的范畴。中学常见含碳无机物有: 2.有机物的特点 在结构上: 在性质上: 在反应上: 考点2:碳原子的成键特点和结合方式 1.C原子的成键特点 (1)通常以共价键与其它原子结合——所以有机物多数是共价化合物。 (2)总是形成4个价键——是有机物种类繁多的一个重要原因。 (3)C原子的价键具有一定的空间伸展方向——这样有机物就有一定的立体空间形状。 2.C原子结合方式 有机物中C原子可以以单键结合,也可以以双键、三键结合,还可以像苯环这样介于单双键之间的独特方式相结合。C原子可以结合成链状,也可以结合成环状。 考点3:有机物分子结构 1.有机分子的空间结构及表示方法—— 有机物绝大多数为共价化合物,分子中原子之间依靠共价键结合。通常用 式表示有机物分子中原子间的结合情况。对于环状化合物,用键线式表示则比较方便。 由于共价键具有一定的空间伸展方向,这使得有机物分子具有一定的空间形状。若一个碳原子周围是一个双键和两个单键,其双键和单键的夹角总接近120o,若是一个三键和一个单键,则它们的夹角总接近180o,若碳原子形成四个单键,则它们的夹角总接近109.5o。 有机物的空间结构可以用粗略表示。下面是几种具有代表性的有机物分子结构。
高三数学第一轮复习教案(1)
第1页 共64页 高考数学总复习教案 第一章-集合 考试内容:集合、子集、补集、交集、并集.逻辑联结词.四种命题.充分条件和必要条件. 考试要求: (1)理解集合、子集、补集、交集、并集的概念;了解空集和全集的意义;了解属于、包含、相等关系的意义;掌握有关的术语和符号,并会用它们正确表示一些简单的集合. (2)理解逻辑联结词“或”、“且”、“非”的含义理解四种命题及其相互关系;掌握充分条件、必要条件及充要条件的意义. §01. 集合与简易逻辑 知识要点 一、知识结构: 本章知识主要分为集合、简单不等式的解法(集合化简)、简易逻辑三部分: 二、知识回顾: (一) 集合 1. 基本概念:集合、元素;有限集、无限集;空集、全集;符号的使用. 2. 集合的表示法:列举法、描述法、图形表示法. 集合元素的特征:确定性、互异性、无序性. 集合的性质: ①任何一个集合是它本身的子集,记为A A ?; ②空集是任何集合的子集,记为A ?φ; ③空集是任何非空集合的真子集; 如果B A ?,同时A B ?,那么A = B. 如果C A C B B A ???,那么,. [注]:①Z = {整数}(√) Z ={全体整数} (×) ②已知集合S 中A 的补集是一个有限集,则集合A 也是有限集.(×)(例:S=N ; A=+N ,则C s A= {0}) ③ 空集的补集是全集. ④若集合A =集合B ,则C B A = ?, C A B = ? C S (C A B )= D ( 注 :C A B = ?). 3. ①{(x ,y )|xy =0,x ∈R ,y ∈R }坐标轴上的点集. ②{(x ,y )|xy <0,x ∈R ,y ∈R }二、四象限的点集. ③{(x ,y )|xy >0,x ∈R ,y ∈R } 一、三象限的点集.
【化学】化学认识有机化合物的专项培优练习题附答案解析
【化学】化学认识有机化合物的专项培优练习题附答案解析 一、认识有机化合物练习题(含详细答案解析) 1.结合已学知识,并根据下列一组物质的特点回答相关问题。 (1)邻二甲苯的结构简式为____(填编号,从A~E中选择)。 (2)A、B、C之间的关系为____(填序号)。 a.同位素 b.同系物 c.同分异构体 d. 同素异形体 (3)请设计一个简单实验来检验A与D,简述实验操作过程:_____________。 (4)有机物同分异构体的熔沸点高低规律是“结构越对称,熔沸点越低”,根据这条规律,判断C、D、E的熔沸点由高到低的顺序:______(填编号)。 【答案】E b 取少量A、D分别装入两支试管中,向两支试管中滴入少量酸性KMnO4溶液,振荡,若溶液褪色,则为间二甲苯;若溶液不褪色,则为苯; E>D>C 【解析】 【分析】 (1)邻二甲苯表示苯环相邻位置各有1个甲基; (2)结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物; (3)苯不能被酸性KMnO4溶液氧化,间二甲苯能被酸性KMnO4溶液氧化; (4)根据结构越对称,熔沸点越低解题。 【详解】 (1)C为对二甲苯,D为间二甲苯,E为邻二甲苯,故答案为:E; (2)A、B、C的结构简式中都含有苯环,分子式依次相差1个“CH2”,符合通式C n H2n-6(n≥6),所以它们互为同系物,故答案为:b; (3)苯不能被酸性KMnO4溶液氧化,间二甲苯能被酸性KMnO4溶液氧化,则检验苯与间二甲苯的操作为取少量A、D分别装入两支试管中,向两支试管中滴入少量酸性KMnO4溶液,振荡,若溶液褪色,则为间二甲苯;若溶液不褪色,则为苯; (4)对二甲苯的对称性最好,邻二甲苯的对称性最差,故熔沸点由高到低:E>D>C。 2.N A为阿伏加德罗常数,下列说法正确的是() A.7.8g苯所含碳碳双键数目为0.3N A B.28g乙烯所含共用电子对数目为6N A C.标准状况下,11.2 L二氯甲烷所含分子数为0.5N A D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为2N A
2019年高考化学第12章第1讲认识有机化合物复习题及答案
2019年高考化学第12章第1讲认识有机 化合物复习题及答案 1.下列有关化学用语表达正确的是() A.次氯酸的电子式: B.CCl4的比例模型: C.乙醛的结构简式:CH3CHO D.乙醇的结构式:CH3CH2OH 解析:选C。次氯酸的电子式为:,A错误;是CH4分子的比例模型,若是CCl4分子的比例模型,则Cl原子大一些,B错误;乙醛的结构简式是CH3CHO,C正确;乙醇的结构式为。 2.下列说法正确的是() A.丙烷是直链烃,所以分子中3个碳原子也在一条直线上 B.丙烯所有原子均在同一平面上
C.所有碳原子一定在同一平面上 D.至少有16个原子共平面 解析:选D。直链烃是锯齿形的,A错误;CH3CH===CH2中甲基上至少有两个氢不和它们共平面,B错误;因为环状结构不是平面结构,所以所有碳原子不可能在同一平面上,C错误;该分子中在同一条直线上的原子有8个 (),再加上其中一个苯环上的8个原子,所以至少有16个原子共平面,D正确。 3.有关CHCHCHF2CCCH3分子结构的下列叙述中,正确的是() A.除苯环外的其余碳原子有可能都在一条直线上 B.所有的原子都在同一平面上 C.12个碳原子不可能都在同一平面上 D.12个碳原子有可能都在同一平面上 解析:选D。本题主要考查苯环、碳碳双键、碳碳三键的空间结构。按照结构特点,其空间结构可简单表示为下图所示:
由图形可以看到,直线l一定在平面N中,甲基上3个氢只有一个可能在这个平面内;—CHF2基团中的两个氟原子和一个氢原子,最多只有一个在双键决定的平面M中;平面M 和平面N一定共用两个碳原子,可以通过旋转碳碳单键,使两平面重合,此时仍有—CHF2中的两个原子和—CH3中的两个氢原子不在这个平面内。要使苯环外的碳原子共直线,必须使双键部分键角为180°。但烯烃中键角为120°,所以苯环以外的碳不可能共直线。 4.下列各有机化合物的命名正确的是() A.CH2===CH—CH===CH21,3二丁烯 B.3丁醇 C.甲基苯酚 D.2甲基丁烷 解析:选D。A项中化合物应命名为1,3丁二烯;B项中化合物应命名为2丁醇;C项中化合物应命名为邻甲基苯酚。 5.下列对有机化合物的分类结果正确的是() A.乙烯CH2===CH2、苯、环己烷同属于脂肪烃
高三物理一轮复习选修3-3全套学案
第1课时 分子动理论 内能 导学目标 1.掌握分子动理论的内容,并能应用分析有关问题.2.理解温度与温标概念,会换算摄氏温度与热力学温度.3.理解内能概念,掌握影响内能的因素. 一、分子动理论
1.请你通过一个日常生活中的扩散现象来说明:温度越高,分子运动越激烈. 2.请描述:当两个分子间的距离由小于r0逐渐增大,直至远大于r0时,分子间的引力如何变化?分子间的斥力如何变化?分子间引力与斥力的合力又如何变化? [知识梳理] 1.物体是由____________组成的 (1)多数分子大小的数量级为________ m. (2)一般分子质量的数量级为________ kg. 2.分子永不停息地做无规则热运动 (1)扩散现象:相互接触的物体彼此进入对方的现象.温度越______,扩散越快. (2)布朗运动:在显微镜下看到的悬浮在液体中的__________的永不停息地无规则运 动.布朗运动反映了________的无规则运动.颗粒越______,运动越明显;温度越______,运动越剧烈. 3.分子间存在着相互作用力 (1)分子间同时存在________和________,实际表现的分子力是它们的________. (2)引力和斥力都随着距离的增大而________,但斥力比引力变化得______. 思考:为什么微粒越小,布朗运动越明显? 二、温度和温标 [基础导引] 天气预报某地某日的最高气温是27°C,它是多少开尔文?进行低温物理的研究时,热力学温度是2.5 K,它是多少摄氏度? [知识梳理] 1.温度 温度在宏观上表示物体的________程度;在微观上是分子热运动的____________的标志. 2.两种温标 (1)比较摄氏温标和热力学温标:两种温标温度的零点不同,同一温度两种温标表示的数 值________,但它们表示的温度间隔是________的,即每一度的大小相同,Δt=ΔT. (2)关系:T=____________. 三、物体的内能 [基础导引] 1.有甲、乙两个分子,甲分子固定不动,乙分子由无穷远处逐渐向甲靠近,直到不再靠近为止,在这整个过程中,分子势能的变化情况是() A.不断增大B.不断减小 C.先增大后减小D.先减小后增大 2.氢气和氧气的质量、温度都相同,在不计分子势能的情况下,下列说法正确的是() A.氧气的内能较大B.氢气的内能较大 C.两者的内能相等D.氢气分子的平均速率较大
高三数学第一轮复习教学案
天印中学2010届高三数学第一轮复习教学案 主备人:李松 2009-12-1立体几何2) 课题:线面平行与面面平行(B 级) 【教学目标】 1. 掌握直线与平面平行,判定定理和性质定理,并能运用它们进行论证和解决有关问题; 2. 掌握平面与平面平行,判定定理和性质定理,并能运用它们进行论证和解决有关问题。 〖走进课本〗——知识整理 1.直线与平面的位置关系有 ; ; 三种 2.直线与平面平行的判定定理: 用符号表示为 3.直线与平面平行的性质定理: 用符号表示为 4.两个平面平行的判定定理 有符号表示为 5.两个平面平行的性质定理 有符号表示为 〖基础训练〗——提神醒脑 1.直线a ⊥平面α,直线α||b ,则a 与b 的关系是( ) A.b a || B. b a ⊥ C. b a ,一定异面 D. b a ,一定相交 2.如果直线a 平行于平面α,则( ) A.平面α内有且只有一条直线与a 平行; B. 平面α内无数条直线与a 平行; C. 平面α内不存在与a 垂直的直线; D. 平面α内有且只有一条直线与a 垂直; 3.若直线a 与平面α内无数条直线平行,则a 与α的位置关系是( ) A.α||a B. α?a C.α||a 或α?a D. α?a 4.已知直线b a ,和平面α,那么b a ||的一个必要不充分的条件是( ) A.α||a ,α||b B. α⊥a ,α⊥b C. α?b 且α||a D. b a ,与α成等角 5.以下六个命题:其中正确命题的序号是 ①两个平面分别与第三个平面相交所得的两条交线平行,则这两个平面平行; ②平行于同一条直线的两个平面平行; ③平行于同一平面的两个平面平行; ④一个平面内的两相交直线与另一个平面内的两条相交直线分别平行,则这两个平面平行; ⑤与同一条直线成等角的两个平面平行; ⑥一个平面上不共线三点到另一平面的距离相等,则这两个平面平行;
高三物理一轮复习精品学案:动量守恒定律及“三类模型”问题
第2讲动量守恒定律及“三类模型”问题 一、动量守恒定律 1.内容 如果一个系统不受外力,或者所受外力的矢量和为零,这个系统的总动量保持不变. 2.表达式 (1)p=p′,系统相互作用前总动量p等于相互作用后的总动量p′. (2)m1v1+m2v2=m1v1′+m2v2′,相互作用的两个物体组成的系统,作用前的动量和等于作用后的动量和. (3)Δp1=-Δp2,相互作用的两个物体动量的变化量等大反向. (4)Δp=0,系统总动量的增量为零. 3.适用条件 (1)理想守恒:不受外力或所受外力的合力为零. (2)近似守恒:系统内各物体间相互作用的内力远大于它所受到的外力. (3)某一方向守恒:如果系统在某一方向上所受外力的合力为零,则系统在这一方向上动量守恒.
自测 1关于系统动量守恒的条件,下列说法正确的是() A.只要系统内存在摩擦力,系统动量就不可能守恒 B.只要系统中有一个物体具有加速度,系统动量就不守恒 C.只要系统所受的合外力为零,系统动量就守恒 D.系统中所有物体的加速度为零时,系统的总动量不一定守恒 答案 C 二、碰撞、反冲、爆炸 1.碰撞 (1)定义:相对运动的物体相遇时,在极短的时间内它们的运动状态发生显著变化,这个过程就可称为碰撞. (2)特点:作用时间极短,内力(相互碰撞力)远大于外力,总动量守恒. (3)碰撞分类
①弹性碰撞:碰撞后系统的总动能没有损失. ②非弹性碰撞:碰撞后系统的总动能有损失. ③完全非弹性碰撞:碰撞后合为一体,机械能损失最大. 2.反冲 (1)定义:当物体的一部分以一定的速度离开物体时,剩余部分将获得一个反向冲量,这种现象叫反冲运动. (2)特点:系统内各物体间的相互作用的内力远大于系统受到的外力.实例:发射炮弹、爆竹爆炸、发射火箭等. (3)规律:遵从动量守恒定律. 3.爆炸问题 爆炸与碰撞类似,物体间的相互作用时间很短,作用力很大,且远大于系统所受的外力,所以系统动量守恒. 自测
选修五第一章《认识有机化合物》综合测试题
选修五第一章《认识有机化合物》综合测试题 1.下列化学用语表达不正确的是() ①丙烷的球棍模型②丙烯的结构简式为CH3CHCH2 ③某有机物的名称是2,3-二甲基戊烷④与C8H6互为同分异构体 A.①②B.②③C.③④D.②④ 2.某烃的结构简式如图所示,若分子中共线碳原子数为a,可能共面的碳原子最多为b,含四面体结构碳原子数为c,则a、b、c分别是() A.3,4,5 B.4,l0,4 C.3,l0,4 D.3、14,4 3.某期刊封面上有如下一个常见分子的球棍模型图图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子,该模型图代表的有机物中含有的官能团是() A.氨基和羧基B.碳碳双键和羧基C.碳碳双键和羟基D.氨基和醛基 4.化学式为C4H8的链状烃有(考虑顺反异构体)() A.3种B.4种C.5种D.6种 5.根据下表中烃的分子式排列,判断空格中烃的同分异构体数目是() A.3 B.4 C.5 D.6 6.下列有机化合物的分类不正确的是()
7.下列化合物的1H-NMR谱图中吸收峰的数目不正确的是() 8.某有机物的结构简式如图所示,下列说法正确的是() A.1mol该物质可以和4molNaOH反应 B.分子中含有六种官能团 C.可发生加成反应、中和反应、水解反应、酯化反应、氧化反应和消去反应D.在水溶液中该有机物中的羟基和羧基均能电离出氢离子 9.在核磁共振氢谱中出现两组峰,其氢原子数之比为3∶2的化合物是()
A. B. C. D. 10.某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。下列说法中正确的是() ①该化合物仅含碳、氢两种元素②该化合物中碳、氢原子个数比为1∶4 ③无法确定该化合物是否含有氧元素④该化合物中一定含有氧元素 A.①②B.②④C.③④D.②③ 11.某烷烃的一个分子里含有9个碳原子,其一氯代物只有两种,该烷烃的名称是() A.正壬烷B.2,6-二甲基庚烷 C.2,2,4,4-四甲基戊烷D.2,3,4-三甲基己烷 12.下列名称的有机物实际上不可能存在的是() A.2,2-二甲基丁烷B.2-甲基-4-乙基-1-己烯 C.3-甲基-2-戊烯D.3,3-二甲基-2-戊烯 13.分子式为C4H9Cl的同分异构体(含对映异构)有() A.2种B.3种C.4种D.5种 14.列各组中的两种有机化合物,属于同系物的是() A.2-甲基丁烷和丁烷B.新戊烷和2,2-二甲基丙烷 C.间二甲苯和乙苯D.1-己烯和环己烷 15.柠檬烯具有特殊香气。可溶于乙醇或乙醚,不溶于水,其结构简式如图所示: 有关柠檬烯的说法正确的是()
高三数学第一轮复习 函数的奇偶性教案 文
函数的奇偶性 一、知识梳理:(阅读教材必修1第33页—第36页) 1、 函数的奇偶性定义: 2、 利用定义判断函数奇偶性的步骤 (1) 首先确定函数的定义域,并判断定义域是否关于原点对称; (2) 确定与的关系; (3) 作出相应结论 3、 奇偶函数的性质: (1)定义域关于原点对称; (2)偶函数的图象关于y 轴对称,奇函数的图象关于原点对称; (3)为偶函数 (4)若奇函数的定义域包含0,则 (5)判断函数的奇偶性,首先要研究函数的定义域,有时还要对函数式化简整理,但必须 注意使定义域不受影响; (6)牢记奇偶函数的图象特征,有助于判断函数的奇偶性; (7)判断函数的奇偶性有时可以用定义的等价形式: 4、一些重要类型的奇偶函数 (1)、f(x)= (a>0,a) 为偶函数; f(x)= (a>0,a) 为奇函数; (2)、f(x)= (3)、f(x)= (4)、f(x)=x+ (5)、f(x)=g(|x|)为偶函数; 二、题型探究 [探究一]:判断函数的奇偶性 例1:判断下列函数的奇偶性 1. 【15年北京文科】下列函数中为偶函数的是( ) A .2sin y x x = B .2cos y x x = C .ln y x = D .2x y -= 【答案】B 【解析】 试题分析:根据偶函数的定义()()f x f x -=,A 选项为奇函数,B 选项为偶函数,C 选项定 义域为(0,)+∞不具有奇偶性,D 选项既不是奇函数,也不是偶函数,故选B. 考点:函数的奇偶性. 2. 【15年广东文科】下列函数中,既不是奇函数,也不是偶函数的是( )
A .2sin y x x =+ B .2cos y x x =- C .122x x y =+ D .sin 2y x x =+ 【答案】A 【解析】 试题分析:函数()2 sin f x x x =+的定义域为R ,关于原点对称,因为()11sin1f =+,()1sin1f x -=-,所以函数()2sin f x x x =+既不是奇函数,也不是偶函数;函数 ()2cos f x x x =-的定义域为R ,关于原点对称,因为 ()()()()2 2cos cos f x x x x x f x -=---=-=,所以函数()2cos f x x x =-是偶函数;函数()122x x f x =+的定义域为R ,关于原点对称,因为()()112222x x x x f x f x ---=+=+=,所以函数()122 x x f x =+是偶函数;函数()sin 2f x x x =+的定义域为R ,关于原点对称,因为 ()()()sin 2sin 2f x x x x x f x -=-+-=--=-,所以函数()sin 2f x x x =+是奇函 数.故选A . 考点:函数的奇偶性. 3. 【15年福建文科】下列函数为奇函数的是( ) A .y x = B .x y e = C .cos y x = D .x x y e e -=- 【答案】D 【解析】 试题分析:函数y x = 和x y e =是非奇非偶函数; cos y x =是偶函数;x x y e e -=-是奇 函数,故选D . 考点:函数的奇偶性. [探究二]:应用函数的奇偶性解题 例3、【2014高考湖南卷改编】 已知)(),(x g x f 分别是定义在R 上的偶函数和奇函数,且1)()(23++=-x x x g x f ,则=+)1()1(g f ( ) A. 3- B. 1- C. 1 D. 3
第1讲 认识有机化合物
第1讲认识有机化合物 【 2021·备考】 2017版课程标准素养落地 1.了解常见有机物的结构,辨识有机物分子中的官能团并分析其化学性质,判断碳原子的饱和程度、键的类型。2.能辨识同分异构现象,书写符合特定条件的同分异构体,举例说明立体异构现象。 3.了解有机物分子式的确定方法,了解测定有机物分子结构的常用仪器分析方法(如质谱、红外光谱、核磁共振氢谱等),并分析判断有机物的分子结构。4.认识官能团的种类,依据官能团对有机物进分分类与命名。1.宏观辨识与微观探析:能从不同层次认识有机物的多样性,能按不同的标准对有机物进行分类,并认识有机物的组成、结构、性质和变化,形成“结构决定性质”的观念。能从宏观和微观相结合的视角分析与解决实际问题。 2.证据推理与模型认知:可以通过分析、推理等方法认识有机物的本质特征、构成要素及其相互关系,建立模型。能运用模型解释化学现象,揭示现象的本质和规律。 考点一有机化合物的分类及官能团的识别 『知识梳理』 1.根据分子组成中是否含有C、H以外的元素,分为烃和烃的衍生物。 2.根据分子中碳骨架的形状分类
3.按官能团分类 (1)相关概念 烃的衍生物:烃分子里的氢原子被其他原子或原子团所代替,衍生出一系列新的有机化合物。 官能团:决定化合物特殊性质的原子或原子团。 (2)有机物的主要类别、官能团和典型代表物。 类别官能团代表物名称、结构简式 烷烃甲烷CH4 烯烃 (碳碳双键) 乙烯CH2===CH2炔烃—C≡C—(碳碳三键) 乙炔HC≡CH 芳香烃苯 卤代烃—X(卤素原子) 溴乙烷C2H5Br 醇 —OH(羟基) 乙醇C2H5OH 酚苯酚C6H5OH 醚 (醚键) 乙醚 CH3CH2OCH2CH3 醛 (醛基) 乙醛CH3CHO
高三物理一轮复习 动能定理导学案
2012届高三物理一轮复习导学案 六、机械能(3) 动能定理 【导学目标】 1、正确理解动能的概念。 2、理解动能定理的推导与简单应用。 【知识要点】 一、动能 1、物体由于运动而具有的能叫动能,表达式:E k =_____________。 2、动能是______量,且恒为正值,在国际单位制中,能的单位是________。 3、动能是状态量,公式中的v 一般是指________速度。 二、动能定理 1、动能定理:作用在物体上的________________________等于物体____________,即w=_________________,动能定理反映了力对空间的积累效应。 2、注意:①动能定理可以由牛顿运动定律和运动学公式导出。②可以证明,作用在物体上的力无论是什么性质,即无论是变力还是恒力,无论物体作直线运动还是曲线运动,动能定理都适用。 3、动能定理最佳应用范围:动能定理主要用于解决变力做功、曲线运动、多过程动力学问题,对于未知加速度a 和时间t ,或不必求加速度a 和时间t 的动力学问题,一般用动能定理求解为最佳方案。 【典型剖析】 [例1] 在竖直平面内,一根光滑金属杆弯成如图所示形状,相应的曲线方程为y=2.5cos (kx+ 3 2 π)(单位: m),式中k=1 m -1 .将一光滑小环套在该金属杆上,并从x=0处以v 0=5 m/s 的初 速度沿杆向下运动,取重力加速度g=10 m/s 2 .则当小环运动到x= 3 m 时的速度大小v= m/s;该小环在x 轴方向最远能运动到x= m 处. [例2]如图所示,质量为m 的小球用长为L 的轻细线悬挂在天花板上,小球静止在平衡位置.现用一水平恒力F 向右拉小球,已知F=0.75mg ,问: (1)在恒定拉力F 作用下,细线拉过多大角度时小球速度最大?(2)小球的最大速度是多少? [例3]总质量为M 的列车,沿平直轨道作匀速直线运动,其末节质量为m 的车厢中途脱钩,待司机发觉时,机车已行驶了L 的距离,于是立即关闭油门撤去牵引力.设运动过程中阻力始终与质量成正比,机车的牵引力是恒定的.当列车的两部分都停止时,它们之间的距离是多少?
高考化学培优专题复习认识有机化合物练习题含答案
高考化学培优专题复习认识有机化合物练习题含答案 一、认识有机化合物练习题(含详细答案解析) 1.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。它能在酸性溶液中能发生如下反应: (1)有机物(I)在铂催化下与足量的氢气发生加成反应生成物质X,X所含的官能团的名称是 __________;X的结构简式为__________。 (2)有机物(II)的化学式为_______;分子中化学环境不同的氢原子共有_____种。 (3)下列关于MMF说法正确的是__________(选填字母编号)。 a.能溶于水 b.1 mol MMF最多能与3 mol NaOH完全反应 c.能发生取代反应和消去反应 d.镍催化下1 mol MMF最多能与6 mol H2发生加成反应 (4)1 mol的有机物(I)在单质铜和氧气的作用下可以氧化为醛基的—OH有____mol;有机物(II)在加热和浓硫酸的条件下发生消去反应的化学方程式为_________。 【答案】羧基、羟基 C6H13O2N 5 b 1 【解析】 【分析】 (1)有机物(I)在铂催化下与足量的H2发生加成反应生成物质X,和H2发生加成反应的是苯环和碳碳双键,根据有机物(Ⅰ)结构判断X的结构,根据X的结构判断含有的官能团。 (2)根据断键方式和原子守恒判断有机物(Ⅱ)的化学式,断键物质为酯基,根据氢原子的物质判断其种类。 (3)根据MMF的结构判断其性质,MMF中含有的官能团是酚羟基、碳碳双键、酯基,可能具有酚、酯和烯烃的性质。 (4)连有醇羟基的碳原子上有2个氢原子时,醇羟基才能发生催化氧化生成醛;醇若能发生消去反应,消去反应后生成物含有碳碳双键。 【详解】 (1)有机物(Ⅰ)在铂催化下与足量的H2发生加成反应生成物质X,能和H2发生加成反应的是
第一章:认识有机化合物全套测试卷及答案
第一章各节测试题 第一、二节 有机化合物的分类、结构特点 小测 班级__________________________学号_____________ ( )1、有机化学主要研究有机化合物所发生的反应,下列化合物中不是有机物的是 A 、CO 2 B 、C 2H 6 C 、HCHO D 、CH 3OH ( )2、自然界中化合物的种类最多的是 A 、无机化合物 B 、有机化合物 C 、铁的化合物 D 、碳水化合物 ( )3、某有机物的结构如右图,它不具有的官能团是 A 、 —C — B 、—OH C 、 C C D 、—Cl ( )4、观察以下物质的结构 CH CH 3 CH 32H 5 CH 3 ,它的主链上含有______个碳原子, A 、四个 B 、五个 C 、六个 D 、七个 ( )5、乙醇(CH 3CH 2OH )和二甲醚(CH 3—O —CH 3)互为_______的同分异构体, A 、位置异构 B 、官能团异构 C 、手性异构 D 、碳链异构 ( )6、甲烷分子中C —H 键的键角为 A 、120O 20’ B 、112 O 30’ C 、109 O 28’ D 、60 O ( )7、戊烷(C 5H 12)的同分异构体共有_____个 A 、2个 B 、3个 C 、4个 D 、5个 ( )8、四氯化碳按官能团分类应该属于 A 、烷烃 B 、烯烃 C 、卤代烃 D 、羧酸 ( )9、下列化学式只能表示一种物质的是 A 、C 3H 8 B 、C 4H 10 C 、C 4H 8 D 、C 2H 4Cl 2 ( )10、0.1mol 化合物甲在足量的氧气中完全燃烧后生成4.48LCO 2(标况下测量),推测甲是 A 、CH 4 B 、C 2H 4 C 、C 2H 6 D 、C 6H 6 11、用直线连接有机物和它所对应的类别: CH 3CH 2CH 3 CH 2=CH —CH 3 CH 3COOCH 3 CH 3—C —H || O H 3C —OH CH 3CH 2COOH 12、戊烷(C 5H 12)的某种同分异构体只有一种一氯代物,试书写它的结构简式和键线式。 酯 羧酸 醛 醇 烯烃 烷烃
2019-2020最新高三数学一轮复习第1讲集合教案
——教学资料参考参考范本——2019-2020最新高三数学一轮复习第1讲集合教案 ______年______月______日 ____________________部门
课标要 求1.集合的含义与表示 (1)通过实例,了解集合的含义,体会元素与集合的“属于”关系; (2)能选择自然语言、图形语言、集合语言(列举法或描述法)描述不同的具体问题,感受集合语言的意义和作用; 2.集合间的基本关系 (1)理解集合之间包含与相等的含义,能识别给定集合的子集; (2)在具体情境中,了解全集与空集的含义; 3.集合的基本运算 (1)理解两个集合的并集与交集的含义,会求两个简单集合的并集与交集;(2)理解在给定集合中一个子集的补集的含义,会求给定子集的补集;(3)能使用Venn图表达集合的关系及运算,体会直观图示对理解抽象概念的作用。 命题走 向 有关集合的高考试题,考查重点是集合与集合之间的关系,近年试题加强了对集合的计算化简的考查,并向无限集发展,考查抽象思维能力,在解决这些问题时,要注意利用几何的直观性,注意运用Venn图解题方法的训练,注意利用特殊值法解题,加强集合表示方法的转换和化简的训练。考试形式多以一道选择题为主,分值5分。 预测2017年高考将继续体现本章知识的工具作用,多以小题形式出现,也会渗透在解答题的表达之中,相对独立。具体题型估计为: (1)题型是1个选择题或1个填空题; (2)热点是集合的基本概念、运算和工具作用。 教 学 准 备 多媒体
教学过程要点精讲: 1.集合:某些指定的对象集在一起成为集合。 (1)集合中的对象称元素,若a是集合A的元素,记作A a∈;若b不是集 合A的元素,记作A b?; (2)集合中的元素必须满足:确定性、互异性与无序性; 确定性:设A是一个给定的集合,x是某一个具体对象,则或者是A的元素,或者不是A的元素,两种情况必有一种且只有一种成 立; 互异性:一个给定集合中的元素,指属于这个集合的互不相同的个体(对象),因此,同一集合中不应重复出现同一元素; 无序性:集合中不同的元素之间没有地位差异,集合不同于元素的排列顺序无关; (3)表示一个集合可用列举法、描述法或图示法; 列举法:把集合中的元素一一列举出来,写在大括号内; 描述法:把集合中的元素的公共属性描述出来,写在大括号{}内。 具体方法:在大括号内先写上表示这个集合元素的一般符号及取值(或变 化)范围,再画一条竖线,在竖线后写出这个集合中元素所具有的共同特征。 注意:列举法与描述法各有优点,应该根据具体问题确定采用哪种表示 法,要注意,一般集合中元素较多或有无限个元素时,不宜采用列举法。 (4)常用数集及其记法: 非负整数集(或自然数集),记作N; 正整数集,记作N*或N + ; 整数集,记作Z; 有理数集,记作Q; 实数集,记作R。 2.集合的包含关系: (1)集合A的任何一个元素都是集合B的元素,则称A是B的子集(或 有的学 生对整 数包括 哪些数 还不太 清楚, 后面还 要通过 具体题 目增强 认识。
