硫化碱生产工艺流程复习过程
硫化钠的生产工艺

硫化钠的生产工艺
硫化钠是一种重要的化工原料,广泛应用于造纸、纺织、玻璃、草酸等行业,以下为硫化钠的生产工艺。
硫化钠通常采用传统的还原硫化法生产。
主要步骤如下:
1. 原料准备:原料主要包括硫酸钠和硫粉。
硫酸钠通常通过钠盐与硫酸反应制得,硫粉主要是通过硫磺的提纯和粉碎得到。
2. 反应槽装载:将一定比例的硫酸钠和硫粉按照配比放入反应槽中。
同时加入一定量的水,使反应槽内的温度保持在适宜的范围。
3. 反应:将混合物进行充分搅拌,并加热至适宜的温度,通常为120-160摄氏度,加热时间一般为1-2小时。
在反应槽内进
行还原反应,硫粉与硫酸钠反应生成硫化钠。
4. 沉淀:反应完成后,关闭加热装置,将生成的硫化钠悬浊液放置静置,使其中的硫化钠沉淀到底部。
5. 过滤和洗涤:将底部的硫化钠沉淀进行过滤,得到的硫化钠固体产品,然后用适量的水对其进行洗涤,以除去其中的杂质。
6. 干燥和包装:将洗涤后的硫化钠固体产物进行脱水干燥,通常采用红外或热风等方法进行脱水。
脱水后的硫化钠即为成品,可以进行包装。
以上就是硫化钠的生产工艺。
在实际生产过程中,需要注意反应温度、反应时间、原料质量比等控制参数,以确保产品质量和生产效率。
硫化碱脱硫、膜吸收脱硫、微生物脱硫技术及工艺与优缺点图文并茂详解
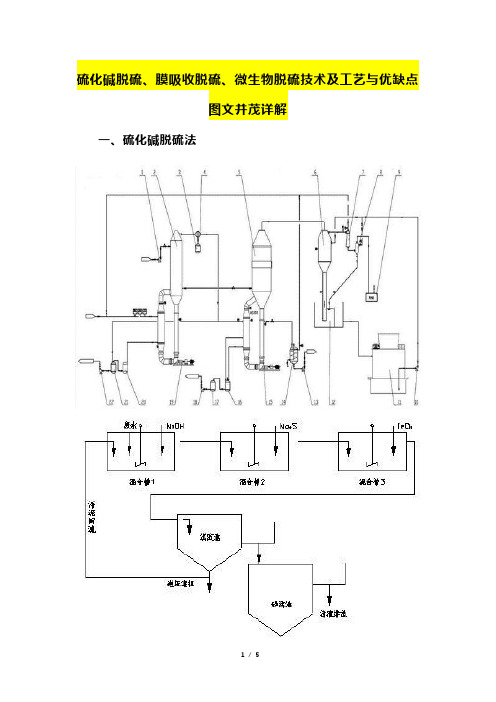
硫化碱脱硫、膜吸收脱硫、微生物脱硫技术及工艺与优缺点图文并茂详解一、硫化碱脱硫法硫化碱脱硫法主要利用工业级硫化纳作为原料来吸收SO2工业烟气,产品以生成硫磺为目的。
反应过程相当复杂,有Na2SO4、Na2SO3、Na2S203、S、Na2Sx等物质生成,由生成物可以看出过程耗能较高,而且副产品价值低,过程中的各种硫的化合物含量随反应条件的改变而改变,将溶液pH值控制在5.5—6.5之间,加入少量起氧化作用的添加剂TFS,则产品主要生成Na2S203,过滤、蒸发可得到附加值高的5H 0·Na2S203,而且脱硫率高达97%,反应过程为:SO2 Na2S=Na2S203 S。
二、膜吸收脱硫法以有机高分子膜为代表的膜分离技术是一种气体分离新技术,已得到广泛的应用,尤其在水的净化和处理方面。
利用膜来吸收脱出SO2气体,效果比较显著,脱硫率达90%。
过程是:他们利用聚丙烯中空纤维膜吸收器,以NaOH溶液为吸收液,脱除SO2气体,其特点是利用多孔膜将气体SO2气体和NaOH吸收液分开,SO2气体通过多孔膜中的孔道到达气液相界面处,SO2与NaOH迅速反应,达到脱硫的目的。
此法是膜分离技术与吸收技术相结合的一种新技术,能耗低,操作简单,投资少。
三、微生物脱硫技术根据微生物参与硫循环的各个过程,并获得能量这一特点,利用微生物进行烟气脱硫。
机理为:在有氧条件下,通过脱硫细菌的间接氧化作用,将烟气中的SO2氧化成硫酸,细菌从中获取能量。
生物法脱硫与传统的化学和物理脱硫相比,基本没有高温、高压、催化剂等外在条件,均为常温常压下操作,而且工艺流程简单,无二次污染。
以地热发电站每天脱除5t量的H:S为基础;计算微生物脱硫的总费用是常规湿法50%。
无论对于有机硫还是无机硫,一经燃烧均可生成被微生物间接利用的无机硫SO2,微生物烟气脱硫技术在实验室条件下,选用氧化亚铁杆菌进行脱硫,在较低的液气比下,脱硫率达98%。
硫化钠制备及工艺

硫化钠设计专篇一、性质1、化学分式Na2S2、化学分子量78.043、结构组织纯品的硫化钠为无色结晶粉末,工业品是带不同结晶水的混合物,并含有杂质,其色泽呈粉红色、棕红色、土黄色等,密度、熔点、沸点也因组成不同而异。
硫化钠吸潮性强。
易溶于水,微溶于乙醇,不溶于醚。
其水溶液呈强碱性反应,触及皮肤和毛发时会造灼伤。
故硫化钠俗称硫化碱。
在空气中易氧化,遇强酸会产生硫化氢。
可与多种重金属盐溶液反应生成难溶于水的金属硫化物沉淀。
二、用途硫化钠在工业用途中十分广泛,在染料工业中用以制造硫化染料,硫化青、硫化蓝或染料中间体还原剂、媒染剂等。
在有色冶金工业中用作矿石的浮选剂。
制革工业中生皮的脱毛剂。
造纸工业中纸张的蒸煮剂。
硫化钠还用于硫化硫酸钠,多硫化钠,硫氢化钠等产品的制造。
在电镀中用于氰化镀锌,镀银镉合金电解液中以及回收银。
也广泛用于颜料、橡胶等工业中。
并在很多日用化工,水处理中使用。
三、生产方法碳还原法:将硫酸钠溶解用白煤或白煤的替代物还原而得。
该工艺成熟,生产设备及操作简单,原料价廉且来源方便。
四、主要制法流程(附图)将Na2SO4用自动上料机打入料斗,送入燃烧室内,用煤气进行吹烧,当温度达到884°d时硫酸钠变成液态物质。
溶解后的硫酸钠化学物质变得不稳定,SO4很容易被分解。
用黄磷煤气中的一氧化碳对原子进行化学置换,其反应如下:Na2SO4+4CO Na2S+4CO2当炉内的火焰从兰色的火焰变成红色的火焰时,一氧化碳的置换反应就进入终结,这时的一氧化碳只能作为燃料对炉内进一步升温。
当温度升至1100°d 时加入少量的白煤,观察炉内,当炉内有黄色烛炪现即为反应终点。
其化学反应如下:Na2SO4+2C Na2S+2CO2反应好的含Na2S70%左右的黑灰熔体出料,稍经冷却后放入化碱器内,用5-8°Be´碱化液注入化碱器,让Na s S大量溶入水中。
当水到一定量时浸泡30分钟,即放入洗渣器内。
硫化钠工艺流程

硫化钠工艺流程一、工艺概述硫化钠是一种重要的化工原料,广泛应用于纺织、皮革、造纸、橡胶、化肥等行业。
硫化钠的制备工艺主要包括石灰石焙烧、石灰石浸出、硫化渣的提取、硫湿粉的合成和产品精制等环节。
目前主要的工艺流程包括火法制备和湿法制备两种,其中湿法制备是目前较为常用的制备工艺。
二、湿法制备硫化钠的工艺流程湿法制备硫化钠主要通过石灰石的焙烧、浸出、硫化渣的提取、硫化渣的水热分解和精制等环节制备得到。
下面将详细介绍湿法制备硫化钠的工艺流程。
1. 原料准备硫化钠的原料主要有石灰石、硫磺和氯化钠。
石灰石是制备硫化钠的主要原料,需要经过破碎、干燥和颗粒化等处理后用于焙烧。
硫磺用于硫化渣的提取,需要研磨成粉末状。
氯化钠用于精制硫化钠产品,需要经过晒制、干燥和粉碎等处理。
2. 石灰石的焙烧石灰石经过破碎、干燥和颗粒化处理后,装入焙烧炉内进行焙烧。
焙烧炉内加热至高温后,石灰石中的碳酸钙将发生分解反应,生成氧化钙和二氧化碳。
氧化钙是硫酸分解生成硫酸的主要原料。
3. 石灰石的浸出经过焙烧后的石灰石将被送入浸出罐中进行浸出处理。
在浸出过程中,向浸出罐中加入足量的水,使氧化钙与水发生反应生成氢氧化钙。
产生的氢氧化钙与硫磺反应生成硫化钙。
4. 硫化渣的提取浸出后的石灰石浆液将被送入硫化渣提取罐中进行提取处理。
在提取罐中,将硫化渣与水混合,使硫化渣溶解于溶液中,生成硫化钠溶液。
经过过滤、离心和浓缩处理,可得到含有硫化钠的硫化渣溶液。
5. 硫化渣的水热分解硫化渣溶液经过水热分解后,会分解生成二硫化钠和硫磺。
水热分解是利用高温高压条件下,加氢硫酸钠钠盐结晶水的热裂解产生。
饱和度较低的硫化钠结晶将被另外一部分剖离和分解,用来生成二氧化气体同时还有些硫石膏生成。
6. 产品精制精制硫化钠产品主要包括结晶、过滤、干燥和包装等步骤。
经过结晶处理后,硫化钠产品将用于过滤,使得溶液中的杂质得到去除。
过滤后的硫化钠产品将被送入干燥设备进行干燥处理,最后经过包装,成为成品硫化钠产品。
硫化钠生产中热溶工序的探讨分析

第6期硫化钠生产中热溶工序的探讨分析25生产与应用:硫化钠生产中热溶工序的探讨分析华国友(丹棱县应急管理局,四川眉山,620200)摘要介绍煤还原法生化钠工艺与热溶工序的三种工艺,以及这三种工艺的优缺点。
对解决安题的转式热溶和强化热溶进行了分析比较,并提出了#关键词:硫化钠热溶对比硫化钠,化学式为Na?S,俗称硫化碱,广泛应用于染料、制革、纺织和工业;在有色冶金工业中用作矿石的浮选剂。
目前,国内绝分厂家硫化生产工艺为煤还原芒硝法,而热溶(又称热化、热浸和化碱)工序是生产中一个重要环节,传统工艺采用自#,传统自然浸取工艺已不能满安全、环保的生产需求,为此,一些热溶的新工艺渐被开发应用。
本文针对热溶新工艺进行分析。
1硫化钠生产工艺流程硫化钠生产的主要化学反应式为:Na SO4+ 2C=Na S+2CO?。
硫化钠目前生产工艺如图1所示。
无水硫酸钠和料煤按一定比例(约10:3)进行计量配比,混合后送入转炉内,在高温(900—11500$%下锻烧还原生成硫化钠粗碱熔体(半成品,俗称“灰饼”,含Na?S 质量分数65%—70%口%)。
灰饼用低浓度的热碱液(约80C)2进行热溶解浸取,产生的浓碱液转入澄清桶,碱渣(主要成分为不溶解的煤渣)经多次热水后综合利用。
澄清后,澄清桶内上层清液转入蒸发工序进行蒸发浓缩,浓缩后的碱液(Na S 含量60%以上)送入制片工序进行制片包装,制得状硫化钠产品。
澄清桶底部沉降下来的下层碱泥液转入压滤机,经多次洗涤、压滤,再经烘干后综合利用,洗涤水返回热溶工序和洗泥回用。
炉产生的烟气经余热锅炉回收热量、除尘、脱硫脱硝后达标排放,热溶尾气经洗涤后达标排放。
热锅炉产生的蒸汽用于蒸发工序,蒸汽不足部分由另的锅炉供给。
图1硫化钠生产工艺流程图i锻烧—片余热回收—[灰饼i热溶一碱渣[碱液I澄清下层碱泥J!_[上层碱液i蒸发j I—i制片包装—厂2热溶工艺介绍化生,热工的主要目的是饼的有效成分硫化钠几乎全部溶解进入液相,并实现固液分离,控制生成浓度为25%—30%$啲浓碱液。
硫化碱生产工艺流程图

.2 工艺流程说明本项目对原装置部分使用价值较高的设备进行搬迁.生产工艺流程仍按照搬迁前的进行设计.以焦炭粉为还原剂.采用含铬芒硝和脱水芒硝为原料生产工业低铁硫化碱。
生产工序主要包括备料上料工序、煅烧工序、化坯洗渣工序、沉淀洗泥工序、低铁硫化碱制液工序、蒸发工序、制片包装工序。
工艺流程如下:<1> 备料上料工序由于十水芒硝不能满足硫化碱生产原料的要求.首先要对十水芒硝进行脱水处理。
十水芒硝先进入化硝罐.加入热水进行溶解.溶解液体进入蒸发器进行蒸发.蒸发热源采用蒸发工序二次蒸汽.蒸发液送入结晶罐进行冷却结晶.然后再通过皮带输送机送至离心机进行离心分离.分离后的固体为无水芒硝.送至仓库备用.离心母液再返回至蒸发器中进行循环。
原料含铬芒硝和脱水芒硝分别存入专门的储仓.经过破碎后保证进入工艺系统的芒硝粒径不超过50mm.芒硝、焦炭粉分别通过斗式提升机、皮带计量机送至混料机.按一定比例混合.再通过混料皮带输送机送入储料仓.然后经送料螺旋机送入煅烧工序。
<2> 煅烧工序物料在长转炉<Φ2500×45000>内进行还原反应所需的热量由燃料煤燃烧提供。
燃料煤由煤库经皮带输送机送至雷蒙机研磨后.再用斗式提升机送到煤粉仓.由皮带输送机送到炉头煤粉斗.再经下端送料螺旋机送入送风管道内.由罗茨鼓风机吹入长转炉内燃烧。
来自储料仓的芒硝与焦炭粉先进入预热器.然后进入长转炉尾部.燃料煤粉从转炉头部进入.与原料成逆向流动.当炉内温度为1050-1150℃时.芒硝与焦炭粉发生如下化学反应:Na2SO4+2C+→Na2S+2CO2生成硫化碱;Cr6++C→Cr3+毒性较大的Cr6+变为无毒稳定的Cr6+;同时.在有水蒸汽存在条件下.发生副反应Na2S+CO2+H2O→Na2CO3+H2S生成碳酸钠和硫化氢。
物料在转炉内经预热、熔化、沸腾、成熟制得熔体黑灰.从炉头送入热熔罐中.进入化坯洗渣工序.进行热溶。
制碱工艺流程

制碱工艺流程制碱是指将氢氧化钠或者碳酸钠等碱性物质的生产过程。
碱性物质在工业生产中有着广泛的应用,比如用于造纸、化工、冶金和石油等行业。
在下面的文章中,我们将会详细介绍碱的制备工艺流程。
原料准备制碱的原料主要包括盐类矿石和电解液两种。
盐类矿石是碱制备的主要原料,主要有岩盐、卤化镁、卤化钾和石灰等。
电解液则是在电解盐溶液时形成氢氧化汗或者氯化铝等。
焙烧盐类矿石需要进行焙烧来脱除其结晶水和二氧化碳等杂质。
通常情况下,焙烧的温度会根据不同的矿石种类和含量而有所不同。
比如岩盐的焙烧温度需要在600-800摄氏度。
溶解经过焙烧后的盐类矿石需要进行溶解,通常可采用热水淋滤的方式,在溶解过程中,因为氯化镁和卤化钾的成分实心比较难溶于水,所以需要采用硫酸甩钾和硫酸脱氯铝的方式分离产生的氯碱液,并借此生成NaCl。
电解经过溶解的盐类矿石会形成氯化物的溶液,然后将溶液经过离子膜电解的方式进行电解,电解会将Na和Cl分别析出为钠和氯气,从而生成氢氧化钠。
析出经过电解生成的氢氧化钠需要通过湿法或者干法来进行析出,湿法就是用纯化的盐水来析出,而干法是通过排水除去水分。
在析出过程中,需要根据要求的浓度来控制水分,通常情况下浓度为10% ~ 30%。
精制经过析出的氢氧化钠需要进行精制,以去除杂质和提高纯度。
精制的方法主要包括晒盐、蒸馏和结晶,其中结晶法是最为常用的一种。
包装经过精制的氢氧化钠需要进行包装,通常采用25kg、50kg或者500kg的包装袋来进行包装,以便于销售和储存。
质检氢氧化钠的产品需要进行质检,主要检测其纯度、颗粒度和水分等指标。
通常情况下,氢氧化钠的纯度要求在96%以上,颗粒度要求在40目-60目之间,水分不得超过2%。
储存经过质检的氢氧化钠产品需要进行储存,通常情况下储存的环境要求干燥通风,避免日晒和雨淋,避免与酸性物质和有机物质接触。
氢氧化钠一般在室内储存,不得超过一年。
供应最后,经过储存的氢氧化钠产品需要按照客户的需求进行供应,包括散装和包装的供应。
硫化钠制备及工艺

硫化钠设计专篇一、性质1、化学分式Na2S2、化学分子量78.043、结构组织纯品的硫化钠为无色结晶粉末,工业品是带不同结晶水的混合物,并含有杂质,其色泽呈粉红色、棕红色、土黄色等,密度、熔点、沸点也因组成不同而异。
硫化钠吸潮性强。
易溶于水,微溶于乙醇,不溶于醚。
其水溶液呈强碱性反应,触及皮肤和毛发时会造灼伤。
故硫化钠俗称硫化碱。
在空气中易氧化,遇强酸会产生硫化氢。
可与多种重金属盐溶液反应生成难溶于水的金属硫化物沉淀。
二、用途硫化钠在工业用途中十分广泛,在染料工业中用以制造硫化染料,硫化青、硫化蓝或染料中间体还原剂、媒染剂等。
在有色冶金工业中用作矿石的浮选剂。
制革工业中生皮的脱毛剂。
造纸工业中纸张的蒸煮剂。
硫化钠还用于硫化硫酸钠,多硫化钠,硫氢化钠等产品的制造。
在电镀中用于氰化镀锌,镀银镉合金电解液中以及回收银。
也广泛用于颜料、橡胶等工业中。
并在很多日用化工,水处理中使用。
三、生产方法碳还原法:将硫酸钠溶解用白煤或白煤的替代物还原而得。
该工艺成熟,生产设备及操作简单,原料价廉且来源方便。
四、主要制法流程(附图)将Na2SO4用自动上料机打入料斗,送入燃烧室内,用煤气进行吹烧,当温度达到884°d时硫酸钠变成液态物质。
溶解后的硫酸钠化学物质变得不稳定,SO4很容易被分解。
用黄磷煤气中的一氧化碳对原子进行化学置换,其反应如下:Na2SO4+4CO Na2S+4CO2当炉内的火焰从兰色的火焰变成红色的火焰时,一氧化碳的置换反应就进入终结,这时的一氧化碳只能作为燃料对炉内进一步升温。
当温度升至1100°d 时加入少量的白煤,观察炉内,当炉内有黄色烛炪现即为反应终点。
其化学反应如下:Na2SO4+2C Na2S+2CO2反应好的含Na2S70%左右的黑灰熔体出料,稍经冷却后放入化碱器内,用5-8°Be´碱化液注入化碱器,让Na s S大量溶入水中。
当水到一定量时浸泡30分钟,即放入洗渣器内。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.2.1.2 工艺流程说明
本项目对原装置部分使用价值较高的设备进行搬迁,生产工艺流程仍按照搬迁前的进行设计,以焦炭粉为还原剂,采用含铬芒硝和脱水芒硝为原料生产工业低铁硫化碱。
生产工序主要包括备料上料工序、煅烧工序、化坯洗渣工序、沉淀洗泥工序、低铁硫化碱制液工序、蒸发工序、制片包装工序。
工艺流程如下:
(1) 备料上料工序
由于十水芒硝不能满足硫化碱生产原料的要求,首先要对十水芒硝进行脱水处理。
十水芒硝先进入化硝罐,加入热水进行溶解,溶解液体进入蒸发器进行蒸发,蒸发热源采用蒸发工序二次蒸汽,蒸发液送入结晶罐进行冷却结晶,然后再通过皮带输送机送至离心机进行离心分离,分离后的固体为无水芒硝,送至仓库备用,离心母液再返回至蒸发器中进行循环。
原料含铬芒硝和脱水芒硝分别存入专门的储仓,经过破碎后保证进入工艺系统的芒硝粒径不超过50mm,芒硝、焦炭粉分别通过斗式提升机、皮带计量机送至混料机,按一定比例混合,再通过混料皮带输送机送入储料仓,然后经送料螺旋机送入煅烧工序。
(2) 煅烧工序
物料在长转炉(Φ2500×45000)内进行还原反应所需的热量由燃料煤燃烧提供。
燃料煤由煤库经皮带输送机送至雷蒙机研磨后,再用斗式提升机送到煤粉仓,由皮带输送机送到炉头煤粉斗,再经下
端送料螺旋机送入送风管道内,由罗茨鼓风机吹入长转炉内燃烧。
来自储料仓的芒硝与焦炭粉先进入预热器,然后进入长转炉尾部,燃料煤粉从转炉头部进入,与原料成逆向流动,当炉内温度为1050-1150℃时,芒硝与焦炭粉发生如下化学反应:
Na2SO4+2C+→Na2S+2CO2 生成硫化碱;
Cr6++C→Cr3+ 毒性较大的Cr6+变为无毒稳定的Cr6+;
同时,在有水蒸汽存在条件下,发生副反应
Na2S+CO2+H2O→Na2CO3+H2S 生成碳酸钠和硫化氢。
物料在转炉内经预热、熔化、沸腾、成熟制得熔体黑灰,从炉头送入热熔罐中,进入化坯洗渣工序,进行热溶。
每台转炉配套一台特制预热器,高温转炉烟气先经过预热器对生料进行预热,然后经降尘室降尘,再用麻石水膜除尘器进行除尘,除尘后进入脱硫塔进行脱硫,达标后排空。
回收粉尘经过酸洗后外运至园区指定地点,可用作制砖。
(3)化坯洗渣工序
由煅烧工序来的熔融态黑灰由炉头直接进入热溶罐进行热溶,在搅拌机的作用下,用沉淀洗泥工序的洗渣水(稀卤水)直接制取浓卤碱水,当溶液中Na2S浓度达到23%左右时,用浓卤液下泵将其打至沉淀罐,沉淀罐上层清液送至沉淀洗泥工序浓卤储槽。
沉淀泥渣经过一号铰刀输送至一洗罐,在一洗罐中进一步浸取泥渣中含有的Na2S,一洗罐洗净的渣泥经二号绞刀送至二洗罐,当渣泥中碱含量小于1%时,将渣泥进行酸洗后外运至园区指定地点。
洗
渣用水为沉淀洗泥工序送来的洗泥水(稀卤水),洗渣水送至热熔罐循环使用。
化坯过程中,Na2S与H2O反应产生少量的H2S气体,故热溶罐为封闭装置,热溶过程中产生的碱雾及H2S气体经喷淋塔洗涤后,由高度为15m的排气筒排空,洗涤液循环使用,浓度增加至一定值时送至热溶罐;喷淋塔污泥定期排至热溶罐,供化坯用。
(4)沉淀洗泥工序
由化坯工序来的浓度为23%的浓卤碱水进入浓卤储槽,通过浓卤泵送入低铁澄清罐中,通入蒸汽,加热浓卤水碱水至70-80℃后恒温静置16小时以上,然后经过浓卤泵送至箱式压滤机进行压滤,压滤后合格的23%的清液送至浓卤清液中转槽中,然后用清液泵送至低铁反应罐进行制备低铁硫化碱。
滤渣卸至洗泥地罐,热水洗涤,当洗涤液中碱含量小于1%时,将渣泥送至酸洗罐进行酸洗后外运至园区指定地点,用于制砖。
洗泥水送至化坯洗渣工序化坯用。
(5)低铁硫化碱制液工序
制备原理:硫化碱浓卤中的铁是以FeS的胶团微粒形式存在,并处于亚稳定状态。
由于浓卤中含有较多的Na2CO3、Na2SO4、Na2S2O3、Na2SO3等可溶性杂质,会影响产品的质量和颜色,本工艺选择加入硫化钡溶液和氧化锌,硫化钡溶液可与这些杂质生成沉淀而除去,硫酸锌和硫化钠生成硫化锌沉淀,沉淀的生成破坏了溶液中FeS胶粒的稳定性,同时生成的沉淀将FeS微粒包裹、吸附、共沉淀,从而达到除铁目的。
工艺流程:
1)硫化钡的制备
焦炭粉和重晶石分别通过斗式提升机、下料管预热器。
然后送入原小长转炉(Φ2000×32000)内进行高温煅烧,煅烧热源同煅烧芒硝相同,燃料煤粉由罗茨鼓风机吹入长转炉内燃烧,与重晶石成逆向流动,当炉内温度为1100℃左右时,重晶石与焦炭粉发生如下化学反应: BaSO4+2C+→BaS+2CO2 生成硫化钡。
转炉烟气先经过预热器回收余热,加热生料重晶石,然后再用麻石水膜除尘器进行除尘,除尘后进入脱硫塔进行脱硫,达标后排空。
回收粉尘与渣泥一同经过酸洗外运至园区指定地点,用于制砖。
2)硫化钡溶液的制备
煅烧来的熔融态黑灰由炉头直接进入硫化钡浸取槽进行热溶,在电机搅拌的作用下,用新鲜水直接制取硫化钡溶液,洗涤至一定浓度后,将硫化钡溶液送至硫化钡溶液储罐备用。
硫化钡溶液制取工艺流程简图
3)低铁硫化碱制液
浓卤清液进入低铁反应罐后,将配制好的硫化钡溶液及氧化锌加入到低铁反应罐内搅拌20min左右,使溶液中的Na2CO3、Na2SO4、FeS等杂质充分与除铁剂反应,静置16-24h后,将沉淀下的不溶物通过溜槽排放到低铁地下泥槽,然后将泥渣送至沉淀洗泥工序洗泥地罐进行洗泥;除杂后的澄清液用低铁清液泵送至低铁清液储槽中以备蒸发。
(6)蒸发工序
将低铁清液送入列管蒸发器,通入蒸汽进行加热真空浓缩,当碱液浓缩至34-38%时,调整碱液温度到100℃,直接浓缩至60%后,通过成品液泵打入成品罐。
蒸发产生的二次蒸汽送至备料上料工序,用作制备无水芒硝,蒸汽冷凝生成的冷凝水送回锅炉装置。
(7)制片包装工序
由成品罐来的60%浓卤液经泵缓慢送至制片机,经冷却后得到低铁硫化碱,通过皮带输送机输送到自动包装机料斗,包装后送库房储存待售。
低铁硫化碱工艺流程简图
4.2.2 物料平衡说明
物料平衡图见附图3。
4.2.3 工艺消耗定额
原材料及动力消耗定额
4.3 主要设备选择
本项目属于搬迁项目,为了减少投资,只淘汰部分落后及废旧设备,其余设备仍用以前硫化碱生产设备,本项目主要设备选择如下:
一、搬迁设备
(1)雷蒙机:燃料煤每小时消耗量为2.96t,原厂5R4018摆式磨煤机1台,磨煤量为2~5t/h,可满足本项目使用要求。
(2)长转炉:煅烧芒硝,炉长度45米,炉体直径2.5m,共2台;煅烧重晶石,炉长度32米,炉体直径2m,共1台,转炉内砌筑高铝耐火砖,另外附属设备有转炉减速机、托辊、托带、挡轮、密封装置等,可满足本项目使用要求。
(3)沉淀罐:沉淀浓卤碱液中的较大颗粒渣体,入口设有隔板,外设保温层,设备直径3米。
(4)蒸发器:按照进液浓度和蒸发使用蒸汽的温度进行计算,仍用以前换热面积为43m2和120m2的强制外循环蒸发器各1台,换热面积为90m2的强制外循环蒸发器2台,能够保证生产正常运行。
(5)制片机:浓度为60%的片碱产量为4.8t/h,因此设计中选择5台生产能力为1 t/h的制片机。
二、新增更换设备
(1)热化罐:设备附件有搅拌装置和布料盘,考虑到物料的冲刷腐蚀等因素,设备壁厚应选δ=20 mm;考虑劳保卫生条件,化灰槽上方设置集气罩。
(2)钡卤浸取箱:钢板厚度δ=20mm;内设搅拌桨,设备尺寸为长5米,宽1.6米,高1米。
(3)低铁反应罐:钢板厚度δ=20mm;内设搅拌桨,设备尺寸为直径3米,高2米。
(4)洗泥地罐:回收沉淀洗泥工序中残留的硫化钠,钢板厚度δ=20mm,内设搅拌桨。
主要设备一览表。
