渗透性脱髓鞘综合
渗透性脱髓鞘综合征

大多预后好,使病人增强信心,配合治 疗。
(五)健康指导
疾病知识指导 指导病人及家属掌握本病有关 知识及自我护理方法,认识肢体功能锻炼的重 要性,减少并发症,如出现并发症立即就诊。
生活指导 建立健康的生活方式,注意营养均 衡,增强体质和机体抵抗力;避免受凉、感冒、 疲劳和创伤等诱因。
ODS的治疗
• 低钠血症治疗
治疗
• 快速地纠正低钠血症导致ODS发生,故有人提出是一种” 医源性”的结果
• 低钠血症是指血清钠浓度低于135mmol/L。急性低钠血症 为低钠血症48h内或血钠降低>0.5mmol/h,慢性低钠血 症为48h以上持续低钠血症或血钠降低<0.5mmol/h
• 按血清钠浓度分为轻度(<125-134mmol/L)、中度(< 120-124mmol/L)、重度(<120 mmol/L)
CPM的临床表现及诊断标准较熟悉,而对EPM不熟悉 ➢ EPM受累的部位不一,既可能单独累及小脑、基底核、外
侧膝状体、外囊等部位(累及发生率按上述顺序);又可 同时累及桥脑(EPM+CPM) • EPM常见的症状为小脑与基底核损害引起的小脑共济失调, 不自主运动及帕金森综合征等运动障碍为中心的临床表现
护理措施
(一)一般护理
饮食护理 高热量、高蛋白、丰富维生素 易消化饮食。喂食速度要慢,以免呛咳, 严重者鼻饲。进食时及食后30min宜抬高床 头,防止窒息。
预防并发症 经常更换体位; 保持瘫痪肢体的功能位; 早期做好肢体的运动训练。
(二)病情观察
呼吸困难及程度,注意肺活量及血气分析变化。 呼吸肌麻痹致缺氧的表现:呼吸费力、烦躁、出汗、
lability)
中枢神经系统脱髓鞘疾病

原发进展型 (primary-progressive,PP)
约10%的MS患者表现为本类型。病程大于1年, 疾病呈缓慢进行性加重,无缓解复发过程
继发进展型
大约50%的复发-缓解型患者在患病10~15年
后疾病不再有复发缓解,呈缓慢进行性加重
(secondary-progressive,SP) 过程
进展复发型
治疗
MS急性发作期治疗
对激素治疗无效者、处于妊娠或产后阶段的患IG:0.4g/(kg•d) ×5天
无效
停用
有效
继续使用1次/周×3~4周
3)血浆置换:对MS的疗效不肯定,不作为急性期的常规 治疗;对既往无残疾的急性重症MS患者有一定疗效
治疗
MS缓解期治疗
1)复发型(β-干扰素、醋酸格拉默、米托蒽醌、那他珠 单抗、芬戈莫德、特立氟胺等)
IFN-β-lb:非糖基化重组哺乳动物细胞产物, (Betaseron) 17位丝氨酸被半胱氨酸所取代
β-干扰素治疗MS
商品名 化学成分 适应症
用法
Avonex (国内未上
市)
IFN-β-la CIS, RRMS
起始7.5μg/次 im×1次/周,逐 渐增至30μg/次 im×1次/周
Betaseron IFN-β-lb
治疗
MS急性发作期治疗
1)糖皮质激素:急性发作期的治疗首选,主张大剂量、短 疗程
ü 病情较轻者,静滴1g/d×3~5天
恢复明显,直接停用 疾病仍进展,转为阶梯减量法
ü 病情较重者,静滴1g/d×3~5天,此后剂量阶梯依次减半, 每个剂量2~3天,至120mg以下,改口服60~80mg/天,每 个剂量2~3天,继续阶梯依次减半,直至减停,原则上总 疗程不超过3~4周
渗透性脱髓鞘综合征(ODS)

渗透性脱髓鞘综合征(ODS)渗透性脱髓鞘综合征(osmotic demyelination syndrome,ODS),也称渗透性髓鞘溶解综合征,包括:1.脑桥中央髓鞘溶解症(central pontine myelinolysis,CPM)2.脑桥外中央髓鞘溶解症(extrapontine myelinolysis,EPM),占10%左右。
两者可合并存在。
【病因】病因未明。
水、电解质平衡紊乱(特别是低钠血症)及快速纠正史、慢性酒精中毒均可引起,另外,肝移植术后、肾衰、肝衰、严重烧伤、败血症、癌症、糖尿病、AIDS、妊娠呕吐、神经性厌食、急性卟啉病、放/化疗后、垂体危象、脑外伤、肾透析后等也有报道。
【病理】CPM:脑桥基底部对称性脱髓鞘,不伴炎性反应;神经细胞和轴索相对完好。
EPM:一般在丘脑、内囊、小脑、新纹状体、杏仁核、屏状核、外侧膝状体等。
【临床表现】青壮年多发。
1.CPM皮质脑干束损害:构音障碍、咀嚼和吞咽障碍等;皮质脊髓束损害:四肢瘫;上行网状激活系统损害:不同程度的意识障碍。
2.EPM由于受损的部位不同,可表现为共济失调、行为异常、视野缺损、帕金森综合征、手足徐动、肌张力障碍等。
【影像】症状发生后1-2w后MRI可显示病变。
1.CPM脑桥基底部对称性长/等T1、长T2信号,DWI高信号,横断面上呈圆形或蝴蝶型、冠状面上呈蝙蝠翅膀样,无明显占位效应,增强无明显强化。
病例1:病例2:病例3:2. EPM病例:3.CPM+EPM病例:【鉴别诊断】1.颅内肿瘤:病灶多不对称,MR有明显的占位效应,对比增强多明显。
2.脑梗死:多有脑血管病危险因素,病灶符合血管走形分布,多不对称。
但当基底动脉狭窄或闭塞时偶可引起脑桥双侧对称性病变。
CPM呈环形稍高信号影,脑干梗死则为片状高信号影。
3.可逆性后部白质脑病综合征【治疗】对症、支持治疗为主。
急性期可予甘露醇、呋塞米等控制脑水肿。
早期大剂量糖皮质激素冲击可延缓病情进展。
醉酒的十几种死亡原因

醉酒的十几种死亡原因急诊医生:醉酒的十三种原因因醉酒而死的人不少,但你知道吗?只有极少数是“醉”死的。
多数人一生中都接触过“酒”。
急性酒精中毒也是各大医院常见的急症之一,尤其是气候寒冷地区,且就诊时间多为深夜或凌晨。
作为一位急诊医生,处理急性酒精过量或中毒这些常见问题时,需认识到喝酒是可以死人的;喝酒一般是死不了人的,如发生意外死亡,极少数的患者是真正“醉”死的,而大多数都是有其它原因的。
1、误吸误吸是醉酒患者发生意外死亡的主要原因。
饮酒者胃内往往存有大量的食物,呕吐时胃内容物容易进入气道,导致患者窒息及诱发吸入性肺炎;也可刺激气管,通过迷走神经反射,造成反射性心脏停搏。
故在急诊工作中,常发现一些来院前已经死亡的醉酒病例,在心肺复苏时,常从气管内吸出大量呕吐物,多数是由于误吸所致。
因此,对于急性酒精中毒患者,防止误吸的发生,是“重中之重”。
因此,醉酒患者一定不能仰卧位;头一定要偏向一侧,防止呕吐物进入气管。
并根据情况,进行插胃管洗胃,进行胃排空措施,后者的目的也是防止发生误吸。
另外,判断胃内容物多少,还可根据正位胸部X线平片,如胃泡消失,常提示患者胃处于充盈状态。
2、双硫仑样反应头孢哌酮属第三代头孢菌素类药物,其抗菌谱广,抗菌作用强,主要通过胆道排泄;因此肾功能损害者,可用常用量,有肝功能损害者或胆道梗阻者,也可用常用量,因此时肾脏排泄可增加,代偿胆道排泄减少。
本品毒性低微,易耐受。
因此近年来广泛应用于临床;但应注意的是应用头孢哌酮期间饮酒可出现双硫仑样反应。
在应用头孢哌酮期间直至用药后5天内饮酒皆可出现“双硫仑样反应”,因此在用药期间和停药5d 内患者不能饮酒、口服或静脉输入含乙醇的药物。
含酒精的药物主要有硝酸甘油和氢化可地松;在用头孢类抗生素期间,如静脉用硝酸甘油或氢化可地松,也可出现双硫仑样反应,很容易误诊为药物过敏。
应用药物(头孢类)后饮用含有酒精的饮品(或接触酒精)导致的体内乙醛无法降解,蓄积在体内,造成乙醛中毒现象,又称双硫醒反应。
渗透性髓鞘脱失综合症

Sห้องสมุดไป่ตู้ndrome, ODS)
概述
• 渗透性髓鞘脱失综合症是一种发生在中枢 神经系统的特殊脱髓鞘疾病。
• 脑桥中央髓鞘溶解症( central pontine myelinolysis, CPM):脑桥基底部出现对 称性的髓鞘溶解病灶。
性肿瘤、肝肾功能衰竭、严重烧伤、产后 大出血伴垂体机能不全、持续癫痫发作后、 肝移植手术等
病因及发病机制
• 发病机制与颅内渗透压失衡相关
• 血钠下降时,水进入细胞内导致脑水肿, 当低钠血症被快速纠正时,细胞外渗透压 迅速增高,细胞内外渗透压差过大,导致 脑细胞皱缩。少突胶质细胞在细胞容积缩 小时,容易死亡,出现髓鞘脱失、溶解;
• 有的患者经过适当治疗后甚至可完全恢复 • 是一种自限性疾病,应积极救治
病例回顾
• 张XX,男,58岁 • 主因“肝癌术后一过性恶心、呕吐26天,
发音困难、四肢无力14天”于20**-11-12 入院。
现病史
• 20**年10月15日因“肝右叶占位”在我院肝胆外科行手术治 疗
• 10月17日患者出现恶心、呕吐 • 10月19日查血钠113.2mmol/L,对症治疗 • 10月21日血钠101.6mmol/L,给予10%氯化钠注射液50ml
• 一般不伴强化,或表现为轻度均一或周边强 化
其他辅助检查
• 脑干诱发电位典型表现为Ⅰ-Ⅴ波或Ⅲ-Ⅴ波 间脑潜伏的异常延长
• PET-CT显示脑桥病灶区早期高代谢,晚期 低代谢
• 脑电图检查可见弥漫性低波幅慢波,无特 征性
• 脑脊液检查蛋白及髓鞘碱性蛋白可增高
低钠血症
低钠血症发生速度:急性、慢性 血钠浓度:轻度(血钠120-135mmol/L)
胼胝体损害
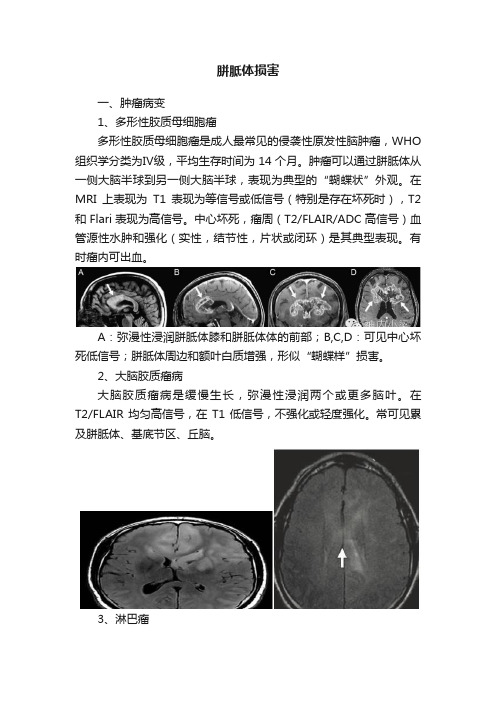
胼胝体损害一、肿瘤病变1、多形性胶质母细胞瘤多形性胶质母细胞瘤是成人最常见的侵袭性原发性脑肿瘤,WHO 组织学分类为Ⅳ级,平均生存时间为14个月。
肿瘤可以通过胼胝体从一侧大脑半球到另一侧大脑半球,表现为典型的“蝴蝶状”外观。
在MRI上表现为T1表现为等信号或低信号(特别是存在坏死时),T2和Flari表现为高信号。
中心坏死,瘤周(T2/FLAIR/ADC高信号)血管源性水肿和强化(实性,结节性,片状或闭环)是其典型表现。
有时瘤内可出血。
A:弥漫性浸润胼胝体膝和胼胝体体的前部;B,C,D:可见中心坏死低信号;胼胝体周边和额叶白质增强,形似“蝴蝶样”损害。
2、大脑胶质瘤病大脑胶质瘤病是缓慢生长,弥漫性浸润两个或更多脑叶。
在T2/FLAIR均匀高信号,在T1低信号,不强化或轻度强化。
常可见累及胼胝体、基底节区、丘脑。
3、淋巴瘤淋巴瘤常常累及胼胝体、室周白质和基底节区,均匀强化不伴有中心坏死。
在免疫力低下或者极少免疫力正常患者中,淋巴瘤以周围强化多见,或者轻度,不强化。
周围水肿和中心坏死可见于HIV相关淋巴瘤。
和多形性胶质母细胞瘤相比,瘤周水肿,坏死和出血较少见。
对放射和类固醇治疗敏感。
A-B图:右侧胼胝体膝部淋巴瘤;C-D图:1个半月后显示右侧额叶和胼胝体体部病灶,呈现环形强化和均匀强化。
4、脑膜瘤脑膜瘤为第二大原发性中枢神经系统肿瘤。
发源于中线与旁矢状面的硬脑膜表面,可以累及胼胝体。
在CT上表现为高密度;在MRI 一般呈均匀强化,有时在大病灶中可见出血、空穴、坏死。
5、其他原发性脑肿瘤胼胝体受累在其他原发性肿瘤中较少见,包括毛细胞性星形细胞瘤、生殖母细胞瘤。
6、转移瘤转移瘤累及胼胝体比较少见,影响特点主要和原发性肿瘤有关,常常表现为占位效应,血管源性水肿和不均匀强化。
下图为肺癌转移二、脱髓鞘疾病1、多发性硬化在多发性硬化中胼胝体常常受累,分隔胼胝体的病灶对诊断具有特异性。
下图为两个不同的多发性硬化患者,A图显示胼胝体前部的分隔胼胝体病灶;B图显示多个分隔胼胝体病灶。
渗透性脱髓鞘综合征

01 渗 透 性 脱 髓 鞘 综 合 征 的 概 述 02 渗 透 性 脱 髓 鞘 综 合 征 的 病 因 03 渗 透 性 脱 髓 鞘 综 合 征 的 治 疗 方 法 04 渗 透 性 脱 髓 鞘 综 合 征 的 预 防 措 施 05 渗 透 性 脱 髓 鞘 综 合 征 的 康 复 与 护 理 06 渗 透 性 脱 髓 鞘 综 合 征 的 并 发 症 与 预 后
预后评估:根据患者的病情、治 疗情况、康复训练等因素进行综 合评估
预防措施:针对可能影响预后的 因素,采取相应的预防措施,如 控制血糖、血压、血脂等
添加标题
添加标题
添加标题
添加标题
影响因素分析:包括年龄、性别、 病因、病程、治疗方式、康复训 练等多种因素
康复训练:针对患者的具体情况, 制定个性化的康复训练计划,促 进患者恢复功能
肺部感染:保持室内空气流通,避免吸烟和吸入二手烟,必要时使用抗生素治疗 尿路感染:保持外阴清洁,勤换内裤,多饮水,必要时使用抗生素治疗 褥疮:定期翻身拍背,保持皮肤清洁干燥,必要时使用抗生素治疗 静脉血栓:抬高患肢,避免剧烈运动,使用抗凝药物进行治疗 焦虑和抑郁:进行心理疏导和支持,必要时使用抗焦虑和抗抑郁药物进行治疗
自我管理:患者应保持良好的心态,积极面对疾病;适当进行康复锻炼, 如散步、太极拳等;遵医嘱按时服药,定期复查。
随访时间:根据病 情和医生建议,定 期进行随访
随访内容:了解病 情变化,评估康复 效果,调整治疗方 案
复查项目:包括神 经系统检查、影像 学检查、血液检查 等
注意事项:遵循医 生指导,按时服药, 注意饮食和生活习 惯的调整
康复训练的重要性
康复训练的方法和步骤
康复训练的注意事项
康复训练的评估与调整
渗透性髓鞘溶解综合征MRI表现

0引言渗透性髓鞘溶解征(osmotic demyelination synd-rome ,ODS )是由于脑的渗透压波动引起的一类较少见的具有潜在致命风险的脱髓鞘疾病[1],包括脑桥中央髓鞘溶解症(central pontine myelinosis ,CPM )、脑渗透性髓鞘溶解综合征MRI 表现赵海峰1,吕秀花2*,周永怀1,焦飞涵2,张天敏1(1.甘肃医学院附属医院磁共振室,甘肃平凉744000;2.空军军医大学第一附属医院放射科,西安710032)作者简介:赵海峰(1991—),男,住院医师,主要从事中枢神经系统、乳腺影像诊断方面的研究工作。
通信作者:吕秀花,E-mail :****************桥外髓鞘溶解症(extra pontine myelinolysis,EPM),两者可以单独发生,也可合并发生。
MRI是ODS最为有效的影像学检查方法。
尽管有文献报道[2]MRI的异常表现与ODS预后并不存在明确的相关性,但是早期发现病变并做出正确的诊断,仍有助于临床及时开展有效治疗、降低死亡率。
本研究回顾性分析14例ODS患者的病历资料及其在MRI各序列上的表现,旨在提高对ODS的认识,以达到尽早诊断的目的。
1资料与方法1.1一般资料回顾性分析2014—2019年经临床及影像确诊的14例ODS患者的病历资料,其中男9例、女5例,年龄3~62岁,中位年龄46.5岁。
纳入标准:(1)伴有可导致低钠血症(血钠水平低于136mmol/L)的基础疾病,或者有酗酒、厌食等不良生活习惯;(2)临床上有以下运动障碍,如下肢瘫、四肢瘫或帕金森综合征为主的精神神经系统症状[3]。
排除标准:(1)有中毒病史者;(2)有缺血、缺氧病史者;(3)临床和(或)实验室检查结果支持肝豆状核变性或有相关疾病家族史者;(4)合并自身免疫性疾病者;(5)病毒性脑炎或其他可能导致腰穿脑脊液检查结果异常者。
本研究经过医院医学研究伦理委员会审核并批准,且患者均签署知情同意书。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
发病机制
• 低血钠纠正越快,渗透压增高越快,细胞内外渗透压差越 大,越易导致细胞萎缩 • 脑桥、大脑皮层、丘脑、壳核、外侧膝状体等其它脑桥外 结构中,少突神经元嵌在大神经元之间,并相互交织成网, 在容积缩小时,尤其容易死亡,出现髓鞘脱失、溶解 • 另外,细胞凋亡、渗透性血管内皮细胞损伤、髓鞘毒性物 质释放、营养不良致维生素B1缺乏、免疫学说可能均起到 一定作用
治疗
• 低钠血症治疗 • 快速地纠正低钠血症导致ODS发生,故有人提出是一种” 医源性”的结果 • 低钠血症是指血清钠浓度低于135mmol/L。急性低钠血症 为低钠血症48h内或血钠降低>0.5mmol/h,慢性低钠血 症为48h以上持续低钠血症或血钠降低<0.5mmol/h • 按血清钠浓度分为轻度(<125-134mmol/L)、中度(< 120-124mmol/L)、重度(<120 mmol/L) • 低钠的症状包括头痛、乏力、食欲减退和肌肉痉挛等。中 枢性症状有精神萎靡、恶心、头痛、昏睡、意识模糊、痫 性发作、昏迷甚至死亡,而且缺乏局灶的神经体征 • 慢性低钠血症可以毫无症状
半年后复查颅脑MRI示双侧豆状核、尾状核、双侧额叶、颞叶病灶消失, 双侧丘脑可见T2略高信号小灶
病例2
• 赵ⅩⅩ ,50F,住院号128977,因言语不能,四肢活动不 灵1.5月于2005年10月21日入院 • 1.5月前因咯血,肺CT示右肺癌入省立医院胸外科 • 常规查体:未见明显异常,血钠80mmol/L,给予高渗钠后 血钠恢复正常。3-4天后出现双下肢无力,神经科会诊治疗 无效,病人逐渐出现全身无力,言语不清,吞咽障碍,鼻 饲治疗 • 1月前,病人上述症状逐渐加重,言语不能,四肢活动不能, 诊断为“副肿瘤综合症”转入我院 • 入院查体:神志清、木僵状态,颈部强直后仰,构音障碍, 四肢肌力III级,肌张力齿轮样升高、病理症(+),双足下 垂 • 辅助检查:肺CT示右肺中部大圆形阴影(外院) • 头颅MRI:双侧基底节、脑桥长T1长T2信号(外院)
病例分析1
T2加权像
病例分析1
T2 Flair像
病例分析1
• 病历复印资料:血生化(入院第10天):
病例分析1
• 当地医院治疗: • 0.9%氯化钠220ml+ 10%氯化钠30-100ml静滴7天 • 甘露醇、甘油果糖、异丙嗪、地西泮、胃复安、格拉 司琼氯化钠、三磷酸胞苷等
诊断
• 脑桥外髓鞘溶解症(extrapontine myelinolysis, EPM)
鉴别诊断
• 缺氧代谢性疾病:也可呈对称性改变,详尽准确的病史十 分重要 • 迟发性齿状核红核苍白球路易体萎缩症:在没有突出白质 脑病而又有明显脑桥病灶时可见相似的改变,鉴别困难, 该病多表现为小脑性共济失调、痴呆、舞蹈症等,病史有 助鉴 • 当病变累及皮质时需与皮质层状坏死鉴别,后者的MRI特 征是皮质短T1和长T2信号改变,T1WI高信号且不被增强, 在第2周开始出现,Flair高信号在1月更明显,可持续1年。 慢性期时可见延迟的皮质萎缩。缺氧、梗死、肝脑、线粒 体脑病、阳桃、H2S中毒、低钠血症、痫性发作及吸毒是 其主要原因
治疗
• ODS的治疗 • 甲状腺释放激素(TRH):增强左旋多巴的作用和增加局 部血液供应。 Chemaly使用TRH 0.6m g/d静脉滴注6周, 使用后几天即有所改善,直至完全康复 • 类固醇激素:保持BBB的稳定性从而减轻水肿及少突胶质 细胞的损害、减少血管外物质通过BBB,进而减少脱髓鞘 的病灶、影响巨噬细胞的流入和活性等,而后者最终导致 动物模型上的髓鞘溶解 • 免疫球蛋白:脉滴注丙种球蛋白0.4g/kg,可以减少髓鞘 毒性物质、抗髓鞘抗体形成及支持髓鞘再生,连用5天后 有效 • 血浆置换 :清除髓鞘毒性物质。 首先每天1次,4天后 变为每周2次连续3周的血浆置换 ,交换总量500020000ml • 高压氧疗法
病因
• 慢性酒精中毒、营养不良是比较肯定的病因,约占39% • 1986年后低钠血症的过快纠正成为第二大病因,约占 21.5% 引起低钠的疾病有肝硬化、大量补液、吸毒、抗利尿 激素分泌异常综合征、垂体手术、肺癌及肠癌、长期使用 利尿剂等 • 同年报道的CPM17%由肝移植所致,使其成为第三大病因。 尤其在肝移植后30天内,主要因素包括败血症、代谢紊乱、 肝性脑病、缺氧、他克莫司和环孢菌素的使用等
临床表现
• 依病灶的大小、定位,轻者可毫无症状,重者会出现昏迷 • CPM表现为四肢瘫和不同程度的脑干功能障碍,如假性延 髓麻痹,偶有闭锁综合征、缄默症 • EPM主要表现为运动障碍、肌张力障碍、帕金森综合征等, 仅出现小脑体征者罕见 • Hawthorne等最近报道了1例因过快纠正低钠血症后出现动 眼神经麻痹、成像异常及旋转性眼震等中脑受损表现的病 例。若存在快速纠正低钠的病史,则症状常在纠正后2~7 天内出现 • ODS常伴有精神症状,如行为异常、认知和情感障碍、紧 张、情绪不稳、缄默、兴奋、妄想、幻觉等,提示额叶受 损
发病机制
• 目前该病的发病机制尚不明确,很多观点认为与BBB破坏、 内皮细胞的渗透性改变致少突胶质细胞有害代谢髓鞘中毒 有关 • 低血钠时:血浆低渗 Na 迅速到细胞外液
H2O 有机酸 1-数天到细胞外液
• 迅速纠正低血钠(48h后):
细胞外高钠 有机酸 大量H2O 血浆高渗 少量Na进入细胞 细胞皱缩
渗透性脱髓鞘综合征
Osmotic demyelination syndrome (ODS ) 山东省千佛山医院神经内科 王爱华
病例分析1
• 陈ⅩⅩ,20F, 住院号156878,因脑外伤半月、烦躁不安1 周,突发无语1天入我院 • 患者半月前因“脑外伤昏迷伴呕吐2小时入当地医院内科 治疗1周后病情好转出院。 治疗、血生化、血常规(不 详),头颅CT示脑肿胀 • 1周前出现烦躁不安,伴头晕、恶心、呕吐,并出现癫痫 大发作,每次持续2Min,每天3-4次,再次当地医院就诊 头颅MRI示左颞叶硬膜下血肿 • 1天前,家属发现言语缓慢,眼神呆滞,未予重视。当天 同房间病友去世,病人突然无语,烦躁不安加重,省精神 卫生中心考虑”脑外伤后精神障碍“ • 为进一步治疗于2008年11月12日入我院神经科
治疗
• 低钠血症治疗 • 目前推荐的理想的纠正低钠的速度是不超过8mmol/L/d或 0.5mmol/L/h • 最初的补钠速度为1~2 mmol/L/h,低钠脑病患者建议用 高渗盐,但有潜在的危险,至少每2h监测一次血钠,48h 不应该超过20mmol/L • 但无论什么情况下,无症状且神经系统未受累的患者无论 血钠多少均不应输注高渗钠 • 低钾时应先纠正或与低钠同时纠正 • 慢性低钠血症纠正过快患ODS的风险高,需早期准确分析
病例分析1
病例分析1
病例分析1
• 查体:T37.2℃,双肺湿罗音。神志欠清楚,精神差,烦 躁不安,不能言语,左侧鼻唇沟稍浅,吞咽不能,肢体对 疼痛刺激有伸缩反应。双病理征(+) • 入院诊断:脑外伤后精神障碍 症状性癫痫 硬膜下血肿 • 血常规、血生化、甲功能、甲状旁腺激素检查均未见异常 • 给予抗炎、抗病毒、脱水、鼻饲治疗,躁动明显抗精神药 物(精神卫生中心会诊:奋乃静、舒必利、安坦、氟哌丁 醇),VPA、地西泮控制癫痫。
发病机制
• 最初认为ODS典型的组织病理学表现为少突胶质细胞的缺 失,轴突和神经元相对完整,无炎症细胞浸润,由此可以 鉴别多发性硬化和急性播散性脑脊髓炎 • 病灶大小不一,大者2cm×1cm,小的仅为0.2cm× 0.3cm,且不损害皮质延髓束、皮质脊髓束和被盖部,所 以,仅有如此小的病灶就无临床表现。 • 最近的一项研究发现了轴突损害,此种改变也见于其他有 炎性渗出的脱髓鞘疾病中,这或许是大剂量激素治疗有效 的依据 • CPM的特征性损害集中在脑桥基底部,包括中线,显示为 对称性三角形或蝙蝠翅膀形的髓鞘脱失,伴有少量轴突的 损害
诊断
• • • • • • CO中毒? 乙型病毒性脑炎? 肝豆状核变性? 霉变甘蔗中毒? 脑桥外髓鞘溶解症? 以上病变均可出现长T1长T2信号
• 脑脊液压力320mmH2O,铜蓝蛋白正常,K- F环(-)
病例分析1
• • • • • 首先考虑脑桥外髓鞘溶解症 家属交代病情,询问家属有无低钠血症病史,家属不清楚 反复询问家属当地医院有无谈过患者“缺盐” 患者病历一直未能复印过来 病人病情逐渐加重,持续高热、深昏迷,疼痛刺激无任何 反应,双瞳孔直径约6mm,对光反射消失 • 2008年11月21日(入院第9天)复查MRI
影像学特征
• CT上表现为脑桥中央或脑桥外病灶处的低密度影,但CT 不能反映疾病的真实程度 • MRI能更好地反映病灶的数量和程度。早期可无异常 • 出现症状后1周DWI上可发现高信号;急性期表现为对称 的T1WI低信号,亚急性期可能是由于内皮细胞受损所致 的微出血而显示T2WI高信号 • FLAIR显示病灶高信号更清楚,能更好地显示临近脑脊液 的病灶,比如大脑皮质,应作为常规检查 • 大约在发病2~3周时异常信号最为明显
病例分析1
• 入院第5天(2008.11.17)我院MRI示双侧豆状核、尾状 核、右颞叶皮层长T1、长T2信号,T2Flair像高信号,脑 干未见异常 • 病人当天症状进一步加重,高热、昏迷、抽搐、尿便失禁、 四肢肌张力升高
病例分析1
T2加权像权像
T2 Flair像
影像学特征
• 结合病史及临床表现如果考虑ODS的诊断,在MRI检查正 常的情况下,在出现症状后10~14天复查MRI是十分重要 和必要的 • 有的病灶缩小可能提示水肿、脱髓鞘以及星形胶质细胞反 应的减轻,但患者好转并不依赖于MRI的表现,有的可能 终身不消失
诊断
• 慢性酒精中毒、低钠血症的过快纠正、肝移植及其他严重 疾病等相关病史 • 突然出现假性延髓麻痹、闭锁综合征、缄默症、意识障碍 等皮质脊髓束和皮质脑干束受损或运动障碍、肌张力障碍、 帕金森综合征等基底节区受损的表现,应高度怀疑ODS • 一旦出现对称性脑桥中央T1WI低信号、T2WI、Flair和 DWI高信号的三角形到蝙蝠翼形病灶,对CPM诊断意义 • 两侧纹状体和丘脑,尤其是壳核和豆状核区的T1WI低信 号 、 T2WI和Flair高信号提示EPM,还可对称性地累及胼 胝体、皮质下白质、小脑或小脑脚、外侧膝状体、黑质等 • 确诊需要病理活检
