烷烃 自由基取代反应共34页
合集下载
烷烃自由基取代反应PPT学习教案

CH2 CHCH2
H
CH2 CHCH2 H
均裂
H=359.8kJ/mol (88kcal/mol)
共价键均裂时所需的能量称为键解离能。 键解离能越小,形成的自由基越稳定。
CH2 > CH2 CHCH2 > (CH3)3C > (CH3)2CH
苯甲基自由基
烯丙基自由基 三级丁基自由基 异丙基自由基
> CH3CH2 > CH3 >
第18页/共36页
甲烷氯化反应势能图的分析
1 第一步反应的活化能比较大,是速控步骤。 2 第二步反应利于平衡的移动。 3 反应 1 吸热,反应 2 放热,总反应放热,所以反应
只需开始时供热。 4 过渡态的结构与中间体(中间体是自由基)相似,
所以过渡态的稳定性顺序与自由基稳定性顺序一致。 推论:3oH最易被取代,2oH次之,1oH最难被取代。
反应机理是根据很多实验事实总结后提出的,它有 一定的适用范围,能解释很多实验事实,并能预测反应 的发生。如果发现新的实验事实无法用原有的反应机理 来解释,就要提出新的反应机理。反应机理已成为有机 结构理论的一部分。
第8页/共36页
4.4 烷烃的结构和反应性分析
1. 稳定。对强酸,强碱,强氧化剂,强还原剂 都不发生反应。 2. 烷烃的多数反应都是通过自由基机理进行的。
第9页/共36页
4.5 自由基反应
1. 自由基 定义:带有孤电子的原子或原子团称为自由基
。碳自由基:含有孤电子碳的体系称为碳自由 基。 4.5.1 碳自由基:含有孤电子碳的体系称为碳自由基。
CH3CH2 一级碳自由基
CH3CHCH3 二级碳自由基
CH3CCH3 CH3
三级碳自由基
第4章烷烃自由基取代反应ppt课件

例如: 正丁烷的沸点:- 0.5℃ 异丁烷的沸点:- 11.7℃
二 熔点
取决于分子间的作用力和晶格堆积的密集度。
烷烃熔点的特点
(1) 随相对分子质量增大 而增大。
(2) 偶数碳烷烃比奇数碳 烷烃的熔点升高值 大 (如右图)。
(3)相对分子质量相同的烷 烃,支链增多,熔点下降。
高度对称的烷烃分子熔点比同分子量的直链烷烃高。
伯,仲,叔氢原子的反应活性
2.溴化
C H 3 C H 2 C H 3 + B r 2
B r
1 2 7 o CC H 3 C H C H 2 B r+C H 3 C H C H 3 h v
3 %
9 7 %
Br
C H 3C H C H 3 +Br2
127oC C H 3C H C H 2Br+C H 3CC H 3 hv
第 四 章 烷烃 自由基取代反应
Chapter 2 Alkanes and free radical substitution reaction
4.1 烷烃的分类
4.2 烷烃的物理性质
外
观: 状态, 颜色, 气味
1-4 气态 5-16 液态 17- 固态 t
物理常数: 沸点(b.p.) 熔点(m.p.)
C HC H 2+B r2
C H 2 C H 2 C HC HC H 2 B r B r B r B r
4.12 烷烃的来源
(1) 石油(分馏产物); (2) 天然气
干天然气--甲烷86%~99%(体积) 湿天然气--甲烷60%~70%,还含有一定的乙烷,
丙烷,丁烷等气体. (3) 油田气--低级烷烃,如甲烷,乙烷,丙烷,丁烷和戊烷等; (4) 煤层气,沼气--甲烷等; (5) 甲烷冰.
二 熔点
取决于分子间的作用力和晶格堆积的密集度。
烷烃熔点的特点
(1) 随相对分子质量增大 而增大。
(2) 偶数碳烷烃比奇数碳 烷烃的熔点升高值 大 (如右图)。
(3)相对分子质量相同的烷 烃,支链增多,熔点下降。
高度对称的烷烃分子熔点比同分子量的直链烷烃高。
伯,仲,叔氢原子的反应活性
2.溴化
C H 3 C H 2 C H 3 + B r 2
B r
1 2 7 o CC H 3 C H C H 2 B r+C H 3 C H C H 3 h v
3 %
9 7 %
Br
C H 3C H C H 3 +Br2
127oC C H 3C H C H 2Br+C H 3CC H 3 hv
第 四 章 烷烃 自由基取代反应
Chapter 2 Alkanes and free radical substitution reaction
4.1 烷烃的分类
4.2 烷烃的物理性质
外
观: 状态, 颜色, 气味
1-4 气态 5-16 液态 17- 固态 t
物理常数: 沸点(b.p.) 熔点(m.p.)
C HC H 2+B r2
C H 2 C H 2 C HC HC H 2 B r B r B r B r
4.12 烷烃的来源
(1) 石油(分馏产物); (2) 天然气
干天然气--甲烷86%~99%(体积) 湿天然气--甲烷60%~70%,还含有一定的乙烷,
丙烷,丁烷等气体. (3) 油田气--低级烷烃,如甲烷,乙烷,丙烷,丁烷和戊烷等; (4) 煤层气,沼气--甲烷等; (5) 甲烷冰.
烷烃自由基取代反应

28%
72% Cl
CH3CHCH3 + Cl2 CH3
35 oC hv
(CH3)2CHCH2Cl + (CH3)3CCl
63%
37%
V1oH : V2oH = 28/6 : 72/4 = 1 : 4
V1oH : V3oH = 63/9 : 37/1 = 1 : 5.3
氯化 V1oH : V2oH : V3oH = 1 : 4 : 5.3
自由基反应:
取代反应
(原有旳化学键发生均裂) 加成反应
离子型反应: (原有旳化学键发生异裂)
亲电反应: 取代反应 加成反应
取代反应 亲核反应:
加成反应
协同反应: (旧键断裂和新键形成相互协调地同步完毕)
二、反应机理
反应机理是指反应旳详细环节(或者说是指反
应所经历旳详细途径)。
如,甲烷氯代反应
CH4 + Cl2
第十二节 烷烃旳起源
一、起源于自然界:天然气和石油 二、人工制备
二、与氯和溴反应
+ Br2 r.t + Cl2 FeCl3
BrCH2CH2CH2Br ClCH2CH2CH2Cl
三 、与氢碘酸反应 CH3 + HI
I 开环 CH3CHCH2CH3
此反应是离子型机理,极性大旳键易 打开;三元环比四元环易发生此反应,其 它环不发生此反应。
开环反应活性:
三员环>四员环>>一般环
CH3 O O 单自由基
第六节 烷烃旳卤化
一、甲烷旳氯化
反应式 CH4 + Cl2
hv
CH3Cl + HCl
卤代反应 分子中旳原子或 基团被卤原子取代 旳反应称为卤代反 应。
第四章 烷烃 自由基取代反应
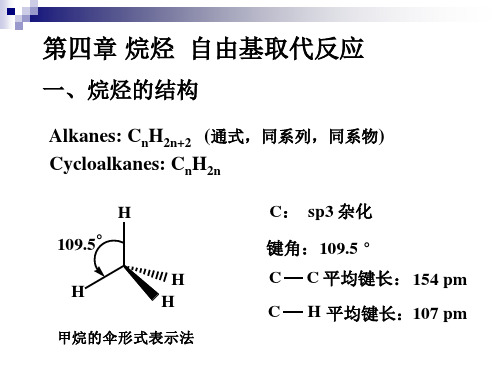
键解离能 平均键能和自由基
1、键解离能 和自由基稳定性
键的解离能: 某一键断裂所吸收的热量, 是键解离反应的焓( ΔHο反应热),用 DHο 表示,如: CH3-H → CH3 ·+ H · ΔHο= DHο= + 439.3 kJmol-1
1
CH3CH2- H → CH3CH2 ·+ H · CH3CH2CH2-H → CH3CH2CH2 ·+ H · ( CH3 )2CH-H → ( CH3 )2CH · + H ·
甲烷氯化的反应热如下所示:
(1) Cl2 (+242.7 ) (2)Cl · CH4 + (+439.3 ) (3)CH3· Cl2 + CH3· HCl + (- 431.8) CH3Cl + Cl · ΔHο= (+439.3 )+(-431.8) = + 7.5 kJmol-1 ΔHο = (+ 242.7)+ (-355.6) 2Cl · ΔHο= + 242.7 kJmol-1
第四章 烷烃 自由基取代反应
一、烷烃的结构
Alkanes: CnH2n+2 (通式,同系列,同系物) Cycloalkanes: CnH2n
H 109.5° H H H C: sp3 杂化 键角:109.5 ° C C C 平均键长: 154 pm H 平均键长:107 pm
甲烷的伞形式表示法
二、烷烃的结构特点 1、非极性分子,偶极矩为0 2、在运动中可以产生瞬时偶极矩 3、分子间有色散力(瞬时偶极矩间的相互 作用)、vander waals 引力
一步反应 A + BC [A---B---C] 过渡态 AB + C
二步反应 A + B 反应物 C 中间体 D 产物
第四章 烷烃自由基取代反应
3. 有机反应的分类
按反应时键断裂和生产的方式 :自由基型、离子型、协同 亲电反应: 决进攻而发生的反应。 协同反应: 旧键的断裂与新键的生成都相互协调地在同一步骤中完成。 按反应物和生成物的结构关系 : 酸碱 (acid-base) 、 取代 ( substitution reaction) 、 加成 (addition reaction) 、 消除 (elimination reaction) 、 重排 ( rearrangement reaction) 、氧化还原( oxidation and reduction) 、缩合( condensation) 。
→ R3COOH + R3C·
过氧化物易产生爆炸的原因: -O-O-键是个弱键,在适当温度下很容易分解,产生自由基,自由基引发链反应,产生大量自由基,促使反应很快 进行,并放出大量热。
10. 烷烃的硝化
烷烃与硝酸或四氧化二氮进行气相(400~450℃)反应,生成硝基化合物(RNO2) 。 硝基烷烃可以转变成多种其他类型的化合物,如胺、羟胺、腈、醇、醛(Nef 反应) 、酮及羧酸等。硝基烷烃在工业上是很有用的溶剂,例如溶 解醋酸纤维、假漆、合成橡胶以及其他有机化合物。低级硝基烷烃都是可燃的,而且毒性很大。
6. 自由基反应
自由基碳呈 sp2 杂化(碳正离子 P 248 也是一样;碳负离子一般为 sp3 杂化,中的一对负电子占用的轨道会对其他 σ 轨道有排斥, 而成三角锥形,即这对负电子占有一个 sp3 杂化轨道) , p 轨道被一个孤电子占据。 在同系列中第一个化合物往往是比较特殊的。 解离能越低的碳自由基越稳定。 数据表明断裂 C-C 键所需的能量比 C-H 键小,因此 C-C 键易断同时还可以看出断裂 CH3CH2CH2CH3 中 C-C 键,形成两个 CH3CH2· 时H 最小, 说明大分子在中间断裂的机会是比较多的。 慢引发,快增长,速终止,有转移。 自由基反应的特点是没有明显的溶剂效应,酸、碱等催化剂对反应也没有明显影响当反应体系中有氧气(或有一些能捕捉自由基的杂质存在,如 下)时,反应往往有一个诱导期。所以自由基反应要做到防水防氧防铁。
第4章烷烃 自由基取代反应

4.5.3. 自由基反应的共性
定义:由化学键均裂引起的反应称为自由基反应。 共 (1)反应机理包括链引发、链增长、链终止三个阶段。 性
(2)反应必须在光、热或自由基引发剂的作用下发生。 (3)溶剂的极性、酸或碱催化剂对反应无影响。 (4)氧气是自由基反应的抑制剂。
C H + O O 3
双自由基
C H O O 3
支链烷烃比同碳数的直链烷烃更稳定。
4.11小环烷烃的开环反应
大环的环烷烃是稳定的,而小环的环烷烃不稳 定,由于张力较大,易开环进行加成反应。 1、与氢反应
H2/Ni
80 ℃
CH 3CH 2CH 3
H2/Ni
200℃
CH 3CH 2CH 2CH 3
思考题:为什么环丙烷易开环发生亲电加 成反应?
(1)“弯曲键”重叠程度小,键能下降, 从而产生角张力——恢复正常σ 键的倾 向,开环后即可形成正常的σ 键,所以 易开环。 (2)“弯曲键”使电子云暴露在成键两 原子(核连线)的外侧,类似于烯烃中 的π 键,易受亲电试剂的进攻。
结论:烷烃异构体中,直链烷烃的燃烧热最大, 支链越多,燃烧热越小,其焓值越小,越稳定。 每增加一个CH2,燃烧热平均增加659klmol-1
⑵生成热:由标准状态下的元素生成某一化合物 的反应中焓的变化。用△Hf¢表示。
化合物的生成热若为负值,表示它比生成它的元素更稳定。 烷烃的生成热为负值,生成热越小,越稳定。
苯甲基自由基 烯丙基自由基 三级丁基自由基 异丙基自由基
>C H C H C H 3 2 > 3 >
乙基自由基 甲基自由基 苯基自由基
两点说明
•影响自由基稳定 性的因素是很多 的,如: 电子离 域,空间阻碍, 螯合作用和邻位 原子的性质等; •碳自由基的最外 层为七个电子, 反应时总要寻找 另外的电子来达 到八隅体结构, 所以是亲电的。
第二章 烷烃和环烷烃 自由基取代反应
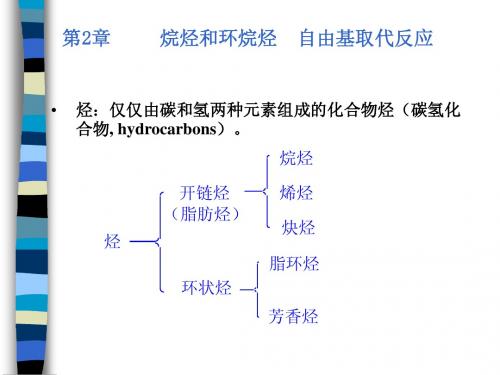
中文命名时:优先基团编号大!
4-丙基-8-异丙基十一烷 4-isopropyl-8-propylundecane
3. 命名编号取代基 • Name the substituents as alkyl groups. • Every carbon belongs to either the longest chain or a substituent, not both. • Each substituent needs its own number
•
二、系统命名法
1.
系统命名法(续) • 系统命名法适用于所有的有机化合物。
• 烷烃的命名:对于直链烷烃,根据烷 烃分子中碳原子命名为“某烷”;对 于含有支链的烷烃,将其看作直链烷 烃的取代衍生物来命名。
构造式
CH4 CH3CH3 CH3CH2CH3 CH3(CH2)2CH3 CH3(CH2)3CH3
中文名称
甲烷 乙烷 丙烷 正丁烷 正戊烷
英文名称
methane Ethane Propane n-butane n-pentane
构造式
中文名称
英文名称
n-octane n-nonane n-decane n-undecane n-dodecane
CH3(CH2)6CH3 正辛烷 CH3(CH2)7CH3 正壬烷 CH3(CH2)8CH3 正癸烷 CH3(CH2)9CH3 十一烷 CH3(CH2)10CH 十二烷
• •
二、系统命名法
5. 环烷烃的命名 2). 螺环烷烃的系统命名
2
1
6
7 8
1
4 5
5 3 4 10 9
3 2 7 6
螺[4. 5]癸烷 spiro[4. 5]decane
yq有机chapt-04 烷烃 自由基取代反应 2

支链烷烃比同碳数的直链烷烃更稳定。
4.9 小环烷烃的开环反应
大环的环烷烃是稳定的,而小环的环烷烃不稳定,由于张力 较大,易开环进行加成反应。
1、与氢反应 +
H2
Ni 80℃ Ni 120℃ Pt 300℃
CH3CH2CH3
+ +
H2
CH3CH2CH2CH3
H2
CH3(CH2)3CH3
环己烷则很难发生加氢反应。
物理性质:不牵涉物质分子化学组成 改变的性质,是物质本力:是电子在运动中产生的瞬时偶极力,与分子的 极化率、分子的接触面积有关。 又称为诱导偶极-诱导偶极相互作用。
色散力与分子中原子的数目大小约成正比。它弱于其 它分子间作用力,但是普遍存在的。
偶极力:极性分子间的相互作用力,为一分子偶极正端 对另一分子偶极负端的相互吸引作用。 也称为偶极-偶极相互作用。
4.5.3 高级烷烃的卤化
1.氯化
CH3CH2CH2CH3 + Cl2 35 oC hv CH3CH2CH2CH2Cl + CH3CH2CHCH3 28% 72% Cl
CH3CHCH3 + Cl2 CH3
35 oC hv
(CH3)2CHCH2Cl + (CH3)3CCl 63% 37%
V1oH : V = 28/6 : 72/4 = 1 : 4 2oH V 1oH : V 3oH = 63/9 : 37/1 = 1 : 5.3 氯化 V 1oH : V 2oH : V 3oH = 1 : 4 : 5.3
Ea (KJ/mol)
F Cl Br I
+4.2 +16.7 +75.3 > +141
