离子浓度大小比较(总结全面)
离子浓度大小的比较

( 2 )水解能力大于电离能力(如NaHCO3 、 Na2HPO4 、NaHS) 练习:试比较NaHCO3溶液中各离子浓度大小。
答案: C(Na+ ) > C(HCO3 –) > C(OH-) > C(H+) > C(CO3 2-) H2CO3?
六、单一正盐(AB型)溶液中离子浓度大小的比 (考虑水解和电离)
5、现有NH4Cl和氨水组成的混合溶液(填“>”、“<”或 “=”) = ①若溶液的pH=7,则该溶液中C(Nt;7,则该溶液中C(NH4+) < C(Cl-); ③若C(NH4+)< C(Cl-),则溶液的pH 7。
变式:NaHCO3溶液
三、质子守恒
在NH4Cl溶液中,存在两个守恒:
由水电离提供的H+与OH-相等(可由电荷守恒及物料守恒推出)。
电荷守恒:c(NH4+)+c(H+)=c(OH-) +c(Cl-) 物料守恒:c(Cl-)=c(NH4+)+c(NH3· 2O) H 两式相加 质子守恒: c(H+) = c(OH-) +c(NH3· 2O) H
4.在Na2CO3溶液中下列关系不正确的是( A ) A. 2c(Na+) = c(CO32-) + c( HCO3-) + c(H2CO3) B. c(Na+) +c(H+)= 2c(CO32-) + c(HCO3-) + c(OH-) C. c(Na+) > c(CO32-) >c(OH-)>c(HCO3-) >c(H+) D.c(OH-)= c(H+)+ c(HCO3-)+2c(H2CO3) 电荷守恒: c(Na+) +c(H+)= 2c(CO32-) + c(HCO3-) + c(OH-) 物料守恒: c(Na+) = 2c(CO32-) +2 c( HCO3-) + 2c(H2CO3) 质子守恒:c(OH-) = c(HCO3-) + c(H+) + 2c(H2CO3)
规律总结:离子浓度大小比较的方法

离子浓度大小比较的方法
离子浓度大小的比较,是历年高考命题的热点。
它涉及的知识点多,综合性强,需平时进行强化训练。
电解质溶液中离子浓度的相对大小的
题目,概括起来有以下几种类型:
(l)一种电解质溶液中各种离子浓度的相对大小比较;
(2)相同浓度的不同电解质溶液pH大
小比较(实质上是或的大小比较);
(3)两种电解质溶液混合后各种离子浓度大小比较;
(4)一种电解质加入不同电解质溶液中比较溶液导电能力的大小(实际上是比较溶液中总离子浓度的大小);
要解决离子浓度的大小问题,必须牢固地掌握以下知识点:
(l)电解质的电离;
(2)弱电解质的电离平衡;
(3)盐类的水解;
(4)溶液的导电性与离子浓度的关系;
(5)电解质间的相互反应。
其中还要掌握两个守恒关系:
(l)质量守恒(物质的量或物质的量浓度守恒);
(2)电荷守恒(溶液中各阳离子的正电荷总量与阴离子的负电荷总量相等)。
离子浓度大小比较
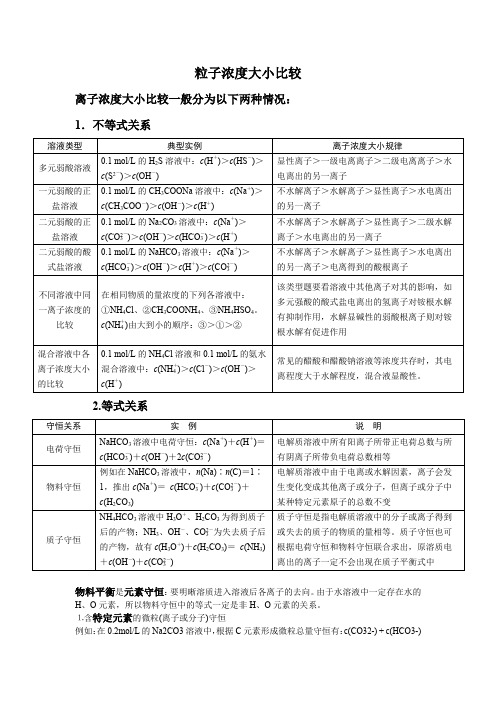
粒子浓度大小比较离子浓度大小比较一般分为以下两种情况:1.不等式关系2.等式关系物料平衡是元素守恒:要明晰溶质进入溶液后各离子的去向。
由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
⒈含特定元素的微粒(离子或分子)守恒例如:在0.2mol/L的Na2CO3溶液中,根据C元素形成微粒总量守恒有:c(CO32-) + c(HCO3-)+ c(H2CO3) = 0.2mol/L。
⒉不同元素间形成的特定微粒比守恒例如:在Na2CO3 溶液中,根据Na与C形成微粒的关系有:c(Na+) = 2[c(CO32- ) + c(HCO3- ) + c(H2CO3 )]分析:上述Na2CO3 溶液中,C原子守恒,n(Na) : n(C)恒为2:13.混合溶液中弱电解质及其对应离子总量守恒例如:相同浓度的HAc溶液与NaAc溶液等体积混合后,混合溶液中有:2c(Na+ )=c(Ac-)+c(HAc)分析:上述混合溶液中,虽存在Ac-的水解和HAc的电离,但也仅是Ac-和HAc两种微粒间的转化,其总量不变。
质子守恒规律:水电离的特征是c(H)=c(OH-),只不过有些会水解的盐会导致氢离子、氢氧根可能会有不同的去向,我们需要把它们的去向全部找出来。
例如:NaHCO3溶液,初始H+ 来源于HCO3- 和H2O的电离,c初(H+) = c(CO32- ) + c(OH- );伴随着的水解的发生,一部分H+转化到H2CO3中,因此,c初(H+) = c现(H+) + c(H2CO3 ),从而得出,溶液中离子浓度的关系如下:c(CO32- ) + c(OH- ) = c(H+) +c(H2CO3 )对同一溶液来说:质子守恒=电荷守恒-物料平衡快速书写质子守恒的方法第一步:确定溶液的酸碱性,溶液显酸性,把氢离子浓度写在左边,反之则把氢氧根离子浓度写在左边。
第二步:根据溶液能电离出的离子和溶液中存在的离子,来补全等式右边。
离子浓度大小的比较方法及规律

离子浓度大小的比较方法及规律
离子浓度是指解离出来的离子在溶液中的浓度,反映了溶液中离子的
数量。
在化学研究和实验中,比较离子浓度的方法及规律可以通过以下几
个方面来进行分析:
1.离子电荷数:离子的电荷数越多,其浓度越低。
因为在相同体积溶
液中,离子电荷越多,相互之间的排斥力越大,导致离子间的互相靠近程
度受到限制,浓度相应降低。
2.溶解度:不同离子化合物的溶解度不同,溶解度高的离子化合物会
使溶液中的离子浓度较高。
一般情况下,溶解度较高的化合物能够解离更
多的离子,在溶液中浓度较高;而溶解度较低的化合物解离的离子数量较少,浓度较低。
3.化学反应:一些化学反应会影响离子浓度,例如溶液中的酸碱反应、沉淀反应等。
在酸碱反应中,溶液中酸和碱的浓度决定了产生的离子浓度;在沉淀反应中,离子会结合形成沉淀,导致溶液中的离子浓度减少。
4.离子迁移速率:在电解质溶液中,离子的迁移速率是影响离子浓度
大小的因素之一、迁移速率较快的离子会在相同时间内在溶液中形成更高
的浓度。
离子迁移速率与离子电荷量、溶液电导率等因素有关。
5.离子浓度计算:通过实验测定,可以使用浓度计算公式来比较不同
离子的浓度。
离子浓度计算方法有多种,例如摩尔浓度、质量浓度、体积
浓度等,可以根据实际情况选择适合的方法来计算。
总结起来,离子浓度的大小可以通过离子电荷数、溶解度、化学反应、离子迁移速率以及浓度计算等方法和规律来进行比较。
因为每个离子都具
有独特的特性和溶液中的溶解度,所以在具体实验、研究和应用中需要详细考虑这些因素,来获得准确的离子浓度大小。
离子浓度大小的比较

【课堂练习】
1.在0.1mol/L Na2CO3溶液中,下列关系正确的是 A.c(Na+)=2c(CO32-)
( A )
【课堂练习】
3.下列叙述正确的是
( BC )
A. 0.1mol/L氨水中,c(OH-)=c(NH4+)
B. 10mL 0.02mol/L HCl溶液与10mL 0.02mol/L
Ba(OH)2溶液充分混合后溶液体积为20mL,则pH=12
C. 在0.1mol/LCH3COONa溶液中,
c(OH-) =c(CH3COOH)+c(H+)
C.C(CH3COOH)>C(CH3COO-)
D.C(CH3COO-)+C(OH-)=0.2 mol/L
【课堂练习】 • 1、现有NH4Cl和氨水组成的混合溶液C(填“>”、“<” 或“=”) • ①若溶液的pH=7,则该溶液中C(NH4+) = C(Cl-); • ②若溶液的pH>7,则该溶液中C(NH4+) > C(Cl-); < • ③若C(NH4+)< C(Cl-),则溶液的pH 7。 • 2、CH3COOH与CH3COONa等物质的量混合配制成稀 溶液,pH值为4.7,下列说法错误的是( B ) • A、CH3COOH的电离作用大于CH3COONa的水解作用 • B、CH3COONa的水解作用大于CH3COOH的电离作用 • C、CH3COOH的存在抑制了CH3COONa的水解 • D、CH3COONa的存在抑制了CH3COOH的电离
高考中“水溶液中离子浓度大小比较规律”总结

高考中“水溶液中离子浓度大小的比较规律”总结“水溶液中离子浓度大小的比较规律”在高考中经常用到,本文对高考中这部分内容出现过的情况进行了总结,并举出一个典型案例以供参考。
一、酸碱溶液:酸溶液中h+ 浓度最大,碱溶液中oh_ 浓度最大:其它离子根据电离度的大小确定。
1.强酸强碱溶液:例如盐酸溶液中离子浓度大小关系为:c( h+ )> c( cl- ) > c( oh_ ),naoh溶液中离子浓度大小关系为:c( oh_ )>c( na+ )>c( h+ )。
2.一元弱酸弱碱溶液,例如hac溶液中离子浓度大小关系为:c( h+ )>c( ac_ )> c( oh_ );nh3?h2o溶液中离子浓度大小关系为:c( oh_ )>c( nh4+ )> c( h+ )。
3.多元弱酸弱碱溶液,多元弱酸以第一步电离为主,例如h2s溶液中离子浓度大小关系为:c( h+ )>c( hs_ )>c( s2- )> c( oh_ );多元弱碱电离方程式一步写到位,但离子浓度大小关系容易判断,例如fe(oh)3 溶液中离子浓度大小关系为c( oh_ )>c( fe3+ )> c( h+ )。
二、盐类溶液:1.强酸强碱盐的溶液不水解,离子浓度不变,例如na2so4 溶液中离子浓度大小关系为:2c( so42- )=c( na+ )> c( h+ )= c( oh_ );再如nahso4溶液中离子浓度大小关系为:c( h+ )> c( so42- )= c( na+ )> c( oh_ )2.一元弱酸或弱碱形成的盐溶液,因为水解导致某些离子浓度变小,例如nh4cl溶液中离子浓度大小关系为:c( cl- )>c(nh4+ ) > c( h+ )> c( oh_ );naac溶液中离子浓度大小关系为:c( na+ )>c(ac_ )> c( oh_ )> c( h+ )。
高中化学盐溶液中离子浓度大小的比较总结
盐溶液中离子浓度的大小比较既是一个重要知识点,也是高中化学一个难点,但只要掌握了有关知识、原理和规律,结合解题技巧,就能轻车熟路,达到举一反三的最佳效果。
一、基本知识在盐溶液中存在着水的电离平衡,可能还有盐的水解、电离平衡,所以就有下列关系:1.c(H+)与c(OH-)的关系:中性溶液:c(H+)=c(OH-)(如NaCl溶液)酸性溶液:c(H+)>c(OH-)(如NH4Cl溶液)碱性溶液:c(H+)<c(OH-)(如Na2CO3溶液)恒温时:c(H+)·c(OH-)=定值(常温时为10-14)2.电荷守恒:盐溶液中阴、阳离子所带的电荷总数相等。
如NH4Cl溶液中:c(NH4+)+c(H+)=c(Cl-)+c(OH-)如Na2CO3溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)3.物料守恒:某元素各种不同存在形态的微粒,物质的量总和不变。
如0.1mol/LNH4Cl溶液中:c(NH4+)+c(NH3·H2O)=0.1mol/L如0.1mol/LNa2CO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol/L二、解题方法和步骤1.判断水解、电离哪个为主。
(1)盐离子不水解不电离:强酸强碱盐,如NaCl、Na2SO4等。
(2)盐离子只水解不电离:强酸弱碱或弱酸强碱形成的正盐,如NH4Cl、Na2CO3等。
(3)盐离子既水解又电离:多元弱酸形成的酸式盐,以水解为主的有NaHCO3、NaHS、Na2HPO4等;以电离为主的有NaHSO3和NaH2PO4等。
(4)根据题意判断:如某温度下NaHB强电解质溶液中,当c(H+)>c(OH-)时,以HB-的电离为主;当c (H+)<c(OH-)时,以HB-的水解为主。
对于弱酸HX与强碱盐(NaX式)的混合溶液中,当c(H+)>c(OH -)时,以HX的电离为主;当c(H+)<c(OH-)时,以X-的水解为主。
离子浓度比较
离子浓度比较离子浓度大小的比较方法--------------------------------------------------------------------------------1.同浓度的不同溶液中,同一离子浓度大小的比较首先,我们应明确强电解质的完全电离产生的离子的浓度比弱电解质的不完全电离产生的离子浓度要大;弱电解质的电离或离子的水解程度均很弱。
情况一:溶质只发生电离。
强电解质的离子的浓度(下角标大的>下角标小的离子的浓度)>弱电解质的>有抑制作用的弱电解质的电离情况二:电离后离子又发生水解。
(1)强电解质的离子的浓度(下角标大>下角标小的离子的浓度);(2)有抑制作用的水解>单一离子的水解>有促进作用的水解(双水解)情况三:对于离子既发生水解又发生电离时,应视电离和水解程度的相对大小而定。
例1:物质的量浓度相同的下列物质,在指定的离子浓度的比较中错误的是()A.c(PO43-):Na3PO4 >Na2HPO4 >NaH2PO4 >H3PO4B.c(CO32-):(NH4)2CO3 >Na2CO3 >NaHCO3 >NH4HCO3C.c(NH4+):(NH4)2SO4 >(NH4)2CO3 >NH4HSO4 >NH4ClD.c(S2-):Na2S >H2S >NaHS>(NH4)2S分析:A:考虑电离后三者电离出的c(H+)逐渐增大,对产生PO43-的电离有抑制作用,故A正确;B:Na2CO3最大,其次是(NH4)2CO3,因为后者要发生水解,NaHCO3和NH4HCO3中由HCO3-电离产生,而NH4HCO3中HCO3-和NH4+相互促进水解,HCO3-浓度较小,NaHCO3 >NH4HCO3,故B错误;C:四种盐均完全电离,(NH4)2SO4 和(NH4)2CO3较大,但后者的阴阳离子会发生相互促进的水解,应为(NH4)2SO4 >(NH4)2CO3,NH4HSO4 与NH4Cl,NH4HSO4 电离产生的H+对NH4+的水解有抑制作用,应为NH4HSO4 >NH4Cl,故C正确;D:Na2S和(NH4)2S较大,但后者发生双水解,应为Na2S>(NH4)2S,H2S 要电离产生S2-,为H2S的二级电离,程度很小,应为H2S >NaHS,故D错误。
离子浓度大小比较的方法和规律
离子浓度大小比较的方法和规律
方法和规律1:通过离子的电荷数比较离子浓度。
根据离子浓
度的定义,以及离子在溶液中的电离平衡反应,可以推导出离子浓度与离子的电荷数成正比关系。
即离子的电荷数越大,离子浓度越高。
因此,可以通过比较离子的电荷数来判断离子浓度的大小。
方法和规律2:通过溶液的浓度比较离子浓度。
根据浓度的定义,溶液中溶质的浓度与物质的量成正比。
离子浓度就是溶液中离子的浓度,可以通过比较溶液浓度来推测离子浓度的大小。
方法和规律3:通过电导率比较离子浓度。
电导率是电解质溶
液中电流通过的能力的度量。
溶液中离子的浓度越高,电导率越大。
因此,可以通过测量溶液的电导率来比较离子的浓度大小。
方法和规律4:通过沉淀反应比较离子浓度。
离子溶液中存在
着沉淀反应的特性,在一定条件下会生成可见的沉淀。
一般情况下,离子浓度较高的溶液会更容易发生沉淀反应。
因此,可以通过观察溶液是否生成沉淀来推测离子浓度的大小。
方法和规律5:通过离子的摩尔浓度比较离子浓度。
摩尔浓度
是指单位体积内的溶质物质的物质的量。
因此,可以通过比较离子的摩尔浓度来判断离子的浓度大小。
需要注意的是,离子浓度的大小比较还需要考虑其他因素,如
溶液的温度、溶解度等。
各种方法和规律可以结合使用,综合判断离子浓度的大小。
离子浓度大小的比较方法及规律
离子浓度大小的比较方法及规律-CAL-FENGHAI.-(YICAI)-Company One1离子浓度大小比较的方法和规律一、离子浓度大小比较的方法和规律1、紧抓住两个“微弱”:a弱电解质的电离是微弱的 b弱根离子的水解是微弱的。
2、酸式酸根离子既能电离又能水解,若电离能力大于水解能力则酸式盐溶液呈酸性,否则呈碱性。
常见呈酸性的是H2PO42-、、HSO3-对应的可溶盐的溶液。
3、不同溶液中同一离子浓度大小的比较,要看溶液中其它离子对其产生的影响。
如在相同物质的量浓度的下列溶液中:①NH4Cl②NH4HSO4③CH3COONH4④NH3H2O。
c(NH4+)由大到小的顺序为②>①>③>④4、混合溶液中离子浓度大小的比较,首先要分析混合过程中是否发生化学反应,若发生反应,则要进行过量判断(注意混合后溶液体积的变化);然后再结合电离、水解等因素进行分析。
5、对于等体积、等物质的量浓度的NaX和弱酸HX混合求各微粒的浓度关系题,要由混合后溶液的PH大小判断电离和水解的关系。
常见的CH3COOH与CH3COONa等体积、等物质的量浓度混合、NH3H2O 与NH4Cl等体积、等物质的量浓度的混合都是电离大于水解。
6、三个重要的守恒关系①电荷守恒电解质溶液中,无论存在多少种离子,溶液总呈电中性,即阳离子所带的正电荷总数一定等于阴离子所带的负电荷总数。
如Na2CO3溶液: c(Na+)+ c(H+)=cC( HCO3-) +2c( CO32-)+c( OH-)②物料守恒如Na2CO3溶液,虽CO32-水解生成HCO3-,HCO3-进一步水解成H2CO3,但溶液中n(Na): n(C)=2:1 ,所以有如下关系:c(Na+)=2{c( HCO3-)+c( CO32-)+c( H2CO3)}③质子守恒即水电离出的OH-的量始终等于水电离出的H+的量。
如Na2CO3溶液,水电离出的H+一部分与CO32-结合成HCO3-,一部分与CO32-结合成H2CO3,一部分剩余在溶液中,根据c(H+)水=c (OH-)水,有如下关系:c(OH-)=c( HCO3-)+ 2c(H2CO3)+ c(H+)二、技巧1、在解题过程中,若看到选项中有“=”,则要考虑3个守恒关系:2、若守恒关系中只有离子,则考虑电荷守恒关系,若守恒关系中同时出现分子和离子,则考虑物料守恒和质子守恒;3、若选项中离子浓度关系以“>”连接,则主要考虑弱电解质的电离、弱根离子的水解以及各离子之间的相互影响等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
⑶混合溶液中离子浓度的大小比较-不反应型
变式训练2:将0.1 mol•L-1HCN溶液与等体积等浓度的NaCN溶液混合,溶液 显碱性,下列关系正确的是( )
A.c(CN-)+c(HCN)=0.2mol/L C.c(CN-)>c(Na+)> c(OH-)> c(H+)
B.c(CN-)>c(HCN) D.c(Na+)+ c(H+)= c(CN-)+ c(OH-)
⑶混合溶液中离子浓度的大小比较-不反应型
⑶混合溶液中离子浓度大小比较-相互反应型
恰好中和型
• 例1:等体积等浓度的MOH强碱溶液和HA弱 酸溶液混和后,混和液中有关离子的浓度 应满足的关系是( ) A.c(M+)>c(OH-)>c(A-)>c(H+) B.c(M+)>c(A-)>c(H+)>c(OH-) C.c(M+)>c(A-)>c(OH-)>c(H+) D.c(M+)+c(H+) =c(OH-)+c(A-)
⑵单一不同溶液中比较同一离子浓度的大小
• (3)比较相同浓度的①HCOONa、② CH3COONa、③Na2CO3 、④苯酚钠、⑤ NaHCO3 、⑥NaCl、⑦MgCl2、⑧AlCl3 ⑨ NaHSO4⑩Ba(OH)2 11 NaOH八种溶液pH值的 大小
⑶混合溶液中离子浓度的大小比较-不反应型
弱酸酸式盐:
⑵单一不同溶液中比较同一离子浓度的大小
例1:25℃时,在浓度为0.1 mol·L-1的 (NH4)2SO4、(NH4)2 CO3、(NH4)2Fe(SO4)2的溶 液中,测得c(NH4+)分别为a、b、c(单位为 mol·L-1)。下列判断正确的是( )
A.a=b=c
B.a>b>c
C.a>c>b
⑶混合溶液中离子浓度大小比较-相互反应型
恰好中和型
变式训练1:等体积等浓度的MOH碱溶液和 HA酸溶液混和后,混和液中有关离子的浓度 的关系是c(A-)>c(M+)>c(H+)>c(OH-),则下列说 法正确的是( )
A.MOH是强碱, HA是强酸 B. MOH是强碱, HA是弱酸 C. MOH是弱碱, HA是强酸 D.无法判断
• 例2:在0.1 mol·L-1的NH3·H2O溶液中,下列关系 正确的是 A.c(NH3·H2O)>c(OH-)>c(NH4+)>c(H+) B.c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+) C.c(NH3·H2O)>c(NH4+)=c(OH-)>c(H+) D.c (NH3·H2O)>c (NH4+)>c (H+)>c (OH-)
D.c>a>b
⑵单一不同溶液中比较同一离子浓度的大小
• 例2:(1996年上海高考题)物质的量浓度
相同的下列溶液中,NH4+浓度最大的是
• A. NH4Cl C.CH3COONH4
B.NH4HSO4 D.NH4HCO3
⑵单一不同溶液中比较同一离子浓度的大小
• 变式训练:
• (1)对比同浓度的下列溶液中c(NH4+)的大
㈠单一溶液中离子浓度大小比较-正盐溶液 水解是微弱的
• 例3:写出CH3COONa溶液中所有离子浓度 大小顺序:
㈠单一溶液中离子浓度大小比较-正盐溶液
• 例4:在氯化铵溶液中,下列关系式正确的 是( ) A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(NH4+)>c(Cl-)>c(H+)>c (OH-) C.c(Cl-)=c(NH4+)>c(H+)=c(OH-) D.c(NH4+)=c(Cl-)>c(H3 ②(NH4)2CO3 ③NH4HSO4 • ④(NH4)2SO4 ⑤CH3COONH4 ⑥NH3`H2O
⑵单一不同溶液中比较同一离子浓度的大小
• 变式训练: • (2)物质的量浓度相同的下列各溶液,由
水电离出的OH-的浓度由大到小的顺序 ________________________________ • ①NaHSO4 ② NaHCO3 ③ Na2CO3 ④ Na2SO4
㈠单一溶液中离子浓度大小比较-正盐溶液
• 例5:在Na2CO3溶液中所有离子浓度大小顺序:
变式1:在Na2S溶液中所有离子浓度大小顺序:
㈠单一溶液中离子浓度大小比较-正盐溶液 变式2:在(NH4)2SO4溶液中所有离子浓度大小顺序:
㈠单一溶液中离子浓度大小比较-酸式盐溶液 强酸酸式盐: 中强酸酸式盐:
高二化学选修四化学反应原理
溶液中离子浓度大小比较
氧气老师
分析溶液中微粒浓度关系的思维流程
㈠单一溶液中离子浓度大小比较-酸溶液 电离是微弱的
• 例1:在0.1 mol·L-1的CH3COOH溶液中 ,c(CH3COO-)、c(OH-)、c(H+)、c(CH3COOH)的 大小关系为:
㈠单一溶液中离子浓度大小比较-碱溶液
⑶混合溶液中离子浓度大小比较-相互反应型
• 变式训练2:将pH=3的盐酸溶液和pH=11的 氨水等体积混和后,溶液中离子浓度关系正 确的是
• A.c(NH4+)>c(Cl-)>c(H+)>c(OH-) • B.c(NH4+)>c(Cl-)>c(OH-)>c(H+) • C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) • D.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
例1:用等浓度等体积的NH4Cl和 NH3 ·H2O溶液混合,则混合后的溶液中离子浓度大小顺序是:
⑶混合溶液中离子浓度的大小比较-不反应型
• 变式训练1 :用物质的量都是0.1 mol的 CH3COOH和CH3COONa配制成1 L混合溶液, 对该混合溶液的下列判断正确的是( ) A. c(OH-)>c(H+) B.c(CH3COOH)+c(CH3COO-)=0.2 mol·L-1 C.c(CH3COOH)>c(CH3COO-) D.c(CH3COO-)+c(OH-)=0.2 mol·L-1
⑶混合溶液中离子浓度大小比较-相互反应型
PH等于7型
• 例2:常温下,将甲酸和氢氧化钠溶液混合 ,所得溶液PH=7,则此溶液中
• A.c(HCOO-) > c(Na+) • B. c(HCOO-) < c(Na+) • C. c(HCOO-) = c(Na+) • D.无法确定c(HCOO-) 与c(Na+)的关系
