有机化学中的手性概念与立体异构体
有机化学基础知识点整理立体异构与手性化合物

有机化学基础知识点整理立体异构与手性化合物有机化学基础知识点整理立体异构与手性化合物介绍:有机化学是研究有机物的结构、性质和反应的学科。
其中,立体异构与手性化合物是有机化学中的重要概念。
本文将为您整理基础的有机化学知识点,重点探讨立体异构和手性化合物。
一、立体异构1.1 定义立体异构是指分子的空间结构相同,但是在立体构型方面存在不同的化学物质。
即同一分子式的化合物,其空间结构不同,化学性质和物理性质也会相应变化。
1.2 分类1.2.1 构型异构构型异构是指分子内部原子的排列方式不同,导致空间结构也不同。
主要有以下几种形式:1.2.1.1 同分异构同分异构是指同种原子通过共价键连接,在排列或转动时可形成不同的构型。
如顺反异构、轴官能团异构等。
1.2.1.2 二面角异构二面角异构是指由于碳链之间存在着特定的旋转角度,分子在空间中不同部位产生不同构型的异构体。
如转平面异构。
1.2.2 空间异构空间异构是指构成分子的原子的连接方式不同,导致分子空间结构不同,无法通过旋转或转动使其重合。
主要有以下几种形式:1.2.2.1 键位置异构键位置异构是指在分子中,原子的连接方式或位置不同,导致分子的空间结构也会不同。
如环异构。
1.2.2.2 空间位阻异构空间位阻异构是指分子内部的原子或官能团由于空间位阻的影响,影响了分子的空间构型,从而导致异构体的产生。
二、手性化合物2.1 定义手性化合物是指分子或物体不重合与其镜像体的物质。
手性化合物包括手性立体异构体和不对称分子。
2.2 手性中心手性中心是指分子中一个碳原子与四个不同基团连接。
手性中心是产生手性的必要条件。
根据手性中心的性质,分子可以分为两种类型:2.2.1 单手性中心单手性中心的分子有两个镜像异构体,即L体和D体。
2.2.2 多手性中心多手性中心的分子有2的n次方个立体异构体,其中n为手性中心的个数。
2.3 光学异构体光学异构体是指由于手性中心的存在而产生的非重合的光学异构体。
有机化学基础知识点整理立体化学中的对映异构体

有机化学基础知识点整理立体化学中的对映异构体立体化学是有机化学领域中非常重要的一个分支,它主要研究物质在三维空间中的结构和性质。
其中,对映异构体是立体化学中的一个重要概念。
对映异构体简单来说就是在化学结构上镜像对称,但不能通过旋转、平移或振动使两者完全重合的两个分子。
本文将对立体化学中的对映异构体进行基础知识整理。
一、手性与立体中心手性是指物体或分子无法与其镜像重合的性质。
立体中心是一种导致手性的结构特征,具有四个不同的官能团或原子团(即存在手性碳原子)的分子会呈现手性。
在有机化学中,立体中心通常由手性碳原子或其他原子的立体位阻决定。
二、对映异构体的定义与性质对映异构体是指在化学结构上具有镜像对称但不能通过旋转、平移或振动使两者完全重合的分子。
对映异构体之间的镜像异构体称为对映体。
对映体具有相同的物理性质(如熔点、沸点),但在手性环境下却表现出截然不同的化学性质,如旋光性质(光学活性)。
三、对映异构体的表示方法1. 立体化学式:用空间模型或平面投影式表示对映异构体之间的空间关系。
2. 简化表示法:用R和S确定对映异构体之间的关系,即锚定的立体中心按顺时针或逆时针方向连接优先级不同的四个官能团或原子团。
四、对映异构体的生成和分类1. 通过手性诱导合成方法生成对映异构体,例如利用手性酯生成手性醇。
2. 对映异构体可分为绝对配置异构体和相对配置异构体。
- 绝对配置异构体是指两个对映异构体之间无法通过化学手段相互转化,它们的构型不同,但可能在反应活性上相似或相异。
- 相对配置异构体是指两个对映异构体在特定条件下可以通过化学手段相互转化,也就是互为可逆异构体,它们的构型不同,但在反应机理上是等价的。
五、对映异构体的应用与重要性1. 有机合成中的对映选择性:对映异构体在化学反应中体现出不同的活性和选择性,对映选择性是有机合成中非常重要的一个概念。
2. 药物研发与药理学:许多药物是对映异构体,其中一种对映体可能具有治疗效果,而另一种对映体却可能产生毒副作用。
一 手性---立体(三维)异构 - 分子识别与功能重点实验室 …
“ELN脯氨酰 4-氢化酶”的活性,导致“缺氧诱导 因子”水平下降。
黄皮中分离出来的,(Байду номын сангаас)-黄皮酰胺具有抗衰老,抗缺氧及 促智等作用,(+)-黄皮酰胺不仅无正作用,还有一定抑制 作用。
手性药物的药理作用
通过药物分子与体内的大分子之间严格的手性识别和匹配 而实现的。生物体的酶和细胞表面受体是手性的,两个对 映体在体内以不同的途径被吸收、活化或降解。 多 为例 以DOPA(多巴)为例:
这三位科学家获奖的意义还在于: “他们的发明帮助人们在认识和改造世界中
L-多巴生产工艺
不对称合成中最大的工业化例子 (Novatis, 1996):
(S)-异丙甲草胺除草剂(>10,000 >10 000 吨/年)
还有,如: 硫醚的不对称氧化:生产抗胃溃疡药,奥美拉唑,的新工艺 应用不对称异构化反应生产薄荷醇---日本高砂公司
5
B)化合物带有三价的杂原子, 如:N, S, P 等
具有角锥形结构,三个基团和孤对电子形成假四面体排列,可能 带有不对称性,即形成中心手性。
Cl N H CH3 N Cl H CH3 N H3C O Ph Ph
在溶液中稳定存在的三元杂环体系,不易翻转。 可分离到稳定的对映体。
Troger碱
两个N原子被环内亚甲 在室温下,N原子中心翻转很快,使对映体无法分离。 在室温下,与磷相邻的键翻转较慢,有可能得到手性膦, 即含磷的手性化合物。 基的固定,三级胺的翻 转受阻,两个对映体可 被拆分。
3.1 手性分子的命名(构型)规则
Fisher命名法则: 相对构型:将尽可能多的手性化合物与标准化合物的构型 相关联,用以推导这些化合物的构型。
高三化学有机化合物的立体化学与手性

高三化学有机化合物的立体化学与手性在有机化学中,立体化学是研究分子的空间构型和异构体之间的关系的重要分支,而手性是其中一个重要的概念。
本文将就高三化学有机化合物的立体化学与手性展开讨论。
一、立体化学概述立体化学是研究分子化学结构的三维空间构型以及其中的隐性和显性不对称现象的学科。
在有机化合物中,由于碳原子的四个键对外围的四个方向是等效的,因此它有可能形成立体异构体。
立体异构体是指化学结构相同但空间构型不同的化合物。
二、手性的定义与特点1. 定义:手性是指一种分子或物体与其镜像体不能完全重合的性质。
一个有手性的分子称为手性分子。
2. 特点:(1)不对称性:手性分子的特点是它们在镜像平面的两个像上没有重叠,无法通过旋转或平移使其与其镜像体完全一致。
(2)旋光性:大部分手性分子都能使平面偏振光绕其传播方向旋转,这种现象称为旋光性。
(3)非超可重合性:手性分子与其镜像体之间的对映异构体无法通过旋转或平移重合。
(4)不於酸碱反应:手性分子的酸碱反应常常只发生在一个对映异构体上,另一个对映体则无反应。
三、手性源手性源是导致分子手性的原因,主要有以下几类:1. 手性碳原子:当一个碳原子的四个键中的三个键与不同的基团相连接时,该碳原子就是手性碳原子,即手性中心。
手性中心通常以希腊字母R和S表示。
2. 不对称碳原子:不对称碳原子是指两个或多个不同的基团连接在一个碳原子上,这个碳原子不是手性中心,但其分子整体仍然是手性的。
3. 手性配体:配体是指连接在过渡金属中心的分子或离子,具有手性的配体能够形成手性的配合物。
四、手性的表示方法1. 立体公式:Fischer投影式和Newman投影式是常用的手性分子的表示方法。
Fischer投影式用交叉吸引表示手性中心,箭头指向较低优先级的基团;Newman投影式用与碳原子键相互垂直的线表示手性中心。
2. 绝对构型:分子的立体构型分为R型和S型两种,根据手性碳原子的各个取代基团的优先级进行判断。
有机化学基础知识点整理立体化学中的手性识别

有机化学基础知识点整理立体化学中的手性识别立体化学中的手性识别手性是有机化学中一个非常重要的概念,广泛应用于药物合成、材料科学等领域。
手性识别作为手性合成的前提和基础,是有机化学中的基础知识点之一。
本文将对手性的概念、手性分子的产生原因以及手性识别的方法进行整理和介绍。
一、手性的概念手性是指分子不具备轴对称性或面对称性,不能与其镜像重合的性质。
手性分子由手性中心或手性轴引起,具有两种不同的立体异构体,称为对映异构体或对映体。
对映体之间的相互转化需要打破化学键,因此具有非常高的化学和生物活性差异,尤其在药物研发中具有重要的作用。
二、手性分子的产生原因手性分子的产生主要有两种原因:空间异构和动力学异构。
1. 空间异构空间异构是由于手性分子的分子结构产生的,包括手性中心、手性轴和手性面。
手性中心是指一个分子中有一个碳原子与四种不同的基团连接,或者是一个原子具有两个或两个以上的非环顺式键。
手性中心对称关系下的两个异构体通过对称中心对立,互为镜像。
手性轴是指没有手性中心的分子,但其结构存在旋转轴。
手性轴的旋转将分子转化为其镜像分子。
手性面是指没有手性中心和手性轴的分子,但其结构存在镜面反射形成的平面。
2. 动力学异构动力学异构是指分子在一定条件下,通过化学反应或物理作用发生构象变化而产生的异构体。
这种异构体的转化一般不需要打破化学键,可以通过温度、溶剂等因素来控制。
三、手性识别的方法手性识别的方法主要包括实验方法和理论方法两种。
1. 实验方法实验方法是通过物理性质或化学性质的差异来进行手性的识别。
常用的实验方法包括:(1)旋光法:利用手性分子旋光光线的性质来确定其手性。
(2)质谱法:利用手性分子在质谱仪上的质谱图特征来判断其手性。
(3)核磁共振法:利用手性分子在核磁共振谱仪上的信号差异来区分其手性异构体。
2. 理论方法理论方法是通过计算机模拟和量子化学方法来预测和解释手性分子的性质和行为。
常用的理论方法包括:(1)密度泛函理论:利用电子结构计算方法和密度泛函理论来预测手性分子的光学旋光性质。
手性名词解释有机化学

手性名词解释有机化学1.“手性”的来历:手性是指化学反应中,原子或基团的空间构型和对映体之间存在的某种关系。
两个或多个对映异构体如能很好地重叠,则形成有确定熔点的固体,但是很少会在蒸气压低于3.6kPa下形成固体。
非极性键之间通过共价键相结合而产生手性,这些原子在空间上形成一定的角度,称为“手性棱镜”。
所有碳原子都具有手性,除了C=C、 O、 F、Br、 Cl。
等元素的原子,其它都没有手性。
其中:只有C=C、 F、 Br 是非对映异构体。
非对映异构体互为同分异构体,也就是说他们的构型和物理性质是一样的,仅仅由于不同的原因造成立体结构的不同。
它们的主要区别在于,在对映体形成时所使用的原子排列不同,从而在晶体结构中表现出不同的空间群。
手性一般是以共价键和非共价键相结合而表现出来的,它有几何构型的概念,一般在每一类型的手性中,每一个手性分子都含有一个分子轨道。
手性分子中每一个碳原子和其余4个原子以共价键结合。
当分子中含有N个碳原子时,可以有(1)N个异构体; (2)N个立体异构体。
手性分子对周围环境敏感,因此常将手性分子配成药物或调节剂。
在实际操作中经常需要手性分子的混合物,因此最大可能获得纯净的手性分子是重要的,且纯度要高,另外要求分子量准确。
如果手性分子的某些官能团有毒,在制备前要考虑如何去除这些官能团。
尽管目前已经建立了许多高效的分离方法,但要获得特定的纯净的分子仍然很困难。
手性分为正、负两种,用箭头的方向表示原子排列的方向,即与键合的化学键方向相反者为手性分子。
例如,顺磁性的H、 NH、 OH 等在溶液中会因为磁场的作用转变为正手性分子,如HClH。
反磁性的RN、 NR、 NHR等在磁场作用下则会变成反手性分子。
相反,酸性的H、 NH、 OH等在强碱作用下则变成负手性分子,如HClNH。
手性参数(手性常数):在非共价键力作用下,构型参数L、 L 的最小值为0。
式中M、 M、 M分别是原子序数、半径、电负性。
有机化学中的立体化学

有机化学中的立体化学立体化学是有机化学中的重要分支,研究有机化合物中分子的空间结构和立体构型的相关规律。
随着分析仪器和实验技术的发展,立体化学在有机合成和药物研发等领域中具有重要的应用价值。
一、立体化学的基本概念立体化学关注有机分子中的空间结构和分子的各个部分的排列方式。
在立体化学中,我们关注的主要是手性和立体异构体。
1. 手性:手性是指一个分子无法与其镜像重叠的特性。
具有手性的分子称为手性分子,两个互为镜像的手性分子称为对映异构体。
例如,氨基酸和糖类等有机分子都有手性。
2. 立体异构体:立体异构体是指拥有相同分子式但不同立体结构的化合物。
立体异构体分为构象异构体和对映异构体两种。
构象异构体是由于分子的旋转或扭曲而产生的不同构型,它们在空间结构上有一定的自由度。
例如,环状化合物的立体异构体就是构象异构体,如环己烷的椅式和船式异构体。
对映异构体是由于分子的立体中心存在不对称而产生的异构体。
对映异构体在物理和化学性质上通常非常相似,但与其他对映异构体之间的相互作用却往往存在巨大差异。
拥有对映异构体的有机分子是手性分子,也是立体化学中研究的重点。
二、立体化学的研究方法立体化学的研究方法主要包括实验方法和理论方法。
实验方法主要包括X射线衍射、核磁共振(NMR)光谱、圆二色光谱、旋光度测量和质谱等技术。
这些技术通过测量和分析分子的物理性质来确定其立体结构,为揭示分子构形提供了重要的实验依据。
理论方法主要包括量子化学、分子力学和分子动力学等。
量子化学通过计算分子在不同构型下的能量和性质来预测和解释分子的立体结构、反应机理和性质。
分子力学和分子动力学通过计算机模拟方法模拟和预测分子的构型和动态行为。
三、立体化学的应用立体化学广泛应用于有机合成、药物研发和生物化学等领域,并取得了重要的研究成果。
1. 有机合成:立体化学对于有机合成的研究具有重要的指导意义。
在合成有机化合物的过程中,了解分子的立体结构能够预测和解释反应的立体选择性和对称性。
异形同构的概念

异形同构的概念异形同构的概念异形同构是指在化学结构上不同但在分子式、原子数和原子种类等方面相同的有机化合物。
这些化合物中,原子的排列方式不同,但它们之间具有相似的物理和化学性质。
异形同构体可以分为两种类型:立体异构体和位置异构体。
一、立体异构体立体异构体是指分子中存在不同空间排列方式的化合物。
它们之间的差别在于它们所包含的立体异性中心(或称手性中心)不同。
在有机化学中,立体异构体通常用R/S符号来表示。
1. 手性手性是指分子或离子不能通过旋转重叠而完全重合的特性。
手性分为左右手性,即对映异构体(也称为镜像对映异构体)。
由于对映异构体具有相反的光学旋光性质,因此它们往往在生物学、药学等领域非常重要。
2. 立体异构立体异构是指由于空间排列方式不同而导致分子具有不同的物理和化学性质。
例如,在乙烯基环丙烷中,如果氢原子被取代,则会出现两种不同的立体异构体,分别是顺式异构体和反式异构体。
二、位置异构体位置异构体是指分子中原子的相对位置不同,但它们所包含的原子数和种类相同。
位置异构体通常用数字和字母组合来表示。
1. 二甲基苯二甲基苯是一种具有三个位置异构体的化合物。
这三种化合物分别为:1,2-二甲基苯、1,3-二甲基苯和1,4-二甲基苯。
这三种化合物在物理和化学性质上都有所不同。
2. 氨基酸氨基酸是一类具有两个手性中心的化合物。
它们可以通过改变手性中心的配置而形成四种不同的立体异构体。
这些立体异构体在生物学、药学等领域非常重要。
总结:异形同构是指在分子式、原子数和原子种类等方面相同但在化学结构上不同的有机化合物。
它们可以分为两种类型:立体异构体和位置异构体。
立体异构是由于空间排列方式不同而导致分子具有不同的物理和化学性质,而位置异构则是由于分子中原子的相对位置不同。
异形同构体在生物学、药学等领域非常重要,因为它们具有不同的物理和化学性质,可以用于制备新的药物或化合物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化学中的手性概念与立体异构体有机化学是研究有机物结构、合成和性质的科学领域。
在有机化学中,手性(chirality)是一个重要的概念,涉及到分子的空间结构和立
体异构体的存在。
本文将介绍手性的定义,手性的表现形式以及立体
异构体的种类与分类。
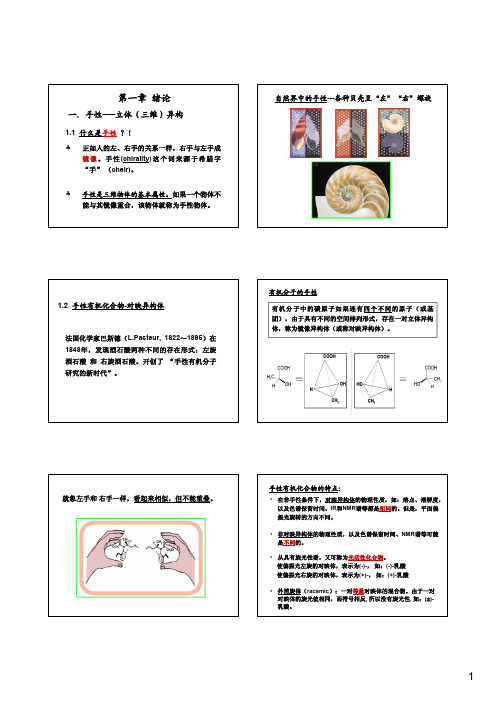
一、手性的定义
手性是指物体不与其镜像完全重合的性质。
也就是说,一个手性分
子的镜像结构与原分子并不相同。
这种不对称性在有机化学中非常常见,并且对于分子的性质和功能有着重要的影响。
二、手性的表现形式
手性可以通过不同的方式表现出来,其中最常见的是手性中心、手
性轴和手性面。
1. 手性中心
手性中心是指分子中一个碳原子上的四个取代基围绕着该碳原子排
列成一个四面体的结构。
当这四个取代基中的任意两个取代基不能通
过旋转互相重合时,就存在手性中心。
2. 手性轴
手性轴是指分子中存在着旋转对称性,但在沿着该旋转轴方向的一
侧存在着不同的官能团取代的情况。
这种情况下,分子仍然是手性的。
3. 手性面
手性面是指分子中的一个平面,该平面上的取代基不能通过翻转互
相重合。
例如,苯环上的取代基就可以形成手性面。
三、立体异构体的种类与分类
立体异构体是指在空间结构上相互非重合、形状不同的同分异构体。
根据手性的不同表现形式,立体异构体可以分为两类:对映异构体和
旋光异构体。
1. 对映异构体
对映异构体是指存在手性中心的分子,其镜像结构与原结构不完全
重合。
两个对映异构体是非重叠的、无法相互转化的,它们构成了一
对对映异构体。
2. 旋光异构体
旋光异构体是指分子对极性光的旋光性质呈现不同的现象。
旋光异
构体包括旋光异构体和旋光体系。
旋光异构体在化学反应中的行为和
性质常常有所不同。
根据旋光性质的不同,旋光异构体可以分为两类:左旋异构体和右
旋异构体。
这两种异构体的旋光度(旋光光度的绝对值)和旋光方向
都是不同的。
四、手性在生物体中的重要性
手性在生物体中具有重要的作用和意义。
一方面,生物体内的许多
分子都是手性的,比如葡萄糖、氨基酸等。
手性的存在可以影响分子
与其他分子之间的相互作用和反应,从而决定了生物体内许多生理过
程的进行。
另一方面,手性药物的研究和制备也是有机化学中的重要领域之一。
手性药物的左旋异构体和右旋异构体可能具有不同的药理活性和副作用,因此对于手性药物的研究和应用需要更加细致的分析和控制。
总结:
有机化学中的手性概念与立体异构体是研究有机物结构的重要内容。
手性的存在通过手性中心、手性轴和手性面等形式进行表现,而立体
异构体则可分为对映异构体和旋光异构体。
手性在生物体中扮演着重
要角色,不仅影响生物体内的许多分子相互作用和反应,还对手性药
物的研究和应用具有重要影响。
对手性的深入理解和应用将进一步推
动有机化学研究的发展。
