第十九章:碳水化合物
有机化学 高鸿宾 第四版 答案 第十九章_糖

第十九章 碳水化合物(一) 写出D-(+)-葡萄糖的对映体。
α和β的δ-氧环式D-(+)-葡萄糖是否是对映体?为什么?解:D-(+)-葡萄糖的对映体为CH 2OHHOH H HO OH H HOH CHO (L- (-)-葡萄糖)。
α和β的δ-氧环式D-(+)-葡萄糖不是对映体,因为α和β的δ-氧环式D-(+)-葡萄糖之间不具有实物与镜像的关系。
α和β的δ-氧环式D-(+)-葡萄糖分子中均含有五个手性碳原子,其中有四个手性碳的构型相同,只有苷原子的构型不同,所以它们互为差向异构体或异头物。
(二) 写出下列各化合物立体异构体的投影式(开链式):(1)O OH OHOHOCH 2OH H (2)OOHHOC OHOH H 2OH(3)OOHHOC NH 2OH H 2OH解:(1)CH 2OHOH HHO H HO H OH HCHO (2)CH 2OHOH HH OH H OH OH HCHO (3)CH 2OHHOH OH H NH 2H HOH CHO(三) 完成下列反应式:(1)COOH CH 2OHOH HH OH HOH CH 2OHO HO323(2) OOHHOHOOH CH 2OH3dry HClOOHHOHOOCH 3CH 2OH(3)CHOCH 2OH OH HH OH 3内消旋酒石酸(4)4CHOCH 2OHOH HHO H 旋光性丁四醇(5)OOHHO HO OCH 3CH 2OHHIO 4+ HCOOH COCOCH3C H H OO H 2OH(6)2KOHOOPhCH 2OOCH 3O O PhPhCH 2H O OHOOCH 3OO Ph(7) CH 2OHOH H OH H H HCHO HIO CHOH H CHO HCOOH HCHO ++(8)(CH CO)OH O CH 2OHCH 2OH HOCH 2HO HOOHO OHOCH 2OOCCH 3CH 2OOCCH 3CH 3COOCH 2CH 3COO CH 3COOOO OOCCH 3CH 3C OCCH 3O 蔗糖八乙酸酯(四) 回答下列问题:(1) 单糖是否均是固体?都溶于水?都不溶于有机溶剂?都有甜味?都有变旋光现象? 答:一般一般情况下,是。
食品化学 第十九章 碳水化合物 半缩醛形成机理最清楚

(甲) 氧化
A.溴水氧化和硝酸氧化
单糖具有还原性,多种氧化剂如溴水、硝酸、Fehling or Tollen’s试剂等,都能将单糖氧化。
COOH
COOH
Br2/H2O
HNO3
葡萄糖酸
葡萄糖
COOH
葡萄糖二酸
醛糖 Br2/H2O 酮糖 Br2/H2O
糖酸
x
问题:如何用化学方法区别葡萄糖和果糖?
解:
葡萄糖 果糖
CH2OH O
HO
HO
H OH
OH
a-D-(+)-葡萄糖
x
CH2OH H HO O OH
OH
OH
HO CH2OH O
HO
OH
OH
x
H
b-D-(+)-葡萄糖
CH2OH OH HO O H
OH
OH
(4) 单糖的化学性质
(甲) 氧化 (乙) 还原 (丙) 脎的生成 (丁) 苷的生成
(4) 单糖的化学性质
(红)
糖(醛糖or酮糖)+ Ag(NH3)2NO3 OH- Ag + 氧化产物
(银镜)
单糖与Fehling or Tollen’s的反应可用来区别还原糖和非 还原糖。 定义: 还原糖——能与Fehling or Tollen’s发生反应的糖。
酮糖能与Fehling or Tollen’s反应的原因——差向异构化
(C5上羟甲基与苷羟基不同侧) a-D-(-)-呋喃果糖
1
2 C=O
3 4 5 6
6
HOH2C O OH
5
H
4
HO 2 3 C1H2OH
OH
b-D-(-)-果糖 (C5上羟甲基与苷羟基同侧)
碳水化合物

有机化学课程教案编写日期:2009 年 12月 28日章、节(或课题、单元)名称第十九章碳水化合物授课学时 3目的要求1、掌握糖类化合物的涵义、分类和命名方法。
2、掌握葡萄糖和果糖的构造式、构型式(Fischer式、Haworth式)和构象式以及确定葡萄糖构型的方法及其推导过程。
3、了解葡萄糖在水溶液中的存在形式(环状半缩醛),掌握变旋现象和半缩醛羟基的涵义,并能够解释产生变旋现象的原因和α,β-异头物在结构上的差别。
4、掌握糖苷、苷元、吡喃型糖和呋喃型糖的涵义,学会把单糖开链的Fischer 投影式转换成Haworth透视式的方法。
5、掌握单糖的化学性质,并且要注意每个性质的具体用途,比如在化学鉴别方面。
7、掌握双糖中蔗糖、麦芽糖、纤维二糖、乳糖的糖苷键类型和苷键形成的过程。
8、了解淀粉和纤维素的组成及结构特征以及它们在结构、性质上的主要区别和它们不具有还原性的原因;重点:葡萄糖、果糖、麦芽糖、蔗糖、淀粉、纤维素的结构和性质。
难点:1、单糖开链式的Fischer投影式与Haworth透视式的转换2、糖苷、苷元、α-1,4-糖苷键和β-1,4-糖苷键的形成3、蔗糖的结构教学组织教学方法:课堂教学采用多媒体教学,以ppt为主。
作业:P609二、三(6、7、8除外)、五(2、4)、六、十(选做)参考书目文献:1、汪小兰编,有机化学(第三版) ,北京:高等教育出版社,1997, 213~2392、徐寿昌编,有机化学(第二版) ,北京:高等教育出版社,1993, 431~4493、刘庄、丁辰元主编,普通有机化学,北京:高等教育出版社,1993. 300~3124、袁履冰主编,有机化学,北京:高等教育出版社,1999, 393~4205、甘景镐等.天然高分子化学. 北京:很内行教育出版社,1993. 163~2426、杜灿屏等主编. 21世纪有机化学发展战略. 北京:化学工业出版社,2002. 217~220授课小结授课情况基本正常。
碳水化合物
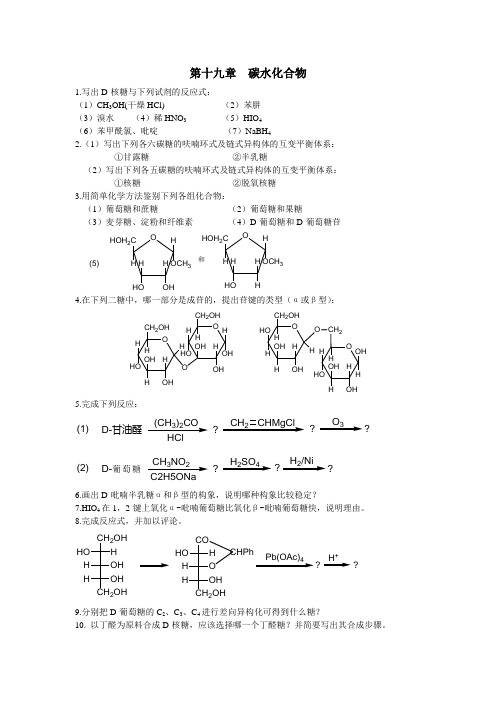
第十九章 碳水化合物1.写出D-核糖与下列试剂的反应式:(1)CH 3OH(干燥HCl) (2)苯肼 (3)溴水 (4)稀HNO 3 (5)HIO 4 (6)苯甲酰氯、吡啶 (7)NaBH 42.(1)写出下列各六碳糖的呋喃环式及链式异构体的互变平衡体系:①甘露糖 ②半乳糖(2)写出下列各五碳糖的呋喃环式及链式异构体的互变平衡体系:①核糖 ②脱氧核糖3.用简单化学方法鉴别下列各组化合物:(1)葡萄糖和蔗糖 (2)葡萄糖和果糖(3)麦芽糖、淀粉和纤维素 (4)D-葡萄糖和D-葡萄糖苷OHOH 2C H H HOH OHH OCH 3和OHOH 2C H H HOH HH OCH 3(5)4.在下列二糖中,哪一部分是成苷的,提出苷键的类型(α或β型):OCH 2OHHH HOOH HH OHH OOCH 2OHHH HO OH H OHH OH OCH 2OHHHOHOH HH OHO H CH 2O HH HOOH HH OHOH H5.完成下列反应:D-甘油醛(CH 3)2CO ?CH 2CHMgCl?O 3?(1)D-葡萄糖CH 3NO 2?H 2SO 4?H 2/Ni?(2)6.画出D-吡喃半乳糖α和β型的构象,说明哪种构象比较稳定?7.HIO 4在1,2-键上氧化α-吡喃葡萄糖比氧化β-吡喃葡萄糖快,说明理由。
8.完成反应式,并加以评论。
CH 2OH HO H H OH CH 2OHHOH COHO H H O CH 2OHHOH CHPh4?H +?9.分别把D-葡萄糖的C 2、C 3、C 4进行差向异构化可得到什么糖?10. 以丁醛为原料合成D-核糖,应该选择哪一个丁醛糖?并简要写出其合成步骤。
11.2-庚酮糖——景天庚糖-1,7-二磷酸酯可通过赤藓糖-4-磷酸酯和二羟基丙酮磷酸酯的醇醛缩合反应进行生物合成。
用反应物的结构式指出醇醛缩合的过程及写出缩合产品的结构式(不必指出两个新手性中心的构象)。
南京医科大学有机化学Chap19-碳水化合物练习题
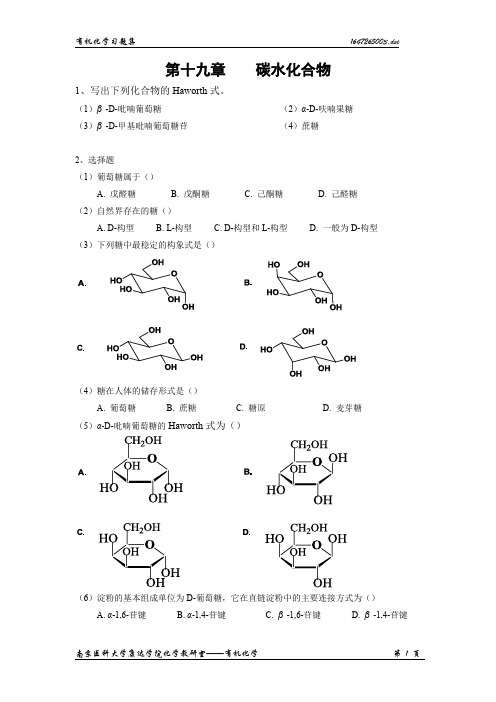
第十九章碳水化合物1、写出下列化合物的Haworth式。
(1)β-D-吡喃葡萄糖(2)α-D-呋喃果糖(3)β-D-甲基吡喃葡萄糖苷(4)蔗糖2、选择题(1)葡萄糖属于()A. 戊醛糖B. 戊酮糖C. 己酮糖D. 己醛糖(2)自然界存在的糖()A. D-构型B. L-构型C. D-构型和L-构型D. 一般为D-构型(3)下列糖中最稳定的构象式是()(4)糖在人体的储存形式是()A. 葡萄糖B. 蔗糖C. 糖原D. 麦芽糖(5)α-D-吡喃葡萄糖的Haworth式为()(6)淀粉的基本组成单位为D-葡萄糖,它在直链淀粉中的主要连接方式为()A. α-1,6-苷键B. α-1,4-苷键C. β-1,6-苷键D. β-1,4-苷键(7)下列糖与HNO3反应后,产生内消旋体的是()(8)互为差向异构体的两种糖,一定互为()A. 端基异构B. 互变异构C. 对映体D. 非对映体(9)D-吡喃葡萄糖与1mol无水乙醇和干燥HCl反应得到的产物属于()A. 醚B. 酯C. 缩醛D. 半缩醛(10)下列叙述正确的是()A. 糖类又称为碳水化合物,都符合C m(H2O)n通式B. 葡萄糖和果糖具有相同分子式C. α-D-葡萄糖和β-D-葡萄糖溶于水后,比旋光度都会增大D. 葡萄糖分子中含有醛基,在干燥HCl下,与1mol甲醇生成半缩醛,与2mol甲醇生成缩醛3. 是非题(1)变旋光现象是由于糖在溶液中发生水解而产生的一种现象。
()(2)糖苷通常由糖的半缩醛羟基和任一具有羟基的配体化合物脱水而生成。
()(3)由于β-D-葡萄糖的构象为优势构象,所以在葡萄糖水溶液中,其含量大于α-D-葡萄糖。
(4)葡萄糖、果糖、甘露糖三者既为同分异构体,又互为差向异构体。
()(5)β-D-甲基吡喃葡萄糖苷在酸性水溶液中会产生变旋光现象。
()。
有机化学 第19章 碳水化合物

D–葡萄糖
CH2OH CO HO H H OH H OH CH2OH
D–果糖
HO C
H OH HO H
H OH H OH
CH2OH
D–葡萄糖
OH C
HO H H OH
HO H HO H
CH2OH
L–葡萄糖
CH2OH
CO HO H
H OH H OH
CH2OH
CH2OH
CO H OH HO H HO H
D-葡萄糖脎
NH2 NH2 (产物同上)
D-果糖脎
NH2 NH2 (产物同上)
D-甘露糖脎
CH2OH
CH2OH
糖脎有一定熔点,生成脎的反应用于鉴定 或鉴别醛糖、酮糖。
(4) 糖苷(糖甙)的生成
单糖氧环式的甙羟基(半缩醛羟基)比醇羟 基活泼,在酸或酶催化作用下很容易与醇反
应生成缩醛:
HO HO
CH2OOH HO CHOH
CH3OH
干 HCl 或酶
CH2OOH
HO HO
+ OCH3
OH
甲基-β-D-葡萄糖苷
HO HO
CH2OOH HO OCH3
反应可逆。
甲基葡萄糖苷没有甙羟基,在水溶液中
不能转化成开链式,因此不能使Tollens试剂
和Fehlig试剂还原,所以糖苷没有还原性。
(5) 糖醚和糖酯的生成
单糖在碱的存在下,与硫酸二甲酯作用, 所有羟基都醚化:
OH
H+
或酶
CH2OH O
HO HO
+
1CH2OH
O
6CH2OH
2 HO5
HOOH
HO 3 4 OH
蔗糖[α]20D= +66°
《碳水化合物》课件

成人每天碳水化合物的适宜摄入量为 占总能量的50-65%,即250-350克/ 天。
儿童碳水化合物摄入量
儿童每天碳水化合物的适宜摄入量为 占总能量的40-60%,具体摄入量根据 年龄、性别和活动水平等因素而有所 不同。
膳食建议
选择全谷类
全谷类是碳水化合物的主要来源 ,含有丰富的膳食纤维、维生素 和矿物质,建议每天食用1-2份全
谷类食物。
控制糖分摄入
糖分摄入过多会增加肥胖、糖尿病 和心血管疾病的风险,建议限制添 加糖的摄入,如糖果、甜饮料等。
注意食物搭配
碳水化合物应与蛋白质、脂肪等营 养素搭配食用,以提供更全面的营 养。
特殊人控制碳水化合物 的摄入量,选择低升糖指数(GI )的食物,如全谷类、蔬菜和水 果等。
碳水化合物与其他营养素的关系
总结词
碳水化合物与其他营养素之间存在密切的关系,它们之间的相互作用对人体的健康和疾 病发展产生重要影响。
详细描述
碳水化合物是人体所需的重要营养素之一,它与蛋白质、脂肪等其他营养素之间存在密 切的关系。它们之间的相互作用对人体的健康和疾病发展产生重要影响,如碳水化合物 和脂肪之间的相互作用对糖尿病、肥胖等疾病的发展具有重要影响。因此,了解它们之
水果类食物
总结词
水果类食物含有一定量的碳水化合物,是人们日常饮食中的重要组成部分。
详细描述
水果中含有果糖、葡萄糖和蔗糖等糖类物质,是人体能量的重要来源之一。同时 ,水果还富含维生素、矿物质和膳食纤维等营养素,对人体健康有益。
蔬菜类食物
总结词
蔬菜类食物含有一定量的碳水化合物, 是人们日常饮食中的重要组成部分。
碳水化合物在生物医学领域的应用
总结词
第十九章 糖类化合物

单糖中最常见的是葡萄糖和果糖。这两种糖从结构和性质上都 可以作为各种单糖的代表。所以我们以这两种糖为例来讨论单糖的 构造、构型、构象和她它们的性质。
一、单糖的构造式
对葡萄糖分子式的推导 问:经验式CH2O,相对分子质量为180,求葡萄糖的分子式?
C6H12O6
根据下列信息推出葡萄糖的分子结构: 1、用钠汞齐还原得己六醇,进一步用HI还原得正己烷
2、构型的标记和表示方法
糖类化合物的R,S标记法 当投影式最小的基团在横线上, 顺时针——S 逆时针——R 当投影式最小的基团在竖线上, 顺时针——R 逆时针——S
(i) 写为糖的 Fischer 投影式,
(ii) 将手性碳上的氢省略 (iii) 将手性碳上的醛基与羟基省略(注意羟甲基的写法)
CHO H OH HO H H OH H OH CH OH 2 CHO OH HO OH OH CH OH 2 CHO
Br2/H2O Br2/H2O
x
Ç Ë Ì á
问题:如何用化学方法区别葡萄糖和果糖?
萄 糖 解 : 葡 果 糖
B r / H O 2 2
褪 色
不 褪 色
C.硝酸氧化
对醛糖的氧化 将醛糖氧化成糖二酸,氧化的部位分别链端的醛基和链尾的 羟甲基
CHO
HNO3
COOH
CH 2 OH
D-葡萄糖酸
COOH
D-葡萄糖二酸
木糖还原后生成木糖醇,其第三个碳原子成为假不对称碳原子,无旋光性。
CHO OH HO OH CH2OH NaBH4 HO OH CH2OH CH2OH OH
D-葡萄糖和L-古罗糖还原后生成同一多元醇——葡萄糖醇。
CH O OH HO HO OH NaBH 4 OH CH OH 2 OH OH CH OH 2 HO CH OH 2 CH OH 2 OH HO HO CH OH 2 HO HO OH NaBH 4 HO CH OH 2 OH CH O
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
O
H
HO
C C-OH
H
C HO-C-H
O
H
CH2OH 烯醇式 ( c) CH2OH C=O
CH2OH D-果糖(31%)
=
CH2OH D-甘露糖 (3%)
2. 生成糖脎反应 醛或酮的羰基与苯肼反应生成苯腙: C=O + H2N-NH苯肼
C=N-NH苯腙
醛糖或酮糖与苯肼反应生成糖脎。 CHO + 3 H2N-NHCH2OH
酮氧化后引起碳链的断裂
CH2OH C=O (CHOH)3 CH2OH
HNO3
复杂的产物
葡萄糖与HCN加成后水解生成六羟基酸,再被HI还原 得正庚酸—— 证明葡萄糖是醛糖。 CHO (CHOH)4 CH2OH HO
HCN
葡萄糖
CN CH (CHOH)4 CH2OH
HO
H2O
H+
COOH CH (CHOH)4 CH2OH
酮糖—— 多羟基酮
C3糖—— 丙糖 (或三碳糖)
单糖根据含 碳数可分为 C4糖—— 丁糖(或四碳糖) C5糖—— 戊糖(或五碳糖) C6糖—— 己糖(或六碳糖)
一、单糖的构造式(以葡萄糖和果糖为例)
(以葡萄糖和果糖为例)
1. 经元素分析知葡萄糖、果糖分子中有C、H、O三种元素。 分子式:C6H12O6
三、单糖的化学反应
1.差向异构化
在碱性水溶液中,D-葡萄糖可以转化为D-甘露糖和 D-果糖的混合物。(通过羰基-烯醇式互变)
这三种糖有三个手性碳构型完全相同,只有C2中的
碳原子不同,称为差向异构体。
CHO CHO
CH2OH C=O
CH2OH D-葡萄糖
CH2OH D-甘露糖
CH2OH
D-果糖
C H-C-OH (a) CH2OH D-葡萄糖 (64%)
碳水化合物依水解性质可分为三类: 单糖——不能再被水解的碳水化合物, 如葡萄糖等 特点:白色结晶,一般有甜味,可溶于水。 低聚糖—— 水解后能生成2~10个单糖。以二糖最为 重要。 如 蔗糖
多糖 —— 水解后得到10个以上的单糖。 如 淀粉、纤维素。
自然界中存在的糖类是由绿色植物通过光合作用合成 的。在日光的作用下,绿色植物利用体内的叶绿素将自然 界中的CO2和H2O经过一系列复杂的反应过程变为糖类。 6 CO2 + 6 H2O
2. 与Ag(NH3)2+反应—— 说明含羰基 C=O + Ag (NH3)2+ Ag ↓ + R-COO -
3. 与5分子 (CH3CO)2O 反应—— 说明有5个-OH 4. 证明是支链或直链糖 CHO CHOH 故初证葡萄糖为: CHOH CHOH CHOH CH2OH
5. 进一步证明是醛糖或是酮糖 醛氧化后得相应的酸,糖链不变 COOH CHO HNO3 (CHOH)4 (CHOH)4 COOH CH2OH
D2 CH2OH
D-葡萄糖 OH -
COOH
+ Cu2O ↓ CH2OH
D-葡萄糖酸
(砖红色)
果糖虽然为酮糖,但也能被托伦试剂和斐林试剂氧化。 原因是由于反应在碱性条件下进行,糖会发生异构化,变为 醛糖。
CH2OH C=O
Ag(NH3)2+ OH
hν 叶绿素
C6H12O6 + 6 O2
葡萄糖
反应为一吸收能量的过程,将太阳能储存在糖的分子 中。当糖的分子进入人体体内,经过一系列复杂的分解过 程,最后变为CO2和水,释放出能量,作为生命的能源。 C6H12O6 + O2
葡萄糖 代谢
CO2 + H2O + Q
§19-2
醛糖—— 多羟基醛
单糖
CHO CHOH CHOH CHOH CHOH CH2OH CH2OH C=O CHOH CHOH CHOH CH2OH
1 2 R 3 S 4 5
6
2R,3S,4R,5R-2,3,4,5,6-五羟基己醛 相对构型(D系列和L系列): CHO *CHOH CH2OH
甘油醛
以甘油醛为标准
CHO H-C-OH CH2OH
D-(+)-甘油醛
CHO HO-C-H CH2OH
L-(-)-甘油醛
单糖分子中距离羰基最远的一个手性碳原子上的羟基构 型和D-甘油醛构型相同时(羟基在右侧)确定为D 构型,反 之(羟基在左侧)为L 构型。 CHO CH2OH C=O OH CH2OH
第十九章
碳水化合物
§19-1
概述
§19-2
§19-3 §19-4
单糖
双糖 多糖
§19-1
概述
碳水化合物是自然界中分布最广的一类有机化合物,几 乎存在于所有生物体中,与人类有着十分密切的关系。
组成包括: C、H 、O 三种元素 其 中: H : O = 2 : 1 通式表示: Cm(H2O)n
如:葡萄糖:C6H12O6 = C6(H2O)6 蔗 糖:C12H22O11 = C12(H2O)11
D-果糖
OH CH2OH
D-葡萄糖
CHO HCN H-C-OH CH2OH
D-(+)-甘油醛
CN CHO COOH * H-C-OH H3O+ H-C-OH Na-Hg H-C-OH H-C-OH CH2OH CH2OH D-(+)-赤藓糖 CN COOH CHO * HO-C-H Na-Hg H3O+HO-C-H H-C-OH H-C-OH CH2OH CH2OH D-(+)-苏阿糖
CH=N-NHH2N-NH-
C=N-NH-
CH2OH
D-葡萄糖
CH2OH
D-甘露糖
CH2OH
D-果糖
CH2OH
D-葡萄糖脎
3. 氧化反应
① 与托伦(Tollens)试剂及斐林(Fehlieg)试剂反应 CHO COOH
+ Ag(NH3)2
CH2OH
D-葡萄糖
+
OH -
+ Ag ↓
(银镜)
CH2OH
D-葡萄糖
CH=N-NHC=N-NH-
CH2OH
D-葡萄糖脎
糖脎为淡黄色晶体,不同的糖成脎时间、结晶形状不 同,结构上完全不同的糖脎熔点不同,利用该反应可鉴定 糖。
单糖在C1和C2上发生,若糖只是C1或C2构型或羰基不同, 其它手性碳都相同,则生成的脎也相同。
CHO CHO OH HO
CH2OH C=O
HI P
COOH CH2 (CH2)4 CH3 正庚酸
CHO CHOH CHOH CHOH CHOH CH2OH 葡萄糖
CH2OH C=O CHOH CHOH CHOH CH2OH
果糖
对映体的构型可用R、S标记
如 D-(+)-葡萄糖
CHO H-C-OH HO-C-H H-C-OH H-C-OH CH2OH
