第十一章 酚和醌
第11章酚和醌2011

对苯醌是有效的自由基链 反应阻聚剂,用于延长不 饱和树脂储存寿命,高温 有效。
O O
(2) 由芳烃氧化制备
O
O2,V2O5 365 0C
Ce2(SO4)2 电解
O 83% O
蒽醌是重要 染料中间体
O
Ce2(SO4) 3是催化量的,+3价铈先被电解氧化为+4价铈,后者在 把蒽氧化为蒽醌, +4价铈被还原为+4价铈。
OCH2CH=C* H2 200 0C
OH C*H2CH=CH2
OCH2CH=C* H2
H3C
CH3
200 0C
相当于进行了两次Claisen 重排
OH
H3C
CH3
CH2CH=CH2*
Claisen重排反应历程
O
O
O H
互变异构
CH2CH=CH2
OH CH2CH=CH2
如果邻位有取代基,不能进行互变 异构,重排将继续到对位
R'
O
酮式
但在酚中, 这种烯醇式却是稳定的。因为酚羟基氧上的孤 电子对可与苯环发生共扼, 故酚与醇中的羟基在性质上不同, 它们属两类化合物。
2. 分类
OH
OH
OH
OH
NO2
一元酚
CH3
二元酚
OH
OH
OH
OH
OH
OH
三元酚
OH
OH
OH
OH
OH
OH
OH OH
OH
3. 命名
一般在“酚”字前加上芳环的名称作母体,再加上其它取代
一、酚
11.1 酚的结构、分类与命名
酚是羟基(―OH)与苯环直接相连的化合物,具有ArOH通式。
第十一章酚和醌

O CH2COOH Cl Cl
2,4-二氯苯氧乙酸(2,4-D) 酚醚化学性质比酚稳定,不易氧化,而且与HI作 用,分解为酚,此反应可用来保护酚羟基。
OCH3 OH
+
2015/11/28
HI
+
习题13
CH3I
23
克莱森重排
定义:烯丙基芳基醚在高温下可以重排为邻烯 丙基酚或对烯丙基酚,这称为克莱森重排。
X
X
亲核性比醇弱
O O CH3
成酯:
OH + CH3COOH + CH3COCl + (CH3CO)2O
OH + CH3COOH
O
98%H2SO4 4h/55%
O C CH3
乙酸苯酯
2015/11/28
25
在酸催化下,酚与羧酸作用也能生成酯,但比醇 难。通常采用酰氯或酸酐与酚反应。例如:
O C Cl + HO
14
OCH2CH=CH2
OH
200oC
14
OH
CH2CH=CH2
200oC
14
O
CH2CH CH2
190-220C 6h
OH CH2CH CH2
CH2CH=CH2
O H3C
CH2CH CH2 CH3 H3C
OH CH3
CH2CH CH2
2015/11/28
24
(3)酯的生成
难
OH + HX
对 10.00 10.26 10.21 9.81 9.38 9.26 9.20 7.15
《有机化学》第11章酚和醌

优先次序判断),要以最优先的基团作为主官能团, 由主官能团决定母体的名称,此时将羟基作取代基 处理。
羟基连在稠环上的化合物,其命名与苯酚类似, 但须遵循稠环芳烃的编号原则。
3
CH3
OH
HOOC
OH
2-甲基苯酚 邻甲苯酚
4-羟基苯甲酸 对羟基苯甲酸
苯酚的卤代非常容易,不需要L酸的催化。
OH
Br2 / H2O Br
Br
OH (白色) 过量 Br2 / H2O Br Br
Br
Br O (黄色)
Br
——用于酚的定性、定量分析
Br
OH Br2 / HBr
30℃
Br
酸性溶剂
OH
Br2 / CCl4 10℃
Br
OH
非极性溶剂
17
(2)硝化反应 室温下用稀硝酸就可将苯酚硝化,生成邻位、
O CH3
OH
+ HI
+ CH3I ——保护酚羟基
14
(3)酚酯的生成 酚与羧酸直接酯化比较困难,需要用反应活性
更强的酸酐或酰氯反应。
O
OH + Cl C
苯甲酰氯
10% NaOH 40~45℃
O OC
苯甲酸苯酯
O
CH3 C
OH +
O
H3C C O
乙酸酐
15% NaOH 30~40℃
O O C CH3
HO
OH
均苯三酚
OH
偏苯三酚
1,3,5-苯三酚 1,2,4-苯三酚 39
无溶剂条件下
40~150℃
Cl
OH
第11章酚和醌2解读

本章主要内容: 1、酚、醌的分 类与命名——掌 握
2、酚、醌的结 构——理解
3、酚、醌的物 理性质——了解
4、酚、醌的化 学性质——掌握
第一节 酚
一、命名
§11-1 酚
酚的命名,一般是在“酚”字前面加上芳环的名 称作母体,再加上其他取代基的名称和位次。
OH
一
元 酚
CH3
间-甲苯酚
§11-1 酚
B 酚醚的生成 (—威廉森合成p237) 酚金属与烷基化剂在弱碱性溶液中作用可得
二苯基醚可用酚金属与芳卤衍生物作用而得
酚醚与氢碘酸作用,分解而得到原来的酚
有机合成中用来保 护酚羟基 P493
§11-1 酚
C 酯的生成 酚与酸酐或酰氯作用可得
酚与羧酸直接 酯化困难
§11-1 酚
2 .芳环上亲电取代 反应灵敏,可用于苯酚测定。
反应历程:自由基反应
稀硫酸分解
§11-1 酚
2. 从芳卤衍生物制备
注意反应条件!
Cl
ONa
350~370℃,20MPa
+ 2 NaOH
Cu催化剂
+ NaCl + H2O
ONa
OH
反应时的中间体更加稳定--
+ HCl
+ N中aC间l 体的负电荷得到分散
当卤原子的邻位或对位有强的吸电子基时,水解反 应容易进行。
3-甲苯酚
OH
1-萘酚 (a-萘酚)
OH CO2H
邻-羟基苯甲酸
OH
O2N
NO2
NO2
2,4,6-三硝基苯酚 (苦味酸)
HO
SO3H
4-羟基苯磺酸
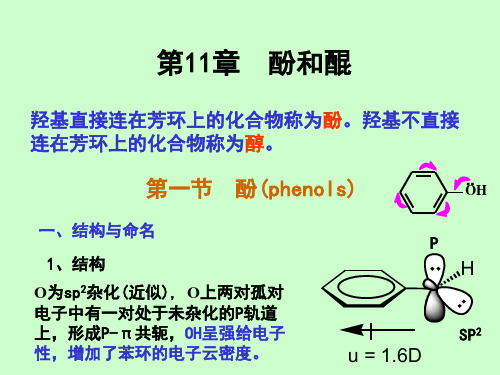
二、结构
第11章 酚和醌
克莱森重排本质上是乙烯基烯丙基的重排
CH2 CH O CH2CH CH2 CH2 CH CH2 CH CH OH 互变
CH2 CH CH2 CH2 CHO
4、与三氯化铁显色 凡具有烯醇式结构的化合物遇FeCl 烯醇式结构的化合物遇 凡具有烯醇式结构的化合物遇FeCl3溶液都有显色反应
NO2
NO2
NO2
苦味酸
Pka = 7.22
4.00
0.71
吸电子基团越多,酸性越强。 吸电子基团越多,酸性越强。
OH
OH < <
OH OCH3 <
OH
吸电子诱导 给电子共轭
OCH3
OCH3
Pka =
10.21
10.0
9.98
9.65
另外,酚的邻位上如有体积很大的取代基,由于苯氧负离 另外,酚的邻位上如有体积很大的取代基, 子的溶剂化受到阻碍,其酸性特别弱。 子的溶剂化受到阻碍,其酸性特别弱。如2,4,6-三新戊 基苯酚中液氨中与金属钠不起反应。 基苯酚中液氨中与金属钠不起反应。
OH (CH3)3C H2C CH2 C(CH3)3 CH2 C(CH3)3
2、酚酯的生成及傅瑞斯(Fries)重排 酚酯的生成及傅瑞斯(Fries)重排 (Fries) 由于酚中存在P 由于酚中存在P-π共轭,降低了氧周围的电子云密度,使其 共轭,降低了氧周围的电子云密度, 亲核性比醇弱。所以酚类不能直接与酸成酯, 亲核性比醇弱。所以酚类不能直接与酸成酯,而要与酸酐或 酰氯作用才能成酯。 酰氯作用才能成酯。
醇钠在水中几 乎全部水解
绝大部分酚类化合物不溶或微溶于水,但能溶于碱性水溶液, 绝大部分酚类化合物不溶或微溶于水,但能溶于碱性水溶液,又 能被酸从碱液中析出。利用这一性质可分离和提纯酚类化合物。 能被酸从碱液中析出。利用这一性质可分离和提纯酚类化合物。
酚和醌ppt

OH
O----H----O
对苯醌
氢醌
醌氢醌
电 荷 转 移 络 合 物
O
2.加成
O 2 O Br Br O Br Br O H+ 2 KCN O CN 1)HNO3 1)HNO3 2)HCl Cl CN NOH 2Br2 O NH2OH NOH
OH
CN OH
2)HCl 3)HNO3 Cl
CN O
[合成题]
CH3 C CH3 O OH
3. 重氮盐法
NH2 NaNO2 H2SO4
+ N HSO 2 4
OH
H3O+
4. 卤苯水解
Cl NO2 NaOH H2O NO2
ONa NO2 H+
OH NO2
NO2
NO2
[抗氧剂]
OH HO O
OH
OH
OH
HO
OH
(CH3)3C
C(CH3)3
OH
CH3
Ⅱ醌
含有共轭环己二烯二酮结构单元的化合物。
1) HO a HO b Cl HO c
a OH 2)
b OH NO2
c OH
d OH
NO2
2. 与FeCl3的显色反应
6C6H5OH + FeCl3
C C OH OH
NO2
Fe(OC6H5)6
3-
+ 6H+ + 3Cl-
用于定性分析
3. 酚酯的形成和Fries(弗里斯)重排
OH O CH3CCl or (CH3CO)2O OCOCH3 + HCl (CH3COOH)O O O邻苯醌O
O
1,4-萘醌
徐寿昌《有机化学》(第2版)课后习题(酚和醌)【圣才出品】

(8)2,6-二叔丁基-4-硝基苯酚
(9)2,6-二氯ห้องสมุดไป่ตู้酚
(10)4-乙基-2-溴苯酚
答:(1)间苯三酚:
+ 3 SO3
HO3S
SO3H NaOH
SO3H
H+ HO
OH OH
(2)4-乙基-1-3-苯二酚
(3)对亚硝基苯酚
(4)苯乙醚
OH + (C2H5)SO4 NaOHaq
OC2H5
(5)2,4-二氯苯氧乙酸
答:化合物(A)丌溶于氢氧化钠,遇 FeCl3 无颜色反应,由此可以判断化合物(A) 丌含有酚羟基。但是该化合物能不一个或两个羟氨分子结合,说明化合物(A)含有两个羰
基。化合物(A)的可能结构为:
。化合物(B)能溶于氢氧化钠,且不 FeCl3 有
(6)对羟基苯磺酸
(7)1-甲基-2-萘酚
(8)9-蒽酚
(9 )1 ,2 ,3-
苯三酚
(10)5-甲基-2-异丙基苯酚 (11)5-硝基-1-萘酚
(12)β-氯蒽醌
1 / 11
圣才电子书 十万种考研考证电子书、题库视频学习平台
2.写出下列各化合物的构造式: (1)对硝基苯酚 (2)对氨基苯酚 (3)2,4,二氯苯氧(基)乙酸(2,4-D) (4)2,4,6-三溴苯酚 (5)邻羟基苯乙酮 (6)邻羟基乙酰苯 (7)4-甲基-2,6-二叔丁基苯酚(二六四抗氧剂) (8)1,4,萘醌-2-磺酸钠 (9)2,6,蒽醌二磺酸(ADA) (10)醌氢醌 (11)2,2-(4,4′-二羟基二苯基)丙烷(双酚 A) (12)对苯醌单肟 答:
答:
3 / 11
圣才电子书 十万种考研考证电子书、题库视频学习平台
《有机化学》徐寿昌 第二版 第11章 酚和醌

◆邻硝基苯酚和对硝基苯酚可通过水蒸汽蒸馏分开.
邻位-氢键
邻硝基苯酚通过分子内氢键形成六元环螯合物,可随水蒸汽挥发. 对硝基苯酚只能通过分子间的氢键缔合,不能随水蒸汽挥发.
下列化合物哪些能形成分子内氢键?
(Ⅰ) 邻硝基苯酚; (Ⅱ)对羟基苯乙酮; (Ⅲ)邻氯苯酚 (Ⅳ) 间溴苯酚; (Ⅴ)邻氨基苯酚; (Ⅵ)邻羟基苯甲酸 (Ⅶ) 邻氯甲苯; (Ⅷ)邻羟基苯甲醛
-COOH, -SO3H, -COOR, -COX, -CONH2, -CN, -CHO, >C=O, -OH(醇), -OH(酚), -SH, -NH2, -OR, R烷基, -NO2, -X
例如:
OH
OH
OH
SO3H对羟基苯磺酸Fra bibliotekCSOH32HOH 对羟基苯甲醇
OSOC3HH3 对甲氧基苯酚
11.2 酚的制法
苯酚
苯甲醇(苄醇)
◆酚的分类:按照酚类分子中所含羟基的数目多少,
分为一元酚和多元酚.
◆酚的命名:以苯酚作为母体,苯环上连接的其他
基团作为取代基.
例如: 一元酚
二元酚 三元酚
◆带有优先序列取代基的命名: 按取代基的排列次序的先后来选择母体,当取代基
的序列优于酚羟基时,酚羟基作为取代基。 取代基的先后排列次序为:
◆ 苯酚能溶解于氢氧化钠水溶液;通入二氧化碳,
苯酚即游离出来(酸性:碳酸>苯酚).
苯酚溶于NaOH,但不溶于NaHCO3。工业上利 用苯酚能溶于碱,而又可用酸分离的性质来处理和回 收含酚废水; 酚的提纯分离.
◆苯环上取代基对苯酚酸性的影响
pKa
吸电子基团(硝基)使羟基氧上负电荷更好地离域移向苯 环(诱导和共轭效应),生成更稳定的对硝基苯氧负离子,酸 性增强。吸电子基团硝基愈多,酸性愈强。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(一) 酚一.酚的分类和命名根据羟基所连芳环的不同,酚类可分为苯酚、萘酚、蒽酚等。
根据羟基的数目,酚类又可分为一元酚、二元酚和多元酚等。
酚的命名是根据羟基所连芳环的名称叫做“某酚”,芳环上的烷基、烷氧基、卤原子、氨基、硝基等作为取代基,若芳环上连有羧基、磺酸基、羰基、氰基等,则酚羟基作为取代基。
例如:1-萘酚 或 α-萘酚 苯酚(石炭酸) 4-乙基苯酚 5-甲氧基-2-溴苯酚2,4,6-三硝基苯酚 3-甲基-4-羟基苯磺酸 1,3,5-苯三酚 1,2,3-苯三酚 (苦味酸) (均苯三酚) (连苯三酚)二.酚的物理性质常温下,除了少数烷基酚为液体外,大多数酚为固体。
由于分子间可以形成氢键,因此酚的沸点都很高。
邻位上有氟、羟基或硝基的酚,分子内可形成氢键,但分子间不能发生缔合,它们的沸点低于其间位和对位异构体。
纯净的酚是无色固体,但因容易被空气中的氧氧化,常含有有色杂质。
酚在常温下微溶于水,加热则溶解度增加。
随着羟基数目增多,酚在水中的溶解度增大。
酚能溶于乙醇、乙醚、苯等有机溶剂。
三.酚的化学性质酚和醇具有相同的官能团,但酚羟基直接与苯环相连,氧原子的p 轨道与芳环的π轨道形成p —π共轭体系,导致氧原子的电子云密度降低,使得碳氧键的极性减弱而不易断裂,不能像醇羟基那样发生亲核取代反应或消除反应。
同时,酚羟基中氧原子的电子云密度降低致使氧氢键的极性增加,与醇相比,酚的酸性明显增强。
另外,由于酚羟基的给电子效应,使苯环上的电子云密度增加,芳环上的亲电取代反应更容易进行。
OH OH OH 2H 5OHBrCH 3OOHOHOHNO 2O 2N2SO 3H CH 3HOOHHOOH苯酚中p-π共轭示意图综上所述,酚的主要化学性质可归纳如下:1.酸性酚类化合物呈酸性,大多数酚的pKa 都在10左右,酸性强于水和醇,能与强碱溶液苯酚的酸性比碳酸弱,能溶于碳酸钠溶液,但不能溶于碳酸氢钠溶液,在苯酚钠的溶液中通入二氧化碳能使苯酚游离出来。
利用此性质可进行苯酚的分离和提纯。
芳环上取代基的性质对酚的酸性影响很大。
当芳环上连有供电子基时,使酚羟基的氧氢键极性减弱,释放质子的能力减弱,因而酸性减弱;当芳环上连有吸电子基时,使酚羟基的氧氢键极性增强,释放质子的能力增强,酸性增强。
例如:OH + NaHCO 3H 2O ONa + CO 2苯酚钠+-ONa + H 2O + NaOHOH ++ H O OHpKa=9.95pKa 10.2 9.95 7.17 0.382.与三氯化铁的显色反应酚与三氯化铁溶液作用生成有色的配合物:6C 6H 5OH + FeCl 3 —→ [ Fe (C 6H 5O)6] 3+ 6H + + 3Cl ―不同的酚与三氯化铁作用产生的颜色不同。
除酚以外,凡具有稳定的烯醇式结构的化合物都可发生此反应。
例如:O OH COC 2H 5CH 3C = CH由于分子内形成π-π共轭体系,且分子内以氢键连接成环,该烯醇式结构较为稳定,可与三氯化铁作用显色。
因此,可利用此反应来鉴别酚类化合物和具有稳定烯醇式结构的化合物。
3.酚醚和酚酯的生成由于酚羟基与苯环形成p-π共轭体系,酚不能直接进行分子间的脱水反应生成醚,也不能直接与羧酸反应生成酯。
通常是用酚盐与卤代烃反应来制备醚,用酚与活性更高的酰卤或酸酐反应来制备酯。
例如:4.芳环上的取代反应酚羟基对苯环既产生吸电子的诱导效应(―I ),又产生给电子的共轭效应(+C ),两者综合作用的结果使苯环上的电子云密度增加,使羟基的邻、对位活化,更容易发生芳环上的亲电取代反应。
例如:OH + (CH 32O 3 + CH 3COOHO OONa + C 2H 52CH 3 + Na I Cl ClONa + Cl NO Cl Cl O NO 2 (除草醚)OH OHOHOHNO 2NO 22CH 3O 2NBrBrOH + 3Br 2()2,4,6-三溴苯酚(白色)苯酚与溴水的反应灵敏度高,一般溶液中苯酚含量达10mg/kg 即可检出,且反应是定量的,所以常用于苯酚的定性和定量分析及饮用水的监测。
苯酚的硝化和磺化反应一般在室温下进行。
例如:2,4,6-三硝基苯酚(苦味酸)33H+ H 2SO 4 (浓OH5.氧化反应 四.个别化合物 1.苯酚 2.甲苯酚 3.苯二酚 4.苯三酚5.维生素E*第二节 醌一.醌的结构和命名OH + HNO 3(稀)室温NO 2OH OH 2+OH + (浓) HNO 3 H SO (浓)OH NO 2NO 22N醌是一类特殊的环状不饱和二酮,分子中含有如下的醌型结构:醌的结构中虽然存在碳碳双键和碳氧双键的π-π共轭体系。
但不同于芳香环的环状闭合共轭体系,所以醌不属于芳香族化合物,也没有芳香性。
醌一般由芳香烃衍生物转变而来,命名时在“醌“字前加上芳基的名称,并标出羰基的位置。
例如:对苯醌(1,4-苯醌) 邻苯醌(1,2-苯醌) 1,4-萘醌 1,2-萘醌 黄色结晶 红色结晶 黄色结晶 橙黄色结晶蒽醌 菲醌 淡黄色结晶 橙红色结晶二.醌的物理性质醌为结晶固体,都具有颜色,对位醌多呈黄色,邻位醌则常为红色或橙色。
对位醌具有刺激性气味,可随水蒸气汽化,邻位醌没有气味,不随水蒸气汽化。
三.醌的化学性质醌分子中含有碳碳双键和碳氧双键的共轭体系,因此醌具有烯烃和羰基化合物的典型反应,能发生多种形式的加成反应。
1. 加成反应(1)羰基的加成 醌分子中的羰基能与羰基试剂等加成。
如对-苯醌和羟氨作用生成单肟和二肟:对苯醌单肟 对苯醌双肟O O OOO OO OOOOH N OHH N OH N OH OHH 2N +O(2)双键的加成 醌分子中的碳碳双键能和卤素、卤化氢等亲电试剂加成。
如对-苯醌与氯气加成可得二氯或四氯化物。
2,3,5,6-四氯-1,4-环己二酮(3)1,4-加成 由于碳-碳双键与碳-氧双键的共轭,所以醌可以发生1,4-加成反应。
如对苯醌与氯化氢加成后,生成对苯二酚的衍生物。
2. 还原反应对苯醌容易被还原为对苯二酚(或称氢醌),这是对苯二酚氧化的逆反应。
在电化学上,利用二者之间的氧化-还原性质可以制成氢醌电极,用来测定氢离子的浓度。
这一反应在生物化学过程中有重要的意义。
生物体内进行的氧化还原作用常是以脱氢或加氢的方式进行的,在这一过程中,某些物质在酶的控制下所进行的氢的传递工作可通过酚醌氧化还原体系来实现。
四.自然界的醌1.维生素K*2.泛醌*第二节 醌二. 醌的结构和命名醌是一类特殊的环状不饱和二酮,分子中含有如下的醌型结构:OO HCl重排OH OH ClO O OH OH 对苯醌对苯二酚(氢醌)O Cl Cl Cl Cl Cl 2O Cl Cl + ClO醌的结构中虽然存在碳碳双键和碳氧双键的π-π共轭体系。
但不同于芳香环的环状闭合共轭体系,所以醌不属于芳香族化合物,也没有芳香性。
醌一般由芳香烃衍生物转变而来,命名时在“醌“字前加上芳基的名称,并标出羰基的位置。
例如:对苯醌(1,4-苯醌) 邻苯醌(1,2-苯醌) 1,4-萘醌 1,2-萘醌 黄色结晶 红色结晶 黄色结晶 橙黄色结晶蒽醌 菲醌 淡黄色结晶 橙红色结晶二.醌的物理性质醌为结晶固体,都具有颜色,对位醌多呈黄色,邻位醌则常为红色或橙色。
对位醌具有刺激性气味,可随水蒸气汽化,邻位醌没有气味,不随水蒸气汽化。
三.醌的化学性质醌分子中含有碳碳双键和碳氧双键的共轭体系,因此醌具有烯烃和羰基化合物的典型反应,能发生多种形式的加成反应。
3. 加成反应(1)羰基的加成 醌分子中的羰基能与羰基试剂等加成。
如对-苯醌和羟氨作用生成单肟和二肟:对苯醌单肟 对苯醌双肟(2)双键的加成 醌分子中的碳碳双键能和卤素、卤化氢等亲电试剂加成。
如对-苯醌与氯气加成可得二氯或四氯化物。
O O OOOO OO OOOOH N OHH N OH N OH OHH 2N +O2,3,5,6-四氯-1,4-环己二酮(3)1,4-加成 由于碳-碳双键与碳-氧双键的共轭,所以醌可以发生1,4-加成反应。
如对苯醌与氯化氢加成后,生成对苯二酚的衍生物。
4. 还原反应对苯醌容易被还原为对苯二酚(或称氢醌),这是对苯二酚氧化的逆反应。
在电化学上,利用二者之间的氧化-还原性质可以制成氢醌电极,用来测定氢离子的浓度。
这一反应在生物化学过程中有重要的意义。
生物体内进行的氧化还原作用常是以脱氢或加氢的方式进行的,在这一过程中,某些物质在酶的控制下所进行的氢的传递工作可通过酚醌氧化还原体系来实现。
四.自然界的醌1.维生素K*2.泛醌*三、醌1.特征① 凡醌类都具有颜色。
② 醌式结构中不存在苯环。
2.性质① 加成反应 a .羰基上的加成OO HCl重排OH OH Cl OO OH OH 对苯醌对苯二酚(氢醌)OCl Cl Cl ClCl 2OCl Cl + Cl Ob .烯键上的加成c .双烯合成d .1,4加成② 还原O O HO O NOHNOH NOHH 2O -H 2N-OHH 2N-OH H O-单肟二肟OOOOBr 2Br2OOBr BrBr Br-HBrOOBrOOBrBr-HBr组成氧化还原偶对。
⒊制备:酚和苯胺的氧化。
OO OH OH。
