第十一章 酚和醌
第十一章酚和醌

O CH2COOH Cl Cl
2,4-二氯苯氧乙酸(2,4-D) 酚醚化学性质比酚稳定,不易氧化,而且与HI作 用,分解为酚,此反应可用来保护酚羟基。
OCH3 OH
+
2015/11/28
HI
+
习题13
CH3I
23
克莱森重排
定义:烯丙基芳基醚在高温下可以重排为邻烯 丙基酚或对烯丙基酚,这称为克莱森重排。
X
X
亲核性比醇弱
O O CH3
成酯:
OH + CH3COOH + CH3COCl + (CH3CO)2O
OH + CH3COOH
O
98%H2SO4 4h/55%
O C CH3
乙酸苯酯
2015/11/28
25
在酸催化下,酚与羧酸作用也能生成酯,但比醇 难。通常采用酰氯或酸酐与酚反应。例如:
O C Cl + HO
14
OCH2CH=CH2
OH
200oC
14
OH
CH2CH=CH2
200oC
14
O
CH2CH CH2
190-220C 6h
OH CH2CH CH2
CH2CH=CH2
O H3C
CH2CH CH2 CH3 H3C
OH CH3
CH2CH CH2
2015/11/28
24
(3)酯的生成
难
OH + HX
对 10.00 10.26 10.21 9.81 9.38 9.26 9.20 7.15
《有机化学》第11章酚和醌

优先次序判断),要以最优先的基团作为主官能团, 由主官能团决定母体的名称,此时将羟基作取代基 处理。
羟基连在稠环上的化合物,其命名与苯酚类似, 但须遵循稠环芳烃的编号原则。
3
CH3
OH
HOOC
OH
2-甲基苯酚 邻甲苯酚
4-羟基苯甲酸 对羟基苯甲酸
苯酚的卤代非常容易,不需要L酸的催化。
OH
Br2 / H2O Br
Br
OH (白色) 过量 Br2 / H2O Br Br
Br
Br O (黄色)
Br
——用于酚的定性、定量分析
Br
OH Br2 / HBr
30℃
Br
酸性溶剂
OH
Br2 / CCl4 10℃
Br
OH
非极性溶剂
17
(2)硝化反应 室温下用稀硝酸就可将苯酚硝化,生成邻位、
O CH3
OH
+ HI
+ CH3I ——保护酚羟基
14
(3)酚酯的生成 酚与羧酸直接酯化比较困难,需要用反应活性
更强的酸酐或酰氯反应。
O
OH + Cl C
苯甲酰氯
10% NaOH 40~45℃
O OC
苯甲酸苯酯
O
CH3 C
OH +
O
H3C C O
乙酸酐
15% NaOH 30~40℃
O O C CH3
HO
OH
均苯三酚
OH
偏苯三酚
1,3,5-苯三酚 1,2,4-苯三酚 39
无溶剂条件下
40~150℃
Cl
OH
第11章 酚和醌(食品2)

2、氯苯水解 、
Cl
+
NaOH
Cu ,20MPa 350~370℃
ONa
HCl
OH
优点: 操作简便,副产物易分离; 优点: 操作简便,副产物易分离; 缺点: 需要高温、 高压反应, 缺点 : 需要高温 、 高压反应 , 且碱对设备的腐蚀严 重,反应困难。 反应困难。 若苯环上连有强吸电子基,水解较易。 若苯环上连有强吸电子基,水解较易。 强吸电子基
OH
H3C CH3 C CH2
OH
+
CH3
浓 H2SO4
(CH3)3C
C(CH3)3
4-甲基 甲基-2,6-二 甲基 二 叔丁基苯酚
20
CH3
酚也较容易发生酰基化反应, 酚也较容易发生酰基化反应,但酚羟基上易发生酯 容易发生酰基化反应 化反应,而使酚的酰基化反应产率较低。 化反应,而使酚的酰基化反应产率较低。
二、酚的制法 1、异丙苯氧化法
O OH
OH
O2 / 过过酸过 110~120℃
稀 H2SO4 75~80℃
O
+
氢过氧化异丙苯 聚合橡胶的引发剂
此法是目前工业生产苯酚最主要 最好的方法 最主要和 的方法, 此法是目前工业生产苯酚最主要和最好的方法, 原料廉价易得,可连续化生产, 原料廉价易得,可连续化生产,副产品丙酮也是常用 的有机试剂、有机溶剂之一。 的有机试剂、有机溶剂之一。
酚过量: 酚过量:
OH
HCHO
2
H or OH
+
-
HO
CH2
OH CH2 或
OH
OH
23
以上中间产物与甲醛、苯酚继续作用, 以上中间产物与甲醛、苯酚继续作用,就可得到 线型酚醛树脂: 线型酚醛树脂:
第十一章酚和醌

)6 ]
3-
+ 6 H + 3Cl
+
-
蓝紫色
不同的酚显示不同的颜色,利用酚的这个特殊的显
色反应,可以用来检验酚羟基的存在。
OH OH OH OH OH OH 兰 紫 色 CH 3 兰 紫 色 兰 色 深 绿 色 OH
OH O
O
OH 暗 绿 色 淡 棕 色
与FeCl3的显色反应并不限于酚,具有烯醇式结构 的脂肪族化合物也有此反应。
OH HO
O 2N
OH NO2
OH HO
OH HO OH
OH OH OH
邻苯二酚 1,2-苯二酚
间苯二酚 1,3-苯二酚
均苯三酚 偏苯三酚 1,3,5-苯三酚 1,2,4-苯三酚
11.3
酚的制法
H P O 3 4 C H C H C H + 3 2 2 5 0 ℃ , 加 压
1、异丙苯法
C H 3 C H C H 3
Br Br
OH
H B r 3
(白 )
如需要制取一溴代苯酚,则要在非极性溶剂
(CS2,CCl4)和低温下进行。
OH + B r 2 CS 2 0 ℃ Br OH + OH Br +3 H B r
如反应在酸性溶液中反应,可得到2,4-二卤代酚。
Br 2,HBr
OH
30℃
Br Br
OH
2. 硝化
苯酚的硝化在室温下即可进行,但因苯酚易被氧化, 故产率较低。
11.1 11.2 11.3 11.4
酚
酚的构造、分类和命名 酚的制法 酚的物理性质 酚的化学性质
11.1 酚的结构、分类和命名
1、酚的结构、分类
第11章 酚和醌
克莱森重排本质上是乙烯基烯丙基的重排
CH2 CH O CH2CH CH2 CH2 CH CH2 CH CH OH 互变
CH2 CH CH2 CH2 CHO
4、与三氯化铁显色 凡具有烯醇式结构的化合物遇FeCl 烯醇式结构的化合物遇 凡具有烯醇式结构的化合物遇FeCl3溶液都有显色反应
NO2
NO2
NO2
苦味酸
Pka = 7.22
4.00
0.71
吸电子基团越多,酸性越强。 吸电子基团越多,酸性越强。
OH
OH < <
OH OCH3 <
OH
吸电子诱导 给电子共轭
OCH3
OCH3
Pka =
10.21
10.0
9.98
9.65
另外,酚的邻位上如有体积很大的取代基,由于苯氧负离 另外,酚的邻位上如有体积很大的取代基, 子的溶剂化受到阻碍,其酸性特别弱。 子的溶剂化受到阻碍,其酸性特别弱。如2,4,6-三新戊 基苯酚中液氨中与金属钠不起反应。 基苯酚中液氨中与金属钠不起反应。
OH (CH3)3C H2C CH2 C(CH3)3 CH2 C(CH3)3
2、酚酯的生成及傅瑞斯(Fries)重排 酚酯的生成及傅瑞斯(Fries)重排 (Fries) 由于酚中存在P 由于酚中存在P-π共轭,降低了氧周围的电子云密度,使其 共轭,降低了氧周围的电子云密度, 亲核性比醇弱。所以酚类不能直接与酸成酯, 亲核性比醇弱。所以酚类不能直接与酸成酯,而要与酸酐或 酰氯作用才能成酯。 酰氯作用才能成酯。
醇钠在水中几 乎全部水解
绝大部分酚类化合物不溶或微溶于水,但能溶于碱性水溶液, 绝大部分酚类化合物不溶或微溶于水,但能溶于碱性水溶液,又 能被酸从碱液中析出。利用这一性质可分离和提纯酚类化合物。 能被酸从碱液中析出。利用这一性质可分离和提纯酚类化合物。
酚和醌ppt

OH
O----H----O
对苯醌
氢醌
醌氢醌
电 荷 转 移 络 合 物
O
2.加成
O 2 O Br Br O Br Br O H+ 2 KCN O CN 1)HNO3 1)HNO3 2)HCl Cl CN NOH 2Br2 O NH2OH NOH
OH
CN OH
2)HCl 3)HNO3 Cl
CN O
[合成题]
CH3 C CH3 O OH
3. 重氮盐法
NH2 NaNO2 H2SO4
+ N HSO 2 4
OH
H3O+
4. 卤苯水解
Cl NO2 NaOH H2O NO2
ONa NO2 H+
OH NO2
NO2
NO2
[抗氧剂]
OH HO O
OH
OH
OH
HO
OH
(CH3)3C
C(CH3)3
OH
CH3
Ⅱ醌
含有共轭环己二烯二酮结构单元的化合物。
1) HO a HO b Cl HO c
a OH 2)
b OH NO2
c OH
d OH
NO2
2. 与FeCl3的显色反应
6C6H5OH + FeCl3
C C OH OH
NO2
Fe(OC6H5)6
3-
+ 6H+ + 3Cl-
用于定性分析
3. 酚酯的形成和Fries(弗里斯)重排
OH O CH3CCl or (CH3CO)2O OCOCH3 + HCl (CH3COOH)O O O邻苯醌O
O
1,4-萘醌
第十一章 酚和醌
(一) 酚一.酚的分类和命名根据羟基所连芳环的不同,酚类可分为苯酚、萘酚、蒽酚等。
根据羟基的数目,酚类又可分为一元酚、二元酚和多元酚等。
酚的命名是根据羟基所连芳环的名称叫做“某酚”,芳环上的烷基、烷氧基、卤原子、氨基、硝基等作为取代基,若芳环上连有羧基、磺酸基、羰基、氰基等,则酚羟基作为取代基。
例如:1-萘酚 或 α-萘酚 苯酚(石炭酸) 4-乙基苯酚 5-甲氧基-2-溴苯酚2,4,6-三硝基苯酚 3-甲基-4-羟基苯磺酸 1,3,5-苯三酚 1,2,3-苯三酚 (苦味酸) (均苯三酚) (连苯三酚)二.酚的物理性质常温下,除了少数烷基酚为液体外,大多数酚为固体。
由于分子间可以形成氢键,因此酚的沸点都很高。
邻位上有氟、羟基或硝基的酚,分子内可形成氢键,但分子间不能发生缔合,它们的沸点低于其间位和对位异构体。
纯净的酚是无色固体,但因容易被空气中的氧氧化,常含有有色杂质。
酚在常温下微溶于水,加热则溶解度增加。
随着羟基数目增多,酚在水中的溶解度增大。
酚能溶于乙醇、乙醚、苯等有机溶剂。
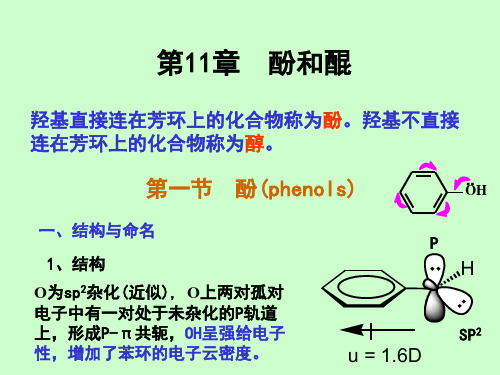
三.酚的化学性质酚和醇具有相同的官能团,但酚羟基直接与苯环相连,氧原子的p 轨道与芳环的π轨道形成p —π共轭体系,导致氧原子的电子云密度降低,使得碳氧键的极性减弱而不易断裂,不能像醇羟基那样发生亲核取代反应或消除反应。
同时,酚羟基中氧原子的电子云密度降低致使氧氢键的极性增加,与醇相比,酚的酸性明显增强。
另外,由于酚羟基的给电子效应,使苯环上的电子云密度增加,芳环上的亲电取代反应更容易进行。
OH OH OH 2H 5OHBrCH 3OOHOHOHNO 2O 2N2SO 3H CH 3HOOHHOOH苯酚中p-π共轭示意图综上所述,酚的主要化学性质可归纳如下:1.酸性酚类化合物呈酸性,大多数酚的pKa 都在10左右,酸性强于水和醇,能与强碱溶液苯酚的酸性比碳酸弱,能溶于碳酸钠溶液,但不能溶于碳酸氢钠溶液,在苯酚钠的溶液中通入二氧化碳能使苯酚游离出来。
有机化学第十一章酚与醌
氧化反应
酚易被氧化,如苯酚在空气中放置会逐渐氧 化成粉红色。
缩合反应
酚可与醛或酮发生缩合反应,生成酚醛树脂 或酚酮树脂。
醌的反应及应用
加成反应
醌可与亲核试剂发生加成反应,如与氢氰酸加成生成α-羟基腈。
还原反应
醌可被还原成酚,常用的还原剂有金属氢化物、硫化物等。
取代反应
醌环上的氢原子可被卤素、硝基等取代,生成相应的卤代醌或硝基醌。
实验安全注意事项
实验过程中需佩戴防护眼镜和 手套,避免试剂飞溅或接触皮
肤。
1
使用浓硫酸时应特别小心,避 免溅到皮肤或衣物上。若不慎 接触,应立即用大量清水冲洗
并就医。
加热回流过程中应注意控制温 度,避免温度过高引发危险。
实验结束后应妥善处理废液和 废弃物,保护环境。
06
知识拓展与前沿动态
酚和醌在自然界中的存在和作用
实验操作步骤详解
01
在圆底烧瓶中加入适量苯酚和乙醇,加热回流。
02
通过滴液漏斗缓慢滴加浓硫酸,同时观察反应现象。
03
反应完成后,将反应液冷却并用氢氧化钠溶液中和,析
出醌。
实验操作步骤详解
4. 醌的性质实验
将醌溶于少量有机溶剂 (如乙醇)中,观察其溶 解性。
取少量醌晶体,观察其颜 色、状态。
向醌溶液中滴加溴水或氯 化铁溶液,观察颜色变化。
有机化学第十一章 酚与醌
contents
目录
• 酚的概述与性质 • 醌的概述与性质 • 酚与醌的合成方法 • 酚与醌的反应及应用 • 实验操作与注意事项 • 知识拓展与前沿动态
01
酚的概述与性质
酚的定义与分类
定义
羟基直接连在芳香环上的化合物称为 酚。
第十一章_酚和醌
2. 从芳卤衍生物制备 4. 从芳胺制备
无水AlCl3 + CH3CH=CH2 85-95 0C
CH3 CH
O2(air)
CH3 110-120 0C
CH3 10%H2SO4
C OOH CH3
90 0C
OH + CH3COCH3
氢过氧化异丙苯重排还可用
CH2 CH n
强酸性离子交换树脂为催化剂
酚的碱性比醇弱,不能直接与酸成 酯;只能与酰卤和酸酐成酯。
OH
+ CH3COCl
N
OCOCH3
H3C
CH3
H3C
OH CO2H
+ (CH3CO)2O
浓 H2SO4 60 0C
CH3 75%
OCOCH3 CO2H
2.芳环上的反应
OH
O-
OH:邻对位 定位基
O-是比OH- 更强的定位基
因此,a)苯酚比苯易于亲电取代,条件更温 和,甚至要加以控制。b)往往发生多取代。
第十一章 酚和醌
第一节 酚
(一)酚和芳醇的分类、命名
1.羟基连在芳环上为酚。 2.根据羟基数目分一元酚和多元酚。 3.命名时常以芳基名称加“酚”; 4.如遇“位次”高的取代基,羟基变为取代基。
一元酚:
OH
OH
OH
OH
Cl
苯酚 3-氯苯酚 (石炭酸) 间氯苯酚
NO2
CH3
4-硝基苯酚 5-甲基-1-萘酚
OH
OH
OH
OH
CH2
CH2
+
n CH2
OH
CH2
OH n CH2OH
OH
OH
《有机化学》徐寿昌 第二版 第11章 酚和醌
傅-克反应:
9,10-蒽醌
邻苯二甲酸酐
邻苯甲酰苯甲酸
◆蒽醌性质很稳定,不易被氧化和发生亲电取代反应. 蒽醌在保险粉的碱溶液中可被还原生成9,10 -二羟
基蒽的血红色溶液,用来检验蒽醌的存在。
9,10-二羟基蒽
1,4-萘醌的制备1
1,4-萘醌的制备2 双烯合成
氧化
1,4-萘醌的应用: (1)磺化制萘醌-2-磺酸钠盐,工业上用作脱硫剂。
(2)2-甲基萘醌又名维生素K3,它与维生素K1都是 良好的止血剂:
11.10 蒽醌 ◆蒽醌可有9种异构体,已知的有三种(1,2-; 1,4-; 9,10-).
其中最重要的是9,10-蒽醌,简称蒽醌。 ◆蒽醌的制备:
解:
(Ⅰ)、(Ⅲ)、(Ⅴ)、(Ⅵ)、(Ⅷ)能形成分子内氢键
③磺化反应
苦味酸
羟基苯磺酸
4-羟基-1,3-苯二磺酸 2,4,6-三硝基苯酚
如何由苯酚合成2,6-二溴苯酚?
④烷基化和酰基化反应 由于酚羟基的活化,酚比芳烃容易进行傅-克反应。
催化剂一般不用AlCl3 (易形成络合物ArOAlCl2).
烷基化剂:醇或烯烃
-COOH, -SO3H, -COOR, -COX, -CONH2, -CN, -CHO, >C=O, -OH(醇), -OH(酚), -SH, -NH2, -OR, R烷基, -NO2, -X
例如:
OH
OH
OH
SO3H
对羟基苯磺酸
CSOH32HOH 对羟基苯甲醇
OSOC3HH3 对甲氧基苯酚
11.2 酚的制法
◆邻硝基苯酚和对硝基苯酚可通过水蒸汽蒸馏分开.
邻位-氢键
邻硝基苯酚通过分子内氢键形成六元环螯合物,可随水蒸汽挥发. 对硝基苯酚只能通过分子间的氢键缔合,不能随水蒸汽挥发.
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+ CH3COOH
OH COOH + (CH3CO)2O
水杨酸
H2SO4 65-80 ℃
OCOCH3 COOH + CH3COOH
乙酰水杨酸 (阿司匹林)
2.芳环上的亲电取代反应来自··6羟基是强的邻对位定位基,由于羟基与苯环的 P-π共轭,使苯环上的电子云密度增加, 亲电反应容易进行。
(1)卤代反应 苯酚与溴水在常温下可立即反应生成 2,4,6 三溴苯酚白色沉淀。
Cu 催化剂
ONa
OH
+ HCl
ONa
+ NaCl + H2O
+ NaCl
这个方法等于用空气中的氧将苯间接氧化成苯酚,是合成苯酚的一个很经济的方法,但 由于连在芳环上的卤素很不活泼,很难水解,需要在高温、高压和铜作催化剂的条件下进 行。
⑶ 异丙苯氧化。
··
2
这是目前生产苯酚最主要和最好的方法。优点是生产一吨苯酚同时获得 0.6 吨的丙酮, 得到的丙酮也是重要的化工原料。异丙苯可来源于石油化工产品丙烯和苯,因而经济合理。
OH + NaOH OH
+ Na2CO3
CO2+ H2O ONa
HCl
X
OH + NaHCO3
OH + NaCl
利用醇、酚与NaOH和NaHCO3反应性的不同,可鉴别和分离酚和醇。 当苯环上连有吸电子基团时,酚的酸性增强;连有供电子基团时,酚的酸性减弱。(见
5
··
P290表 10-5。
(2)与FeCl3的显色反应
OH KMnO4 + H2SO4 O
多元酚更易被氧化。
O O 对苯醌(棕黄色)
OH 2AgBr
OH
O + 2Ag + HBr
O
对苯二酚是常用的显影剂。 酚易被氧化的性质常用来作为抗氧剂和除氧剂。 四、重要的酚 (自学)
醌
§ 11.4 苯醌
醌类是一类特殊的环状不饱和二酮,包括一系列化合物,如:
··
8
醌类都有颜色。 许多动植物来源的有色物质属于醌类,如茜类 不少生理活性物质是醌类,如维生素K1,就是萘醌的衍生物。
OH NaOH
ONa
RCH2Br
OCH2R + NaBr
(CH3)2SO4 CH2=CHCH2Br
OCH3 + NaBr 苯甲醚(茴香醚 )
OCH2CH=CH2 + NaBr 苯基烯丙基醚
在有机合成上常利用生成酚醚的方法来保护酚羟基。 酚也可被卤素取代,但不象醇那样顺利;酚也可以生成酯,但比醇困难。
酚 § 11.1 酚的结构及命名
1.结构 酚是羟基直接与芳环相连的化合物(羟基与芳环侧链的化合物为芳醇),即酚是烃的羟 基衍生物。 2.命名 酚的命名一般是在酚字的前面加上芳环的名称作为母体,再加上其它取代基的名称和位 次。特殊情况下也可以按次序规则把羟基看作取代基来命名。例见P289~290。
§ 11.2 酚的制法:
9
··
两种萘酚都可由萘磺酸钠经碱熔而制得。
SO2Na
2NaOH, 300~320OC
ONa
+ Na2SO3 + H2O OH
HCl + NaCl
SO2Na
①NaOH, 300OC
OH
② HCl
纯粹α-萘酚的制备:
萘酚可制备许多衍生物,广泛用于制备偶氮染料,它们是重要的染料中间体,如 H 酸、 变色酸;β-萘酚还可用作杀菌剂、抗氧剂。工业上,产生的含有酚和其衍生物的废水是有
反应机理:
+ H+
+ CH3 O C CH3
H OH
OH
H3C
+
C O + H+
H3C
2.对苯二酚。
它本身是一个还原剂。
①能把感光后的溴化银还原为金属银。是照相的显影剂。
3
··
②常用作抗氧化剂,以保护其他物质不被自动氧化。如苯甲醛易于自动氧化,它可与氧生 成过氧酸。加入千分之一的对苯二 酚就可抑制其自动氧化。 ③是一个阻聚剂。如苯乙烯易聚合,因此储藏时,常加入对苯二酚作阻聚剂。 3.萘酚。
OH
OH
OH
NaNO2, H2SO4
稀 HNO3
7~8 ℃
O
NO
NO2
对亚硝基苯酚( 80% )
7
··
上述反应是制得不含邻位异构体的对硝基苯酚的方法。 (4)缩合反应 酚羟基邻、对位上的氢可以和羰基化合物发生缩合反应,例如,在稀碱存在下,苯酚 与甲醛作用,生成邻或对羟基苯甲醇,进一步生成酚醛树脂。 3.氧化反应 酚易被氧化为醌等氧化物,氧化物的颜色随着氧化程度的深化而逐渐加深,由无色而 呈粉红色、红色以致深褐色。例如:
··
4
害的,会影响到水生物的生长和繁殖,污染饮用水源,因此含酚废水的处理是环境保护工 作中的重要课题。
§ 11.3 酚的物理性质和光谱性质 (略) § 11.4 酚的化学性质
羟基即是醇的官能团也是酚的官能团,因此酚与醇具有共性。但由于酚羟基连在苯环
上,苯环与羟基的互相影响又赋予酚一些特有性质,所以酚与醇在性质上又存在着较大的
差别。
1.酚羟基的反应
(1) 酸性
OH
O +H
PKa ≈ 10 (不能使石蕊试纸变色)
酚的酸性比醇强,但比碳酸弱。
CH3CH2OH PKa 17
OH 10
H2CO3 6.5
故酚可溶于NaOH但不溶于NaHCO3,不能与Na2CO3、NaHCO3作用放出CO2,反之通入 CO2于酚钠水溶液中,酚即游离出来。利用酚的这种能溶于碱,而又可用酸将它从碱溶液中 有离出来的性质,工业上常被用来回收和处理含酚污水。
OH + 稀 HNO3
20 ℃
OH
OH
NO2 +
NO2 可用水蒸汽蒸馏分开
邻硝基苯酚易形成分子内氢键而成螯环,这样就削弱了分子内的引力;而对硝基苯酚
不能形成分子内氢键,但能形成分子间氢键而缔合。因此邻硝基苯酚的沸点和在水中的溶
解度比其异构体低得多,故可随水蒸气蒸馏出来。
(3) 亚硝化 苯酚和亚硝酸作用生成对亚硝基苯酚。
第十一章 酚和醌
学习要求:
1.掌握酚、醌的分类及其命名法。
2.掌握酚和醌的结构特点与化学性质。 3. 理解酚及取代酚的酸性,比较醇和酚的酸性。 4.了解酚、醌的制备方法。 5.了解苯酚、对苯二酚、萘酚的制法和用途。 6. 了解环氧树脂、离子交换树脂。 7.了解重要的醌。 重点:醇、醚的化学性质、碳正离子的重排。 难点:E1 与 SN1,E2 与 SN2 之间的竞争及影响因素。
酚能与FeCl3溶液发生显色反应,大多数酚能起此反应,故此反应可用来鉴定酚。
6ArOH + FeCl3
[ Fe(OAr)6 ] 3- + 6H+ + 3Cl -
蓝紫色 棕红色
不同的酚与FeCl3作用产生的颜色不同。见P292表 10-6。 与FeCl3的显色反应并不限于酚,具有烯醇式结构的脂肪族化合物也有此反应。 (2) 酚醚的生成 醚不能分子间脱水成醚,一般是由醚在碱性溶液中与烃基化剂作用生成。
⑴ 苯磺酸盐碱熔法。
1
··
SO3Na
+ NaOH
300~320OC 共熔
ONa
+ Na2SO3 + H2O
ONa
OH
+ H+
优点:产率较高、产品纯度好、设备简单;缺点:操作工序多,不易连续化,耗用 大量硫酸和烧碱等无机化工原料,成本较高。
⑵ 氯苯水解。
Cl
+ 2NaOH 350~370OC, 20MPa
OH + Br2(H2O)
OH
Br
Br
+ 3HBr
Br
反应 很灵敏,很稀的苯酚溶液(10ppm)就能与溴水生成沉淀。故 此反应可用作苯酚 的鉴别和定量测定。
如需要制取一溴代苯酚,则要在非极性溶剂(CS2,CCl4)和低温下进行。
OH
+ Br2
CS2 0℃
OH +
Br
OH
Br + 3HBr
(2)硝化 苯酚比苯易硝化,在室温下即可与稀硝酸反应。
