烷烃和环烷烃讲解
烷烃和环烷烃

烷烃与环烷烃区别
一、结构不同
1、烷烃:是开链的饱和链烃(saturated group),分子中的碳原子都以单键相连,其余的价键都与氢结合而成的化合物。
2、环烷烃:含有脂环结构的饱和烃。
有单环脂环和稠环脂环。
含有1个脂环且环上无取代烷基的环烷烃,分子通式为CnH₂n。
二、范围不同
烷烃包括环烷烃,环烷烃是烷烃的一种。
三、性质不同
1、烷烃:低沸点(boiling point)的烷烃为无色液体,有特殊气味;高沸点烷烃为黏稠油状液体,无味;烷烃的物理性质随分子中碳原子数的增加,呈现规律性的变化;烷烃中的氢原子被卤原子(即第七主族元素)取代的反应称为卤化反应(halogenation)。
2、环烷烃:环烷烃有很高的发热量,凝固点低,抗爆性介于正构烃和异构烃之间。
化学性质和烷烃相似。
其中以五碳脂环和六碳脂环的性质较稳定。
有机化学-烷烃和环烷烃

成键的电子云并不沿轴向重叠,而是形成一种弯曲键。 造成重叠程度小, 键能下降,产生角张力。
开链或较大脂环化合物 中轨道可达到最大重叠
Banana bond
环丙烷分子中 轨道部分重叠
H
H
C
105.5°
H
60°
H
C
C
CH2
亚甲基
CH
次甲基
系统命名法
关键是如何确定主链和处理取代基的位置
分三步:一选主链、二编号、三写全称。 1.选主链(母体):选取代基最多的最长碳链 2.编号: 从靠近取代基一端开始 3.写全称:按先小后大,把取代基的位次、数
目及名称列在母体前。
在英文命名中,取代基按词首的字母排列顺序先后列出
烷烃系统命名法的要点:
张力学说:
1885年,Baeyer AV 假定,环烷烃具有平面正多边形的结构 :
60° 90° 108° 120°
128.6 135°
• 环上C-C之间的键角偏离正常键角109°28′,
•环丙烷每个键必须向内偏转24.75°,就会产生角张力。
•环丁烷、环己烷分别向内偏转9.75°, 0.75°。
•环己烷每个键向外偏转5.25°。
第二节、烷烃的命名
(一)普通命名法 (二)系统命名法(IUPAC法)
(一)普通命名法
• 1~10以内的碳原子数用天干字表示:
甲、乙、丙、丁、戊、己、庚、辛、 壬、癸。从十一个碳原子开始用中文数
字表示。
• 直链的烷烃称“正某烷”,“正”(n-)一般 略去。如:
CH3CH2CH3
丙烷
CH3(CH2)10CH3 十二烷
烷烃、环烷烃

烷烃烷烃即饱和烃(saturated group),是只有碳碳单键的链烃,是最简单的一类有机化合物。
烷烃分子里的碳原子之间以单键结合成链状(直链或含支链)外,其余化合价全部为氢原子所饱和。
烷烃分子中,氢原子的数目达到最大值,它的通式为CnH2 n+2。
分子中每个碳原子都是sp3杂化。
最简单的烷烃是甲烷。
烷烃中,每个碳原子都是四价的,采用sp3杂化轨道,与周围的4个碳或氢原子形成牢固的σ键。
连接了1、2、3、4个碳的碳原子分别叫做伯、仲、叔、季碳;伯、仲、叔碳上的氢原子分别叫做伯、仲、叔氢。
为了使键的排斥力最小,连接在同一个碳上的四个原子形成四面体(tetrahedro n)。
甲烷是标准的正四面体形态,其键角为109°28′(准确值:arccos(-1/3))。
理论上说,由于烷烃的稳定结构,所有的烷烃都能稳定存在。
但自然界中存在的烷烃最多不超过50个碳,最丰富的烷烃还是甲烷。
由于烷烃中的碳原子可以按规律随意排列,所以烷烃的结构可以写出无数种。
直链烷烃是最基本的结构,理论上这个链可以无限延长。
在直链上有可能生出支链,这无疑增加了烷烃的种类。
所以,从4个碳的烷烃开始,同一种烷烃的分子式能代表多种结构,这种现象叫同分异构现象。
随着碳数的增多,异构体的数目会迅速增长烷烃还可能发生光学异构现象。
当一个碳原子连接的四个原子团各不相同时,这个碳就叫做手性碳,这种物质就具有光学活性。
烷烃失去一个氢原子剩下的部分叫烷基[1],一般用R-表示。
因此烷烃也可以用通式RH来表示。
烷烃最早是使用习惯命名法来命名的。
但是这种命名法对于碳数多,异构体多的烷烃很难使用。
于是有人提出衍生命名法,将所有的烷烃看作是甲烷的衍生物,例如异丁烷叫做2-一甲基丙烷。
现在的命名法使用IUPAC命名法,烷烃的系统命名规则如下:找出最长的碳链当主链,依碳数命名主链,前十个以天干(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)代表碳数,碳数多于十个时,以中文数字命名,如:十一烷。
烷烃和环烷烃知识点详解

H H
部分重叠式 (反叠式)
CH3
H 3C
H
H
H
H
邻位交叉式 (顺错式)
H 3CC H 3
H H
H H
全重叠式 (顺叠式)
正丁烷不同构象的能量曲线图
2.4.2 环烷烃的构象 Conformation
(1)环丙烷和环丁烷的构象
(2)环戊烷的构象
环戊烷 rotamer
蝴蝶型(环丁烷)
信封型
扭曲型
Envelope conformation twist conformation
0.25nm
5
6
1
3
0.18nm
4
5
6
1
4 2
H
3
2
H
5 H
H 6 HH
H
4 H
3 H
1 H
H 2
H
H H 4H
5
H3 H
H
H 6
H 1 H
HH 2 H
Conformational inversion
船型分子中 存在扭转张 力和氢原子 之间的非键 张力
(4)环己烷椅式构象中的竖键和横键
环己烷中的碳氢键可分为两种类型,每个碳原子上有一 个a键和一个e键,在环中上下交替排列。
CH2 亚甲基
CHCH3 亚乙基
CH2CH2 1,2-亚乙基
C (C H 3)2 亚异丙基
CH2(CH2)4CH2 1,6-亚己基(或六亚甲基)
(B)普通命名法(习惯命名法)
• 碳原子数用“天干”字——甲、乙、丙、丁、戊、己、
庚、辛、壬、癸和十一、十二……等数目字表示。
• 用“正”、“异”、“新”等前缀区别不同的构造异构
烷烃与环烷烃

象; 部分重叠式:甲基和氢互相重叠,能量较高,但比全重叠式的能量低。
构象稳定性 对位交叉式 邻位交叉式 部分重叠式 全重叠式
有机化学 (第9版)
第四章
烷烃和环烷烃
第一节 烷烃 第二节 环烷烃
重点难点
掌握 烷烃及环烷烃的命名,烷烃及环烷烃的构象异构, 烷烃的卤代反应,环烷烃的开环加成反应。
熟悉 烷烃的理化性质,自由基反应的机制。
了解 药物构效关系及自由基作用在医学中的应用。
第Байду номын сангаас节
烷烃
有机化学 (第9版)
一、结构
1. 烷烃中碳原子均采用sp3杂化。
顺-1,2-二甲基环己烷
反-1,2-二甲基环己烷 ee(优势构象)
1. 烷烃碳原子采取SP3杂化,分为伯、仲、叔、季四种类型。
2. 烷烃及环烷烃化合物的命名。 3. 烷烃在光照或加热条件下可进行自由基反应,反应活性与烷烃结构和卤素种类有关。 4. 环烷烃加热可发生氢化开环或亲电加成反应。 5. 烷烃存在构象异构,交叉式为稳定的优势构象,可以用锯架势和纽曼投影式表达。 6. 环烷烃存在椅式构象和船式构象,椅式构象为优势构象,较多取代基位于e键上的 取代为优势构象。
三、构象异构
(二)丁烷的构象
丁烷构象的能量变化及稳定性
正丁烷C2—C3旋转时各种构象的能量曲线
有机化学 (第9版)
三、构象异构
(三)药物构效关系
药物分子的构象与药物作用效果存在一定的关系,通常优势构象具有更好的作用效果。
多巴胺 (抗震颤麻痹药)
第二章 烷烃和环烷烃
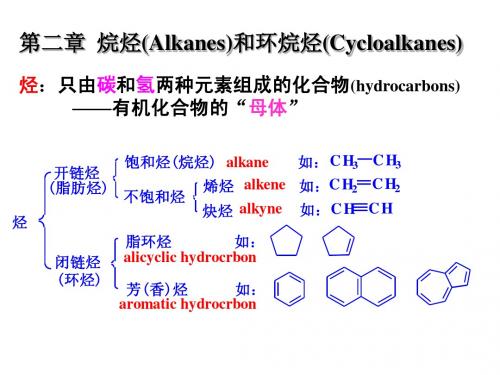
C H3C H2C H2 C H3C H2C H2C H2 C H3C HC H 2 C H3
(正)丁基 Bu 异丁基 i -Bu
C H3C HC H C H3 仲丁基 2 s-Bu C H3 C H3 C C H3 叔丁基 t-Bu
在生理状况下,机体自由基一方面不断产 生,另一方面又不断清除,活性氧处于产生与清 除平衡状态。一旦活性氧的产生和清除失去平衡 ,过多的自由基就会造成对机体的损害,从而引 起多种疾病,并可诱发癌症和导致衰老。 天然抗氧化酶系统:超氧化物歧化酶(SOD) 、 过 氧 化 氢 酶 ( CAT)、 谷 胱 甘 肽 过 氧 化 物 酶 (GSH-Px)
构象异构
(一) 烷烃的构造异构(constitutional isomerism)
戊烷有3种碳链异构体
CH3 CH3CH2CH2CH2CH3 CH3CHCH2CH3
正戊烷 异戊烷
CH3 CH3-C-CH3 CH3
新戊烷
碳原子数 异构体数 4 5 6 7 2 3 5 9
碳原子数 8 9 10 20
异构体数 18 35 75 366 319
天然抗氧剂(自由基清除剂):VE、 Vc、 2巯基乙胺、谷胱甘肽、辅酶Qn(泛醌)、-硫辛酸 等
第二节 环 烷 烃
一、脂环烃的分类和命名
(一) 分类 C3-C4
根 据 环 数 多 少 分
小环 普通环
单脂环烃
C5-C6
C7-C12
中环
C13以上 大环 多脂环烃 桥环 螺环
(二) 命名
1. 单脂环烃: 在相应的烃名前加“环”字;英文名加词头cyclo
《烷烃和环烷烃》课件
第二章 烷烃和环烷烃
8
例1 CH3-CH2 5
32 1
CH2-CH-CH2 -CH-CH2-CH3
CH2
CH3
CH3
3-甲基-5-乙基辛烷
取读 代作 基: 位位 次
连基 母
字名 体
符
名
例2 CH3-CH2-CH—CH-CH2-CH3 CH3-CH CH-CH3 CH3 CH3
2,5-二甲基-3,4-二乙基己烷 2,5-甲基-3,4二乙基己烷 2,5-2甲基 3,4-2乙基己烷
8 7 65 43 2 1
CH3
2024/8/14
22
第二章 烷烃和环烷烃
2、确定取代基小结
(给主链编号)
(1)近取代基端编号;
CH3
CH2CH3
(2)若两个不同取代 基位于相同位次时, 按次序规则使小取代
CH3CH2CHCH 2CHCHCH 2CH2CH3 CH2CH2CH3
CH3 CH3
基编号较小(不考虑 下一个取代基);
12
456
例3 6CH3-5CCHH-3CH2—3CCHH—2CCHH—3 1CH3
CH3 CH3
2,5-二甲基-3-异丙基己烷 2,5-二甲基-4-异丙基己烷
上页 下页 首页
第二章 烷烃和环烷烃
①
CH3 CH3
C7 H3C6 H25CH4CH3CHC2 HC1H 3 CH2 CH3
③
CH2 CH3
正戊烷
(CH3)2CHCH2CH3 (CH3)2C(CH3)2
异戊烷 新戊烷
第二章 烷烃和环烷烃
碳链异构的特点:
随着分子中碳原子数目增加,异构 体数目急剧增加。
例: C6H14 异构体数目 5个
2第二章烷烃和环烷烃
H
109°28′
1.09×10 –10m
415 kJ/mol
2 乙烷的结构
H H
H H
H H C C H H H
H
H
C C
H
H
H H
H
乙烷的分子轨道示意图
烷烃碳链的锯齿状
伯碳原子(1 ):与一个碳原子相连 仲碳原子(2 ):与两个碳原子相连
。
。
仲(20)
碳 原 子 类 型
CH3 CH3 季(40)
(2)Cl• + CH4 链增长 (3)CH3• + Cl2 (4)Cl• + CH3Cl (5)CH2Cl• + Cl2 Cl• + Cl•
2Cl•
CH3• + HCl 反复 CH3Cl + Cl • 进行 CH2Cl• + HCl
CH2Cl2 + Cl•
Cl2 CH3Cl CH3CH3
链终止
Cl• + CH3• CH3• + CH3•
正丁烷C2—C3键旋转时的分子的位能曲线图
稳定性:对位交叉式>邻位交叉式>部分重叠式>全重叠式
一、状态
1、1~4:气体 2、5~16:液体 3、≥17:固体
二、沸点(b.p.)
四 烷 烃 物 b.p. 36.1oC 25oC 理 性 三、熔点(m.p.) m.p. 质 M越大,m.p.越大
结构越对称,m.p.越大
第二章 烷烃和环烷烃
烷 被 【 烃 氢 烷 】 完 】 通 指 全 取 式 碳 饱 完 氢 和 全 化 ; 之 合 【 意 物 烃 , 。 碳
ting
:
CnH2n+2
第一节
2.烷烃和环烷烃
③ 写出少二个碳原子的直链式为主链
CH3 H3C C CH3
CH3
新戊烷
第一节 分类、构造异构和碳原子的级
烃:仅由C、H两种元素组成的化合物。
烷烃 脂肪烃 烯烃 烃 脂环烃 炔烃
芳香烃
(2)单环烷烃的构造异构 环的大小和环上取代基的不同而引起的异构; 与单烯烃互为异构。
C4H8
H2C C CH3 CH3
e
四、环己烷的构象
1、椅式、船式和扭船式构象 角偏差(α) = (109.5o-120o) / 2=-5.25o 较大。
通过环内C-Cσ键旋转,调整其内角接近109.5o, 使完全无角张力——椅式和船式构象。
(1)椅式构象
H
H
H
5
H
6
H
1
H
4
3H
H
H
2
H
H
① 无角张力。
② C1、C3、C5上或C2、C4、C6上处于竖直向上或 向下的三个氢原子间距离为2.3Å,约等于氢原子范 德华半径之和(2.5Å)——无范德华排斥力(跨环张力)。
把支链作为取代基。
1、常见的烷基: 相应的烷烃去掉一个氢原子后留下的原子团。
通式:CnH2n+1
常以 R- 表示
甲基(Me)—— CH3乙基(Et) —— C2H5-
异丙基(i-Pr)—— H3C CH
CH3
正丁基(n-Bu)—— CH3CH2CH2CH2-
异丁基(i-Bu)—— H3C CH CH2
一、烷烃的结构
结构
C:sp3 Csp3-Hs Csp3-Csp3 σ键
1、σ键:轴向重叠形成的共价键(头碰头), 呈圆柱形轴对称。
2、σ键特性 ① 原子轨道轴向重叠(重叠程度大,键较牢固)。 ② 成键轨道呈轴对称,可“自由旋转”。
烷烃和环烷烃
10 只与一个碳原子相连 20 与两个碳原子相连 30 与三个碳原子相连 40 与四个碳原子相连
2o 1o
CH3 CH3 3o 2o 2o 1o H3C C4o CH2CHCH2CH2CH3 H3C C3o CH3 CH3 CH3
CH3CH2CH CH3
CH3CH2CH2CH2
叔丁基 tert-butyl
第四章 烷烃和环烷烃
重点讲解内容 一、烷烃的结构 二、烷烃的命名 三、烷烃的物理性质 四、烷烃的化学性质 五、烷烃的构象异构
烃(hydrocarbon):仅由碳和氢两种元素组
成的有机化合物。
烷烃(alkane):烃分子中的碳原子彼此以C-C
单键连接,碳的其余键都与氢原子相连。
最简单的烷烃为甲烷:Molecular formula CH4
CH3
CH3CH2CH CHCH CHCH3 2,3,5- 三甲基-4-丙基庚烷 CH3 CH2 CH3 CH2CH3
(B)主链的编号(最近、最小、小小)
原则:从最靠近支链的一端开始编号,用 1 , 2 , 3……表示,即取代基位次最小。有几个取代基 时,取代基位次的和最小。和相同时,小的取 代基位次小为宜。
另外,若要画出三维结构,可用下述方法表示:
F Cl C Br H
表示该键指向纸面的背后 表示该键指向纸面的前面
二、构造异构和命名 (一)碳链异构
烷烃同系列中,甲、乙、丙无同分异构,丁烷有: CH3CH2CH2CH3 C4H10 b.p. -0.5℃ CH3CHCH3 C4H10 b.p. -10.2℃
重叠式的能量比交叉式高12.6kJ/mol(单键旋转的能垒 一般在12.6~41.8kJ/mol),这种能垒非常低,室温下的 分子热运动即可达到,因此常温下分离不出纯的烷烃的分 子构象)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
叔碳(3°):三级碳原子,只与3个其他碳原子直接相连
季碳(4°):四级碳原子,只与4个其他碳原子直接相连
CH 3
CH 3
H3C C CH 2
3° 2°
H
伯氢(1°H):伯碳上的H
仲氢(2°H):仲碳上的H
叔氢(3°H):叔碳上的H
C
4°
CH 3
CH 3
1°
不同类型的氢
反应活性不一样
二、烷烃的命名(P23-25)
烃的主要来源:
天然气 甲烷(主要)、乙烷、丙烷、丁烷、戊烷
石 油 各种烃的混合物:汽油 C5-11,煤油C11-15,
柴油 C15-18, 润滑油C16-20,石蜡C18-30,
沥青C30-40
煤
芳香烃等
第一节 烷烃 Alkane
一、烷烃的结构
结构特征:C为sp3杂化,各原子间以单键相连(键)。
C2H6 乙烷 ethane C4H10 丁烷 butane C6H14 己烷 hexane C8H18 辛烷 octane
•用“正”、“异”、“新”等字区别同分异构体
n-
iso- neo-
例如:
CH3CH2CH2CH2CH3
(正)戊烷 n-pentane
CH3CHCH2CH3 CH3
异戊烷 isopentane
药效构象
如:多巴胺是体内合成去甲肾上腺素的前体, 其药效构象为
NH 2
H
H
H
H
OH OH
四、烷烃的化学性质
1. 稳定性 室温下烷烃与强酸、强碱、强氧化剂或强还原 剂不发生反应或反应很慢。
2. 卤代反应 (Cl2、Br2) halogenation
CH4
Cl2 光
Cl2
CH3Cl 光
CH2Cl2
Cl2 光
P119
第二章 烷烃和环烷烃
烃 hydrocarbons 只含有碳和氢两种元素的化合物
饱和烃——烷烃
脂肪烃 aliphatic
烯烃 不饱和烃
炔烃
hydrocarbon 脂环烃
烃
alicyclic hydrocarbon
芳香烃 aromatic hydrocarbon
苯型芳香烃 非苯型芳香烃
链烃 环烃
近109º28’。
键的特点:键能大,极化度小,稳定,且成键原子可绕键轴旋转。导 致烷烃化学性质稳定,且具有特殊异构现象——构象异构 。
烷烃分子组成可用通式CnH2n+2表示。
同系列(homologous series):具有相同的组成通式和 结构特征的一系列化合物
同系物(homolog):同系列中的化合物互称为同系物 同系差:相邻两同系物之间的组成差别。烷烃同系物的 系差为CH2 。
H
锯架式
H
H H
H
HH
H
Newman 投影式
H
H
H
H
H
H
H
H
H
HH
H
HH
H
(2)正丁烷的构象 有四种典型conformation:
2 3
CH3
H
H
H
H
CH3
对位交叉式 优势构象
CH3
H
CH3
H
H
H
邻位交叉式
H CH3
H3C CH3
HH
CH3 H
HH
H H
部分重叠式 全重叠式 最不稳定构象
药物分子的构象与其生物活性有着密切关系。许多药 物分子是以特定的构象与受体结合发挥作用。
有机化合物的分子组成相同而结构不同的现象 ——同分异构现象
具有相同的分子式但结构式不同的化合物称为 异构体 isomer 1. 碳链异构 carbon chain isomerism(P4)
随着碳原子数增加(4C以上)出现不同碳链结构的构 造异构体。
如:戊烷有三个碳链异构体
2. 构象异构 conformational isomerism(P98) 烷烃分子中成键原子可绕单键自由旋转,导
CH3 CH3 C CH3
CH3
新戊烷 neopentane
烃分子中去掉一个氢原子后剩下的原子团叫做烃基(R-)
常见的烷基见P24 其中1~4C 烷基英文名称要记住(词尾“ane”改为“yl”)
2. 系统命名法 选主链 碳链最长,取代最多
编号 位次最低
取代基 先小后大(优先基团后列出),同基合并 用中文小写“二、三、四”表明取代基数 目,在英文名称中,基团按字母顺序先后 列出,用“di、tri、tetra”表示取代基数目
同系物具有相似的化学性质,但反应速率往往有较大的差 异;物理性质一般随碳原子数的增加而呈现规律性变化。 同系列中的第一个化合物往往具有明显的特性。
碳原子的类型
饱和碳原子分为伯、仲、叔、季四种类型
伯碳(1°):一级碳原子,只与1个其他碳原子直接相连
仲碳(2°):二级碳原子,只与2个其他碳原子直接相连
CH3 CH CH2 CH CH2 CH3
CH2
CH2
CH2
CH2
CH3
CH3
4-甲基-6-乙基壬烷
6-ethyl-4-methylnonane
CH3 CH2 CH CH2 CH CH3
CHCH3 CH3
CH3
2,5-二甲基-3-乙基己烷 3-ethyl-2,5-dimethylhexane
三、烷烃的异构现象 isomerism
致分子中原子或基团在空间的排列方式不同而产 生的立体异构现象——构象异构。这种空间排列 方式——构象 conformation
(1)乙烷的构象
H3C
CH 3
当C-C键旋转时, 可产生无数个构象
有两种典型conformation:
乙烷的两种典型构象的表示方法
优势构象
交叉式 staggered
H
重叠式 eclipsed
1. 普通命名法 •按分子中碳原子总数叫“某烷” ≤10C 用甲、乙、丙、丁、戊、己、庚、辛、壬、癸 表示, >10C 用十一、十二 等中文数字表示。
烷烃的英文名称:表示碳原子数的词头 + ane 词尾组成
CH4 甲烷 methane C3H8 丙烷 propane C5H12 戊烷 pentane C7H16 庚烷 heptane
CHCl3
Cl2 光
甲烷和氯气的光照卤代反应包括链引发、链增长、链终止三步。 free radical reaction
➢chain-initiating step Cl:Cl 光或热 Cl· + Cl·
➢chain-propagating step Cl· + CH4 —>CH3· + HCl CH3· + Cl2 —>CH3Cl + Cl·
如:
H
CH4 , H C H
甲烷
H
Tetrahedral,
all orbital bond
angles are 109.5o.
H
σ sp3-s
键角109º28’ 正四面体构型
H H
H
H
CH3 CH3 , H C
乙烷
H
H
由于C上所连基团不同,
CH σsp3-s 键角有所变化,但也接
H
σsp3-sp3
