16种多环芳烃的结构式

SIGMA-ALDRICH
16种多环芳烃
中文名英文名结构式分子式分子量CAS号价格(元)
萘 Naphthalene
(NAP)C10H8 128.17 91-20-3 148.59元/0.25g
484.59元/1g
analytical standard
(Fluka)
553.41元
5000 μg/L
Analytical
standard
(Supelco)
苊烯Acenaphthyle
ne
(ANY)C12H8 152.19 208-96-
8
544.05元
5000 μg/mL i n methanol, analytical
standard (Supelco)
苊Acenaphthene ?
C12H10 154.21 83-32-9276.12元
200 μg/mL i n methanol, analytical
standard (Supelco)
芴Fluorene
(FLU)C13H10 166.22 86-73-7 544.05元
5000 μg/mL in methanol,analytical
standard (Supelco)
菲Phenanthren
e
(PHE)C14H10 178.23 85-01-8 544.05元
5000 μg/mLin methanol,analytical
standard (Supelco)
蒽 Anthracene
(ANT)C14H10 178.23 120-12-
7
221.13元/0.25g
analytical standard (Cerilliant)
荧蒽Fluoranthen
e C16H10 202.25206-44
-0
544.05元
5000 μg/mLin methanol,analytical
standard (Supelco)
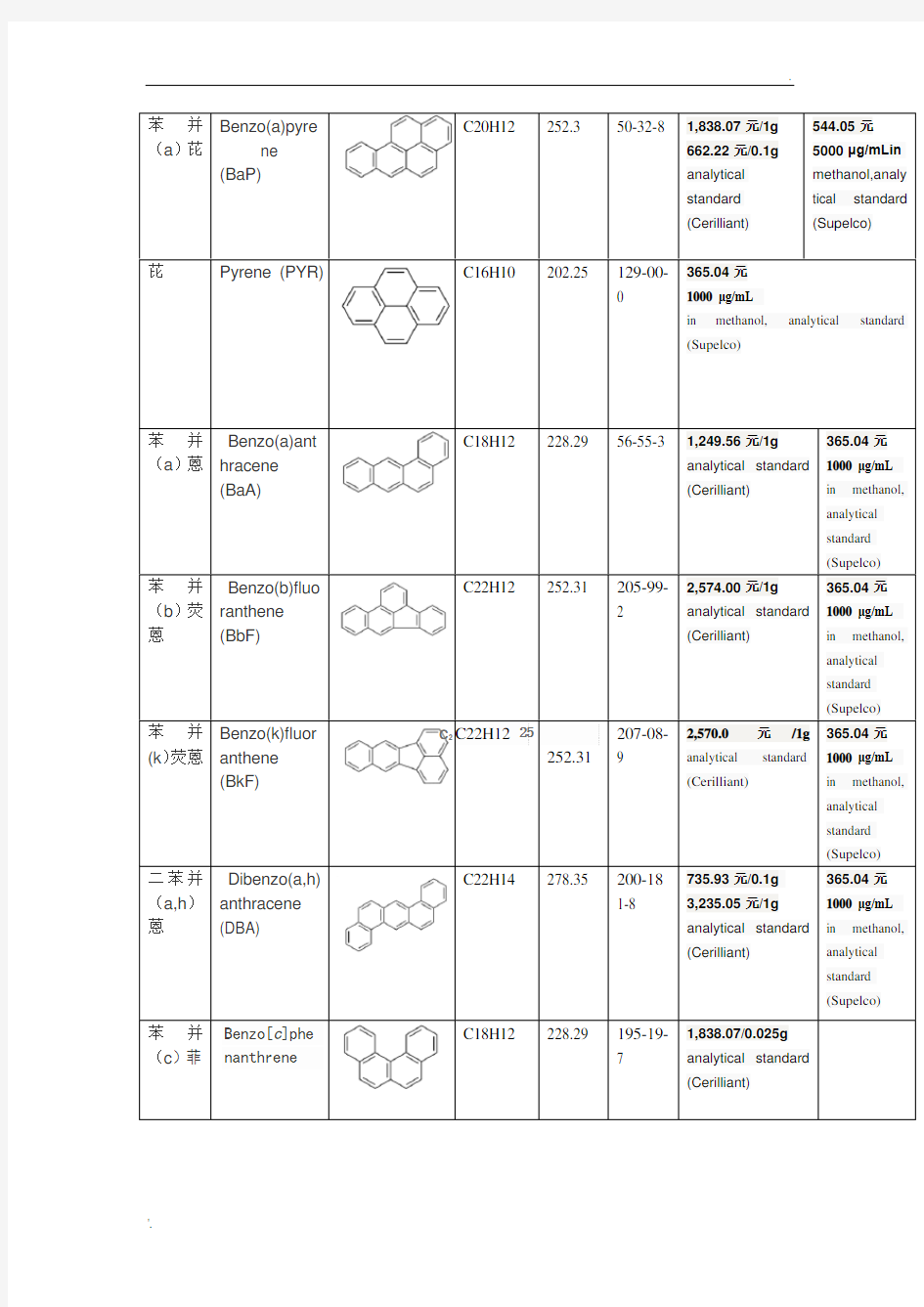
苯并(a)芘Benzo(a)pyre
ne
(BaP)
C20H12 252.3 50-32-8 1,838.07元/1g
662.22元/0.1g
analytical
standard
(Cerilliant)
544.05元
5000 μg/mLin
methanol,analy
tical standard
(Supelco)
芘Pyrene (PYR)C16H10 202.25 129-00-
0 365.04元
1000 μg/mL
in methanol, analytical standard (Supelco)
苯并(a)蒽 Benzo(a)ant
hracene
(BaA)
C18H12 228.29 56-55-3 1,249.56元/1g
analytical standard
(Cerilliant)
365.04元
1000 μg/mL
in methanol,
analytical
standard
(Supelco)
苯并(b)荧蒽 Benzo(b)fluo
ranthene
(BbF)
C22H12 252.31 205-99-
2
2,574.00元/1g
analytical standard
(Cerilliant)
365.04元
1000 μg/mL
in methanol,
analytical
standard
(Supelco)
苯并(k)荧蒽Benzo(k)fluor
anthene
(BkF)
C2 C22H1225
252.31
207-08-
9
2,570.0元/1g
analytical standard
(Cerilliant)
365.04元
1000 μg/mL
in methanol,
analytical
standard
(Supelco)
二苯并(a,h)蒽 Dibenzo(a,h)
anthracene
(DBA)
C22H14 278.35 200-18
1-8
735.93元/0.1g
3,235.05元/1g
analytical standard
(Cerilliant)
365.04元
1000 μg/mL
in methanol,
analytical
standard
(Supelco)
苯并(c)菲Benzo[c]phe
nanthrene
C18H12 228.29 195-19-
7
1,838.07/0.025g
analytical standard
(Cerilliant)
苯并(ghi)苝Benzo[ghi]p
erylene C22H12
?2
276.33
191-24-26618.69元/1g
441.09元/0.025g
analytical standard
(Cerilliant)
304.2
100 μg/mL
in methanol,
analytical
standard
(Supelco)
茚并[1,2,3-c d]芘Indeno[1,2,
3-cd]pyrene
C22H12276.33 193-39-
5
9927.45元/1g
735.93元/0.025g
analytical standard
(Cerilliant)
276.12元
100 μg/mL
in methanol,
analytical
standard
(Supelco)
16种常见多环芳烃的物理性质
16种常见多环芳烃的 物理性质 -CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN
萘英文名称NAP Naphthalene分子量 128.18 物理性质;密度1.162 熔点80.5℃,沸点217.9℃,凝固点,80.5℃,闪点78.89℃,折射率1.58212(100℃)恒压燃烧热:40264.1J/g(标准大气压,298.15K)恒压燃烧热:40205J/g(标准大气压,298.15K)。不溶于水,溶于乙醇和乙醚等。易挥发,易升华溶于乙醇后,将其滴入水中,会出现白色浑浊。化学性质(1)萘的氧化温和氧化剂得醌,强烈氧化剂得酸酐。萘环比侧链更易氧化,所以不能用侧链氧化法制萘甲酸。电子云密度高的环易被氧化。(2)萘的还原(3)萘的加成(4)萘的亲电取代反应萘的a-位比b-位更易发生亲电取代反应。a-位取代两个共振式都有完整的苯环。b-位取代只有一个共振式有完整的苯环。在萘环上主要发生亲电取代,同苯环一样,但活性比苯环强从中间对称的两个C旁边的C开始标,其中1,4,5,8号碳活性完全一样(称为阿尔法碳),2,3,6,7号碳性质完全一样(称为贝塔碳)。一般情况下,阿尔法碳活性大于贝塔碳,取代基在阿尔法位上,这是由动力学控制,温度较高时,阿尔法碳[1]上取代基会转移到贝塔碳上。但在萘的弗瑞德-克来福特酰基化反应,不加热却生成了阿尔法位和贝塔位的混合物。如用硝基甲烷为溶剂,则主要生成贝塔酰化产物。 苊烯ANY Acenaphthylene 分子量:152.200 性质:黄色棱柱状或板状结晶。熔点92-93℃,沸点265-275℃(部分分解),156-160℃(3.73千帕),相对密度0.8988(16/2℃),易溶于乙醇、甲醇、丙醇、乙醚、石油醚、苯,不溶于水。能在强酸中聚合。 苊ANA Acenaphthene 英文别名:1,8-Ethylenenaphthalene 分子量:154.21性状描述:白色或略带黄色斜方针状结晶。物理参数:密 度:1.0242(99/4°C) 熔点:96.2°C 沸点:279°C 闪点:125°C 折射率:1.6048(95°C) 芴FLU Fluorene分子量:166.22 性状描述:白色叶状至小片状结晶物理参数:密度:1.202 g/mL 熔点:116-117°C 沸点:295°C 闪点:151°C
16种多环芳烃的结构式
SIGMA-ALDRICH 16种多环芳烃 中文名英文名结构式分子式分子量CAS号价格(元) 萘 Naphthalene (NAP)C10H8 128.17 91-20-3 148.59元/0.25g 484.59元/1g analytical standard (Fluka) 553.41元 5000 μg/L Analytical standard (Supelco) 苊烯Acenaphthyle ne (ANY)C12H8 152.19 208-96- 8 544.05元 5000 μg/mL i n methanol, analytical standard (Supelco) 苊Acenaphthene ? C12H10 154.21 83-32-9276.12元 200 μg/mL i n methanol, analytical standard (Supelco) 芴Fluorene (FLU)C13H10 166.22 86-73-7 544.05元 5000 μg/mL in methanol,analytical standard (Supelco) 菲Phenanthren e (PHE)C14H10 178.23 85-01-8 544.05元 5000 μg/mLin methanol,analytical standard (Supelco) 蒽 Anthracene (ANT)C14H10 178.23 120-12- 7 221.13元/0.25g analytical standard (Cerilliant) 荧蒽Fluoranthen e C16H10 202.25206-44 -0 544.05元 5000 μg/mLin methanol,analytical standard (Supelco)
16种常见多环芳烃的物理性质
萘英文名称NAP Naphthalene分子量128.18 物理性质;密度1.162 熔点80.5℃,沸点217.9℃,凝固点,80.5℃,闪点78.89℃,折射率1.58212(100℃)恒压燃烧热:40264.1J/g(标准大气压,298.15K)恒压燃烧热:40205J/g(标准大气压,298.15K)。不溶于水,溶于乙醇和乙醚等。易挥发,易升华溶于乙醇后,将其滴入水中,会出现白色浑浊。化学性质(1)萘的氧化温和氧化剂得醌,强烈氧化剂得酸酐。萘环比侧链更易氧化,所以不能用侧链氧化法制萘甲酸。电子云密度高的环易被氧化。(2)萘的还原(3)萘的加成(4)萘的亲电取代反应萘的a-位比b-位更易发生亲电取代反应。a-位取代两个共振式都有完整的苯环。b-位取代只有一个共振式有完整的苯环。在萘环上主要发生亲电取代,同苯环一样,但活性比苯环强从中间对称的两个C旁边的C开始标,其中1,4,5,8号碳活性完全一样(称为阿尔法碳),2,3,6,7号碳性质完全一样(称为贝塔碳)。一般情况下,阿尔法碳活性大于贝塔碳,取代基在阿尔法位上,这是由动力学控制,温度较高时,阿尔法碳[1]上取代基会转移到贝塔碳上。但在萘的弗瑞德-克来福特酰基化反应,不加热却生成了阿尔法位和贝塔位的混合物。如用硝基甲烷为溶剂,则主要生成贝塔酰化产物。 苊烯ANY Acenaphthylene 分子量:152.200 性质:黄色棱柱状或板状结晶。熔点92-93℃,沸点265-275℃(部分分解),156-160℃(3.73千帕),相对密度0.8988(16/2℃),易溶于乙醇、甲醇、丙醇、乙醚、石油醚、苯,不溶于水。能在强酸中聚合。 苊ANA Acenaphthene 英文别名:1,8-Ethylenenaphthalene 分子量:154.21性状描述:白色或略带黄色斜方针状结晶。物理参数:密度:1.0242(99/4°C) 熔点:96.2°C 沸点:279°C 闪点:125°C 折射率:1.6048(95°C) 芴FLU Fluorene分子量:166.22 性状描述:白色叶状至小片状结晶物理参数:密度:1.202 g/mL 熔点:116-117°C 沸点:295°C 闪点:151°C 菲PHE Phenanthrene 分子量:178.23性状描述:类白色粉状结晶体。物理参数密度:1.179 g/mL(25°C) 熔点:101°C 沸点:340°C 折射率:1.59427 蒽ANT Anthracene 分子量178.22物理性状带有淡蓝色荧光的白色片状晶体或浅黄色针状结晶。(纯品为白色带紫色荧光) 相对密度 1.25(27℃);1.283(25℃),熔点217,沸点342,闪点196.1,121.1(闭式)(以上均为℃),蒸汽压[1] 0.13kPa/145℃不溶于水、难溶于
16种多环芳烃的结构式教学文案
16种多环芳烃的结构 式
精品资料 仅供学习与交流,如有侵权请联系网站删除 谢谢2 SIGMA-ALDRICH 16种多环芳烃 中文名 英文名 结构式 分子式 分子量 CAS 号 价格(元) 萘 Naphthalen e (NAP) C10H8 128.17 91-20-3 148.59元/0.25g 484.59元/1g analytical standard (Fluka) 553.41元 5000 μg/L Analytical standard (Supelco) 苊烯 Acenaphthy lene (ANY ) C12H8 152.19 208-96-8 544.05元 5000 μg/mL i n methanol, analytical standard (Supelco) 苊 Acenaphthene ? C12H10 154.2 1 83-32-9 276.12元 200 μg/mL i n methanol, analytical standard (Supelco) 芴 Fluorene (FLU ) C13H10 166.22 86-73-7 544.05元 5000 μg/mL in methanol,analytical standard (Supelco) 菲 Phenanthre ne (PHE ) C14H10 178.23 85-01-8 544.05元 5000 μg/mLin methanol,analytical standard (Supelco) 蒽 Anthracene (ANT) C14H10 178.23 120-12-7 221.13元/0.25g analytical standard (Cerilliant) 荧蒽 Fluoranthen e C16H10 202.2 5 206- 44-0 544.05元 5000 μg/mLin methanol,analytical standard (Supelco) 苯并(a ) 芘 Benzo(a)py rene (BaP) C20H12 252.3 50-32-8 1,838.07元/1g 662.22元/0.1g analytical standard (Cerilliant) 544.05元 5000 μg/mLin methanol,analy tical standard (Supelco)
高效液相色谱测定16种多环芳烃
湖南省环境监测中心站 分析方法验证报告 方法名称:高效液相色谱法测定土壤中16种多环芳烃 研究人员:黄东勤 二○○七年六月十日
高效液相色谱法测定土壤中16种多环芳烃 1.前言 多环芳烃(简称PAHs)主要是有机物在高温下不完全燃烧而产生,广泛存在于土壤、水等自然环境和各种食品中。其中萘、芘等16种PAHs因具有致畸、致癌和致突变作用而被视为最严重的有机污染物类型之一。国家环保总局推荐用高效液相色谱法(HPLC)测定饮用水、地下水、湖水、河水及工业废水中的PAHs,但对土壤中PAHs 的测定方法未作介绍。由于土壤样品基体复杂,PAHs的浓度很低且稳定性差,因此需要对样品进行预处理以富集待测组分,提高检测的灵敏度并降低检测限。 目前国内对PAHs土壤样品的处理多用索氏提取法或微波萃取法,本文研究用加速溶剂萃取土壤中的16种PAHs,提出最佳技术参数,并对实际土壤样品进行测定。 2.方法原理及适用范围 2.1原理 2.1.1萃取:加速溶剂萃取仪是一台可从各种固体或半固体样品中萃取有机组分的自动系统。该方法通过提高溶剂温度加速传统的萃取处理。在萃取池中加压以使萃取过程中萃取池中填充的溶剂始终处于液体状态。加热后,提取物从样品池中冲到收集瓶中以备分析使用。 2.1.2过柱淋洗:用加速溶剂提取获得的土壤提取液为黄褐色粘稠液体,基体复杂,在用HPLC测定前必须净化。本研究选用硅胶柱进
行净化,以溶剂正己烷:二氯甲烷= 3:2进行洗脱。 2.1.3氮吹:氮吹进行溶剂转化。 2.1.4色谱分离原理:HPLC是利用样品中的溶质在固定相和流动相之间分配系数的不同,进行连续的无数次的交换和分配而达到分离的过程。 2.2 适用范围 本方法测定16种多环芳烃,适用于土壤等复杂基体物质。对于饮用水、地下水和地表水以及生活污水和工业污水。第一步前处理条件有待实验,其余过程均可适用。 2.2.1仪器适用范围:0.08-100 m g /L。每小时能测定1个样品。 3.试剂和材料 乙睛、二氯甲烷、正己烷、丙酮、甲醇均为色谱纯;16种多环芳烃混合标准液:美国Supelco公司;实验用水为二次蒸馏水,0.45μm 膜过滤;商用硅胶柱(1g,6mL);水系过滤头;1mL一次性注射器。 4.仪器设备 4.1高效液相色谱仪:LC-10AVP型,日本岛津公司。 4.2加速溶剂提取仪:戴安ASE200。 4.3氮吹仪:哈西Caliper Turbovap II。 4.4超声波发生器。 5. 试样与标准样品的制备 5.1 试样的制备 5.1.1萃取:
多环芳烃
多环芳烃(PAHs)是环境常见的污染物之一,其来源于有机物热解和不完全燃烧, 在空气、水、土壤中广泛分布。由于食品产地环境受到污染, 致使PAHs在食 品中存在,同时加工方式不同, 也会影响食品中PAHs的含量。长期食用含有PAHs的食物对健康将产生潜在威胁[2-5]。不同国家和地区, 烹饪方法和饮 食习惯不同,从食品中摄入的PAHs量也不相同。 不同食品中含有不同种类和浓度的多环芳烃,其主要来源有以下3方面: (1)自 然界天然存在的,如植物、细菌、藻类的内源性合成,使得森林、土壤、海洋 沉积物中存在多环芳烃类化合物; (2)环境污染造成的,现代工业生产和其它许 多方面要使用和产生多环芳烃类化合物;这些物质难免会有一些排放到食品的 生产环境如水源、土壤、空气、海洋中,从而对食品造成污染,这是目前食品 中多环芳烃最主要的来源;(3)食品加工和包装过程中产生的,如食品的烤、炸、熏制和包装材料、印刷油墨中多环芳烃污染,这也是食品中多环芳烃的重要来源。目前,各类食品已检测出20余种PAHs,其中以熏烤类食品污染最严重:如熏 肉吉有屈、苯并[b]荧蒽、苯并[e]芘、苯并[k]荧蒽、苯并[a]芘、1,2,5,6- 二苯并蒽、茚[1,2,3-cd]并芘等PAHs。王绪卿评价了14种熏烤肉中PAHs的污 染水平,并在19份腊昧肉中全部测出屈、苯并[e]芘、苯并[k]荧蒽,其中9份 样品苯并[a]芘量为0.34~27.56μg/kg。另据报道,尼日利亚各种熏烤鱼中均 含有PAHs。比较了现代烤炉与传统烤炉熏烤物中13种PAHs含量,前PAHs<4.5μg/kg。后者苯并[a]芘为0.2~4.1μg/kg(湿质量)。食用植物油及其加热产 物中均含有PAHs[6-7],而且加热后PAHs含量显著增加。实验表明,食用植物油 加温后B(a)P含量是加温前的2.33倍,1,2,5,6-二苯并蒽为4.17倍,而且油烟 雾中其含量更高,厨房空气气态样品中PAHs种类与含量均大于颗粒物,说明厨 房空气中PAHs可能主要是由于食品,特别是动植物蛋白以热油烹炸过程中形成。近年来在各种酒样中也发现了PAHs,但这方面研究尚待深入,Moret等在所有白 酒和啤酒中都检出苯并[b]荧蒽、苯并[k]荧蒽、苯并[a]芘、1,12-苯并苝、 茚[1,2,3-cd]并芘以及芴、苯并a蒽、1,2,5,6-二苯并蒽,其PAHs总量<0.72 μg/kg。目前, 各种蔬菜亦受到不同程度PAHs污染, 其来源可能是根系吸 收及叶面吸附。国际癌症研究机构(IARC,1973)曾报道西红柿中苯并[a]芘为 0.2pg/kg,王爱玲等测定白菜和西红柿中苯并[a]芘分别为1.310~12.316μ g/kg和0.841~4.335μg/kg[8]。在食品制作的过程中,有许多制作方法是不可
气相色谱_质谱法测定蔬菜中的16种多环芳烃
[作者简介] 王建华(1968-),男,博士,高级工程师,主要从事食品卫生检验研究。【化学测定方法】 气相色谱-质谱法测定蔬菜中的16种多环芳烃 王建华1,2,姜海燕3,王 惠2,王修林2 (11青岛出入境检验检疫局,山东青岛 266002;21中国海洋大学,山东青岛 266003; 31山东中粮花生制品进出口有限公司,山东青岛 266001) [摘要] 目的:研究蔬菜中多环芳烃(P AH s)残留量的气相色谱-质谱分析方法。方法:蔬菜经过环己烷提取,硫酸溶液和PS A固相萃取柱净化,用气相色谱-质谱选择离子监测模式(SI M)定性和定量检测多环芳烃。结果:16种P AH s加标回收率范围在60%~120%之间,相对标准偏差为8%~20%,检测限范围为01009~0106μg/kg。结论:本方法适合蔬菜中P AH s检测。 [关键词] 固相萃取;多环芳烃;蔬菜;气相色谱-质谱 [中图分类号] O657163 [文献标识码] A [文章编号] 1004-8685(2006)02-0197-03 环境中的多环芳烃(polycyclic ar omatic hydr ocarbons, P AH s)主要产生于矿物的不完全燃烧,部分P AH s有致畸、致癌、致突变作用,P AH s的监测已越来越受到人们的重视。目前,测定大气、水、土壤中P AH s的文献较多[1~3],蔬菜通过吸收水和大气中的粉尘而含有了P AH s,但关于蔬菜中P AH s测定方法的文献较少[3,4]。本文中,我们首次采用环己烷提取,硫酸溶液和PS A固相萃取柱组合净化,用GC-MS同时定性和定量检测蔬菜中美国EP A优先表中所列的16种P AH s。 1 材料与方法 111 仪器与试剂 Agilent6890气相色谱-5973N质谱联用仪,配7683自动进样器,分流/不分流进样口(美国Agilent公司);毛细管气相色谱柱为HP-5MS(Phenyl Methyl Sil oxane5%二苯基-95%二甲基硅氧烷,30m×0125mm×0125μm);ULTRAT URRAX 均质器(德国I K A公司);离心机(Eppendorf5810);I K A快速混匀器(德国I K A公司中国广州工厂);移液枪:012、110、10m l (法国Gils on公司);GI L S ON ASPEC XL全自动固相萃取仪(法国Gils on公司);PS A固相萃取柱(500mg,6m l,美国Varian公司)。 P AH s标准品(R iedel-dehaen公司):根据需要将10mg/L储备液用环己烷逐级稀释成工作溶液;水经m illi pore 纯水器纯化;硫酸溶液(9mol/L),取硫酸原液,用水稀释一倍。 112 样品处理 提取:称取1010g样品于50m l塑料离心管中,加入环己烷30m l均质2m in,6000r/m in离心5m in,将上清液转入125m l分液漏斗中;将残渣用20m l环己烷重复提取1次,离心后合并上清液于分液漏斗中。 净化:在分液漏斗中加入10m l硫酸溶液进行磺化,充分震荡后静置分层,弃去下层硫酸层(如有必要重复一次);然后加入1g氯化钠粉末,10m l纯水洗涤环己烷层,静置后弃去水层。 将环己烷层转入100m l鸡心瓶中,旋转蒸发至干;精确加入2m l环己烷清洗瓶壁,置于全自动固相萃取仪中,PS A柱先用5m l环己烷活化,取样品液1m l(相当于5g样品)过PS A 柱,加入15m l环己烷洗脱;将洗脱液收集到50m l鸡心瓶中旋转蒸发至干;以1m l环己烷准确定容,充分洗涤瓶壁后转入进样瓶中准备检测。 113 气相色谱-质谱测定 11311 气相色谱条件 载气:高纯氦气,恒压模式1917p si (1p si=6894176Pa),柱温程序:初始温度70℃,保持410m in,以25℃/m in的速率,升温到150℃,以3℃/m in的速率,升温到200℃,再以8℃/m in的速率,升温到280℃保持1010m in;进样量:1μl。 11312 质谱条件 离子源温度:150℃,四极杆温度:230℃,色谱-质谱接口温度:280℃;离子化方式:E I;电子能量:70e V;调谐方式:自动调谐;全扫描(S CAN)测定方式的扫描范围50~450m/z。 2 结果与讨论 211 P AH s的分离和测定 按照所列的色谱/质谱条件,用SC AN方式对16种P AH s 进行扫描,测得其总离子流图(见图1)。然后根据各待测化合物的保留时间和质谱图,确定选择离子监测(SI M)的采集时间和特征离子,并以3倍信噪比计算检测限,结果见表1。 图1 16种多环芳烃的总离子流图 11萘;21苊烯;31苊;41芴;51菲;61蒽;71荧蒽; 81芘;91苯并(a)蒽;101屈;111苯并(k)荧蒽; 121苯并(b)荧蒽;131苯并(a)芘;141茚并(123-cd); 151芘二苯并(a,h)蒽;161苯并(ghi)苝
16种多环芳烃的结构式版
SIGMA-ALDRICH 16种多环芳烃 中文名苊烯 荧蒽英文名 Naphthale ne (NAP) Acen aphthyle (ANY ) Acen aphthe ne Fluorene (FLU) Phenan thre n e (PHE ) An thrace ne (ANT) Fluora nthe n e 结构式分子式分子量CAS号价格(元) C10H8 128.17 91-20-3 148.59 元/0.25g 484.59 元/1g analytical standard (Fluka) 553.41 元 5000 卩g/L Analytical | standard (Supelco) C14H10 C16H10 178.23 178.23 202.25 208-96 8 83-32-9 86-73-7 85-01-8 120-12 7 544.05 元 5000 卩g/mL in methanol, analytical standard (Supelco) 276.12 元 200 卩g/mL in methanol, analytical standard (Supelco) 544.05 元 5000 卩g/mLin methanol,analytical standard (Supelco) 544.05 元 5000 卩g/mLin methanol,analytical standard (Supelco) 221.13 元/0.25g analytical standard (Cerilliant) 206-44 -0 544.05 元 5000 卩g/mLin methanol,analytical standard (Supelco)
多环芳烃来源和性质
多环芳烃来源和性质 自然源 主要包括燃烧(森林大火和火山喷发)和生物合成(沉积物成岩过程、生物转化过程和焦油矿坑内气体),未开采的煤、石油中也含有大量的多环芳烃 人为源 PAHs人为源来自于工业工艺过程、缺氧燃烧、垃圾焚烧和填埋、食品制作及直接的交通排放和同时伴随的轮胎磨损、路面磨损产生的沥青颗粒以及道路扬尘中,其数量随着工业生产的发展大大增加,占环境中多环芳烃总量的绝大部分;溢油事件也成为PAHs人为源的一部分。在自然界中这类化合物存在着生物降解、水解、光作用裂解等消除方式,使得环境中的PAHs含量始终有一个动态的平衡,从而保持在一个较低的浓度水平上,但是近些年来,随着人类生产活动的加剧,破坏了其在环境中的动态平衡,使环境中的PAHs大量的增加。因此,如何加快PAHs在环境中的消除速度,减少PAHs对环境的污染等问题,日益引起人们的注意。 多环芳烃大部分是无色或淡黄色的结晶,个别具深色,熔点及沸点较高,蒸气压很小,大多不溶于水,易溶于苯类芳香性溶剂中,微溶于其他有机溶剂中,辛醇-水分配系数比较高。多环芳烃大多具有大的共扼体系,因此其溶液具有一定荧光。一般说来,随多环芳烃分子量的增加,熔沸点升高,蒸气压减小。多环芳烃的颜色、荧光性和溶解性主要与多环芳烃的共扼体系和分子苯环的排列方式有关.随p电子数的增多和p电子离域性的增强,颜色加深、荧光性增强,紫外吸收光谱中的最大吸收波长也明显向长波方向移动;对直线状的多环芳烃,苯环数增多,辛醇-水分配系数增加,对苯环数相同的多环芳烃,苯环结构越“团簇”辛醇-水分配系数越大。 多环芳烃化学性质稳定.当它们发生反应时,趋向保留它们的共扼环状系,一般多通过亲电取代反应形成衍生物并代谢为最终致癌物的活泼形式。其基本单元是苯环,但化学性质与苯并不完全相似.分为以下几类 ⑴具有稠合多苯结构的化合物 如三亚苯、二苯并 [e,i]芘、四苯并 [a,c,h,j]葱等,与苯有相似的化学稳定性, 说明:电子在这些多环芳烃中的分布是和苯类似的。 图1x电子分布与苯类似的多环芳烃 ⑵呈直线排列的多环芳烃
第七章-多环芳烃
第七章 多环芳烃 1、 联苯及其衍生物 2、 稠环芳烃:萘、蒽、菲及其衍生物的结构和化学性质 1、 芳香体系与休克尔规则 基本要求: 1.熟练掌握稠环芳烃萘蒽等衍生物的命名。 2.熟练掌握萘的化学性质及萘环上亲电取代产物的定位规律。 3.掌握H ückel 规则,理解芳香性的概念,能应用H ückel 规则判断环状化合物的芳香性。 分子中含有多个苯环的烃称作多环芳烃。多环芳烃可分如下三种: 联苯和联多苯类:这类多环芳烃分子中有两个或两个以上的苯环直接以单键相联结。 稠环芳烃:这类多环芳烃分子中有两个或两个以上的苯环以共用两个碳原子的方式相互稠合。 多苯代脂肪类:这类多环芳烃可看作是脂肪烃中两个或两个以上的氢原子被苯基取代。 7.1联苯及其衍生物 联苯是两个苯环通过单键直接连接起来的二环芳烃。 其结构为: 联苯为无色晶体,熔点70℃,沸点254℃。不溶于水而溶于有机溶剂。因其沸点高和具有很好的热稳定性,所以工业上常用它作热传导介质(热载体)。 联苯的化学性质与苯相似,在两个苯环上均可发生磺化、硝化等取代反应。联苯环上碳原子的位置采用下列所示的编号来表示: 联苯可看作是苯的一个氢原子被苯基取代,而苯基是邻对位定位基,所以,当联苯发生取代反应时,取代基进入苯的对邻位和对位。但由于邻位上的空间位阻较大,主要生成对位产物。 7.2稠环芳烃 有多个苯环共用两个或多个碳原子稠合而成的芳烃称为稠环芳烃。简单的稠环芳烃如萘、蒽、菲等。稠环芳烃最重要的是萘。 7.2.1萘(naphthalene) 萘的结构:平面结构,所有的碳原子都是sp 2杂化的,是大π键体系。 分子中十个碳原子不是等同的,为了区别,对其编号如下: 12345 67 8 109αβααα β ββ1、4、5、8位又称为 位αβ2、3、6、7位又称为 位电荷密度αβ>
多环芳烃的分子结构
多环芳烃(PAHs)存在于工业和民用燃烧器、自动化排烟、烟草烟雾中,因有机燃料未完全燃烧而产生的,它还存在于矿物燃料、柴油燃料渗漏、杂酚油倾倒和供水管线的沥青、煤焦油的衬层中。 多环芳烃的结构如下: 多环芳烃是可引起癌症的有毒物质,是环境监测中的重要监测对象。 多环芳烃可用反相键合相柱进行分离,图6-4-62(a)为使用粗内径色谱柱的分离谱图。色谱柱为Vydac C18( 5μm,φ4.6mm*250mm),流动相为水 + 乙腈(体积比为40:60),流量1.5mL/min。图 6-4-62(b)为使用细内径色谱柱的分离谱图。色谱柱为Vydac C18( 5μm,φ2.1mm*250mm)&2633),流动相为水 + 乙腈(体积比为40:60),流量0.42mL/min。
在(a)、(b)两种色谱柱上的梯度洗脱程序相同,如表 6-4-15 所示。 多环芳烃的检测可使用可变波长紫外吸收二极管阵列检测器,检测的不同多环芳烃,对应的最大吸收波长,如表 6-4-16所示。 使用UV PDAD检测器,可用于对土壤、废水和空气中的多环芳烃检测。 当样品中多环芳烃浓度很低时,如饮用水,可用荧光检测器(FD)进行监测,此时对不
同的多环芳烃,应使用的激发波长λex和发射波长λem,如表6-4-17 所示。 对土壤中的PAHs可预先用超临界流体萃取技术预处理,萃取物经ODS预柱捕集,经用1:1四氢呋喃 - 乙腈溶液洗脱后,再进行高效液相色谱分析。 对具有四个苯环的多环芳烃异构作,也可用反相键合相色谱柱分离,如图6-4-63 所示。色谱柱为.C18 (5μm,φ4.6mm*250mm),流动相为乙腈水溶液,从进样开始至30min,乙腈由70%增加至100%,使用UVD(254nm)检测。 多环芳烃混合物,同样可使用μ - Porasil硅胶吸附柱(10μm,φ3.9mm*300mm),以正己烷作流动相实现分离。
多环芳烃
多环芳烃(PAHs)毒作用机制研究进展 多环芳烃(Polycyclic Aromatic Hydrocarbons ,PAHs)是煤,石油,木材,烟草,有机高分子化合物等有机物不完全燃烧时产生的挥发性碳氢化合物,是重要的环境和食品污染物。迄今已发现有几百种PAHs,其中有相当部分具有致癌性,如苯并[α]芘、苯并[α]蒽等。PAHs 广泛分布于环境中,可以在我们生活的每一个角落发现,任何有有机物加工、废弃、燃烧或使用的地方都有可能产生多环芳烃。 多环芳烃的致癌性已被人们研究了200多年,早在1775年,英国医生波特(Pott)就观察到烟囱清洁工常患阴囊皮肤癌,相信阴囊癌的高发病率与他们频繁接触烟灰(煤焦油)有关。到了二十世纪,文献大量报道了石蜡精炼、鲸油加工和煤焦油工业工人高发皮肤癌的现象。在1920s-1930s,科学家从煤焦油中分离出多种化合物。通过生物效应实验,即动物致癌性试验确定了多环芳烃中的苯并[a]芘等具有致癌作用。1950s以前,多环芳烃曾被认为最主要的致癌因素而受到广泛的注意和研究。1950s以后各种不同类型的致癌物大量发现,扩大了人们的眼界,人们认识到多环芳烃只是众多类型致癌物的一类。但是,这并没有因此降低了致癌性多环芳烃的重要性。首先,它至今仍是数量上最多的一类致癌物,在总数己达1000多种的致癌物中,多环芳烃占了三分之一以上。其次,它是分布最广的环境致癌物。近年来的大量调查研究表明,空气、土壤、水体、植物等无不受到多环芳烃的污染。其三,它也是与人类关系最密切的环境致癌物。人类日常生活的某些活动以及某些嗜好常与多环芳烃的产生有密切关系,如吸烟这个嗜好就是产生多环芳烃的重要来源,并已证实是诱发人类肺癌的重要因素;再如油脂食物的煎、烘、熏等烹调过程也产生致癌性多环芳烃,并被认为是某些地区胃癌率增高的主要原因之一。某些偏僻山区的当地居民有室内烤火的习惯,由煤和木材燃烧产生的多环芳烃就弥漫在室内,造成室内极高的多环芳烃浓度,由此造成当地居民中某些呼吸道癌症发病率的升高。多环芳烃不仅具有致癌作用,而且还具有对机体的免疫抑制反应、致畸作用和致突变作用。 由于PAHs的致癌、致畸和致突变作用,以及污染范围的广泛性,所以被各国列为优先控制的环境污染物。至目前,国内外对PAHs毒理学研究取得重大进展,现将其近年来的PAHs 毒作用机制研究进展介绍如下。 一. PAHs的免疫抑制反应研究 PAHs可以引起机体的免疫抑制反应,表现为血清免疫学指标的改变。动物试验表明,烹饪油烟冷凝物对小鼠免疫功能有明显影响,其对T淋巴细胞的影响要比B淋巴细胞更为明显。研究表明,BaP体内染毒对小鼠T淋巴细胞产IL-2(白细胞介素一2)的能力有抑制作用,并影响小鼠脾淋巴细胞的钙稳态。从而导致了机体的免疫抑制反应。工人接触PAHs后有免疫抑制现象,波兰焦炉工血清IgG和IgA明显降低(P<0.001),而血清lgM和lgE都有增高趋势。因此强调工人若长期暴露于PAHs则应定期监测免疫抑制反应水平。 二. PAHs的致癌、致突变和致畸作用 化学致癌是指化学物质引起正常细胞发生转化并发展成肿瘤的过程。化学致癌物可分为直接致癌物和间接致癌物,多环芳烃属于后者,多环芳烃是最早发现且为数最多的一类化学致癌物。 由于苯并[a]芘是第一个被发现的环境化学致癌物,而且致癌性很强,故经常以B[a]P作为PAHs的代表。动物实验已证明B[a]P能诱发皮肤癌、肺癌和胃癌。经多年研究证明,B[a]P 本身是“前致癌物”,需在体内代谢转化后方成为“终致癌物”。B[a]P进入人体后,有很少一部分以原形从尿或经胆汁随粪便排出体外,其余大部分经肝、肺细胞微粒体中的混合功能氧化酶氧化形成环氧化物,然后氧环打开,第10位上的亲电子阳离子与细胞大分子(DNA、RNA、蛋白质等)共价结合,构成癌变的物质基础。
