有机化学反应方程式大全

有机化学
一、烯烃
1、卤化氢加成
(1)
【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】
【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排
(2)
【特点】反马氏规则
【机理】自由基机理(略)
【注】过氧化物效应仅限于HBr、对HCl、HI无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】
2、硼氢化—氧化
【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】 【例】 3、X 2加成 【机理】
【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。不对称的烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃的氧化
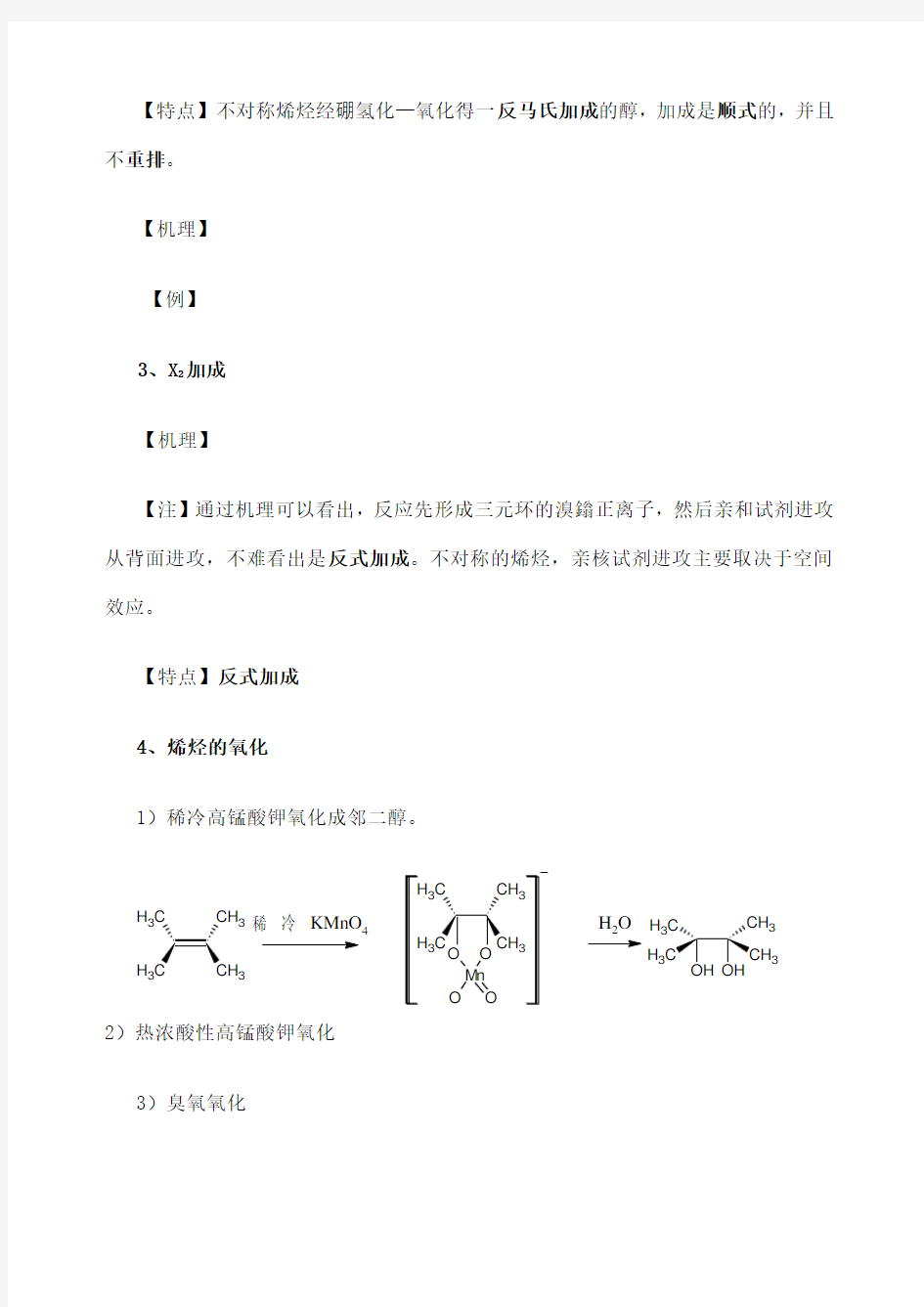
1)稀冷高锰酸钾氧化成邻二醇。
3
H 33
H
3稀冷KMnO
4
33M n O
O
H 2O 3
H 33H 3
2)热浓酸性高锰酸钾氧化
3)臭氧氧化
4)过氧酸氧化
5、烯烃的复分解反应
【例】
6、共轭二烯烃
1)卤化氢加成
2)狄尔斯-阿德尔(Diels-Alder)反应
【描述】共轭二烯烃和烯烃在加热的条件下很容易生成环状的1,4加成产物。
【例】
二、脂环烃
1、环丙烷的化学反应
【描述】三元环由于张力而不稳定,易发生加成反应开环,类似碳碳双键。
【特点】环烷烃都有抗氧化性,可用于区分不饱和化合物。
【注】遵循马氏规则
【例】
2、环烷烃制备
1)武兹(Wurtz)反应
【描述】通过碱金属脱去卤素,制备环烷烃。
【例】
2)卡宾
①卡宾的生成
A、多卤代物的α消除
B、由某些双键化合物的分解
②卡宾与烯烃的加成反应
【特点】顺式加成,构型保持
【例】
③类卡宾
【描述】类卡宾是一类在反应中能起到卡宾作用的非卡宾类化合物,最常用的ZnI。
类卡宾是ICH
2
【特点】顺式加成,构型保持
【例】
三、炔烃
1、还原成烯烃
1)、顺式加成
2)、反式加成2、亲电加成
1)、加X
2【机理】
中间体
Br
+
R2 R1
【特点】反式加成
2)、加HX
R
R
HBr R Br
(一摩尔的卤化氢主要为反式加成)
3)、加H
2
O
【机理】
【特点】炔烃水合符合马式规则。
【注】只有乙炔水合生成乙醛,其他炔烃都生成相应的酮。
3、亲核加成
1)、
2)、
3)、
4、聚合
5、端炔的鉴别
【注】干燥的炔银和炔铜受热或震动时易发生爆炸,实验完毕,应立即加浓硫酸把炔化物分解。
6、炔基负离子
【例】
三、芳烃
1、苯的亲电取代反应
1)卤代
2)硝化
3)磺化
4)傅-克(Friedel-Crafts)反应
①傅-克烷基化反应
【机理】
【注】碳正离子的重排,苯环上带有第二类定位基不能进行傅-克反应。
【例】
②傅-克酰基化反应
【例】
2、苯环上取代反应的定位效应
1)第一类定位基,邻对位定位基,常见的有:
2)第二类定位基,间位定位基,常见的有:
【注】第一类定位基除卤素外,均使苯环活化。第二类定位基使苯环钝化。卤素比较特殊,为弱钝化的第一类定位基。
3、苯的侧链卤代
【机理】自由基机理
4、苯的侧链氧化
1)用高锰酸钾氧化时,产物为酸。
【描述】苯环不易被氧化,当其烷基侧链上有α氢的时候,则该链可被高锰酸钾等强氧化剂氧化,不论烷基侧链多长。结果都是被氧化成苯甲酸。
【例】
2)用CrO 3+Ac 2O 为氧化剂时,产物为醛。 【例】
3)用MnO 2为氧化剂时,产物为醛或酮。 5、萘
【特点】萘的亲电取代反应,主要发生在α位,因为进攻α位,形成的共振杂化体较稳定,反应速度快。
【例】 四、卤代烃 1、取代反应 (1)水解 (2)醇解 (3)氰解 (4)氨解 (5)酸解 (6)与炔钠反应
(7)卤素交换反应
2、消除反应
(1)脱卤化氢
①β-消除
【注】当有多种β-H时,其消除方向遵循萨伊切夫规律,即卤原子总是优先与含氢较少的β碳上的氢一起消除。
【例】
②α-消除
(2)脱卤素
3、与活泼金属反应
(1)与金属镁反应
RX+Mg无水乙醚RM gX
(格式试剂)
(2)与金属钠反应武兹(Wurtz)反应
(3)与金属锂反应
【注】二烷基铜锂主要是与卤代烃偶联成烷烃
4、还原反应
5、氯甲基化 五、醇
1、卢卡斯(Lucas )试剂
无水氯化锌与浓盐酸的很合溶液叫卢卡斯试剂,用于鉴别伯、仲、叔醇 2、把羟基变成卤基
(1)、醇与卤化磷(PX 5、PX 3) (2)、醇与亚硫酰氯(SOCl 2) 3、醇的氧化
(1)沙瑞特(Sarret )试剂
【注】沙瑞特试剂,是CrO 3和吡啶的络合物。它可以把伯醇的氧化控制在生成醛的阶段上,产率比较高,且对分子中的双键无影响。
(2)琼斯(Jones )试剂
【注】琼斯试剂是把CrO 3溶于稀硫酸中,滴加到醇的丙酮溶液中,在室温下就可以得到很高的产率的酮。同样对分子中的双键无影响。
【例】
(3)邻二醇被高碘酸氧化
4、频哪醇重排(pinacol rearrangement)
【机理】
【注】
①羟基脱水,总是优先生成较稳定的碳正离子。
②在不同的烃基中,总是芳基优先迁移。不同的芳基,苯环上连有给电子基团的优先迁移。
③要注意立体化学,离去基团所连的碳原子(如有手性的话)构型发生转化,因为是一个协同反应,准确的机理描述是
④频哪醇重排再有机中是非常普遍的重排反应,只要在反应中形成
C+ C
H
结构的碳正离子(即带正电荷的碳原子的邻近碳上连有羟基),都可以发生频哪醇重排。
【例】
5、制醇
(1)烯烃制备
①酸性水合
【注】碳正机理,生成稳定的碳正离子,可能重排。
②羟汞化-脱汞反应
【特点】反应不发生重排,因此常用来制备较复杂的醇,特别是有体积效应的醇。
③硼氢化-氧化法
【特点】反马氏规则,所以可合成伯醇,上两种方法无法合成。
(2)格式试剂
【例】
(3)制备邻二醇
①顺式邻二醇
②反式邻二醇(环氧化合物的水解)
六、酚
1、傅-克反应
2、傅瑞斯(Fries)重排
【特点】产物很好分离,邻位的产物可随水蒸气蒸出。
3、与甲醛和丙酮反应
【注】生成中药工业原料双酚A(bisphenolA),双酚A可与光气聚合生成制备
高强度透明的高分子聚合物的防弹玻璃,它还可以作为环氧树脂胶粘剂。
4、瑞穆-悌曼(Reimer-Tiemann)反应
【本质】生成卡宾
5、酚的制法
(1)磺酸盐碱融法
工业上的:
【例】
(2)、重氮盐法
七、醚和环氧化合物
1、醚的制法
(1)威廉姆逊(Williamson)合成
(2)烷氧汞化-脱汞
【注】和羟汞化-脱汞反应一样,醇对双键的加成方向符合马氏规则。
2、克莱森(Claisen)重排
【机理】
【注】类似的构型也可发生重排
3、冠醚
【特点】冠醚性质最突出就是他有很多醚键,分子中有一定的空穴,金属例子
可以钻到空穴中与醚键络合。
O
O
O
O
O
K+
冠醚分子内圈氧可以与水形成氢键,
故有亲水性。它的外围都是CH
2
结构,又具有亲油性,因此冠醚能将水相中的试剂包在内圈带到有机相中,从而加速反应,故称冠醚为相转移催化剂。这种加速非均相有机反应称为相转移催化。
4、环氧化合物
(1)开环
①酸性开环
【注】不对称环氧化合物的酸性开环方向是亲核试剂优先与取代较多的碳原子结合。
【例】
②碱性开环
【注】碱性开环,亲核试剂总是先进攻空间位阻较小的,空间效应。
【注】环氧开环不论酸式还是碱式开环,都属于S
2类型的反应,所以亲核试
N
剂总是从离去基团(氧桥)的反位进攻中心碳原子,得到反式开环产物。这种过程犹如在烯烃加溴时,溴负离子对溴鎓离子的进攻。
【例】
(2)环氧的制备
①过氧酸氧化
②银催化氧化(工业)
③β-卤代醇
八、醛和酮
1、羰基上的亲和加成
(1)加氢氰酸
(2)与醇加成
①缩醛的生成
【机理】
【特点】缩醛具有胞二醚的结构,对碱、氧化剂稳定,所以可用此法在合成中做羰基的保护。同样的方法也可制备缩酮,机理相同。
(3)加金属有机化合物 2、与氨衍生物的反应 【例】 3、卤仿反应 【机理】
【注】如果卤素用碘的话,则得到碘仿(CHI 3)为黄色沉淀,利用这种现象可以
鉴别甲基醛、酮,还有这种结构的醇(OH
CH 3R
)。
【例】
CH OH
I 2NaOH
CH 3
O
I 2NaOH
H +
OH
O
4、羟醛缩合
(1)一般的羟醛缩合 ①碱催化下的羟醛缩合
【描述】在稀碱的作用下,两分子醛(酮)相互作用,生成α、β不饱和醛(酮)的反应。
【本质】其实是羰基的亲和加成,她的亲核试剂是一种由醛或酮自生成生的碳负离子,体现了α-H的酸性。
【注】从反应机理看出,醛要进行羟醛缩合必须有α-H,否则无法产生碳负离子亲核试剂。当有一个α-H一般停留在脱水的前一步,形成α羟基醛。其实羟醛缩合反应,只要控制温度就可以停留在羟醛产物。
【例】
②酸催化下的羟醛缩合
【机理】
【本质】在酸催化反应中,亲核试剂实际上就是醛的稀醇式。
【注】酸的作用除了促进稀醇式的生成外,还可以提供活化羰基的醛分子。此外,在酸的条件下,羟醛化合物更容易脱水生成α、β不饱和醛(酮),因为酸是脱水的催化剂。
(2)酮的缩合反应
【例】
(3)分子内缩合
【注】分子内缩合,一般是形成稳定的五、六圆环,因为五、六圆环更稳定。
(4)交叉的羟醛缩合
【描述】两种同时有α-H的醛(酮),可发生交叉羟醛缩合,产物是混合物。
【注】①一般的羟醛缩合反应,最好是一个有α-H的醛(酮),和一个没有α-H 的醛(酮)反应。
【例】
【注】②跟酸碱催化的卤代一样,当脂肪酮有两个不同的烃基的时候,碱催化缩合一般优先发生在取代较少的α碳上,酸催化缩合发生在取代较多的α碳上。但这种反应的选择性不高,常常得到混合物。
【例】
【注】③如果用体积较大的碱,如二异丙基氨基锂(LDA)作缩合催化剂,使之基本上进攻体积较小的一侧。
【例】
5、醛(酮)的氧化
(1)Tollens,吐伦试剂
【描述】氢氧化银溶液氨溶液,被称为吐伦试剂。
(2)Fehling,菲林试剂
【描述】碱性氢氧化铜溶液用酒石酸盐熔合,称为菲林试剂。
(3)拜耶尔-维立格(Baeyer-Villiger)氧化
【描述】酮被过氧酸氧化成脂。
【机理】
【注】
①不对称酮进行拜耶尔-维立格氧化时,会有两种可能,这主要看迁移基团的迁移难度,芳基>叔烃基>伯烃基>甲基。
②醛也可发生拜耶尔-维立格氧化反应,但因优先迁移基团是氢,所以主要产物是羧酸,相当于醛被过氧酸氧化。
【例】
6、醛(酮)的还原
(1)催化氢化
【注】很多基团都可以催化氢化,如碳碳双键、碳碳三键、硝基、氰基……,所以选择催化氢化还原羰基的时候,要看好化合物是否还有其他可以催化氢化的基团。
(2)用LiAlH
4、NaBH
4
还原
【特点】NaBH
4还原醛、酮的过程与LiAlH
4
类似,但它的还原能力不如LiAlH
4
的
强。也正因如此,NaBH
4具有较高的选择性,即NaBH
4
对醛、酮的还原不受脂基、羧
基、卤基、氰基、硝基等基团的干扰,而这些基团都能被LiAlH
还原。
4
(3)①麦尔外因-彭多夫(Meerwein-Ponndorf)还原
【机理】
②欧芬脑(Oppenauer)氧化
【注】麦尔外因-彭多夫还原的逆反应,就是欧芬脑氧化。
【特点】麦尔外因-彭多夫还原和欧芬脑氧化,他们都具有高度的选择性,对双键、叁键或者其他易被还原或易被氧化的官能团都不发生作用。
【例】
(4)双分子还原
【特点】双分子还原的产物是邻二醇,可以在酸的作用下发生频哪醇重排。
(5)克莱门森(Clemmensen)还原
【特点】羰基还原成亚甲基
【注】不适用α、β不饱和醛(酮),双键对其有影响。
(6)乌尔夫-基日聂耳(Wolff-Kishner)还原和黄鸣龙改进法
【特点】羰基还原成亚甲基
【注】不适用α、β不饱和醛(酮),会生成杂环化合物
(完美版)高中有机化学方程式总结
高中有机化学方程式总结 一、烃 1.甲烷 烷烃通式:C n H 2n -2 (1)氧化反应 甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O 甲烷不可使酸性高锰酸钾溶液及溴水褪色。 (2)取代反应 一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl 二氯甲烷:CH 3Cl+Cl 2 CH 2Cl 2+HCl 三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3又叫氯仿) 四氯化碳:CHCl 3+Cl 2 CCl 4+HCl 2.乙烯 乙烯的制取:CH 3CH 2OH H 2 烯烃通式:C n H 2n (1)氧化反应 乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2(2)加成反应 与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br 与氢气加成:H 2C=CH 2+H 2 CH 3CH 3 与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl 与水加成:H 2C=CH 2+H 2O CH 3CH 2OH 点燃 光 光 光 光 浓硫酸 170℃ 高温 催化剂 △ 图1 乙烯的制取
乙烯加聚,生成聚乙烯:n H 2 3.乙炔 乙炔的制取:CaC 2+2H 2O HC ≡CH ↑+Ca(OH)2 (1)氧化反应 乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。 (2)加成反应 与溴水加成:HC ≡CH+Br 2 HC=CH B r CHBr=CHBr+Br 2 CHBr 2—CHBr 2 与氢气加成:HC ≡CH+H 2 H 2C=CH 2 与氯化氢加成:HC ≡CH+HCl CH 2=CHCl (3)聚合反应 氯乙烯加聚,得到聚氯乙烯:n CH 2 n CH n 4.苯 苯的同系物通式:C n H 2n-6 (1)氧化反应 苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。 CH 2-CH 2 点燃 图2 乙炔的制取 催化剂 △ Br CH 2—CH Cl CH=CH 点燃
化学反应方程式及计算
化学反应方程式及计算 TTA standardization office【TTA 5AB- TTAK 08- TTA 2C】
4、化学方程式1、如图,四位同学正在讨论某一化学 方程式表示的意义。下列四个化学方程 式中,同时符合这四位同学所描述的是 () 2、下列化学方程式书写完全正确的是 () 3、下列关于的说法不正确的是() A、水在通电的条件下,生成氢气和氧气 B、分解了的水的质量等于生成的氢气和氧气的质量 C、每2个水分子分解生成2个氢分子和1个氧分子 D、每2g水分解生成2g氢气和1g氧气 4、高铁酸钾是一种新型、高效的多功能水处理剂,受热时发生如下反应 ,则a、R分别是() 5、如图分别表示两种元素的原子,能用该图表示的化学反应是()6.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图,下列说法中正确的是() A.该化学为化合反应 B.丙一定为该反应的催化剂 C.此反应中乙物质和丁物质的质量比为 3:2
D.丁的相对分子质量是甲的2倍 7、某反应的微观示意图如下,下列说法错误的是() A.该反应共涉及三种元素 B.该反应中反应物A、B的质量比为34:32 C.生成物都是氧化物 D.反应前后分子的种类发生了改变 8、写出下列反应的化学方程式:(1)碳在氧气中燃烧 (2)氢气燃烧(3)加热高锰酸钾制取氧气 (4)加热氯酸钾(二氧化锰作催化剂)制取氧气 (5)铁丝在氧气中燃烧(6)镁带在氧气中燃烧 (6)磷在氧气中燃烧(7)分解过氧化氢(二氧化锰作催化剂)制取氧气(8)水通电分解(9)铜在空气中加热 (10)镁条在二氧化碳中点燃 9、配平下列化学方程式: 10、如图所示密闭容器中某反应的微观示意图,分别表示不同原子。(1)反应后方框内应再填入1个微粒(选填序号). (2)该反应所属的基本反应类型是反应. (3)写出符合该微观示意图的一个具体反应的化学方程式. 11.硝酸可发生反应:4HNO34NO2↑+X+2H2O.据此回答: (1)反应的基本类型属于反应. (2)X的化学式为,推断的依据为. (3)硝酸的保存应注意、. 5、根据化学方程式进行计算 1、在A+3B=2C+2D的反应中,14克A完全反应生成44克C和18克D,若A的相对分子质量为28,则B的相对分子质量是() A、16 B、32 C、64 D、96 2、某反应的微观示意图如下,下列说法错误的是()
初中化学方程式反应类型分类总结
化学方程式反应类型分类汇总 一.化合反应 1.镁带燃烧: 2Mg + O 2 ==== 2MgO 2.铁丝燃烧及生锈:3Fe + 2O 2 ==== Fe 3O 4 ; 3.铜丝加热及生锈: 2Cu + O 2 === 2CuO ; 4.铝丝加热或形成氧化膜:4Al + 3O 2 === 2Al 2O 3 5.氢气燃烧或爆炸: 2H 2 + O 2 === 2H 2O 6.碳的燃烧:2C + O 2 ==== 2CO (不完全燃烧);C + O 2 === CO 2(完全燃烧) 7.硫的燃烧:S + O 2 === SO 2 8.磷的燃烧:4P + 5O 2 === 2P 2O 5 9.二氧化碳被碳还原:C + CO 2 === 2CO 11.生石灰溶于水:CaO + H 2O == Ca(OH)2 12.二氧化碳溶于水:CO 2 + H 2O == H 2CO 3 13.二氧化硫溶于水:SO 2 + H 2O == H 2SO 3 15.三氧化硫溶于水:SO 3 + H 2O == H 2SO 4 二.分解反应 1.碳酸氢铵(碳铵)受热分解:NH 4HCO 3 NH 3↑+ CO 2↑+ H 2O 2.碱式碳酸铜(铜绿受热分解):Cu 2(OH)2CO 3 2CuO + H 2O + CO 2↑ 3.加热高锰酸钾制氧气:2KMnO 4 K 2MnO 4 + MnO 2 + O 2↑ 4.二氧化锰催化双氧水制氧气:2H 2O 2 2H 2O + O 2↑ 5.电解水:2H 2O 2H 2↑+ O 2↑ 6.碳酸分解:H 2CO 3 == CO 2↑+ H 2O 7.碳酸钙高温煅烧分解:CaCO 3 CaO + CO 2↑ 三.置换反应 1 氢气还原金属氧化物:Fe 2O 3 + 3H 2 2Fe + 3H 2O ;Fe 3O 4 + 4H 2 3Fe + 4H 2O ; CuO + H 2 Cu + H 2O 2.碳粉还原金属氧化物:2Fe 2O 3 + 3C 4Fe + 3CO 2↑;Fe 3O 4 + 2C 3Fe + 2CO 2↑; 2CuO + C 2Cu + CO 2↑ 4.铝与盐酸、硫酸反应制氢气:2Al + 6HCl == 2AlCl 3 + 3H 2↑;2Al + 3H 2SO 4 == Al 2(SO 4)3 + 3H 2↑ △ 点 点 △ 点点点 点 点 高△ === △ === △ === MnO === 通=== 高=== 高=== 高=== 高=== 高=== 高=== 高===
基础有机化学反应总结【超级全面】
基础有机化学反应总结 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3+ CH 3 C H 3X + CH 3 C H 3 X +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH -
【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。 【机理】 CH 2 C H 33H 32 3H 32 CH CH 2C H 3 2 CH CH=CH (CH 3CH 2CH 2)3 - H 3CH 2CH 2C 22CH 3 CH 2B O CH 2CH 2CH 3 H 3CH 2CH 2C 2CH 2CH 3 + O H - O H B - OC H 2CH 2CH 3CH 2CH 2CH 3 H 3CH 2CH 2B OC H 2CH 2CH 3 CH 2CH 2CH 3H 2CH 2CH 3 HOO -B(OCH 2CH 2CH 3)3 B(OCH 2CH 2CH 3)3 + 3NaOH 3NaOH 3HOC H 2CH 2CH 33 + Na 3BO 3 2 【例】 CH 3 1)BH 32)H 2O 2/OH -CH 3 H H OH 3、X 2加成 C C Br /CCl C C Br 【机理】
大学有机化学反应方程式总结(较全)
大学有机化学反应方程式总 结(较全) -标准化文件发布号:(9556-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII
有机化学 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3+ CH 3 C H 3X + CH 3 C H 3 +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH -
【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。 【机理】 2 C H 33H 32 3H 32 CH CH 2C H 3H BH 2 CH CH=CH (CH 3CH 2CH 2)3 - H 3CH 2CH 2C 22CH 3 CH 2O CH 2CH 2CH 3 H 3CH 2CH 2C 2CH 2CH 3 + O H - O H B - OC H 2CH 2CH 3CH 2CH 2CH 3 H 3CH 2CH 2B OC H 2CH 2CH 3 CH 2CH 2CH 3H 2CH 2CH 3 HOO -B(OCH 2CH 2CH 3)3 B(OCH 2CH 2CH 3)3 + 3NaOH 3NaOH 3HOC H 2CH 2CH 33 + Na 3BO 3 2 【例】 CH 3 1)BH 32)H 2O 2/OH -CH 3H H OH 3、X 2加成 C C Br /CCl C C Br Br 【机理】
化学反应方程式计算
化学反应方程式计算 可能用到的相对原子质量:H-1 C-12 O—16 N-14 Na -23 Mg—24 Al—27 S—32 Cl –35.5 Fe—56 Cu—64 Zn—65 Ag -108 1、将氢气和氧气的混合气体共10g点燃,充分反应后生成9g水.则原混合气体中氢气和氧气的质量分别是多少? 2、加热15.5gKClO3和MnO2的混合物至氧气不再产生,剩余固体的质量为10.7g。求(1)根据质量上守恒定律,生成O2的质量是多少?二氧化锰的质量是多少? 3、将A、B、C三种物质各16g混合加热,充分反应后,混合物中有A物质12g、C物质27g和一定量的D,已知B完全反应,A、B、C、D的相对分子质量分别为16、32、4 4、18,则该反应的化学方程式。 4、在试管中放入铜和氧化铜的混合粉末10g,通入足量氢气并加热,完全反应后冷却,称得固体质量为8.4g。求原混合物粉末中氧化铜的质量。 5、有一包CuO和木炭混合而成的黑色粉末称重50g,将其放入试管内加热,让两者充分反应停止反应并冷却,称量剩余固体混合物的质量为39g,,(碳与试管内少量氧气的反应不计)。(1)反应生成二氧化碳 g(2)参加反应的氧化铜的质量是(3)混合物中氧化铜所占的百分比___________________________________________。 6、26g黄铜(Cu-Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的质量为125.8g。求:(1)黄铜中铜的质量分数;(2)反应后测得溶液中溶质质量分数。 7、为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐 滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液 的质量关系如右图所示.试计算: (1)样品中铜的质量分数;(2)反应所消耗的硫酸溶液质量;(3)反应后所得溶液的 溶质的质量分数. 8、某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物t1、、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):加热时间t1t2t3t4 剩余固体质量(g) 4.24 4.16 4.08 4.08 试计算:(1)完全反应后产生的氧气的总质量为________. (2)样品中氯酸钾的纯度是多少?.
大学有机化学反应方程式总结(较全)
有机化学 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3+ CH 3 C H 3X + CH 3 C H 3 +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH - 【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。 【机理】
2 C H3 3 H3 2 3 H3 2 CH CH2 C H3 2 CH CH=CH (CH3CH2CH2)3 - H3CH2CH2C 22 CH3 CH2 B O CH2CH2CH3 3 CH2CH2C 2 CH2CH3 +O H- O H B-OCH2CH2CH3 CH2CH2CH3 H3CH2CH2 B OCH2CH2CH3 CH2CH2CH3 2 CH2CH3 HOO- B(OCH2CH2CH3)3 B(OCH2CH2CH3)3+3NaOH3NaOH3HOCH2CH2CH33+Na3BO3 2 【例】 CH3 1)BH 3 2)H 2 O 2 /OH- CH3 H H OH 3、X2加成 C C Br 2 /CCl 4 C C Br Br 【机理】 C C C C Br Br C Br +C C Br O H2+ -H+ C C Br O H
第21讲化学反应方程式的计算
第十九讲化学反应方程式的计算 【知识要点】 一、理论依据及常见题型 化学方程式是利用质量守恒定律用化学式来表示化学反应的式子,这样,化学方程式不仅表达了物质在质的方面变化关系,即什么是反应物和什么是生成物,而且还表达物质在量的方面的变化关系,即反应物和生成物之间的质量关系,同时包括反应物和生成物之间的微粒个数关系,这是有关化学方程式计算的理论依据。 利用化学方程式的计算主要包括两种类型:用一定量的反应物最多可得到多少生成物;要制取一定量生成物最少需要多少反应物。无论哪一种类型的计算都是根据化学方程式以质量守恒定律为依据进行的。根据化学方程式的计算,就是依据反应物和生成物间的质量比进行的。已知反应物的质量可以算出生成物的质量,反之,已知生成物的质量也可以算出所需反应物的质量。化学方程式是化学计算的依据,如果化学方程式写错了或者没有配平,化学计算必然会得出错误结果。 二、根据化学方程式计算的步骤 1.设:根据题意设未知数; 2.写:书写正确的化学方程式; 3.找:写出有关物质的相对分子质量(或相对分子质量总和),找出已知量和未知量之间的质量关系; 4.列:列出比例式并求解; 5.答:检查结果,简明作答。 三、根据化学方程式计算应该注意的事项 1.解题格式要规范,运算要准确 (1)设未知量(如:设***的质量为x) (2)根据题意写出并配平化学方程式 (3)求出相关的物质的质量比;将已知量、未知量对准相关物质的化学式。 列式时,各物质的质量单位必须统一,对应关系要正确; (4)列出比例式,求解(5)简明地写出答案 严格要求化学方程式计算的书写格式,目的是培养按照化学特点进行思维的良好习惯。2.正确处理含杂质的反应物或生成物的计算 由于化学方程式反映的是纯净物间的质量比,所以一定要将含杂质的反应物或生成
高一常见化学反应方程式总结
《钠》和《钠的化合物》常用化学方程式(要求熟记) 4Na+O2====Na2O 2Na+O2====Na2O2 2Na+Cl2====2NaCl(常温下也反应) 2Na+S====Na2S(可能爆炸) 2Na+2H2O====2NaOH+H2↑ 2Na+2HCl====2NaCl+H2↑ 2NaOH+CuSO4====Na2SO4+Cu(OH)2 4Na+TiCl4====Ti+4NaCl Na2O+H2O====2NaOH Na2O+2HCl====2NaCl+H2O Na2O+CO2====Na2CO3 2Na2O2+2H2O====4NaOH+O2 2Na2O2+2CO2====2Na2CO3+O2 Ca(OH)2+CO2(少量)====CaCO3↓+H2O Ca(OH)2+2CO2(过量)====Ca(HCO3)2 CaCO3+CO2+H2O====Ca(HCO3)2 2NaOH+CO2(少量)====Na2CO3+H2O NaOH+CO2(过量)====NaHCO3 Na2CO3+H2O+CO2====2NaHCO3 Na2CO3+2HCl====H2O+CO2+2NaCl NaHCO3+HCl====H2O+CO2+NaCl Na2CO3+Ca(OH)2====2NaOH+CaCO3↓ Na2CO3+CaCl2====CaCO3↓+2NaCl NaHCO3+NaOH====Na2CO3+H2O 2NaHCO3+Ca(OH)2(少量)====Na2CO3+CaCO3↓+H2O NaHCO3+Ca(OH)2(过量)====NaOH+CaCO3↓+H2O 2NaHCO3====Na2CO3+H2O+CO2 ·1·
常见有机化学方程式归纳
常见有机化学方程式归纳 物质类别性质反应方程式 一、烷烃 1、燃烧 CH4 + 2O2CO2 + 2H2O 2、取代反应 CH4 + Cl2CH3Cl + HCl CH3Cl + Cl2CH2Cl2 + HCl(或CH4 + 2Cl2CH2Cl2 + 2HCl) CH2Cl2 + Cl2CHCl3 + HCl(或CH4 + 3Cl2CHCl3 + 3HCl) CHCl3 + Cl2CCl4 + HCl(或CH4 + 4Cl2CCl4 + 4HCl) CH3CH3 + Br2CH3CH2Br + HBr 3、高温分解CH4 C + 2H2↑ 二、烯烃 1、燃烧 C2H4 + 3O22CO2 + 2H2O 2、加成反应
3、加聚反应 4、氧化反应 三、炔烃 1、燃烧 2C2H2 + 5O24CO2 + 2H2O 2、加成反应 四、芳香烃 1、卤代 2、硝化
3、加成 4、氧化 五、醇 1、与活泼金属反应2CH3CH2OH +2 Na2CH3CH2ONa + H2↑ 2、消去反应 3、脱水成醚 4、取代反应 5、氧化
6、酯化反应 六、醛1、氧化 2C2H4O + 5O24CO2 + 4H2O
2、还原 七、酮1、加氢还原 八、羧酸 1、酸性 2CH3COOH + 2Na = 2CH3COONa + H2↑ CH3COOH + NaOH = CHCOONa + H2O 2CH3COOH + Na2CO3 = 2CH3COONa + H2O + CO2↑ CH3COOH + NaHCO3 = CH3COONa + H2O + CO2↑ 2、酯化反应参考醇的性质 九、酯1、水解 十一、卤代烃 1、水解反应 2、消去反应 十二、酚1、弱酸性
初中化学化学方程式的计算解题技巧及经典题型及练习题(含答案)
初中化学化学方程式的计算解题技巧及经典题型及练习题(含答案) 一、中考化学方程式的计算 1.Cu–Zn合金可用于工艺品的制作。某化学兴趣小组的同学为了测定某铜锌合金样品的组成,取20克样品于烧杯中,向其中分5次加入相同质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量均为20 g,剩余固体的质量记录于下表: 试回答下列问题: (1)Cu–Zn合金属于___________材料(“金属”或“有机合成”)。 (2)计算Cu–Zn合金完全反应时生成氢气的质量___________。(计算结果保留2位小数) 【答案】金属 0.28g 【解析】 【分析】 【详解】 (1)金属材料包括金属和合金,Cu-Zn合金属于金属材料。故填:金属。 (2)参加反应的锌的质量为20g-10.8g=9.2g。设完全反应时生成氢气的质量为x。 Zn+H SO=ZnSO+H 2442 652 9.2g x 652 = 9.2g x x≈0.28g。 Cu-Zn合金完全反应时生成氢气的质量为0.28g。故填:0.28g。 【点睛】 掌握根据化学方程式的计算即可正确解答本题,细致地分析题意(或图表信息)等各种信息,确定参加反应的锌的质量是正确解答本题的前提和关键。 2.(1)工业上若冶炼出含铁98%的生铁1000t,至少用含氧化铁80%的赤铁矿石的质量是_________t。 (2)取一定量该生铁样品,加入一定溶质质量分数的稀硫酸充分反应,加入稀硫酸的质量与产生氢气的质量之间的关系如图所示。
计算所用稀硫酸的溶质的质量分数______。 【答案】1750 t 9.8% 【解析】 【分析】 【详解】 解:(1)设:至少需要用含氧化铁80%的赤铁矿的质量为x 。 23 23CO +Fe O =2Fe +3CO 160 11280%x 1000t 98% ? 16011280%x 1000t 98% =? x =1750t 至少需要用含氧化铁80%的赤铁矿的质量1750t 。 (2)设:所用稀硫酸的溶质质量分数为y. 24 42Fe +H SO =FeSO +H 98 2y 0.2g ↑ 982y 0.2g = y=9.8g 所用稀硫酸的溶质质量分数为=9.8100%9.8%100g g ?=。 3.初三(112)班的小敬同学将22.5g 的大理石(杂质不参加反应,也不溶于水)放到盛有100g 稀盐酸的烧杯中,发现两者恰好完全反应。反应后烧杯内物质的总质量为118.1g , 请你帮他计算: (反应的方程式: 3222CaCO 2HCl=CaCl H O CO +++↑ ) (1)生成二氧化碳_____g 。 (2)所用100g 稀盐酸中溶质的质量分数。_____(写出计算过程) 【答案】4.4 7.3% 【解析】 【分析】 【详解】 (1)由题意二氧化碳逸出烧杯,反应前后质量的减少量即为生成的二氧化碳的质量,则生
化学反应规律及方程式小结
化学反应规律及方程式小结 一、金属+氧气=金属氧化物: (化合反应、氧化反应) 1、2Mg+O2点燃2MgO 2、3 Fe+2O2点燃 Fe3O4 3、2Cu+O2高温2CuO 二、非金属+氧气=非金属氧化物: (化合反应、氧化反应) 1、C+O2点燃CO2 2C+O2点燃2CO 2、S+O2点燃SO2 3、4P+5O2点燃2P2O5 4、2H2+O2点燃2H2O 三、其它物质在氧气中燃烧:(氧化反应) 1、2CO+O2点燃2CO2 2、CH4+2O2点燃CO2+2H2O 3、C2H5OH+3 O2点燃2CO2+3H2O 4、2CH3OH+3O2点燃2CO2+4H2O 四、金属+非金属;非金属+非金属:(化合反应) 1、2Na+Cl2=2NaCl 2、H2+Cl2=2HCl 五、碱性氧化物+水=碱 (限CaO、BaO、Na2O、K2O)(化合反应) 1、CaO+CO2=Ca(OH)2 2、BaO+CO2=Ba(OH)2 六、酸性氧化物+水=酸(化合反应) 1、CO2+H2O=H2CO3 2、SO2+H2O=H2SO3 3、SO3+H2O=H2SO4 七、碱性氧化物+酸性氧化物=含氧酸盐; (限CaO、BaO、Na2O、K2O)(化合反应) 1、CaO+H2O=CaCO3 2、BaO+H2O=BaCO3 八、碱+酸=盐+水:(复分解反应) 1、Cu(OH)2+2HCl=CuCl2+2H2O 2、Cu(OH)2+H2SO4=CuSO4+2H2O 3、Fe(OH)3+3HCl=FeCl3+3H2O 4、Mg(OH)2+H2SO4=MgSO4+2H2O 5、2NaOH+H2SO4=Na2SO4+2H2O 6、Ca(OH)2+2HCl=CaCl2+2H2O 九、酸+盐=新酸+新盐:(复分解反应) 1、HCl+AgN O3=AgCl↓+HNO3 2、BaCl2+H2SO4=BaSO4↓+2HCl
高中化学有机化学反应类型全总结
有机化学反应类型全总结一、取代反应 定义:有机物分子里的某些原子或原子团被其它原子或原子团 所代替的反应称为取代反应. 取代反应的类型很多, 中学化学中主要有下面几类: 1.卤代反应烷烃、芳香烃、苯酚等均能发生卤代反应如: 2.硝化反应苯及其同系物、苯酚、烷烃等均能发生硝化反应如:
3.磺化反应苯、苯的衍生物, 几乎均可磺化.如: (邻、对位产物为主)4. 酯化反应 (1)羧酸和醇的反应.如: (2)无机含氧酸和醇的反应.如: 5.水解反应: 卤代烃、酯、多糖、二糖、蛋白质都能在一定条件下发生水解反应.如: 6. 与活泼金属的反应: 醇、酚、羧酸等均能与活泼金属如钠反应生成氢气.如:
7.醇与卤化氢(HX)的反应.如: 8.羧酸或醇的分子间脱水. 如:? 二、加成反应 定义有机物分子里不饱和的碳原子跟其它原子或原子团直接结合,生成别的 物质的反应, 叫加成反应分子结构中含有双键或叁键的化合物, 一般能与H 2、X 2 (X为Cl、Br、I)、HX、H 2 O、HCN等小分子物质起加成反应. 如烯烃、二烯烃、炔烃、苯及其同系物、醛、酮、不饱和高级脂肪酸及其甘油脂、单糖等. 说明: 1.羧基和酯基中的碳氧双键不能发生加成反应。 2.醛、酮的羰基只能与H 2 发生加成反应。 3.共轭二烯有两种不同的加成形式。 1.和氢气加成. 2.和卤素加成
3.和卤化氢加成 4.和水加成 三、消去反应 定义:有机化合物在适当条件下, 从一个分子相邻两个碳原子上脱去一个小分子(如O、HX等)而生成不饱和(双键或叁键)化合物的反应称为消去反应, 又称消除H 2 反应 发生消去反应的化合物需具备以下两个条件: (1)是连有一OH(或一X)的碳原子有相邻的碳原子; (2)是该相邻的碳原子上还必须连有H原子. 1.醇的消去反应.如: 2.卤代烃的消去反应.如: 四、聚合反应 定义:由许多单个分子互相结合生成高分子化合物的反应叫聚合反应. 聚合反应有两个基本类型:加聚反应和缩聚反应. 1.加聚反应. 由许多单个分子互相加成, 又不缩掉其它小分子的聚合反应称为加成聚合反应简称加聚反应. 烯烃、二烯烃及含的物质均能发生加聚反应.如: 2.缩聚反应
有机化学反应方程式书写竞赛
有机反应方程式书写竞赛 一.写出下列反应的方程式(注明反应条件,配平物质系数,有机物用其结构简式表示) (一).加成反应 1. 催化剂 加压 CH +CHCHCH 2CCH 2OCCOOH CHO O O H 2 2. + Br 2(发生1,4加成) 3. +H 2 (二).取代反应 1.甲苯侧链的溴代反应 + Br 2蒸气 2.甲苯苯环的溴代反应 + 液Br 2 3.甲苯的硝化反应 4.苯酚的溴代反应 5. 6. C CH 2OH OH O 7. COOH +CH 2OH CH 3 | +3HNO 3 浓硫酸 —OH + 3Br 2 光照 CH 3FeBr 3 CH 3 —CHO CHO
(三).消去反应 1.醇的消去反应 2.卤代烃的消去反应 (1). 与氢氧化钠的醇溶液共热反应 (2). 与氢氧化钠的醇溶液共热反应 (3).与氢氧化钠的醇溶液共热反应 (四)氧化反应 1醛基的氧化反应 (1)写出下列物质与银氨溶液和新制的氢氧化铜悬浊液共热的方程式 ①.CH CHO CHO ②. ③. 2.醇的催化氧化 (五)加聚反应 1.n (六)缩聚反应 1. 浓H2SO4 n HOCH2CH2OH+n HOOC-COOH 2.n 3. —Cl 催化剂 H3C CH浓H2SO
二.写出下列物质与相关物质反应的化学方程式 1. .足量氢氧化钠溶液共热反应 2. 3. 足量氢氧化钠溶液共热反应 足量氢氧化钠溶液共热反应 4. . 足量氢氧化钠溶液共热反应 5. 足量氢氧化钠溶液共热反应 6. 丁子香酚( )与溴水反应的方程式: 7. 8. 足量氢氧化钠的乙醇溶液共热反应 9. 足量氢氧化钠的乙醇溶液共热反应 -CH ―CH ―COOH Br Br —O —C —H HOOC — O +NaHCO 3 → ——OH HO — C H 2 CH 2CH OCH 3 OH 催化剂 HO C O CH 2CH OH C O O CH 22Br |OH
有关化学反应方程式的计算
有关化学反应方程式的计算 根据化学方程式的计算,是化学计算中的一类重要计算。在初中介绍了有关化学方程式的最基本的计算,在高一介绍了物质的量应用于化学方程式的计算。本节据大纲要求又介绍了反应物中有一种过量的计算和多步反应的计算。到此,除有关燃烧热的计算外,在高中阶段根据化学方程式的计算已基本介绍完。把化学计算单独编成一节,在以前学过的关化学方程式基本计算的基础上,将计算相对集中编排,并进一步讨论有关问题,这有利于学生对有关化学方程式的计算有一个整体性和综合性的认识,也有利于复习过去已学过的知识,提高学生的解题能力。教材在编写上,注意培养学生分析问题和解决问题的.能力,训练学生的科学方法。此外,还注意联系生产实际和联系学过的化学计算知识。如在选择例题时,尽量选择生产中的实际反应事例,说明化学计算在实际生产中的作用,使学生能认识到学习化学计算的重要性。在例题的分析中,给出了思维过程,帮助学生分析问题。有些例题,从题目中已知量的给出到解题过程,都以物质的量的有关计算为基础,来介绍新的化学计算知识,使学生在学习新的计算方法的同时,复习学过的知识。本节作为有关化学反应方程式计算的一个集中讨论,重点是反应物中有一种过量的计算和多步反应的计算。难点是多步反应计算中反应物与最终产物间量关系式的确定。 教法建议有关化学方程式的计算是初中、高一计算部分的延续。因此本节的教学应在复习原有知识的基础上,根据本节两种计算的特点,帮助学生找规律,得出方法,使学生形成清晰的解题思路,规范解题步骤,以培养学生分析问题和解决问题的能力。 建议将[例题1]采用如下授课方式:(1)将学生分成两大组,一组用求生成水的质量,另一组用求生成水的质量。各组分别汇报结果(学生对两组的不同结果产生争议)(2)教师让各组分别根据水的质量计算水中氢元素和氧元素的质量。并组织学生根据质量守恒定律讨论两种计算结果是否合理。由此得出过量,不应以过量的的量进行计算。通过学生的实践,感受到利用此方法先试验再验算很麻烦。从而引出如何选择反应物的简化计算过程。并让学生注意解题步骤。
高中化学反应方程式总结参考答案
高中化学反应方程式总结 化学方程式 1.4Na+O 2= 2Na2O 2.2Na+O 2Na2O2 3.4Li+O 22Li 2O 4.2Na+2H 2O=2NaOH+H 2↑ 5.2K+2H 2O=2KOH+H 2↑ 6.2Na2 O2+2H 2O=4NaOH+O 2↑ 7.2Na2 O2+2CO 2=2Na 2CO3+O2 8. 2NaHCO 3 Na2CO3+H 2O+CO 2↑ 9.Na 2CO3+2HCl=2NaCl+H 2O+CO 2↑ 10.NaHCO 3+HCl=NaCl+H 2O+CO 2↑ 11.Na 2CO3+CaCl 2= 2NaCl+CaCO 3↓ 12.NaHCO 3+NaOH = Na2CO3+H2O 13.Na 2SO4+BaCl 2=2NaCl+BaSO 4↓ 14. 2NaCl( 熔融 )2Na+Cl 2↑ 15.2Al+2NaOH+2H 2O= 2NaAlO 2+3H 2↑ 16.2Al+6HCl =2AlCl 3+3H 2↑ 17.Al 2O3+2NaOH =2NaAlO 2+H2 O 18.Al 2O3+6HCl = 2AlCl 3+3H 2O 19.Al 2(SO4)3+6NH 3· H2O= 3(NH 4)2SO4+2Al(OH) 3↓ 20.Al 2(SO4)3+6NaOH = 2Al(OH) 3↓ +3Na2SO4 21.Al(OH) 3+NaOH=NaAlO 2+2H 2O 22.Al(OH) 3+3HCl = AlCl 3+3H 2O 23. 2Al(OH)3 Al 232 O+3H O 24. 2Al 2O3(熔融 )4Al+3O 2↑ 25.AlCl 3 + 4NaOH =NaAlO 2 + 3NaCl+2H 2O 26.AlCl 3+3NaAlO 2 +6H 2O= 4Al(OH) 3↓ +3NaCl 27. 3Fe+4H 2O(g)Fe3O4 +4H 2 28.Fe2O3+3CO2Fe+3CO2 离子方程式 ———————— ———————— ———————— +- 2Na+2H 2O=2Na +2OH +H2 ↑ 2K+2H 2O= 2K + +2OH -+H2↑ 2Na2 O2+2H 2O= 4Na++4OH -+O2↑ ———————— ———————— CO32- +2H += H2O+CO 2↑ HCO 3-+H += H2 O+CO 2↑ CO32- +Ca2+= CaCO3↓ --2- OH +HCO 3= H2O+CO 3 SO42-+Ba 2+= BaSO4↓ ———————— 2Al+2OH -+2H 2O= 2AlO 2-+3H 2↑ 2Al+6H += 2Al 3++3H 2↑ Al 2O3+2OH -=2AlO 2-+H 2O Al 2O3+6H += 2Al 3++3H 2O Al 3++3NH 3· H2O=3NH 4+ +Al(OH) 3↓ Al 3++3OH -= Al(OH) 3↓ Al(OH) 3+OH -=AlO 2-+2H 2O Al(OH) 3+3H += Al 3++3H 2O ———————— ———————— Al 3+ + 4OH - = AlO 2- + 2H 2O Al 3++3AlO 2-+6H 2O= 4Al(OH) 3↓ ———————— ————————
有机化学方程式(70个)64811
有机化学基础反应方程式汇总 1. 甲烷(烷烃通式:C n H 2n +2) 甲烷的制取:CH 3CaO △ 2CO 3+CH 4↑ (1)氧化反应 甲烷的燃烧:CH 4+2O 2点燃2+2H 2O 甲烷不可使酸性高锰酸钾溶液及溴水褪色。 (2)取代反应 CH 4+Cl 光照3Cl(一氯甲烷)+HCl CH 3Cl+Cl 光照2Cl 2(二氯甲烷)+HCl CH 2Cl 2+Cl 光照3(三氯甲烷)+HCl (CHCl 3又叫氯仿) CHCl 3+Cl 光照 4(四氯化碳)+HCl (3)分解反应 甲烷分解:CH 高温2 2. 乙烯(烯烃通式:C n H 2n ) 乙烯的制取:CH 3CH 2浓硫酸2=CH 2↑+H 2O(消去反应) (1)氧化反应 乙烯的燃烧:CH 2=CH 2+3O 点燃2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。 (2)加成反应 与溴水加成:CH 2=CH 2+Br 2Br —CH 2Br 与氢气加成:CH 2=CH 2+H 2催化剂CH 3CH 3 与氯化氢加成:CH 2=CH 2+HCl 催化剂CH 3CH 2Cl 与水加成:CH 2=CH 2+H 2O 催化剂CH 3CH 2OH (3)聚合反应 乙烯加聚,生成聚乙烯:n CH 2=CH 2 催化剂 [CH 2—CH 2 ] n 适当拓展:CH 3CH =CH 2+Cl 3? Cl CH -? Cl CH 2 CH 3CH =CH 2+H 2催化剂CH 3CH 2CH 3 CH 3CH =CH 2+HCl 催化剂CH 3CH 2CH 2Cl 或CH 3? Cl CH CH 3 图2 乙烯的制取 图1 甲烷的制取
化学化学方程式的计算练习题及答案
化学化学方程式的计算练习题及答案 一、中考化学方程式的计算 1.某造纸厂排放的废水中含有 Na 2CO 3和 NaOH 。为测定废水中 Na 2CO 3的质量分数,取 50g 废水样品于烧杯中,将 40g 稀盐酸分成 4 等份分 4 次缓慢加入到烧杯中,产生气体质 量与稀盐酸溶液的质量关系如图曲线所示。回答下列问题: 实验次数 1 2 3 4 稀盐酸的质量 (g ) 10 10 10 10 生成气体质量 (g ) (2)上述生成气体 _______ g 。 (3)计算该废水中 Na 2CO 3 的质量分数 ______ 。 (4)测定 Na 2CO 3 的质量分数,也可用下列方法:另取上述废水样品 50g ,向废水中逐滴 加入 CaCl 2 溶液,至反应完全时,经过滤、洗涤、干燥、 ________ ,即可计算出 Na 2CO 3的 质量分数。 【答案】 0 1.2 2.2 2.2 10.6% 称 量固体质量 【解析】 【分析】 【详解】 解:( 1)由图表信息可知:实验 2,产生气体质量为 0g ;实验 3 产生气体质量为 1.2g ;实 验 4,盐酸过量,则产生气体质量为 2.2g ; (2)上述生成气体的总质量为 2.2g ; (3)设:参加反应碳酸钠的质量为 x 。 Na 2CO 3 + 2HCl = 2NaCl + H 2O + CO 2 106 44 x 2.2g 106 44 x 2.2g x=5.3g 1)请仔细分析如图数据,完成下表实验记 录:
5.3g 废水中Na2CO3的质量分数= 100% 10.6% ; 50g (4)测定Na2CO3 的质量分数,也可用下列方法:另取上述废水样品50g,向废水中逐滴 加入CaCl2 溶液与碳酸钠反应产生碳酸钙沉淀,至反应完全时,经过滤、洗涤、干燥、称量 固体碳酸钙质量,根据该反应的化学方程式,即可计算出Na2CO3 的质量分数。 2.过氧化钙(CaO2)常用于活鱼运输时的增氧剂,过氧化钙与水反应方程式为: 2CaO2+2H2O═2Ca(OH)2+O2↑.某过氧化钙样品中含有少量不溶于水且不与水反应杂质,取该样品15.0g 投入盛有108.0g 水的烧杯中,缓慢搅拌,充分反应,最终收集到氧气质量为3.20g,计算该样品中过氧化钙的质量分数__________ (写出计算过程)。 【答案】96% 【解析】 【分析】 【详解】 解:设过氧化钙质量为x, 2CaO2 2H2O = 2Ca(OH) 2 O2↑ 144 32 x 3.2g 144 = 32 x 3.2g x=14.4g, 14.4g 该样品中过氧化钙的质量分数是:× 100%=96%, 15.0g 答:该样品中过氧化钙的质量分数是96%。 3.利用中和反应可以测定盐酸的浓度。将40 g 0.8%氢氧化钠溶液逐滴加入到20 g盐酸中,边滴加边搅拌。随着氢氧化钠溶液的滴加,溶液pH 变化如图所示。所用盐酸的溶质 分析】详解】
初中所有化学方程式及反应现象总结(方程式)
初中常见的化学方程式 一、化合反应(反应物可以有多个,生成物一定只有一个的为化合反应) 1、红(白)磷在空气中燃烧:4P + 5O2点燃 2P2O5 现象:(1)发出白光(2)放出热量(3)生成大量白烟。 2、铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O4 现象:(1)剧烈燃烧,火星四射(2)放出热量(3)生成一种黑色固体 注意:瓶底要放少量水或细沙,防止生成的固体物质溅落下来,炸裂瓶底。 4、硫粉在空气中燃烧:S + O2点燃 SO2现象:A、在纯的氧气中 发出明亮的蓝紫火焰,放出热量,生成一种有刺激性气味的气体。 B、在空气中燃烧 (1)发出淡蓝色火焰(2)放出热量(3)生成一种有刺激性气味的气体。 6、碳在氧气中充分燃烧:C + O2点燃 CO2 现象:(1)发出白光(2)放出热量(3)澄清石灰水变浑浊 7、氢气中空气中燃烧:2H2 + O2点燃 2H2O 现象:(1)产生淡蓝色火焰(2)放出热量(3)烧杯内壁出现水雾。 8、镁在空气中燃烧:2Mg + O2点燃 2MgO 现象:(1)发出耀眼的白光(2)放出热量(3)生成白色粉末 9、铜在空气中受热:2Cu + O2△ 2CuO现象:铜丝变黑。 10、铝在空气中燃烧:4Al + 3O2点燃 2Al2O3 现象:发出耀眼的白光,放热,有白色固体生成。 11、碳在氧气中不充分燃烧:2C + O2点燃 2CO 12、二氧化碳通过灼热碳层: C + CO2高温 2CO(是吸热的反应) 13、一氧化碳在氧气中燃烧:2CO + O2点燃 2CO2 现象:发出蓝色的火焰,放热,澄清石灰水变浑浊。 14、二氧化碳和水反应(二氧化碳通入紫色石蕊试液): CO2 + H2O === H2CO3 现象:石蕊试液由紫色变成红色。 注意:酸性氧化物+水→酸
