1-18 短周期元素性质归纳
《元素性质的周期性变化规律》元素周期律PPT课件

(2)试从原子结构角度解释同周期元素性质存在周期性变化的原 因。 提示:核外电子层数相同,随着原子序数(核电荷数)的递增,原子 核对核外电子的引力逐渐增强,原子半径逐渐减小,元素原子的 得电子能力逐渐增强,失电子能力逐渐减弱,最终导致元素的非 金属性逐渐增强,金属性逐渐减弱。
【案例示范】 【典例】(2017·全国卷Ⅱ)a、b、c、d为原子序数依 次增大的短周期主族元素,a原子核外电子总数与b原子 次外层的电子数相同;c所在周期数与族数相同;d与a同 族,下列叙述正确的是 ( )
第二节 元素周期律 第1课时 元素性质的周期性变化规律
-.
一、原子结构的周期性变化
结合图1、图2、图3完成下表:
原子 电子 最外层 序数 层数 电子数
1~2 1
3~ 10
_2_
1~2
_1_~__8_
原子半径的 变化(稀有气 体元素除外)
—
由_大__到_小__
最高或最 低化合价 的变化
+1→0
变化。 核外电子排
2.实质:元素性质的周期性变化是原子的___________ 布 ___的周期性变化的必然结果。
知识点一 元素周期表中主族元素的周期性变化规律
【重点释疑】
项目
同周期(左→右)
原 核电荷数 逐渐增大 子 电子层数 相同 结 构 原子半径 逐渐减小
同主族(上→下) 逐渐增大 逐渐增多
③Al向(OAHl)(3O+H3)H3+沉=淀==中= 加Al入3++盐3H酸2O,发生反应的离子方程式: _________________________。
3.钠、镁、铝的最高价氧化物对应水化物的碱性
NaOH 分类 强碱 碱性强弱 结论
化学元素的周期表和性质

化学元素的周期表和性质一、周期表的构成1.周期表是化学元素按照原子序数递增排列的表格,目前包含118种元素。
2.周期表分为七个周期,横排,周期数等于元素原子的最外层电子层数。
3.周期表有十六个族,竖排,族数代表元素原子的最外层电子数。
二、周期表的规律1.周期规律:电子层数相同的元素,从左至右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。
2.族规律:同一族元素,原子半径随着周期数增加而增大,金属性随着周期数增加而增强,非金属性随着周期数增加而减弱。
三、元素的性质1.原子半径:原子核外电子层数越多,原子半径越大;同一周期中,从左至右原子半径逐渐减小。
2.金属性:元素的金属性随着原子序数的增大而减弱;同一族中,金属性随着周期数的增加而增强。
3.非金属性:元素的非金属性随着原子序数的增大而增强;同一族中,非金属性随着周期数的增加而减弱。
4.最高正化合价:主族元素的最高正化合价等于其最外层电子数(O、F元素除外)。
5.最低负化合价:主族元素的最低负化合价等于其最外层电子数减8(O、F元素除外)。
6.周期表在化学反应中的应用:根据元素的位置,判断其在化学反应中的角色,如氧化剂、还原剂等。
7.周期表在材料科学中的应用:根据元素的性质,选择合适的元素制备具有特定性能的材料。
8.周期表在生物体内的应用:了解元素在生物体内的分布和作用,研究生物体生理功能与元素的关系。
五、学习周期表的建议1.熟悉周期表的基本构成,了解各个周期、族的元素分布。
2.掌握周期表的规律,能根据元素的位置判断其性质。
3.了解元素的主要性质和应用,提高对化学知识的运用能力。
4.平时多观察、多思考,将周期表与实际应用相结合,提高学习效果。
习题及方法:1.习题:元素X位于第四周期第Ⅷ族,原子序数为26,请写出元素X的名称。
方法:根据题目信息,我们可以知道元素X位于第四周期第Ⅷ族,原子序数为26。
查看周期表,第四周期第Ⅷ族的元素是铁(Fe)。
所以元素X的名称是铁。
第一章 物质结构元素周期律(知识点总结)

Z 第一章物质结构元素周期律班级姓名一、原子结构质子(Z个)原子核注意:中子(N个)质量数(A)=质子数(Z)+中子数(N) 1.原子(A X)原子序数=质子数= 核电荷数=原子的核外电子数核外电子(Z个)2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层:一(能量最低)二三四五六七对应表示符号: K L M N O P Q3.元素、核素、同位素元素:具有相同核电荷(质子)数的同一类原子的总称。
核素:具有一定数目质子和一定数目中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素(对于原子来说)二、元素周期表1.编排原则:①按原子序数递增的顺序从左到右排列;②将电子层数相同......的各元素从左到右排成一横行..③把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行..(注意:周期序数=原子的电子层数;主族序数=原子最外层电子数)2.结构特点:核外电子层数元素种类第一周期 1 2种元素短周期第二周期 2 8种元素周期第三周期 3 8种元素元(7个横行)第四周期 4 18种元素素(7个周期)长周期第五周期 5 18种元素周第六周期 6 32种元素期不完全周期:第七周期 7 未填满(已有26种元素)表主族:7个主族族副族:7个副族(18个纵行)第Ⅷ族:三个纵行(16个族)零族:稀有气体三、元素周期律1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。
元素性质的周期性变化实质是元素原子核外电..........子排布的周期性变化.........的必然结果。
2.同周期元素性质递变规律(从左到右):电子层数相同,最外层电子数依次增加,原子半径依次减小,金属性减弱,非金属性增强,与H2的化合由难到易,氢化物的稳定性由弱到强。
化学之元素周期表的性质
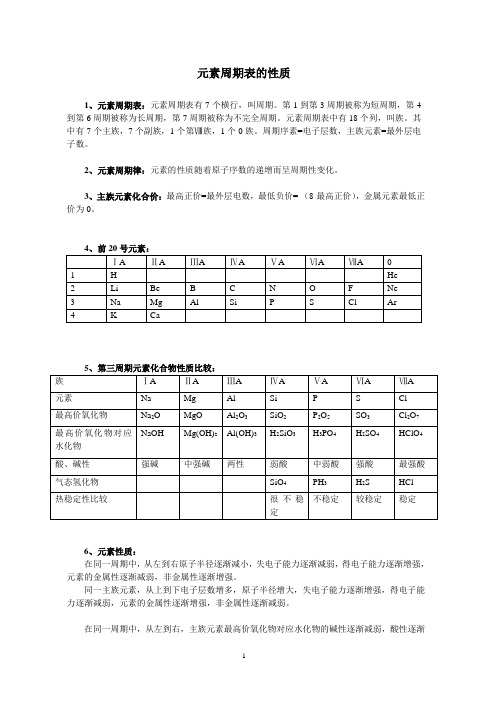
元素周期表的性质1、元素周期表:元素周期表有7个横行,叫周期。
第1到第3周期被称为短周期,第4到第6周期被称为长周期,第7周期被称为不完全周期。
元素周期表中有18个列,叫族。
其中有7个主族,7个副族,1个第Ⅷ族,1个0族。
周期序素=电子层数,主族元素=最外层电子数。
2、元素周期律:元素的性质随着原子序数的递增而呈周期性变化。
3、主族元素化合价:最高正价=最外层电数,最低负价=-(8-最高正价),金属元素最低正价为0。
4、前20号元素:ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 01 H He2 Li Be B C N O F Ne3 Na Mg Al Si P S Cl Ar4 K Ca5、第三周期元素化合物性质比较:族ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA元素Na Mg Al Si P S Cl最高价氧化物Na2O MgO Al2O3SiO2P2O5SO3Cl2O7NaOH Mg(OH)2Al(OH)3H2SiO3H3PO4H2SO4HClO4最高价氧化物对应水化物酸、碱性强碱中强碱两性弱酸中弱酸强酸最强酸气态氢化物SiO4PH3H2S HCl不稳定较稳定稳定热稳定性比较很不稳定6、元素性质:在同一周期中,从左到右原子半径逐渐减小,失电子能力逐渐减弱,得电子能力逐渐增强,元素的金属性逐渐减弱,非金属性逐渐增强。
同一主族元素,从上到下电子层数增多,原子半径增大,失电子能力逐渐增强,得电子能力逐渐减弱,元素的金属性逐渐增强,非金属性逐渐减弱。
在同一周期中,从左到右,主族元素最高价氧化物对应水化物的碱性逐渐减弱,酸性逐渐增强;它们气态氢化物的热稳定性逐渐增强。
在同一主族中,从上到下,元素最高价氧化物对应水化物的酸性逐渐减弱,碱性逐渐增强;它们的气态氢化物的热稳定性逐渐减弱。
原子半径金属性非金属性最高价氧化物对应水化物气态氢化物的稳定性酸性碱性同一横行减小减小增大减小增大增大同一列增大增大减小增大减小减小2011.11.12。
【人教版】高中化学必修第一册第四章 第二节 第1课时 元素性质的周期性变化规律

(5)最高价氧化物对应水化物碱性最强的是_________。
【解析】原子序数为11~17的元素是同周期元素,电子层数 相同,核电荷数越大,原子半径越小,非金属性越强;核电 荷数越小,金属性越强。(1)原子半径最小的是Cl。(2)金属性 最强的是Na。(3)非金属性越强的元素,其最高价氧化物对应 水化物的酸性越强,氯的非金属性最强,其对应的最高价含 氧酸是HClO4。(4)非金属性最弱的非金属元素Si的气态氢化 物最不稳定。(5)金属性最强的Na对应的NaOH的碱性最强。
(3)写出气态氢化物的分子式:__H__C_l_、__H__2S__,比较其稳
定性强弱:__H__C_l_>_H__2S___。 【解析】因A原子的L层电子数与K、M层电子数之和相 等,
所以A的核电荷数为2×8=16,A为硫元素;D原子的K、L层电子 数之和等于电子总数的一半,则D原子的核电荷数是(2+8)×2=20, 为钙元素。根据核电荷数依次增大并都能形成离子,排除氩元素, 则B为氯元素,C为钾元素。
4.(1)试从原子结构的角度分析同周期元素性质的递变规律产生 的原因。 (2)同周期元素从左到右,原子半径逐渐减小吗? (3)随着原子序数的递增,第二周期元素的最高正价是逐渐 递增的吗? (4)你能根据元素周期律,比较H3PO4、H2SO4、HClO4的
酸 性强弱以及P3-、S2-、Cl-的还原性强弱吗?
1.“三看”法比较简单粒子的半径大小
2.粒子半径大小的比较
下列粒子半径大小比较正确的是( B ) A.Na+<Mg2+<Al3+<O2- B.S2->Cl->Na+>Al3+ C.Na<Mg<Al<Si D.Cs<Rb<K<Na
高中化学元素周期律知识点总结

高中化学元素周期律知识点总结-CAL-FENGHAI.-(YICAI)-Company One1第一节课时1元素周期表的结构一、元素周期表的发展历程二、现行元素周期表的编排与结构1.原子序数(1)含义:按照元素在元素周期表中的顺序给元素编号,得到原子序数。
(2)原子序数与原子结构的关系原子序数=核电荷数=质子数=核外电子数。
2.元素周期表的编排原则(1)原子核外电子层数目相同的元素,按原子序数递增的顺序从左到右排成横行,称为周期。
(2)原子核外最外层电子数相同的元素,按电子层数递增的顺序由上而下排成纵行,称为族。
3.元素周期表的结构(1)周期(横行)①个数:元素周期表中有7个周期。
②特点:每一周期中元素的电子层数相同。
③分类(3短4长)短周期:包括第一、二、三周期(3短)。
长周期:包括第四、五、六、七周期(4长)。
(2)族(纵行)①个数:元素周期表中有18个纵行,但只有16个族。
②特点:元素周期表中主族元素的族序数等于其最外层电子数。
③分类④常见族的特别名称 第ⅠA 族(除H):碱金属元素;第ⅦA 族:卤族元素;0族:稀有气体元素;ⅣA 族:碳族元素;ⅥA 族:氧族元素。
课时2 元素的性质与原子结构一、碱金属元素——锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr) 1.原子结构(1)相似性:最外层电子数都是__1__。
(2)递变性:Li ―→Cs ,核电荷数增加,电子层数增多,原子半径增大。
2.碱金属单质的物理性质3.碱金属元素单质化学性质的相似性和递变性 (1)相似性(用R 表示碱金属元素)单质R —⎩⎪⎨⎪⎧与非金属单质反应:如Cl 2+2R===2RCl 与水反应:如2R +2H 2O===2ROH +H 2↑与酸溶液反应:如2R +2H +===2R ++H 2↑化合物:最高价氧化物对应水化物的化学式为ROH ,且均呈碱性。
(2)递变性具体表现如下(按从Li→Cs 的顺序)①与O 2的反应越来越剧烈,产物越来越复杂,如Li 与O 2反应只能生成Li 2O ,Na 与O 2反应还可以生成Na 2O 2,而K 与O 2反应能够生成KO 2等。
元素周期律及其应用2022年高考化学一轮复习过考点(解析版)

考点26 元素周期律及其应用一、1~18号元素性质的周期性变化规律 1.原子最外层电子排布变化规律周期序号 原子序数 电子层数最外层电子数结论第一周期 1→2 1 1→2 同周期由左向右元素的原子最外层电子数逐渐增加(1→8)第二周期 3→10 2 1→8 第三周期11→1831→8规律:随着原子序数的递增,元素原子的核外电子排布呈现周期性变化2.周期序号 原子序数 原子半径(nm)结论第一周期 1→2 ……同周期由左向右元素的原子半径逐渐减小(不包括稀有气体)第二周期 3→9 0.152→0.071大→小 第三周期11→170.186→0.099大→小规律:随着原子序数的递增,元素的原子半径呈现周期性变化3周期序号 原子序数 主要化合价 结论第一周期1→2+1→0 ①同周期由左向右元素的最高正价逐渐升高(+1→+7,O 和F 无最高正价); ②元素的最低负价由ⅣA 族的-4价逐渐升高至ⅦA 族的-1价; ③最高正价+|最低负价|=8第二周期3→9最高价+1→+5(不含O 、F) 最低价-4→-1规律:随着原子序数的递增,元素的主要化合价呈现周期性变化以第三周期元素为例探究元素性质的递变规律。
1.第三周期元素电子层数相同,由左向右元素的原子最外层电子数逐渐增加,原子半径依次减小,失电子的能力依次减弱,得电子的能力依次增强,预测它们的金属性依次减弱,非金属性依次增强。
2.钠、镁、铝元素金属性的递变规律 (1)钠、镁元素金属性强弱的实验探究 ①原理:金属与水反应置换出H 2的难易。
②实验操作:③现象:加热前,镁条表面附着了少量无色气泡,加热至沸腾后,有较多的无色气泡冒出,滴加酚酞溶液变为粉红色。
④结论:镁与冷水几乎不反应,能与热水反应,反应的化学方程式为Mg +2H 2O=====△Mg(OH)2+H 2↑。
结合前面所学钠与水的反应,可得出金属性:Na>Mg 。
(2)镁、铝元素金属性强弱的实验探究AlMg原理最高价氧化物对应水化物的碱性强弱实验操作沉淀溶解情况 沉淀逐渐溶解 沉淀逐渐溶解 沉淀溶解 沉淀不溶解相关反应的化学方程式 Al(OH)3+3HCl ===AlCl 3+3H 2OAl(OH)3+NaOH ===NaAlO 2+2H 2OMg(OH)2+2HCl ===MgCl 2+ 2H 2O实验结论金属性:Mg>Al(3)钠、镁、铝的最高价氧化物对应水化物的碱性NaOH Mg(OH)2 Al(OH)3 分类 强碱中强碱(属于弱碱)两性氢氧化物碱性强弱 NaOH>Mg(OH)2>Al(OH)3 结论金属性:Na>Mg>Al3.Si PSCl最高价氧化物对应水化物的酸性H 2SiO 3:弱酸H 3PO 4:中强酸H 2SO 4:强酸 HClO 4:强酸酸性:HClO 4>H 2SO 4>H 3PO 4>H 2SiO 3 结论Si 、P 、S 、Cl 的非金属性逐渐增强4.同一周期从左到右,元素金属性逐渐减弱,非金属性逐渐增强。
化学1—18号元素的结构性质特点

化学1—18号元素的结构性质特点在化学中,元素是组成所有化学物质的基本单位。
化学元素的结构性质特点描述了每个元素的内部结构以及与其他元素之间的化学性质。
下面将详细介绍化学周期表中1-18号元素的结构性质特点。
1.氢(H):-结构:氢元素的原子结构只有一个质子和一个电子。
它是周期表中最简单的元素。
-特性:氢是最轻的元素,常见于宇宙中,存在于水和有机化合物中。
它的化学性质特别活泼,可以和大多数元素组成化合物。
2.铯(Cs):-结构:铯是一种碱金属元素。
-特性:铯是一种质软、黄金属,易被氧化。
它的熔点很低,非常活泼,在空气中会迅速与氧气反应。
铯由于其低熔点和容易蒸发的性质,在高真空技术中有很多应用。
3.锂(Li):-结构:锂也是一种碱金属元素。
-特性:锂是一种轻金属,具有低密度和高电导率。
它可以形成锂离子的化合物,在锂离子电池中广泛应用。
锂具有很强的同时硫酸和碱浸的性质,可与水剧烈反应。
4.钠(Na):-结构:钠也是一种碱金属元素。
-特性:钠是一种质软的金属,在自然界中以化合物形式存在,如食盐。
钠是一种高度活泼的金属,与水和氧气反应非常迅速。
它在化学工业中被广泛应用。
5.钾(K):-结构:钾也是一种碱金属元素。
-特性:钾是一种质软的金属,具有低密度和高电导率。
它的反应活性非常高,与水和氧气反应迅速,可以与许多非金属和金属形成化合物。
6.铜(Cu):-结构:铜是一种过渡金属元素。
-特性:铜是一种质软的金属,具有良好的导电性和导热性。
它的弹性和可塑性很好,可以被拉伸成细丝和扯成薄片。
铜广泛应用于制造业,特别是电气设备和导线。
7.银(Ag):-结构:银也是一种过渡金属元素。
-特性:银是一种良好的导电体,并且对热和光具有很高的反射率。
因此,它广泛应用于电子器件、镀银和摄影等领域。
8.金(Au):-结构:金是一种过渡金属元素。
-特性:金是一种贵金属,具有良好的延展性和电导性。
它不会氧化或腐蚀,因此可以用于制造珠宝和硬币。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1-18 短周期元素性质归纳
短周期元素性质详细归纳
湖南省郴州市湘南中学:田万福 1号元素 H
1、最外层电子数=电子层数主族序数=周期序数(Be,Al)
2、原子半径最小,最轻的气体单质
3、单质常做还原剂
N+3H? 2NH(工业合成氨,放热反应) 322
H+F=2HF(黑暗处就能反应) 22
H+Cl=2HCl(光照爆炸,点燃苍白色火焰) 22
CuO+H=Cu+HO(吸热反应) 22
4、制备实验室:Zn+HSO= ZnSO+H 24 42
工业制法:C(s)+HO(g)= CO + H 22
5、同位素:质子数相同而中子数不同的核素 H D T (氕氘氚) 2号元素 He
单质无化学键(稀有气体都无化学键,单原子分子)
3号元素 Li
1、最外层电子数是内层电子数的一半(P) 最外层电子数是最内层电子数的一半(Na)
2、密度最小的金属,保存在石蜡油中,防止氧化
3、与水反应生成碱和氢气,与O不能生成过氧化物 2
4号元素 Be
1、最外层电子数,次外层电子数;最外层电子数,电子层数;
2、氧化物为BeO;价态+,价;两性元素,其氧化物和氢氧化物为两性 5号元素 B
最外层电子数比次外层多一个;氢化物BH;硼酸(HBO)可用于洗涤不小心溅在皮肤上的碱液 26336号元素 C
1、最外层电子数是内层电子数的2倍最外层电子数是最内层电子数的2倍(Si)
2、形成化合物种类最多(有机物)
3、同素异形体:石墨,金刚石,C (氧气与臭氧,红磷与白磷,正交硫和单斜硫) 60
4、氧化物 AB AB型 2
CO:有毒,可燃(淡蓝色火焰,S、H、CH、CHOH),还原性气体 2425
CO:电子式温室效应,固态称为干冰,用于人工降雨(还有AgI) 2
检验方法:使澄清石灰水变浑浊(注意与SO区别鉴定) 2
5、氢化物: 10电子体,正四面体结构
6、连续氧化:C C(CH)——CO——CO——HCO 4223
7、NaCO与NaHCO鉴别 233
当两者为固体时,加热的方法方程式
当两者为溶液时,用CaCl溶液(为什么不能用Ca(OH)溶液) 227号元素 N
1、空气中含量最多的元素,N是活泼的非金属,但N性质稳定,做保护气2
2、氧化物 AB AB型为主(还有NO,NO,NO,NO,NO)污染空气,形成光化学烟雾,酸雨 2223225NO:无色有毒气体,中毒原理与CO一样,遇氧气马上变为红棕色NO:红棕色气体(红棕色固体FeO,红棕色液体Br) 2232
2 NO(g)? NO (g) 放热反应 2 24
3、氢化物 10电子体,三角锥形,分子中有氢键,氮族中氢化物沸点最高,水溶液惟一
呈碱性
检验方法:使湿润的红色石蕊试纸变蓝色;遇HCl(g)产生大量白烟 4、连续氧化制HNO N(NH)NO——NO——HNO 3 23——23
93,HNO因溶入NO而呈黄至棕黄色,开盖则逸出棕色浓雾,叫发烟硝酸。
应密闭保存于棕色玻32
璃塞瓶中,不可用无色试剂瓶和橡皮塞,以防见光分解,挥发和腐蚀橡皮。
8号元素 O
1、最外层电子数是内层电子数的3倍,也是电子层数的3倍
2、地壳含量最多的元素(O,Si,Al,Fe);有同素异形现象
3、 2种氢化物都为液体,AB、AB 型 2
HO 电子式: 10电子体,分子晶体,有氢键,氧族中沸点最高的氢化物 2 HO 电子式: 18电子体,强氧化性,消毒杀菌 22
4、制备实验室制法:2HO=2HO+O 2KClO=2KCl+3O 222232 9号元素 F
1、非金属性最强,单质有颜色(淡黄绿色)与水反应剧烈生成O,HF是最稳定的氢化物 2
2、 HF弱酸,其水溶液用于雕刻玻璃,方程式 4HF+SiO=SiF+2HO 24210号元素 Ne
11号元素 Na
1、最外层电子数是最内层电子数的一半
2、银白色光泽,易被氧化变暗,保存在煤油中,钠钾合金是原子反应堆的导热材料,常温小呈液态
3、氧化物有两种,AB AB 222
NaO的电子式: 淡黄色固体(还有S,AgBr),强氧化剂,常做供氧来源 22 NaO的电子式: 白色固体,碱性氧化物,固体溶于水放热 2
NaO+ H2O = NaO+ CO= 22 22 24、焰色反应,钠元素黄色(钾元素紫色,观察方法)
5、与水剧烈反应,浮、游、响、熔、红 Na+HO= 2
6、连续氧化 Na——NaO——NaO——NaOH 222
12号元素 Mg
1、最外层电子数-最内层电子数,次外层电子数是最外层电子数的4倍
2、单质在N,O,CO,Cl中燃烧,Mg遇冷水难反应,遇热水能放H 22222
3、 Mg(OH)为难溶性中强碱;MgN遇水产生白色沉淀和气体,MgCl溶液又称苦卤;MgSO为泻盐。
23224
13号元素 Al
1、最外层电子数=电子层数,主族序数=周期数
2、地壳中含量最多的金属。
单质,氧化物,氢氧化物都能与强酸、强碱反应。
3、铝离子水解应用:明矾净水,Al(SO)与NaHCO为泡沫灭火器的药剂(完全双水解) 2433
4、单质遇冷的浓硝酸和浓硫酸,有钝化现象
14号元素 Si
1、最外层电子数是最内层电子数的2倍,最外层电子数是次外层的一半
2、单质是人工制得纯度最高的元素,常做半导体材料
3、 SiO,天然二氧化硅称为硅石,石英晶体是结晶的二氧化硅。
酸性氧化物,不溶于水,光导纤维的2
重要原料,对应HSiO也不溶于水,是惟一难溶酸。
23
4、硅酸盐的氧化物书写形式:活泼金属氧化物?较活泼金属氧化物?二氧化硅?
水 5、硅酸盐工业,传统的无机非金属材料,水泥、玻璃、陶瓷制玻璃的方程式15号元素 P
1、最外层电子数是内层电子数的一半,水中的富营养元素
2、有同素异形现象,红磷与白磷P4(一分子白磷有6根共价健,易自燃)
3、PO具有很强的吸水性,常用作干燥剂,酸性干燥剂 25
16号元素 S
1、最外层电子数是电子层数的2倍,是最内层电子数的3倍
单质为黄色晶体,俗称硫磺(硫黄)易溶于CS,S可用于除去液态金属Hg,与变价金属生成低价2
硫化物。
与碱共热发生歧化反应:
2、同一主族元素形成两种化合物
SO:含氧量50%,使品红褪色,表现漂白性,与有色物质生成不稳定的无色物质。
使溴水褪色,2
表现还原性。
2SO+O ? 2SO 放热反应 223
SO:含氧量60%,标准状况下固体。
3
4、HS 电子式: 18电子体,臭鸡蛋味气体,有毒,燃烧火焰呈蓝色,HS水溶
液称为氢硫223+2+酸。
与FeCl反应则Fe被还原为Fe:2FeCl+HS,2FeCl+S?+2HCl 33225、连续氧化:S(HS)——SO——SO——HSO 223246、浓硫酸特性,吸水性,脱
水性,强氧化性
2-SO的检验:加盐酸,无现象,再滴加BaCl,有白色沉淀生成 4217号元素 Cl
1、单质为黄绿色气体,有毒,最易液化的气体液氯:液态的氯气,纯净物,储存在钢瓶中氯水:氯气溶于水的溶液,溶质为氯气,有漂白性。
氯气的检验:使湿润的淀粉KI试纸变蓝
2、HCl 电子式: 18电子体,水溶液称为盐酸
3、HClO,最强的酸,HClO弱酸,强氧化性,漂白性 4
4、工业制备:电解饱和食盐水可制Cl, 2
实验室制备:MnO+HCl(浓)= 2
除去氯气中混有的少量氯化氢可用饱和食盐水洗气,若氯化氢中混有少量氯气则可用活性炭除去氯气
18号元素 Ar
思考归纳1-18号元素:
1、单质是气体的有
2、各元素形成化合物是气体的有
3、属于10电子体的原子,分子,单核离子,原子团有那些:属于18电子体的原子,分子,单核离子,
原子团有那些,具有强氧化性的有那些。
