苯巴比妥质量标准
美国CLIA'88能力比对检验的分析质量要求

美国CLIA'88(能力比对检验的分析质量要求)───────────────────────────────────────────────────────────────────分析物或试验可接受范围───────────────────────────────────────────────────────────────────常规临床化学谷丙转氨酶靶值±20%白蛋白靶值±10%碱性磷酸酶靶值±30%淀粉酶靶值±30%谷草转氨酶靶值±20%胆红素靶值±6.84mmol/L(0.4mg/dL)或±20%(取大者)血气PO2 靶值±3s血气PCO2 靶值±5mmHg 或±8%(取大者)血气PH 靶值±0.04钙,总靶值±0.250mmol/L(1.0mg/dL)氯靶值±5%胆固醇靶值±10%高密度脂蛋白胆固醇靶值±30%肌酸激酶靶值±30%肌酸激酶同功酶MB升高(存在或不存在)或靶值±3s肌酐靶值±0.265umol/L(0.3mg/dL)或±15%(取大者)葡萄糖靶值±0.33mmol/L(6mg/dL) 或±10%(取大者)铁靶值±20%乳酸脱氢酶靶值±20%LD同功酶LD1/LD2(+或-)或靶值±30%镁靶值±25%钾靶值±0.5mmol/L钠靶值±4mmol/L总蛋白靶值±10%甘油三酯靶值±25%尿素氮靶值±0.71mmol/L尿素(2mg/dL尿素N)或±9%(取大者)尿酸靶值±17%内分泌皮质醇靶值±25%游离的甲状腺素靶值±3s人绒毛膜促性腺激素(HCG) 靶值±3s或(阳性或阴性)T3 uptake 靶值±3s(方法)三碘甲状腺素原氨酸靶值±3s促甲状腺激素靶值±3s甲状腺素靶值±20%或12.9%(1.0ug/dL)(取大者)毒理学酒精,血靶值±25%血铅靶值±10%或±0.019ummol/L(4ug/dL)(取大者) 酰氨咪嗪(carbamazepine) 靶值±25%地高辛(digoxin) 靶值±20%或0.2ug/L(更大)乙琥胺(ethosuximide) 靶值±20%庆大霉素靶值±25%锂靶值±0.3mmol/L或±20%(更大)苯巴比妥(phenobarbital) 靶值±20%苯妥英(phenytoin) 靶值±25%扑痫酮(primidone) 靶值±25%普鲁卡因酰氨(procainamid)(及代谢物) 靶值±25%奎尼丁(quinidine) 靶值±25%茶碱(theophylline) 靶值±25%妥布霉素(tobramycin) 靶值±25%丙戊酸靶值±25%血液学细胞识别在分类上90%或更大的一致白细胞分类靶值±在不同类型白细胞百分数上的3s 红细胞计数靶值±6%血细胞容积靶值±6%血红蛋白靶值±7%白细胞计数靶值±15%血小板计数靶值±25%纤维蛋白原靶值±20%激活部分凝血酶时间靶值±15%凝血酶原时间靶值±15%一般免疫学a1-抗胰蛋白酶靶值±3s抗核抗体靶值±2个稀释或(阳或阴)抗-HIV 反应或不反应补体3 靶值±3s补体4 靶值±3sa-甲胎蛋白靶值±3s肝炎(HBsAg,anti-HBc,HBeAg) 反应(阳性)或不反应(阴性)IgA 靶值±3sIgE 靶值±3sIgG 靶值±25%IgM 靶值±3s传染性单核细胞增多(症) 靶值±2个稀释或(阳性或阴性)类风湿因子靶值±2个稀释或(阳性或阴性)风疹(Rubella) 靶值±2个稀释或(阳性或阴性)附录2常用质控规则及含义:质控规则是解释质控数据和判断分析批控制状态的标准。
苯巴比妥质量标准
文件名称苯巴比妥质量标准共 3 页第 1 页文件编号TS-02-006 编制部门质量部状态正式版本号00 备份起草人起草日期年月日号审核人审核日期年月日生效日期批准人批准日期年月日年月日分发部门质量部、生产技术部、质保处、质检处、生产车间、物流部目的建立苯巴比妥质量标准,作为采购、QC分析、车间使用的标准依据,确保生产中使用合格的茶碱。
范围本标准适用于茶碱的质量管理。
责任本标准由质量部起草;物流部负责按照本标准采购,QC处负责按本标准检验,QA负责监督;生产车间负责按照本标准使用。
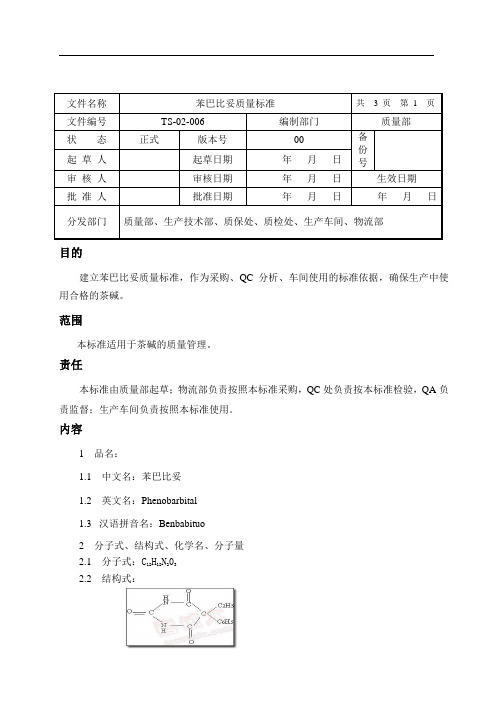
内容1品名:1.1 中文名:苯巴比妥1.2 英文名:Phenobarbital1.3汉语拼音名:Benbabituo2 分子式、结构式、化学名、分子量2.1 分子式:C12H12N2032.2 结构式:2.3 化学名:5-乙基-5-苯基-2,4,6(1H,3H,5H)-吡啶三酮;2.4 分子量:232.24。
3 理化性质3.1 本品为白色有光泽的结晶性粉末,无臭,味微苦,饱和水溶液显酸性反应。
3.2本品在乙醇或乙醚中溶解,在三氯甲烷中略溶,在水中极微溶解,在氢氧化钠或碳酸钠溶液中溶解。
3.3 熔点:本品的熔点(附录Ⅵ C)为174.5-178℃。
4 产品规格和包装形式25kg/桶,双层聚乙烯薄膜袋包装(其中直接接触茶碱的为药用聚乙烯薄膜袋),放于纸板桶中。
5 内部使用代码:1006。
6 经批准的供应商:辽宁省医药物资有限公司。
7 标准依据:中国药典2010年版(ChP2010)。
8 取样、检验方法或相关操作规程编号见《苯巴比妥检验标准操作规程》SOP-08-306和《原辅料取样规程》SOP-08-048。
9 定性和定量的限度要求9.1 鉴别:9.1.1 取本品约10mg,加硫酸2滴与亚硝酸钠约5mg,混合,即显橙黄色,随即转橙红色。
9.1.2 取本品约50mg,置试管中,加甲醛试液1ml,加热煮沸,冷却,沿管壁缓缓加硫酸0.5ml,使成两液层,置水浴中加热,接界面显玫瑰红色。
药物分析

一.填空3.目前公认的全面控制药品质量的法规有GLP 、GMP 、GSP,GCP 。
4.“精密称定”系指称取重量应准确至所取重量的千分之一;“称定”系指称取重量应准确至所取重量的百分之一;取用量为“约”若干时,系指取用量不得超过规定量的±10%2.古蔡氏检砷法的原理为金属锌与酸作用产生_新生态氢气_,与药物中微量砷盐反应生成具挥发性的__砷化氢_,遇溴化汞试纸,产生黄色至棕色的砷斑_,与一定量标准砷溶液所产生的砷斑比较,判断药物中砷盐的含量。
1.巴比妥类药物的母核为巴比妥酸,为环状的丙二酰脲结构。
巴比妥类药物常为白色结晶或结晶性粉末,环状结构与碱液共热时,可发生水解开环。
巴比妥类药物本身微溶或极微溶溶于水易溶于乙醇等有机溶剂,其钠盐易溶于水而难溶于有机溶剂。
2.巴比妥类药物的环状结构中含有1,3-二酰亚胺基团,易发生酮式-烯醇式互变异构,在水溶液中发生二级电离,因此本类药物的水溶液显弱酸性。
3.硫喷妥钠在氢氧化钠溶液中与铅离子反应,生成白色沉淀,加热后,沉淀转变成为黑色PbS 。
4.苯巴比妥的酸度检查主要是控制副产物苯基丙二酰脲。
酸度检查主要是控制酸性杂质的量。
5.巴比妥类药物的含量测定主要有:溴量法、紫外分光光度法、非水溶液滴定、HPLC 法四种方法。
1.芳酸类药物的酸性强度与羧基是否与苯环直接相连有关。
芳酸分子中苯环上如具有—OH 、—OOC—_、—NH2—、—OCH3—等电负性大的取代基,由于共轭效应能使苯环电子云密度降低,进而引起羧基中羟基氧原子上的电子云密度降低和使氧-氢键极性增加,使质子较易解离,故酸性增强。
2.具有酚羟基的芳酸类药物在中性或弱酸性条件下,与FeCL3 试液反应,生成紫色配位化合物。
反应适宜的pH为4~6 ,在强酸性溶液中配位化合物分解。
3.阿司匹林的特殊杂质检查主要包括溶液的澄清度以及水杨酸、易炭化物检查。
4.对氨基水杨酸钠在潮湿的空气中,露置日光或遇热受潮时,也可生成间氨基酚,再被氧化成二苯醌型化合物,色渐变深,其氨基容易被羟基取代而生成3,5,3',5'-四羟基联苯醌,呈明显的红棕色。
甲苯磺酸艾多沙班进口标准

甲苯磺酸艾多沙班进口标准甲苯磺酸艾多沙班(苯巴比妥)是一种重要的中枢神经系统抑制药,常用于治疗癫痫、焦虑和睡眠障碍等疾病。
进口的药品必须符合国家的标准和要求,以确保药品的质量和安全性。
在本文中,我们将深入探讨甲苯磺酸艾多沙班的进口标准,包括其相关的内容、要求和意义。
一、甲苯磺酸艾多沙班的进口标准概述1.进口标准的定义进口标准是指作为进口商品合法性、安全性和质量的评价依据,是国家对进口商品质量的要求和规定。
对于药品来说,进口标准是保障患者用药安全的重要保障。
2.甲苯磺酸艾多沙班的进口标准意义甲苯磺酸艾多沙班作为一种用于治疗严重疾病的药物,其进口标准的意义不言而喻。
严格的进口标准可以保证药品的质量、疗效和安全性,有效地保障患者的用药需求。
3.甲苯磺酸艾多沙班的进口标准内容和要求甲苯磺酸艾多沙班的进口标准内容和要求涉及药品的生产、贮存、运输、质量控制等方方面面,其中包括原料药的质量标准、成品药的质量标准、包装标准、标签标识要求等。
二、甲苯磺酸艾多沙班进口标准的评估1.甲苯磺酸艾多沙班进口标准的深度评估对于甲苯磺酸艾多沙班的进口标准,需要进行深度评估,包括对进口标准的内涵和要求进行详细了解和分析。
还需要了解国际上相关的进口标准,以及不同国家对于这一药品的标准差异,这样才能更全面地评估进口标准的深度。
2.甲苯磺酸艾多沙班进口标准的广度评估除了深度评估,还需要对甲苯磺酸艾多沙班的进口标准进行广度评估,这包括了解不同国家和地区对于这一药品的进口标准要求情况,以及了解国际上对于这一领域的最新发展和要求,从而更好地把握进口标准的整体情况。
三、甲苯磺酸艾多沙班进口标准的撰写1.甲苯磺酸艾多沙班进口标准的关键内容在撰写甲苯磺酸艾多沙班进口标准的文章中,需要重点提及其关键内容,包括对原料药的质量标准、成品药的质量标准、包装标准、标签标识要求等方面进行详细的阐述和分析。
2.甲苯磺酸艾多沙班进口标准的总结和回顾在文章的总结和回顾部分,需要对甲苯磺酸艾多沙班进口标准的要点进行回顾,强调其重要性和必要性,同时也可以对未来的发展和趋势进行展望,为读者提供更加全面、深刻和灵活的理解。
药品质量标准制定原则及内容是怎样的呢

药品质量标准制定原则及内容是怎样的呢除了⾷品安全,⼤家最关注的就是药品质量安全了,那么,⼤家知道药品质量标准是怎样的吗?制定这个标准的原则是什么呢?请⼤家阅读下⾯的⽂章了解!药品质量标准总原则(1)必须坚持质量第⼀,充分体现“安全有效,技术先进,经济合理”的原则,并要尽可能采⽤先进标淮,使标准能起到推动提⾼质量、保证择优发展和促进对外贸易的作⽤。
(2)要从⽣产、流通、使⽤的各个环⾏去考察影响药品质量的因素,有针对性地规定检测项⽬,切实加强对药品内在质量的控制。
(3)检验⽅法的选择,应根据“准确、灵敏、简便、快速”的原则,要强调⽅法的适⽤性,并注意吸收国内科研成果和国外先进经验;既要考虑当前国内实际条件,⼜要反应新技术的应⽤利发展,进⼀步完善和提⾼检测⽔平。
对于某些抗⽣素、⽣化药品和必须采⽤⽣物测定的品种,在不断改进⽣物测定法的同时,也可采⽤化学和仪器分析的⽅法控制其纯度。
(4)标准中的限度的规定,应密切结合实际要保证药品在⽣产、贮存、销售和使⽤过程中的质量,并可能全⾯符合规定:在制定药品质量标准过程中,对⼀些细节有⼀些具体的规定。
标准名称制定药品质量标准时,⾸先应给⼀个药品以法定的名称,根据卫⽣部颁布的《新药审批办法》规定:“新药的名称应明确、科学、简短,不得使⽤代号及容易混同或夸⼤疗效的名称”。
国际上,世界卫⽣组织制定公布了国际⾮专有药品名,审定出版了单⼀药物通-⽤名《国际⾮专利药名》供国际间统⼀使⽤。
WHO的专家委员会对药品命名提出了两个主要原则:(1)药品名称读⾳应清晰易辨,全词不宜过长,且应避免与⽬前已经使⽤的药名相似;(2)属于同⼀药效类别的药物,其名称应⼒求⽤适当的⽅法使之显⽰这⼀关系:凡是易令病⼈从解剖学、⽣理学、病理学和治疗学⾓度猜测药效的名称,⼀般不应采⽤。
我国药典委员会和《新药审批办法》对药品命名的原则规定是:(1)药品的名称包括中⽂名、汉语拼⾳名、英⽂名⼆种。
(2)药品的名称应明确、简短、科学,不⽤代号、政治性名词、容易混同或夸⼤疗效的名称。
药学专业知识一第十章 药品质量与药品标准

第十章药品质量与药品标准1、色谱法用于定量的参数是A:峰面积B:保留时间C:保留体积D:峰宽E:死时间【答案】A【解析】本题考查对色谱法基本概念、术语的掌握程度。
一个组分的色谱峰通常用三项参数来说明:(1)峰高或峰面积,用于定量;(2)峰位(用保留值表示),用于定性;(3)色谱峰区域宽度,用于衡量柱效。
常用的保留值有:保留时间(tR)、死时间(t0)、调整保留时间(t′R)、相对保留值(r,又称选择性因子)。
通常用三个参数表示色谱峰的区域宽度:标准差(σ)、半高峰宽(Wh/2)、峰宽(W)。
该部分内容除以最佳选择题出现外,还以多项选择题和配伍选择题出现。
建议考生熟悉色谱法基本概念、术语。
本题答案应选A。
2、百分吸收系数的表示符号是A:B:C:AD:TE:λ【答案】A【解析】本题考查对光谱分析法中基本符号的熟悉程度。
为百分吸收系数,是当浓度以“g/100ml”为单位时的吸收系数;为比旋光度;A为吸光度;ε为摩尔吸收系数,是当浓度以“mol/L”为单位时的吸收系数;λ是波长符号。
建议考生熟悉各类光谱分析法基本符号。
本题答案应选A。
3、铈量法中常用的滴定剂是A:碘B:高氯酸C:硫酸铈D:亚硝酸钠E:硫代硫酸钠【答案】C4、在体内药物分析中最为常用的样本是A:尿液B:血液C:唾液D:脏器E:组织【答案】B5、《中国药典》规定,称取“2.0g”是指称取A:1.5~2.5gB:1.95~2.05gC:1.4~2.4gD:1.995~2.005gE:1.94~2.06g【答案】B【解析】本题考查对《中国药典》凡例的熟悉程度。
《中国药典》凡例是解释和使用《中国药典》、正确进行质量检定的基本原则。
凡例规定共性,具法律约束力。
《中国药典》规定“称取”或“量取”的量,其精确度可根据数值的有效位数来确定。
称取“0.1g”,是指称取重量可为0.06~0.14g;称取“2g”,是指称取重量可为1.5~2.5g;称取“2.0g”,系指称取重量可为1.95~2.05g;称取“2.00g”,系指称取重量可为1.995~2.005g。
饲料行业现行国家标准和行业标准

饲料行业现行国家标准和行业标准(2007年7月18日)共341项综合标准(19项)1.GB/T 10647—1989 饲料工业通用术语2.GB 10648—1999 饲料标签3.GB 13078—2001(2003年1号修改单)饲料卫生标准4。
GB 13078。
1—2006 饲料卫生标准饲料中亚硝酸盐允许量2006-07—01实施5。
GB 13078。
2-2006 饲料卫生标准饲料中赭曲霉毒素A和玉米赤霉烯酮的允许量2006-07-01实施6.GB 13078。
3—2007 配合饲料中脱氧雪腐镰刀菌烯醇的允许量2007—03-01实施7。
GB/T 16764-2006 配合饲料企业卫生规范2007—03—01实施8。
GB/T 18695—2002 饲料加工设备术语9。
GB/T18823-2002(2003年1号修改单)饲料检测结果判定的允许误差10.GB 19081—2003 饲料加工系统粉尘防爆安全规程11。
GB/T 20192—2006 环模制粒机通用技术规范2006-09-01实施12.GB/T 20803-2006 饲料配料系统通用技术规范2007—03-01实施13.NY 929-2005 饲料中锌的允许量14.NY/T932-2005 饲料企业HACCP管理通则15。
NY/T 1023—2006 饲料加工成套设备质量评价技术规范16.NY/T 1024-2006 饲料混合机质量评价技术规范17.NY/T 1025-2006 青饲料切碎机安全使用技术条件18。
NY/T 1031—2006 饲料安全性评价亚急性毒性试验19。
SBJ 05—1993 饲料厂工程设计规范方法标准(115项)1. GB/T 5917-1986 配合饲料粉碎粒度测定法2。
GB/T 5918-1997 配合饲料混合均匀度的测定3。
GB/T 6432—1994 饲料中粗蛋白测定方法4。
GB/T 6433—1994 饲料粗脂肪测定方法5。
世界卫生组织基本药物标准清单

世界卫生组织基本药物标准清单第16版2009年3月本出版物不提供任何明确的或隐含的保证,出版物的解释与应用责任在于读者自己,世界卫生组织对由于使用本出版物所产生的损害不承担任何责任世界卫生组织已采取一切合理的预防措施来核实本出版物中包含的信息。
但是,已出版材料的分发无任何明确或含蓄的保证。
解释和使用材料的责任取决于读者。
世界卫生组织对于因使用这些材料造成的损失不承担责任。
第16版基本药物世界卫生组织标准清单(2009年3月审阅)解释性说明————————————————————————核心清单是指为基本卫生保健系统所必需的最起码的药物清单,清单中列入对治疗重点疾病最有效、安全和符合成本疗效的药物。
重点疾病的选择系根据目前和将来的公共卫生相关问题及药物的潜在安全性和治疗成本疗效确定。
补充清单列出治疗重点疾病的基本药物,这些重点疾病需要专科诊断或监测设施,和/或专家医疗保健,和/或专家培训。
在有疑问时,很多情况下也可将价格一直较高或成本疗效不太好的药物列入补充清单。
方框符号( )主要目的是指出在一类药物中的相似临床作用。
清单中的药物应是有最佳证据显示有效性和安全性的该类药物中的范例。
在一些情况下,这种药物可能是最初获得销售许可证的药物;在另外一些情况下,后来获得许可证的药物可能更加安全或更加有效。
在有效性和安全性数据方面没有差别的情况下,列入清单的药物应是根据国际药物价格信息来源以最低价格能够广泛获得的药物。
并非所有方框药物都可供儿童使用——详见第二版儿童基本药物目录。
只有在对有效性和安全性审查的基础上并符合世界卫生组织临床准则的情况下才能指出药物的同等治疗效果。
国家药物清单不应使用相似的符号并应在最后的遴选中具有特别性,它们取决于地方的可得性和价格。
a 表示此类药品的使用有年龄限制,具体规定详见表1。
紧接补充清单之后的[c] 表示这些药物需要专门的诊断或监测设施,或/和专门的医疗保障,或/和需要经专门训练的专家在儿童使用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
文件名称苯巴比妥质量标准共 3 页第 1 页
文件编号TS-02-006 编制部门质量部
状态正式版本号00 备
份
起草人起草日期年月日
号
审核人审核日期年月日生效日期
批准人批准日期年月日年月日
分发部门质量部、生产技术部、质保处、质检处、生产车间、物流部
目的
建立苯巴比妥质量标准,作为采购、QC分析、车间使用的标准依据,确保生产中使用合格的茶碱。
范围
本标准适用于茶碱的质量管理。
责任
本标准由质量部起草;物流部负责按照本标准采购,QC处负责按本标准检验,QA负责监督;生产车间负责按照本标准使用。
内容
1品名:
1.1 中文名:苯巴比妥
1.2 英文名:Phenobarbital
1.3汉语拼音名:Benbabituo
2 分子式、结构式、化学名、分子量
2.1 分子式:C12H12N203
2.2 结构式:
2.3 化学名:5-乙基-5-苯基-2,4,6(1H,3H,5H)-吡啶三酮;
2.4 分子量:232.24。
3 理化性质
3.1 本品为白色有光泽的结晶性粉末,无臭,味微苦,饱和水溶液显酸性反应。
3.2本品在乙醇或乙醚中溶解,在三氯甲烷中略溶,在水中极微溶解,在氢氧化钠或碳酸钠溶液中溶解。
3.3 熔点:本品的熔点(附录Ⅵ C)为17
4.5-178℃。
4 产品规格和包装形式
25kg/桶,双层聚乙烯薄膜袋包装(其中直接接触茶碱的为药用聚乙烯薄膜袋),放于纸板桶中。
5 内部使用代码:1006。
6 经批准的供应商:辽宁省医药物资有限公司。
7 标准依据:中国药典2010年版(ChP2010)。
8 取样、检验方法或相关操作规程编号
见《苯巴比妥检验标准操作规程》SOP-08-306和《原辅料取样规程》SOP-08-048。
9 定性和定量的限度要求
9.1 鉴别:
9.1.1 取本品约10mg,加硫酸2滴与亚硝酸钠约5mg,混合,即显橙黄色,随即转橙红色。
9.1.2 取本品约50mg,置试管中,加甲醛试液1ml,加热煮沸,冷却,沿管壁缓缓加硫酸0.5ml,使成两液层,置水浴中加热,接界面显玫瑰红色。
9.1.3本品的红外光吸收图谱应与对照的图谱(光谱集227图)一致。
9.1.4 本品显丙二酰脲类的鉴别反应(附录Ⅲ)。
9.2 检查
9.2.1 酸度:取本品0.20g,加水10ml,煮沸搅拌1分钟,放冷,滤过,取滤液5ml,加甲基橙指示液1滴,不得显红色。
9.2.2 乙醇溶液的澄清度
取本品1.0g加乙醇5ml,加热回流3分钟,溶液应澄清。
9.2.3 有关物质
取本品,加流动相溶解并稀释制成每1ml中含1mg的溶液,作为供试品溶液;精密量取1ml,置200ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液。
照高效液相色谱法(附录Ⅴ D)试验,用辛烷基硅烷键合硅胶为填充剂;以乙腈-水(25:75)为流动相,检测波长为220nm;理论板数按苯巴比妥峰计算不低于2500,苯巴比妥峰与相邻杂质峰的分离度应符合要求。
取对照溶液5ul,分别注入液相色谱仪,记录色谱图至主成分峰的峰
高约为满量程的15%;精密量取供试品溶液与对照溶液各5ul,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍,供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积的2
倍(1.0%)。
9.2.4 中性或碱性物质
取本品1.0g,置分液漏斗中,加氢氧化钠试液10ml溶解后,加水5ml与乙醚25ml,振摇1分钟,分取醚层,用水振摇洗涤3次,每次5ml,取醚液压经干燥滤纸滤过,滤液置105℃恒重的蒸发皿中,蒸干,在105℃干燥1小时,遗留残渣不得过3mg.
9.2.5 干燥失重
取本品,在105℃干燥至恒重,减失重量不得过1.0%(附录Ⅷ L)。
9.2.6 炽灼残渣:不得过0.1%(附录Ⅷ N)。
9.2.7 含量测定
取本品约0.2g,精密称定,加甲醇40ml使溶解,再加新制的3%无水碳酸钠溶液15ml,照电位滴定法(附录Ⅶ A),用硝酸银滴定液(0.1mol/L)滴定。
每1ml硝酸银滴定液
(0.1mol/L)相当于23.22mg的C
12H
12
N
2
3。
按干燥品计算,含苯巴比妥不得少于98.5%。
10 贮存条件和注意事项
密封保存。
11 有效期或复验期
11.1 有效期:四年。
11.2 复验期:一年。
