2015届浙江省高三化学一轮复习课件:大题冲关滚动练之4——速率、平衡图表类综合题(苏教版)
化学(通用) 专题8 题冲关滚动练之四 Word版含答案

大题冲关滚动练之四——电解质溶液的图表类综合题1.下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积K sp(25 ℃)。
CH3COOHCH3COO-+H+H2CO3H++HCO-,3HCO-,3H++CO错误!C6H5OHC6H5O-+H+H3PO4H++H2PO错误!H2PO错误!HHPO错误!H++PO3-,4NH3·H2ONH错误!+OH-BaSO4(s)Ba2+(aq)+SO2-4(aq)BaCO3(s)Ba2+(aq)+CO错误!(aq)(1)由上表分析,若①CH3COOH,②HCO错误!,③C6H5OH,④H2PO-均可看做酸,则它们酸性由强到弱的顺序为______________(填4编号)。
(2)写出C6H5OH与Na3PO4反应的离子方程式________________________。
(3)25 ℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)______c(NH错误!)(填“〉"、“=”或“〈”)。
mol·L-1氨水,混合液中粒子浓度关系正确的是________(填字母序号).A.若混合液pH>7,则V≥10B.若混合液pH〈7,则c(NH错误!)>c(C6H5O-)〉c(H+)〉c(OH -)C.V=10时,混合液中水的电离程度小于10 mL 0.01 mol·L-1苯酚溶液中水的电离程度D.V=5时,2c(NH3·H2O)+2c(NH错误!)=c(C6H5O-)+c (C6H5OH)(5)水解反应是典型的可逆反应,水解反应的化学平衡常数称为水解常数(用K b表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:_______________________________________________________ _________________。
2015届浙江省高三化学一轮复习课件:大题冲关滚动练之3——电原理综合应用题(苏教版)

图1
图2
1
2
3
4
5
6
(2)芒硝化学式为 Na2SO4· 10H2O,无色晶体,易溶于水, 是一种分布很广泛的硫酸盐矿物。该小组同学设想,如 果模拟工业上离子交换膜法制烧碱的方法,用上图 2 所 示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧 化钠,无论从节省能源还是从提高原料的利用率而言都 更加符合绿色化学理念。 ①该电解槽的阳极反应式为__________________。此时 通过阴离子交换膜的离子数 __________( 填“大于”、 “小于”或“等于”)通过阳离子交换膜的离子数。
1
2
3
4
5
6
②制得的氢氧化钠溶液从出口(填“A”、“B”、“C” 或“D”)________导出。 ③通电开始后,阴极附近溶液 pH 会增大,请简述原因: _______________________。 ④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃 料电池,则电池负极的电极反应式为 ____________。已 知 H2 的燃烧热为 285.8 kJ· mol-1,则该燃料电池工作产 生 36 g 液态 H2O 时,理论上有________ kJ 的能量转化 为电能。
1
2
3
4
5
6
6.某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、 Cu。 (1)将上述反应设计成的原电池如图甲所示, 请回答下 列问题:
- 3+ 3+ Cr2O 2 发生反应,生成的 Fe 和 Cr 在阴极区与 7
OH-结合生成 Fe(OH)3 和 Cr(OH)3 沉淀除去。 (1) 若阳极铁质量减少 16.8 g ,则理论上被还原的
2- Cr2O7 的物质的量为________mol。
第七章化学反应速率和化学平衡大题冲关滚动练之二速率、平衡

第七章化学反应速率和化学平衡大题冲关滚动练之二速率、平衡化学人教四川第七章学反化应速率和学化衡平大冲关滚动练题二之― ―率、平速图表类衡综合题题冲关滚大练之动―二速―率、平衡图表综合类1题2 3 4 65大题冲滚关练动之―二速率―平、衡图表类综题合123 4561.及碳化合其物有广的用泛。
途(1)在化学中,常电用碳作电:①在极性酸锰锌电池中干,碳作棒________极。
②若碳用和铁棒棒作电电极解和饱食盐水生烧碱产时碳,棒作________,极反应离的方程子式。
()2将水蒸气通过热的红碳产生水可气:C煤(s)H+2C (O)+g2(Hg)A .升温度C高加.催化剂入Δ=+H1313.kJ mol 1 达到平,后,体积衡不-变,时提高能H O2的平衡化率的转施是_措____(填字_母序号。
).B加增的碳量D.用用C 吸收剂O除去OC大题冲关动练之滚―二―速、平率衡表类综合题图123 456 (3)一定将量的C Og()和H 2(Og)过某通容的恒闭密容中,器发生反应C:(gO+H) 温度2℃/2g(+H2)g()得到下数如:据起始浓/度mo l LC(gO )2.0-1平浓衡/度mol -L1H (g2 ).04900HO2g)( .08通过算,该计应的反衡常数为_平____________________。
_ 大题冲关滚练之二动――率速平衡、表图综类题合12 3 45(46)业工把上水气煤的中混合体气处后,理获得较的纯2H 用于成合氨:HΔ-92=4 kJ. mo-1。
某同l学在不同验条实下模拟件工化产进生实行验,2 N度浓随时变化间图如:大冲题关滚练动二之――速率、衡图表平类合题综213 4 5 6① 与实验Ⅰ比较,实验改变Ⅱ的条件____为___________________________________________________________________。
_ ②验实Ⅲ实比验Ⅰ温度要高的,它其条件相同请,下在图画出实Ⅰ和实验验Ⅲ中NH3 度浓随时变化间的意示。
2015届高三第一轮复习《化学反应速率和化学平衡》单元测试

2018届高三第一轮复习《化学反应速率和化学平衡》单元测试姓名学号相对原子质量:H-1 C-12 N-14 O-16 Mg-24 Si-28一、选择题(共42分)1.[2014天津]化学与生产、生活息息相关,下列叙述错误的是()A.铁表面镀锌可增强其抗腐蚀性B.用聚乙烯塑料代替聚乳酸塑料可减少白色污染C.大量燃烧化石燃料是造成雾霾天气的一种重要因素D.含重金属离子的电镀废液不能随意排放2.[2014天津]运用相关化学知识进行判断,下列结论错误的是()A.某吸热反应能自发进行,因此该反应是熵增反应B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率11.[2014江苏]下列有关说法正确的是()A.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀B.2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0C.加热0.1mol/LNa2CO3溶液,CO32-的水解程度和溶液的pH均增大D.对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大4.[2014上海]向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中()A.C(Ca2+)、C(OH-)均增大B.C(Ca2+)、C(OH-)均保持不变C.C(Ca2+)、C(OH-)均减小D.C(OH-)增大,C(H+)减小5.[2014新课标I]已知分解1 mol H2O2 放出热量98KJ,在含少量I-的溶液中,H2O2的分解机理为:H2O2+I-→H2O +IO-慢H2O2+IO-→H2O +O2+I-快下列有关反应的说法正确的是( )A.反应的速率与I-的浓度有关B.IO-也是该反应的催化剂C.反应活化能等于98KJ·mol-1D.v(H2O2)=v(H2O)=v(O2)6.[2014新课标I]溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( ) A.溴酸银的溶解时放热过程Array B.温度升高时溴酸银溶解速度加快C.60 ℃时溴酸银的K sp约等于6×10-4D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯t/℃7.[2014重庆]在恒容密闭容器中通入X 并发生反应:2X(g) Y(g),温度T 1、T 2下X 的物质的量浓度c(X)随时间t 变化的曲线如题7图所示。
高考化学一轮大题冲关滚动练【5】电解质溶液的图表类综合题ppt课件

大题冲关滚动练之五——电解质溶液的图表类综合题
1 2 3 4 5
(4)25 ℃时,向 10 mL 0.01 mol· L-1 苯酚溶液中滴加 V mL 0.01 mol· L
-1
氨水,混合液中粒子浓度关系正确的是________(填字
母序号)。 A.若混合液 pH>7,则 V≥10
+ B.若混合液 pH<7,则 c(NH4 )>c(C6H5O-)>c(H+)>c(OH-)
1 2 3 4 5
2 .工业上把 Cl2 通入 NaOH 溶液中制得漂白液 ( 主要成分 NaClO)。一化学小组模拟实验得到 ClO-、ClO- 3 等离子其 物质的量(mol)与反应时间 t(min)的关系曲线:
(1)工业制取漂白液的化学反应方程式为________________ __________________________________________________。 (2)图中 a 点混合物所含的三种溶质是 NaCl 和________(填 溶质的化学式),离子浓度从大至小的排列顺序是 _______________。
大题冲关滚动练之五——电解质溶液的图表类综合题
1 2 3 4 5
解析
(1)酸性强弱,可以通过比较弱电解质的电离平衡常数大小
来判断。 (2)苯酚是弱电解质,Na3PO4 是强电解质,根据由强制弱原则, 结合电离平衡常数,反应只能生成 HPO2 4 。 (3)醋酸与氨水的电离平衡常数相等,恰好反应后的盐中阴阳离
大题冲关滚动练之五——电解质溶液的图表类综合题
1 2 3 4 5
解析
(1)Cl2 和 NaOH 反应生成 NaCl、NaClO 和 H2O;
- -
2015届高考化学大题冲关滚动练复习5
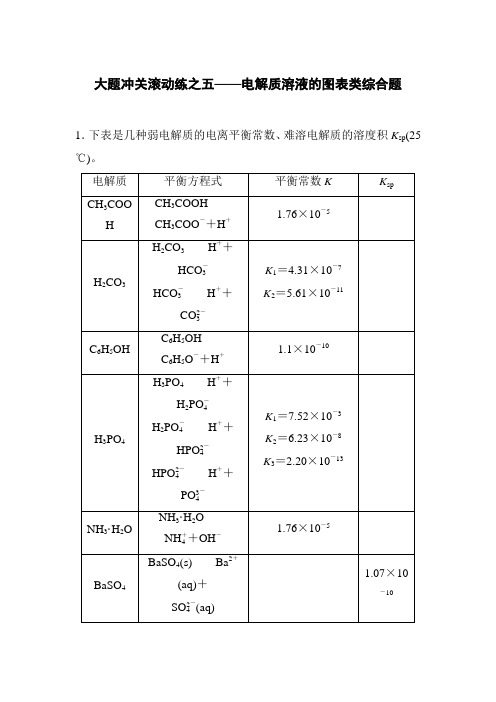
大题冲关滚动练之五——电解质溶液的图表类综合题1.下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积K sp(25 ℃)。
CH3COOHCH3COO-+H+H2CO3H++HCO-3HCO-3H++CO2-3C6H5OHC6H5O-+H+H3PO4H++H2PO-4H2PO-4H++HPO2-4HPO2-4H++PO3-4NH3·H2ONH+4+OH-BaSO4(s)Ba2+(aq)+SO2-4(aq)BaCO3(s)Ba2+(aq)+CO2-3(aq)(1)由上表分析,若①CH3COOH,②HCO-3,③C6H5OH,④H2PO-4均可看做酸,则它们酸性由强到弱的顺序为______________(填编号)。
(2)写出C6H5OH与Na3PO4反应的离子方程式_____________________________________________________________________________________________ _______________。
(3)25 ℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)______c(NH+4)(填“>”、“=”或“<”)。
(4)25 ℃时,向10 mL 0.01 mol·L-1苯酚溶液中滴加V mL 0.01 mol·L-1氨水,混合液中粒子浓度关系正确的是________(填字母序号)。
A.若混合液pH>7,则V≥10B.若混合液pH<7,则c(NH+4)>c(C6H5O-)>c(H+)>c(OH-)C.V=10时,混合液中水的电离程度小于10 mL 0.01 mol·L-1苯酚溶液中水的电离程度D.V=5时,2c(NH3·H2O)+2c(NH+4)=c(C6H5O-)+c(C6H5OH)(5)水解反应是典型的可逆反应,水解反应的化学平衡常数称为水解常数(用K b表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:_________________________________________________________ _______________。
2015浙江省高考化学第27题冲关
2015浙江省高考化学第27题(Ⅱ)冲关1.Ⅱ.石油铁储罐久置未清洗易引发火灾,经分析研究,事故由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1︰3反应生成的黑色物质丙自燃引起。
某研究小组将一定量的丙粉末投入足量的浓盐酸中发生反应,得到4.8 g 淡黄色沉淀和气体乙,乙在标准状况下的密度为1.52 g/L ,过滤后向滤液(假设乙全部逸出)中加入足量的NaOH 溶液,先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24 g 。
已知气体乙可溶于水。
请回答下列问题:(1)甲的化学式为 。
写出丙中非金属元素的离子结构示意图 。
(2)丙在盐酸中反应的化学方程式: (离子方程式表示)。
(3)丙与盐酸反应后的滤液暴露在空气中一段时间后颜色加深,其原因是_____________。
(4)请设计合理的实验方案验证不同温度对丙与盐酸反应速率的影响______________。
(5)为消除火灾隐患,下列措施可行的是____________。
A .石油入罐前脱硫B .定期用酸清洗罐体C .罐体内壁涂刷油漆D .罐体中充入氮气2.(Ⅱ)某研究小组为了探究一种浅绿色盐X (仅含四种元素,不含结晶水,M(X)﹤908 g·mol -1)的组成和性质,设计并完成了如下实验取一定量的浅绿色盐X 进行上述实验,充分反应后得到23.3g 白色沉淀E 、28.8g 红色固体G 和12.8g 红色固体H 。
已知:(1)浅绿色盐X 在570℃、隔绝空气条件下受热分解为非氧化还原反应。
(2)常温下B 呈液态且1个B 分子含有10个电子请回答如下问题:(1)写出B 分子的电子式(2)已知G 溶于稀硝酸,溶液变成蓝色,并放出无色气体。
请写出该反应的离子方程式为(3)X 的化学式是 ,在隔绝空气、570℃温度下加热X 至完全分解的化学反应方程式为(4)一定条件下,NH 3与黑色固体C 发生氧化还原反应得到红色固体和气体丙(丙是大气主要成分之一),写出一个可能的化学反应方程式 ,设计一个实验方案探究 红色固体的成分 。
高考化学复习高考大题冲关滚动练:无机框图题
大题冲关滚动练之四——无机框图题1.从物质A的水溶液出发,有如图所示的一系列变化(参加反应或反应生成的H2O没有表示出来)。
试完成下列问题:(1)写出下列物质的化学式:A ,E ,X ,Y 。
(2)写出步骤①②发生反应的离子方程式:①________________________________________________________________________;②________________________________________________________________________。
2.甲、乙、丙为常见单质。
A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色。
在一定条件下,各物质相互转化关系如图所示。
请回答下列问题:(1)用化学式表示:丙为__________,H为__________。
(2)A的电子式为________________________________________________________________________。
(3)电解E的水溶液时,E起到的作用是________________________________________________________________________。
(4)写出B+C―→D的化学方程式:________________________________________________________________________________________________________________________________________________;写出E+G―→F的离子方程式:________________________________________________________________________________________________________________________________________________。
