乙酰水杨酸片剂及胶囊剂的制备及其溶出度的测定 2
实验六 乙酰水杨酸的制备

实验报告学院:第二临床医学院专业:临床医学年级:级班级:班姓名:学号:日期:2014,6,16 实验课程:有机化学实验实验名称:实验六乙酰水杨酸的制备【实验目的】1.学习制备乙酰水杨酸。
2.熟悉重结晶。
3鉴定水杨酸。
【实验原理】水杨酸是一个双官能团的化合物,它既是酚又是羧酸,因此它能进行两种不同的酯化反应,它既可与醇反应,乙酸酐存在下,形成乙酰水杨酸(阿司匹林),而在过量甲醇存在下,产品则是水杨酸甲酯(冬青油)。
本实验用水杨酸与乙酸酐反应制备乙酰水杨酸。
原理如下:【试验药品】仪器与药品1、仪器5OmL锥形瓶、抽滤瓶、布氏漏斗、表面皿2、药品水杨酸、乙酸酐、浓硫酸、氯化铁溶液【实验步骤】一、制备粗乙酰水杨酸:1.用电子天平称量3.15g水杨酸加入锥形瓶中。
2.用移液管取乙酸酐4.5ml加入锥形瓶中。
3.在锥形瓶中加入浓硫酸5滴,在70°c水浴中摇晃20分钟。
4.再在锥形瓶中加入冷水50ml,搅拌,抽滤。
5.将抽滤后的晶体放入烘箱烘干,称量,计算产率。
二、制备精制乙酰水杨酸:1.用电子天平称量0.5g粗乙酰水杨酸加入烧杯中。
2.在烧杯中加入3ml 95%乙醇放在70°c的水浴箱中溶解,再拿出室温冷却。
3.在冷却之后的烧杯中逐滴加入70°c蒸馏水5ml左右至浑浊,放在70°c水浴箱变澄清透明。
4.将产生的溶液在冰浴中冷却振摇。
5.将溶液抽滤产生晶体并烘干。
三、定性鉴定:1.分别取水杨酸0.1g,粗乙酰水杨酸0.1g,和精制乙酰水杨酸0.1g放入3支试管中。
2.各加入10滴95﹪乙醇,搅匀。
3.在各试管中加入1滴氯化铁,观察各试管中的颜色变化。
【实验结果】1.制备粗乙酰水杨酸经过称量后得到2.090g,原来的反应物水杨酸为3.15g。
C水杨酸=3.15/138=0.0231/ C水杨酸=1/C乙酰水杨酸C乙酰水杨酸=0.023m乙酰水杨酸= C乙酰水杨酸*M乙酰水杨酸=4.11g产率=2.090/4.11*100%=50.9%2.顺序依次为粗的阿司匹林、精制的阿司匹林、水杨酸。
【全版】实验六乙酰水杨酸的制备推荐PPT

实验六 乙酰水杨酸的制备
(两人一组)
实验目的 1. 了解乙酰化反应; 2. 学习并掌握抽滤和重结晶等实验操作。
一、实 验 原 理
O O C CH3 COOH
乙酰水杨酸,临床常用药物,又名阿 司匹林,具有解热镇痛及抗风湿等作用。 白色结晶,难溶于水,易溶于醇、醚和氯 仿。
抽干结晶
写名字 保存 称量纸包好 乙酰水杨酸
计算产率 天平称重
精制品
水浴干燥
转移结晶 表面皿
3. 检验
(1)水杨酸
少量
10滴 95%乙醇 试管
1~2滴 1%FeCl3 颜色?
(2)乙酰水杨酸 10滴 95%乙醇
精制品
试管
少量
1~2滴 1%FeCl3
颜色?
4. 注意事项 (1) 取样时注意吸量管的读数 (2) 节约用冰 (3) 实验后洗净大试管并放回烘箱旁
OH COOH
+
(CH3CO)2O
与FeCl3反应,显紫色
O
O C CH3 COOH
+
浓H2SO4 80~90℃水浴
?
CH3COOH
不与FeCl3反应
副反应产物
OH
CO
O
COOH
水杨酰水杨酸
OCOCH3
CO
O
COOH
乙酰水杨酰水杨酸
二、实 验 步 骤
1. 合成
水杨酸0.7 g (3) 实验后洗净大试管并放回烘箱旁
微型抽滤装置
待滤物
漏斗
接水泵
玻璃钉
抽滤
注意:玻璃钉漏斗抽滤,开始时速度勿过快,用玻棒压
实结晶后,再开大水阀。用少量水洗涤烧杯,将剩余结
乙酰水杨酸的合成及表征
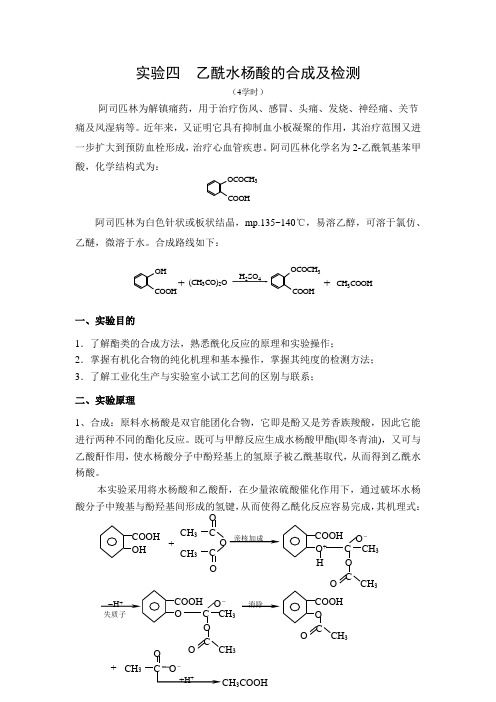
实验四 乙酰水杨酸的合成及检测(4学时)阿司匹林为解镇痛药,用于治疗伤风、感冒、头痛、发烧、神经痛、关节痛及风湿病等。
近年来,又证明它具有抑制血小板凝聚的作用,其治疗范围又进一步扩大到预防血栓形成,治疗心血管疾患。
阿司匹林化学名为2-乙酰氧基苯甲酸,化学结构式为:阿司匹林为白色针状或板状结晶,mp.135~140℃,易溶乙醇,可溶于氯仿、乙醚,微溶于水。
合成路线如下:一、实验目的1.了解酯类的合成方法,熟悉酰化反应的原理和实验操作; 2.掌握有机化合物的纯化机理和基本操作,掌握其纯度的检测方法; 3.了解工业化生产与实验室小试工艺间的区别与联系; 二、实验原理1、合成:原料水杨酸是双官能团化合物,它即是酚又是芳香族羧酸,因此它能进行两种不同的酯化反应。
既可与甲醇反应生成水杨酸甲酯(即冬青油),又可与乙酸酐作用,使水杨酸分子中酚羟基上的氢原子被乙酰基取代,从而得到乙酰水杨酸。
本实验采用将水杨酸和乙酸酐,在少量浓硫酸催化作用下,通过破坏水杨酸分子中羧基与酚羟基间形成的氢键,从而使得乙酰化反应容易完成,其机理式:O O O + CH 3 C OCH 3 C 亲核加成 COOH CH 3 C + O - O C3O O C O -O C CH 3消除COOHO C CH 3O OCOCH 3COOHOH COOH(CH 3CO)2OH 2SO 4CH 3COOH++OCOCH 3COOH2、纯化:由于水杨酸的苯环上既有羟基又有羧基,在反应过程中会形成一种高聚物副产物:可以利用乙酰水杨酸与NaHCO 3反应生成水溶性的钠盐,而高聚物不溶于NaHCO 3溶液的原理,通过过滤将高聚物分离出去。
然后再用酸将乙酰水杨酸沉淀出来,从而达到纯化产品的目的,其反应式如下:3、重结晶:在最终产物中最有可能产生的杂质是水杨酸本身,这是由于乙酰化反应不完全或是产物在分离步骤中发生水解造成的。
因此还可以用乙醇、丙酮或乙酸乙酯对最终产物进行重结晶,从而得到纯度更高的产品——阿司匹林。
乙酰水杨酸纯度的测定

⽅法优点缺点实验室常⽤鉴定⽅法⽤熔点管测定阿司匹林的熔点样品⽤量少,仪器和操作⽅便,管内液体因温度差⽽发⽣对流作⽤,省去⼈⼯搅拌的⿇烦。
温度计的位置和加热的部位都会影响测定的准确度定性检验游离⽔杨酸的存在仪器和操作⽅便不够准确⽤⽐⾊法测定⽔杨酸在产品中的百分含量简便、灵敏、快速,不消耗样品,测定後仍能回收使⽤易被酸⼲扰,⽽且测定混合有机成分时,极不准确⽤容量返滴定法测定阿司匹林的质量可⽤于待测离⼦(如Ba、Sr等离⼦)虽能与EDTA形成稳定的配合物,但缺少变⾊敏锐的指⽰剂。
(2)待测离⼦(如Al、Cr等离⼦)与EDTA的配合速度很慢,本⾝⼜⽔解或对指⽰剂有封闭作⽤的两种情况。
返滴定剂会置换出被测离⼦,引起误差,⽽且终点不敏锐现代先进鉴定⽅法薄层法鉴定产物纯度快速、简便、⾼效、经济、应⽤⼴泛。
可以同时分离多个样品,分析成本低,对样品预处理要求低,对固定相、展开剂的选择⾃由度⼤,适⽤于含有不易从分离介质脱附或含有悬浮微粒或需要⾊谱后衍⽣化处理的样品分析。
⾼效薄层⾊谱法是近年来迅速发展⾼效、快速、操作简便、结果准确。
常规的TLC法存在展开时间长、展开剂体积需求⼤和分离结果差反相⾼效液相⾊谱法同时测定⽔杨酸原料中⽔杨酸和微量杂质苯酚含量三⾼⼀⼴⼀快的特点:〈1〉⾼压;〈2〉⾼效;〈3〉⾼灵敏度;〈4〉应⽤范围⼴;〈5〉分析速度快、载液流速快。
与⽓相⾊谱相⽐各有所长,相互补充。
HPLC的缺点是有“柱外效应”。
在从进样到检测器之间,除了柱⼦以外的任何死空间(进样器、柱接头、连接管和检测池等)中,如果流动相的流型有变化,被分离物质的任何扩散和滞留都会显著地导致⾊谱峰的加宽,柱效率降低。
HPLC检测器的灵敏度不及⽓相⾊谱。
Phazir快速测定阿斯匹林(研究中)由于近红外对于含量越⾼的成分,定性、定量分析结果会越准确,因⽽,Phazir可以分析⾷品药品,⽽且其使⽤⽅法⼗分简单,过程仅需5-10秒。
现今仍在研究开发中参考⽂献:[1]中国医院药学杂志;CHINESE JOURNAL OF HOSPITAL PHARMACY;1995年 11期;[2] 王英.《⾷品安全导刊》,2008,(11)[3] ⾸都师范⼤学化学系北京100037 --《⼤学化学》,2006,(03)。
阿司匹林胶囊剂的制备实验报告

阿司匹林胶囊剂的制备实验报告一、实验目的1、掌握阿司匹林胶囊剂的制备方法。
2、熟悉胶囊剂制备过程中的质量控制要点。
3、了解胶囊剂的特点和应用。
二、实验原理阿司匹林(化学名:乙酰水杨酸)是一种常用的解热镇痛药。
胶囊剂是将药物填充于空心胶囊中制成的固体制剂,具有掩盖药物不良气味、提高药物稳定性、便于服用等优点。
阿司匹林胶囊剂的制备主要包括药物的粉碎、过筛、混合、填充等步骤。
通过合理的工艺操作,使药物均匀分散在胶囊中,保证每粒胶囊的含量准确、质量稳定。
三、实验材料与设备1、材料阿司匹林原料药淀粉滑石粉空心胶囊(0 号)2、设备电子天平粉碎机标准筛(80 目、100 目)混合器胶囊填充板四、实验方法1、阿司匹林的粉碎与过筛称取适量的阿司匹林原料药,放入粉碎机中粉碎。
将粉碎后的阿司匹林通过 80 目筛,收集筛下物备用。
2、辅料的准备称取适量的淀粉,通过 100 目筛,备用。
称取适量的滑石粉,备用。
3、混合将阿司匹林筛下物、淀粉和滑石粉按照一定比例放入混合器中,充分混合均匀。
4、填充胶囊将混合好的药物粉末置于胶囊填充板中,逐个填充空心胶囊。
五、实验过程1、首先,按照实验要求准确称取所需的阿司匹林原料药、淀粉和滑石粉。
在称量过程中,使用电子天平进行精确称量,确保物料的量符合配方要求。
2、对阿司匹林原料药进行粉碎处理,粉碎过程中注意控制粉碎的程度,避免过度粉碎导致药物性质改变。
粉碎完成后,用 80 目筛对药物进行筛选,去除过大的颗粒,以保证药物的粒度均匀。
3、接着,对淀粉进行过筛处理,使用 100 目筛,使淀粉的粒度更加细小,有利于在后续的混合过程中与阿司匹林充分混合。
4、将处理好的阿司匹林、淀粉和滑石粉按照预定的比例加入混合器中。
混合时,设定适当的混合时间和速度,以确保物料混合均匀。
为了验证混合的均匀性,可以在不同部位取样进行含量测定。
5、混合完成后,开始进行胶囊的填充操作。
将混合好的药物粉末小心地倒入胶囊填充板的孔中,然后使用胶囊填充工具将药物压实,并盖上胶囊帽。
11.实验十一 乙酰水杨酸的制备

六、思考题
1.如何检查制得的乙酰水杨酸中是 否含有水杨酸?
2.对有机化合物进行重结晶时,选 择溶剂的条件是什么?
七、实验结果及分析
(一)实验结果
1.乙酰水杨酸粗产品()g、精制产品()g。
3.溶剂的分类 (1)单溶剂 (2)混合溶剂
找不到一个合适的溶剂时,可考虑使 用混合溶剂。混合溶剂必需具备两个条件: 一是两者必须能混溶,如乙醇-水、丙酮水、乙酸-水、乙醚-甲醇、乙醚-石油醚 等;二是样品易溶于其中一种溶剂,难溶 于另一种溶剂,往往使用混合溶剂能得到 较理想的结果。使用混合溶剂时,应先将 样品加热溶于易溶的溶剂中,趁热过滤除 去不溶性杂质后,再趁热滴入难溶溶剂至
1.重结晶应用
一般重结晶只能纯化杂质在5% 以下的固 体有机物,如果杂质含量过高,往往需先经 过其他方法初步提纯,如萃取、水蒸汽蒸馏、 减压蒸馏、柱层析等,然后再用重结晶方法 提纯。
2.重结晶选择溶剂的条件
(1)与被提纯物质不能发生化学反应. (2)被提纯物质的溶解度,随温度升 高迅速增大,随温度降低迅速减小。 (3)对杂质的溶解度非常大或非常小, 且不随温度变化而变化。 (4)沸点不宜太高,也不宜太低,易 挥发除去。 (5)能给出好的结晶。 (6)毒性小,价格便宜,易得。
溶液混浊,放置冷却,使结晶析出。
三、实验仪器与试剂
(一)仪器:锥形瓶、烧杯、量筒、 水浴箱、布氏漏斗、抽滤瓶、真 空泵、电子天平、剪刀、滤纸、 玻璃棒等。
(二)试剂:水杨酸、醋酸酐、浓 硫酸、蒸馏水、乙醇(95%)、 三氯化铁溶液。
四、实验内容
乙酰水杨酸的制备及影响片剂质量因素

乙酰水杨酸的制备及影响片剂质量因素实验目的:1、通过乙酰水杨酸片的制备,掌握湿法制粒生产片剂的工艺流程。
2、掌握片剂质量检查方法。
3、考查压力、粘合剂、润滑剂、崩解剂以及表面活性剂等对片剂质量的影响。
实验原理:(一)、湿法制粒压片的生产过程:1、主辅料的准备和处理;2、制软材和湿颗粒;3、湿颗粒干燥;4、整粒;5、压片前必须对干颗粒及粉末的混合物进行药物的含量测定,然后根据颗粒所含主药的量再进行片重计算。
(二)、片剂的质量检查1、硬度2、崩解度3、溶出度4、片重差异处方:乙酰水杨酸30g淀粉3g滑石粉 1.5g10%淀粉浆适量第四组处方:阿司匹林300g淀粉30g5%羧甲基纤维素钠适量滑石粉15g实验步骤:4月1日:称重,粉碎,过筛(80目),混合。
4月2日:制10%淀粉浆→混合制软材→过20目筛→烘干→过14目,40目筛。
4月6日:过40目筛→加滑石粉→混合→压片→测片重差异。
4月7日:对脆碎度,硬度,崩解时限进行检查。
实验结果(第三组):6.1、外观:药片表面不均匀,不平整,有细纹,不光亮。
、6.2、重量差异:M总=6.221 0.310. 31g2 0.293 0.314 0.335 0.306 0.337 0.298 0.319 031 10 0.32 11 0.31 12 0.30 13 0.30 14 0.31 15 0.31 16 0.32 17 0.31 18 0.29 19 0.31 200.31因为m—m平均均小于7.5% 所以药品合格。
m平均6.3、硬度:编号M1M2M3M4M5M6M7M8M9M10硬度(N)21.3 22.8 23.2 25.9 26.5 24.3 21.7 21.4 25.8 22.2平均硬度n=23.526.4、脆碎度(10片):M1=3.1394 M2=3.0803因为(M1—M2)*100%=0.6%<1%M1所以脆碎度检查合格。
6.5、崩解时限:水温37℃完全崩解时间为3s。
实验九_乙酰水杨酸的制备

实验九_乙酰水杨酸的制备一、实验目的1. 理解酰化反应的基本原理和方法;2. 初步了解乙酰水杨酸的制备过程。
二、实验原理乙酰水杨酸(Acetylsalicylic acid)是一种非处方药,常用于缓解头痛、发热、关节疼痛等症状。
其化学式为C9H8O4,分子量为180.16。
乙酰水杨酸是由水杨酸(Salicylic acid)和乙酸酐(Acetic anhydride)经酰化反应得到的。
酰化反应的反应物一般为一种酸性物质和一种酸酐,反应中首先生成酸酐酯,然后再水解得到目的产物。
三、实验仪器和药品仪器:量筒、漏斗、烧杯、洗瓶、玻璃棒、真空漏斗、滤纸等。
药品:水杨酸(2.0 g)、乙酸酐(4.0 mL)、浓硫酸(3~4滴)、冰醋酸(约20 mL)、乙醇(约40 mL)。
四、实验步骤1. 实验器皿和药品准备称取精制水杨酸2.0 g放入干燥的100 mL烧杯内,加入4.0 mL乙酸酐,搅拌混合均匀。
取约5 mL冰醋酸注入真空漏斗中,准备好。
2. 酰化反应在通风橱内,将烧杯放入水浴中,用玻璃棒不断搅拌,慢慢滴加冰醋酸,同时不断搅拌,继续在水浴中加热30~40 min,直至生成的产物中不存在水杨酸残留。
3. 分离和洗涤将反应液倒入100 mL水中,不断搅拌,使产生的白色沉淀彻底分离出来。
用玻璃棒捞出沉淀,放入干净的烧杯中,在室温下加入少量浓硫酸(3~4滴),搅拌均匀。
这时,核酸的绿色颜色会迅速消失,表示已经完全酰化。
试管中加入约5 mL冰醋酸,并将酰化产物加入其中,搅拌均匀。
将试管放入冷水中冷却,使产物结晶形成。
将产生的乙酰水杨酸用足够的冷水反复洗涤,使其除去杂质并干燥。
五、实验注意事项1. 实验应在通风橱中进行,避免误吸有毒气体;2. 实验过程产生的废液和废弃试剂需按规定处理,不能随意倒入下水道;3. 实验操作中应注意避免烧伤和化学品污染;4. 实验前要进行全面、系统的安全教育,身体健康者方可进行实验。
六、实验结果与分析根据实验操作,可以在反应结束后制备出纯净的乙酰水杨酸,并从产物的重量来计算反应的收率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
xxx 大学生命与环境科学学院药剂学实验报告2014年6月15日乙酰水杨酸片剂及胶囊剂的制备及其溶出度的测定Preparation and Dissolution Rate Determination of Acetyl Salicylic Acid ’s Tablet and Capsule乙酰水杨酸片剂及胶囊剂的制备及其溶出度的测定Xxx(xxx大学生命与环境科学学院,北京,100081)摘要:目的制备乙酰水杨酸的片剂及胶囊剂,并测定两种乙酰水杨酸剂型溶出度。
方法:《中国药典》2005年版中溶出度测定的基本操作和数据处理方法,用紫外分光光度仪在303nm下测定不同时间溶出度。
结果:乙酰水杨酸的片剂溶出度大于其胶囊剂。
关键词:乙酰水杨酸;片剂;胶囊剂;溶出度Preparation and Dissolution Rate Determinationof Acetyl Salicylic Acid’s Tablet and Capsulexxx(College of Life and Environmental Science, xxx, Beijing, 100081)Abstract:Objective: To prepare the Acetyl Salicylic Acid’s tablet and capsule, and determine their dissolution rate. Method: Dissolution rate was determined according to Pharmaeopoeia of China (2005) by testing the light absorption value (A) spectrophotometrically at 530 nm. Result: the Acetyl Salicylic Acid tablet’s dissolution rateis more than that of capsule. Conclusion: provide the scientifical data for choosing the form of Acetyl Salicylic Acid.Keywords: Acetyl salicylic acid;tablet and capsule;dissolution rate前言【研究背景】药物的有效性,不仅取决于药物的有效成分及药物的化学结构,口服固体制剂的溶出度也是影响人体生物利用度的一个重要因素,两者有着明显的相关性,特别是难溶性药物,如乙酰水杨酸,由于颗粒大小或加入赋型剂不同,尽管口服剂量相同,疗效却存在很大差异。
难溶性药物制剂是药典规定需要进行溶出度测定的药物类型之一,由于药物的生物利用度试验操作过程较溶出度试验复杂,因此,在实际工作中,对于具有良好体内外相关性的药物,通过测定体外溶出度来预测难溶性药物的体内生物利用度,进筛选制剂处方和控制其质量具有重要的意义。
乙酰水杨酸也叫阿司匹林,是一种历史悠久的解热镇痛药,用于治感冒、发热、头痛、牙痛、关节痛、风湿病,还能抑制血小板聚集,用于预防和治疗缺血性心脏病、心绞痛、心肺梗塞、脑血栓形成,也可提高植物的出芽率,应用于血管形成术及旁路移植术也有效。
乙酰水杨酸微溶于水,属难溶性药物,其溶出度是重要的质控指标,2010 年版药典规定溶出度不得小于标示量的80%。
对难溶性药物(溶解度小于0.1~1mg%)而言,溶解是其主要过程,崩解时限往往不能作为判断难溶性药物制剂的吸收指标。
因此,对口服固体制剂,尤其是在体内吸收不良的难溶性药物的固体制剂、缓控释制剂,以及治疗量与中毒量接近的药物固体制剂,均应做溶出度检查。
《中国药典》和许多国家药典对口服固体制剂的溶出度及其测定方法都有明确的规定。
溶出度系指药物从片剂或胶囊剂等固体制剂中在规定溶剂中溶出的速度和程度。
是一种模拟口服固体制剂在胃肠道中崩解和溶出的体外试验法。
口服固体制剂在体内胃肠液中需经崩解和溶解过程才能经生物膜被机体吸收,对许多药物而言,其吸收量通常与该药物从剂型中溶出的量成正比,即溶出的药物量愈大,吸收的药量就愈大,药效就愈强。
【研究原理】片剂系指药物与适宜的辅料均匀混合,通过制剂技术压制而成的圆片状或异形片状的固体制剂,可供内服和外用,是医疗中应用最广泛的剂型之一,它具有剂量准确、质量稳定、服用方便、成本低等优点。
片剂成形的原理:1、湿法制粒颗粒形成原理:粉末间相互结合成颗粒与粘附作用和内聚作用有关。
在制颗粒时,粉末间存在的水分可引起粉末的粘附,如果粉末间只有部分空隙充满液体,则所形成的液桥可以使粉末相结合;如果粉末间的空隙都充满液体,并延伸到主孔隙的边缘时,则颗粒表面的表面张力及整个液体空间的毛细管吸力可使粉末结合;当粉末表面完全被液体包围时,粉末可凭借液滴表面张力彼此结合。
湿粒干燥后,粉末间形成固体桥,加强了粉末的结合。
对于无水的药物粉末,颗粒中粉末之间分子间力的作用很强,可使颗粒保持必要的强度。
2、颗粒压制成形的机理:1.机械力的作用,又称齿合力;2.粒子间力的作用;3.压缩致片剂组分熔融形成固体桥;4.可溶性成分重结晶形成固体桥。
制片的方法有制颗粒压片、结晶直接压片和粉末直接压片等。
制颗粒的方法又分为干法和湿法。
现将常用的湿法制粒压片的工艺流程介绍如下。
湿法制粒压片的工艺流程:制成的片剂需要按照药典规定的片剂质量标准进行检查。
检查的项目,除片剂的外观应完整光洁、色泽均匀,且有适当的硬度外,必须检查重量差异和崩解时限。
有的片剂药典还规定检查溶出度和含量均匀度。
并明确凡检查溶出度的片剂,不再检查崩解时限;凡检查含量均匀度的片剂,不再检查重量差异。
片剂重量差异、崩解时限和含量均匀度检查见2000版药典二部附录5~6页和72页,75~78页。
片剂压缩成形性的评价方法:1、硬度与抗张强度(TS):硬度是片剂的径向破碎力(kN),常用孟山都硬度计,硬度测定仪等测定。
抗张强度是表示单位面积的破碎力(kPa或MPa)。
抗张强度的大小反应物料的结合力和压缩成形性的好坏。
2、脆碎度(breakage,Bk):片剂受到震动或磨擦之后容易引起碎片,顶裂,破裂等。
脆碎度反映片剂的抗磨损震动能力,也是片剂质量标准检查的重要项目。
常用Roche脆碎度测定仪。
3、弹性复原率(elastic recovery,ER):将片剂从模中推出后,由于内应力的作用发生弹性膨胀。
把这种现象称为弹性复原或弹性后效。
弹性复原率是将片剂从模孔中推出后弹性膨胀引起的体积增加值和片剂在最大压力下的体积之比。
一般药物片剂的弹性复原率在2~10%,如果药物的弹性复原率较大,片剂的硬度低,甚至易于裂片,可加入可压性好的辅料以改善压缩成形性,裂片现象。
胶囊剂系指药物或加有辅料充填于空心胶囊或密封于软质囊材中制成的固体制剂。
主要供口服用,也可用于直肠、阴道等。
空胶囊的主要材料为明胶,也可用甲基纤维素、海藻酸盐类、聚乙烯醇、变性明胶及其他高分子化合物,以改变胶囊的溶解性或达到肠溶的目的。
根据胶囊剂的硬度与溶解和释放特性,胶囊剂可分为硬胶囊与软胶囊、肠溶胶囊和缓释胶囊。
硬胶囊剂的一般制备工艺流程为:1.空胶囊与内容物准备空胶囊分上下两节,分别称为囊帽与囊体。
空胶囊根据有无颜色,分为无色透明、有色透明与不透明三种类型;根据锁扣类型,分为普通型与锁口型两类;根据大小,分为000、00、0、1、2、3、4、5号八种规格,其中000号最大,5号最小,常用的为0号规格。
内容物可根据药物性质和临床需要制备成不同形式的内容物,主要有粉末、颗粒和微丸三种形式。
2.充填空胶囊大量生产可用全自动胶囊充填机充填药物,填充好的药物使用胶囊抛光机清除吸附在胶囊外壁上的细粉,使胶囊光洁。
小量试制可用胶囊充填板或手工充填药物,充填好的胶囊用洁净的纱布包起,轻轻搓滚,使胶囊光亮。
3.质量检查充填的胶囊进行含量测定、崩解时限、装量差异、水分、微生物限度等项目的检查。
胶囊剂的装量差异检查方法:取供试品20粒,分别精密称定重量后,倾出内容物,硬胶囊用小刷或其他适宜的用具拭净;再分别精密称定囊壳重量,求出每粒内容物的装量与平均装量。
按规定,超出装量差异限度的不得多于2粒,并不得有1粒超出限度1倍。
表1 胶囊剂装量差异限度平均装量装量差异限度0.3g以下±10%0.3g及0.3g以上±7.5%4.包装及贴标签质量检查合格后,定量分装于适当的洁净容器中,加贴符合要求的标签。
【研究目的】制备乙酰水杨酸片剂及胶囊剂,测定固体制剂(片剂、胶囊)溶出度。
1.材料和方法1.1 实验仪器天平、方瓷盘、研钵、不锈钢筛(14目~16目)、烘箱、空胶囊、s-100孔胶囊灌装器、天平、洁净的纱布、刀、指套、称量纸、药匙、圆口PE药用瓶子1.2 实验试剂乙酰水杨酸、淀粉、糊精、蔗糖粉、滑石粉、药物粉末、液状石蜡1.3试验方法1.3.1 乙酰水杨酸片剂的制备1.处方:乙酰水杨酸:20g(主药)、淀粉:280g(填充剂)、糊精:80g(填充剂)、蔗糖粉:40g(填充剂)、10%淀粉浆:适量(粘合剂)、滑石粉:5g(润滑剂)2.制法:乙酰水杨酸细粉与淀粉、糊精、滑石粉、蔗糖粉(需研磨至均匀、细粉、无结块),用等量递加法于研钵中研磨混合、混合均匀后,加淀粉,混匀后,通过100目筛得颗粒,以Ф8mm冲模压片。
3.片重差异:取药片20片,精密称定总重量,求得平均片重后,再分别精密称定各片的重量。
每片重量与平均片重相比较(凡无含量测定的片剂,每片重量应与标示片重比较)超出重量差异限度(见表1)的药片不得多于2片,并不得有1片超出限度1倍。
片重差异(±%)=100平均片重单片重-平均片重表2 重量差异限度平均片重重量差异限度0.30g以下±7.5%0.30g或0.30g以上±5%1.3.2 乙酰水杨酸胶囊剂的制备板装法:将胶囊体插入胶囊板中,将药粉置于胶囊板上,轻轻敲动胶囊板,使药粉落入胶囊壳中,至全部胶囊壳中都装满药粉后,套上胶囊帽。
装量差异检查:①先将20粒胶囊分别精密称定重量②再将内容物完全倾出,再分别精密称定囊壳重量③求出每粒内容物的装量与平均装量④将每粒装量与平均装量进行比较,超出装量差异限度的不得多于2粒,并不得有1粒超出装量差异限度的1倍,则装量差异检查合格。
1.3.3 溶出度测定按中国药典2010 年版,第一法( 转蓝法) 测定,溶出介质:稀盐酸( 取盐酸24 mL 稀释成1 000 mL)。
转速100 r/min,温度( 37±0.5) ℃,经5 min,15 min,30 min,45 min,60 min,取溶液10 mL滤过,每次取样后加溶出空白介质10 mL,精密量取续滤液3 mL 置50 mL 容量瓶中,加0.4% NaOH 液5 mL,置水浴上煮沸5 min,放冷,加稀H2SO4 2.5 mL,并用蒸馏水补至刻度,摇匀。
