硝酸银标准溶液的配制方法
钾离子的测定-硝酸银滴定法GB11896-89

钾离子的测定-硝酸银滴定法GB11896-89
本文档将介绍钾离子测定的一种常用方法:硝酸银滴定法,该方法遵循GB11896-89标准。
下面将详细说明该方法的步骤和注意事项。
实验步骤
1.准备试样:将待测溶液取10 mL,然后用去离子水稀释至100 mL。
2.滴定仪器准备:将硝酸银标准溶液 (0.01 mol/L) 加入滴定瓶中。
3.滴定操作:将稀释后的试样溶液取10 mL,加入滴定瓶中。
使用磁力搅拌器均匀搅拌溶液。
4.滴定终点判断:在滴定过程中,溶液会由无色变为淡黄色,然后逐渐转为浑浊。
当溶液由浑浊变为浅棕色时,即为滴定终点。
5.记录滴定体积:记录滴定瓶中滴定液的滴定体积,即滴定终
点前后的差值。
注意事项
1.硝酸银溶液使用前应经过标定,确保其浓度准确无误。
2.在滴定过程中,试样溶液要充分搅拌,以确保反应充分进行。
3.滴定终点的判断需要观察溶液的颜色变化,并注意变浑浊的
程度。
4.为了获得准确的滴定结果,滴定操作应当尽量精确,滴定液
的滴定速度要适中。
以上就是钾离子测定的硝酸银滴定法的步骤和注意事项。
通过
遵循GB11896-89标准,我们可以准确测定钾离子的含量。
标定硝酸银标准溶液的方法

标定硝酸银标准溶液的方法嘿,你知道吗?标定硝酸银标准溶液那可是个超重要的事儿!咱先说说步骤哈。
首先得准备基准氯化钠,这就好比做菜得有好食材一样。
把氯化钠在高温炉里烘到恒重,哇塞,可不能马虎,这一步很关键呢!然后准确称取一定量的氯化钠,溶解在蒸馏水里。
接着用移液管吸取一定体积的氯化钠溶液,加到锥形瓶里。
再往里面加指示剂,一般用铬酸钾,那颜色变化可神奇啦!最后用待标定的硝酸银溶液滴定,直到出现砖红色沉淀。
滴定的时候一定要慢点儿,可别像个急性子似的。
注意事项也不少呢!称取氯化钠的时候得精确,不然就像做饭盐放多放少都不好吃。
滴定的时候眼睛得盯着,一不留神就过了。
还有啊,溶液的温度也得注意,不能太高也不能太低,这就跟人穿衣服似的,得合适。
安全性方面呢,硝酸银可是有腐蚀性的哦!所以操作的时候一定要小心,戴上手套、护目镜,这就像上战场得穿好盔甲一样。
要是不小心弄到手上,那可不得了,赶紧用水冲洗。
稳定性嘛,配好的溶液要放在合适的地方,不能晒太阳,不能受热,不然就像冰淇淋化了一样不好啦。
这标定硝酸银标准溶液的应用场景可多啦!在化学分析、水质检测等方面都大有用处。
比如检测水中的氯离子含量,没有它可不行。
这就好比侦探破案,硝酸银标准溶液就是那个厉害的侦探工具。
它的优势就是准确、可靠,能给我们提供准确的数据。
我给你讲个实际案例哈。
有一次在水质检测中,用标定好的硝酸银标准溶液检测水中的氯离子含量,结果非常准确,为后续的处理提供了重要依据。
这就像医生准确诊断病情,才能对症下药嘛。
总之,标定硝酸银标准溶液是个很重要的事情,一定要认真对待,这样才能得到准确可靠的结果。
如何准备和校准硝酸银标准溶液

如何准备和校准硝酸银标准溶液硝酸银标准溶液是化学实验中常用的一种试剂,它被广泛应用于定量分析、滴定等实验中。
准确制备和校准硝酸银标准溶液对于实验结果的准确性至关重要。
本文将为您介绍如何准备和校准硝酸银标准溶液。
一、实验所需材料和设备1. 硝酸银粉末(纯度不低于99.9%)2. 去离子水3. 精密电子天平4. 称量瓶5. 滴定管6. 架子和夹子7. 磁力搅拌器8. 酸碱滴定仪二、准备硝酸银标准溶液1. 称量硝酸银粉末在称量瓶上称取一定质量的硝酸银粉末,使用精密电子天平进行准确称量。
为了保证实验的准确性,可以根据需要制备不同浓度的硝酸银溶液,需根据实际需求来确定称取的质量。
2. 加入去离子水将称取好的硝酸银粉末导入干净的称量瓶中,然后加入足够的去离子水,使得硝酸银完全溶解。
在加水的过程中,使用磁力搅拌器进行搅拌,以确保硝酸银充分溶解。
3. 静置和过滤将溶液静置一段时间,待残留的杂质沉淀下来。
然后使用过滤纸或滤膜进行滤过,以去除溶液中的固体杂质。
滤液即为硝酸银标准溶液。
三、校准硝酸银标准溶液1. 准备配制的标准溶液根据实际需要,准备一定浓度的标准溶液。
可以使用已知浓度的硝酸银溶液作为标准溶液,或者根据溶液需求自行配制。
2. 滴定过程a. 将校准溶液装入滴定管中,注意排除气泡。
b. 取一定体积(通常为10mL)的硝酸银标准溶液,加入烧杯中。
c. 加入适量的氯化钠溶液,反应生成白色的沉淀。
d. 在滴定仪的控制下,滴定校准溶液,直至沉淀消失,溶液由乳白变为无色的终点。
四、计算与记录根据滴定过程中消耗的校准溶液体积,结合标准溶液的浓度,计算硝酸银标准溶液的浓度。
记录实验过程中的操作细节、使用的材料和设备、所得结果等重要数据,以备后续参考和复现实验。
五、安全注意事项1. 在制备和校准硝酸银标准溶液的过程中,需注意安全操作。
应佩戴实验室服、眼镜和手套,避免直接接触溶液和化学品。
2. 使用酸碱滴定仪等设备时,需注意其正确使用方法,以免操作失误导致实验失败或危险。
0.01mol.L-1硝酸银溶液配制和标定

0.01mol∙L-1AgNO3标准溶液的配制和标定:
(1) 配制:用洁净小烧杯称取0.43~0.45克AgNO3一份,用少量蒸馏水使之完全溶解,转移到250.00毫升棕色容量瓶中,10毫升左右蒸馏水洗涤烧杯2-3次,洗涤水全部转移至容量瓶中,然后加蒸馏水稀释到刻度线,摇匀;
(2)标定:精确称取优级纯NaCl(s)(0.006~0.008)克(记为W) (读取四位有效数字)于洁净锥形瓶中,加50毫升蒸馏水使之充分溶解,加5%K2CrO4溶液1毫升摇匀,用配制的AgNO3溶液滴定至出现微红黄色沉淀(边滴边摇动),1分钟内不褪色,即为终点,记录消耗的溶液体积V1,平行测定2~3次;
(3)按上述方法做空白样:用移液管移50毫升蒸馏水于洁净锥形瓶中,加入5%K2CrO4溶液1毫升摇匀,用配制的AgNO3溶液滴定至出现微红黄色沉淀(边滴边摇动),1分钟内不褪色,即为终点,记录消耗的溶液体积V0。
(4)计算AgNO3溶液准确浓度C
C=W
58.45×1
V1−V
×1000 (mol∙L−1)。
硝酸银标准滴定溶液

硝酸银标准滴定溶液
c(AgNO3)=0. 1 mol/L
4.21. 1 配制
称取17. 5 g硝酸银,溶于1 000 ml水中,摇匀。
溶液贮存于棕色瓶中。
4.21. 2 标定
按GB/T 9725-1988的规定测定。
其中:称取0. 22 g于500ºC --600ºC的高温炉中灼烧至恒重的工作基准试剂氯化钠,溶于70 ml水中,加10 ml淀粉溶液(10 g/l.),以216型银电极作指示电极,217型双盐桥饱和甘汞电极作参比电极,用配制好的硝酸银溶液滴定。
按GB/T 9725-1988中6. 2. 2条的规定计算V0。
硝酸银标准滴定溶液的浓度〔c(AgNO3)],数值以摩尔每升(mol/L)表示,按式(27)计算: c(AgNO3)= 1 000m / MV (27)
式中:
m:氯化钠的质量的准确数值,单位为克(g);
V:硝酸银溶液的体积的数值,单位为毫升(ml) ;
M:氯化钠的摩尔质量的数值,单位为克每摩尔(g/mol),M(NaCl) = 5 8.442。
2020版《中国药典》硝酸银滴定液配制与标定操作规程
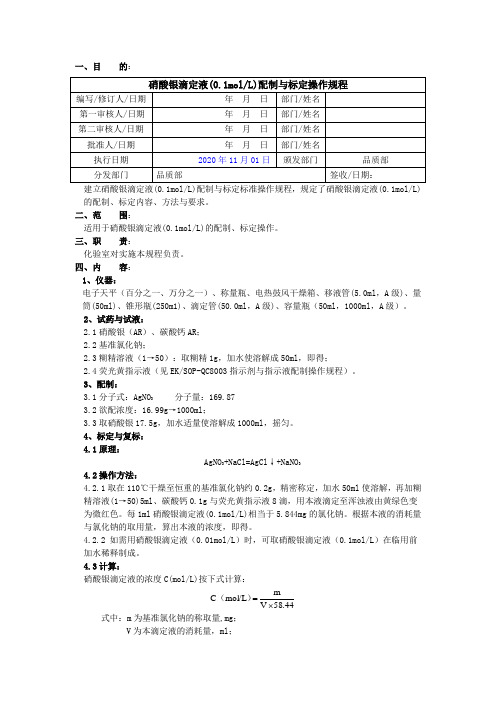
一、目 的:建立硝酸银滴定液(0.1mol/L)配制与标定标准操作规程,规定了硝酸银滴定液(0.1mol/L)的配制、标定内容、方法与要求。
二、范 围:适用于硝酸银滴定液(0.1mol/L)的配制、标定操作。
三、职 责:化验室对实施本规程负责。
四、内 容:1、仪器:电子天平(百分之一、万分之一)、称量瓶、电热鼓风干燥箱、移液管(5.0ml ,A 级)、量筒(50ml)、锥形瓶(250m1)、滴定管(50.0ml ,A 级)、容量瓶(50ml ,1000ml ,A 级)。
2、试药与试液:2.1硝酸银(AR )、碳酸钙AR ;2.2基准氯化钠;2.3糊精溶液(1→50):取糊精1g ,加水使溶解成50ml ,即得;2.4荧光黄指示液(见EK/SOP-QC8003指示剂与指示液配制操作规程)。
3、配制:3.1分子式:AgNO 3 分子量:169.873.2欲配浓度:16.99g →1000ml ;3.3取硝酸银17.5g ,加水适量使溶解成1000ml ,摇匀。
4、标定与复标:4.1原理:AgNO 3+NaCl=AgCl ↓+NaNO 34.2操作方法:4.2.1取在110℃干燥至恒重的基准氯化钠约0.2g ,精密称定,加水50ml 使溶解,再加糊精溶液(1→50)5ml 、碳酸钙0.1g 与荧光黄指示液8滴,用本液滴定至浑浊液由黄绿色变为微红色。
每1ml 硝酸银滴定液(0.1mol/L)相当于5.844mg 的氯化钠。
根据本液的消耗量与氯化钠的取用量,算出本液的浓度,即得。
4.2.2 如需用硝酸银滴定液(0.01mol/L )时,可取硝酸银滴定液(0.1mol/L )在临用前加水稀释制成。
4.3计算:硝酸银滴定液的浓度C(mol/L)按下式计算:44.58V m mol/L C ⨯=)( 式中:m 为基准氯化钠的称取量,mg ;V 为本滴定液的消耗量,ml ;58.44为与每1ml硝酸银滴定液(1.000mol/L)相当以毫克表示的氯化钠质量。
硝酸银标准溶液 标定

硝酸银标准溶液标定硝酸银标准溶液的标定。
硝酸银标准溶液是化学实验室常用的一种重要试剂,它通常用于测定氯离子的含量。
在实验中,准确标定硝酸银标准溶液的浓度是非常重要的,因为只有准确的浓度才能保证实验结果的准确性。
本文将介绍硝酸银标准溶液的标定方法,希望对大家有所帮助。
首先,准备好所需的试剂和仪器设备,包括硝酸银标准溶液、氯化钠固体、双滴定管、PH计等。
确保所有设备和试剂都处于干净整洁的状态,以避免外界因素对实验结果的影响。
接下来,进行硝酸银标准溶液的标定。
首先,取一定量的氯化钠固体溶解于适量的去离子水中,制备出氯化钠的标准溶液。
然后,用双滴定管分别取一定体积的氯化钠标准溶液和硝酸银标准溶液,滴定至沉淀终点。
在滴定的过程中,要注意控制滴液的速度,避免出现过度滴定的情况。
在滴定过程中,可以使用PH计来监测溶液的PH值,以确定滴定终点。
当溶液的PH值发生明显变化时,即可判定为滴定终点。
此时,记录下所耗硝酸银标准溶液的体积,以及滴定所用的氯化钠标准溶液的体积。
根据所耗硝酸银标准溶液的体积和氯化钠标准溶液的体积,可以计算出硝酸银标准溶液的浓度。
具体的计算公式为,C(AgNO3)=V1×C1/V2,其中C (AgNO3)为硝酸银标准溶液的浓度,V1为氯化钠标准溶液的体积,C1为氯化钠标准溶液的浓度,V2为硝酸银标准溶液的体积。
最后,对实验结果进行统计和分析,计算出硝酸银标准溶液的平均浓度,并进行误差分析。
若实验结果符合要求,即可确定硝酸银标准溶液的浓度,以备后续实验使用。
总之,硝酸银标准溶液的标定是化学实验中的一项重要工作,它直接关系到实验结果的准确性。
通过本文介绍的标定方法,相信大家对硝酸银标准溶液的标定有了更加清晰的认识,希望能够在实验中取得准确可靠的结果。
硝酸银标准溶液浓度的标定

实验十AgNO3标准溶液浓度的标定(莫尔法)此实验作为考核用1 方法提要采用莫尔法,在中性或弱碱性溶液中,以K2CrO4为指示剂,用NaCl基准试剂来标定AgNO3的浓度。
2 试剂2.1 硝酸银AgNO32.2 氯化钠NaCl:基准物质,于500~600℃下灼烧至恒重2.3 铬酸钾(K2CrO4)指示剂:50 g/L3 分析步骤3.1 硝酸银标准溶液的配制(供两人使用):0.05 mol/L 此项目15分在台秤上称取 ?g AgNO3,溶于200 mL不含氯离子的水中,将溶液转入棕色细口瓶,摇匀,置暗处保存。
3.2 氯化钠标准溶液的配制此项目25分准确称取 ?~? g NaCl基准物质于100 mL烧杯中,加适量水溶解,定量移入100mL容量瓶中,稀释至刻度,摇匀。
3.3硝酸银标准溶液的标定此项目25分准确移取25.00 mL NaCl标准溶液于250 mL锥形瓶中,加25 mL水,1 mL K2CrO4指示剂,在不断摇动下用AgNO3标准溶液滴定至溶液呈现砖红色(注意:摇动起来看到)即为终点,计算AgNO3标准溶液的浓度。
3.4 空白实验以水代替NaCl标准溶液做空白实验,V0 mL。
4 分析结果的计算此项目35分4.1 数据记录表1 AgNO3标准溶液浓度的标定1 / 2教师签字_______________ 日期:_______________4.2 按下式计算AgNO 3标准溶液的浓度: L mol V V M m c NaCl AgNO /25003-⎪⎭⎫ ⎝⎛= 式中: V ——滴定NaCl 溶液消耗的AgNO 3标准溶液的体积,mLV 0——滴定空白溶液消耗的AgNO 3标准溶液的体积,mLm -氯化钠的质量,g5 思考题(1) 用K 2CrO 4作指示剂时,其浓度太大或太小对测定有何影响?(2) 滴定过程中,为什么要充分摇动溶液?(3) 实验结束后,洗涤仪器是用自来水还是去离子水,为什么?(4)(5)(6)(7)(本资料素材和资料部分来自网络,仅供参考。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
硝酸银标准溶液的配制方法
硝酸银标准溶液是化学实验中常用的一种配制方法,用于定量分析、标定试剂以及质量控制等方面。
合理配制,在保证溶液浓度准确的情
况下,能够提高实验的可靠性和准确性。
本文将介绍硝酸银标准溶液
的配制方法。
一、实验所需材料和设备
1. 硝酸银(AgNO3):化学纯级或分析纯级。
2. 蒸馏水:纯净水或去离子水。
3. 瓶装容器:用于配制和贮存溶液的容器,最好选择特制的玻璃瓶。
4. 滴定管和容量瓶:用于准确测量和洗涤试剂。
5. 手套和护目镜:保护实验者的安全。
二、硝酸银标准溶液的配制步骤
1. 准备容器:先选择一只干净、干燥的玻璃瓶,容量最好能够容纳
所需溶液,也要确保容器没有任何污染或沉淀。
2. 确定溶液浓度:根据实验需要,确定所需硝酸银标准溶液的浓度,一般以mol/L(摩尔/升)表示。
例如,我们需要配制浓度为0.1 mol/L
的硝酸银标准溶液。
3. 称量试剂:使用称量仪器准确称取所需的硝酸银试剂质量。
根据
溶液浓度和计算公式,计算出所需的硝酸银质量。
例如,我们需要配
制500 mL的0.1 mol/L硝酸银标准溶液,根据摩尔浓度计算公式(浓度=质量/摩尔质量*体积),硝酸银的摩尔质量为169.87 g/mol,所需质量=0.1 mol/L * 169.87 g/mol * 0.5 L = 8.4935 g。
4. 溶解试剂:将准确称取的硝酸银试剂加入容器中,并用适量的蒸馏水溶解。
搅拌溶液,直到硝酸银完全溶解,并保持均匀。
5. 完善标定与质控:将配制好的硝酸银标准溶液用容量瓶转移至清洁无污染的分装容器中,并密封储存。
为了准确标定试剂,建议在配制后对标准溶液进行一次准确度校准,可以使用滴定法标定。
6. 实验安全:在配制和使用过程中,务必佩戴手套和护目镜,避免溶液对皮肤和眼睛的伤害。
注意实验室操作规范,保证自身安全。
三、注意事项
1. 实验室操作:在实验室中进行实验时,要遵循实验室的安全操作规范,确保个人安全。
2. 温度控制:在配制过程中,要控制好溶液的温度。
温度的变化会影响化学反应的速率和溶液的浓度。
3. 保质期:标准溶液在密封状态下可以保存较长的时间,但随着时间的推移,可能会出现溶液浓度的变化。
因此,建议定期检查和重新标定溶液。
总之,硝酸银标准溶液的配制是化学实验中一项重要的工作,需要严格按照浓度和配比的要求进行操作。
只有确保配制过程的准确性和
实验安全,才能获得可靠和准确的结果。
希望以上方法能对你有所帮助。
