《中华人民共与国药典》四部 通则0921崩解时限检查法
0101片剂(2020版中国药典四部)

0101 片剂片剂系指原料药物或与适宜的辅料制成的圆形或异形的片状固体制剂。
中药还有浸膏片、半浸膏片和全粉片等。
片剂以口服普通片为主,另有含片、舌下片、口腔贴片、咀嚼片、分散片、可溶片、泡腾片、阴道片、阴道泡腾片、缓释片、控释片、肠溶片与口崩片等。
含片系指含于口腔中缓慢溶化产生局部或全身作用的片剂。
含片中的原料药物一般是易溶性的,主要起局部消炎、杀菌、收敛、止痛或局部麻醉等作用。
舌下片系指置于舌下能迅速溶化,药物经舌下黏膜吸收发挥全身作用的片剂。
舌下片中的原料药物应易于直接吸收,主要适用于急症的治疗。
口腔贴片系指粘贴于口腔,经黏膜吸收后起局部或全身作用的片剂。
口腔贴片应进行溶出度或释放度(通则0931) 检查。
咀嚼片系指于口腔中咀嚼后吞服的片剂。
咀嚼片一般应选择甘露醇、山梨醇、庶糖等水溶性辅料作填充剂和黏合剂。
咀嚼片的硬度应适宜。
分散片系指在水中能迅速崩解并均匀分散的片剂。
分散片中的原料药物应是难溶性的。
分散片可加水分散后口服,也可将分散片含于口中吮服或吞服。
分散片应进行溶出度(通则0931)和分散均匀性检查。
可溶片系指临用前能溶解于水的非包衣片或薄膜包衣片剂。
可溶片应溶解于水中,溶液可呈轻微乳光。
可供口服、外用、含漱等用。
泡腾片系指含有碳酸氢钠和有机酸,遇水可产生气体而呈泡腾状的片剂。
泡腾片不得直接吞服。
泡腾片中的原料药物应是易溶性的,加水产生气泡后应能溶解。
有机酸一般用枸橼酸、酒石酸、富马酸等。
阴道片与阴道泡腾片系指置于阴道内使用的片剂。
阴道片和阴道泡腾片的形状应易置于阴道内,可借助器具将其送入阴道。
阴道片在阴道内应易溶化、溶散或融化、崩解并释放药物,主要起局部消炎杀菌作用,也可给予性激素类药物。
具有局部刺激性的药物,不得制成阴道片。
阴道片应进行融变时限检查(通则0922)。
阴道泡腾片还应进行发泡量检查。
缓释片系指在规定的释放介质中缓慢地非恒速释放药物的片剂。
缓释片应符合缓释制剂的有关要求(指导原则9013)并应进行释放度(通则0931)检查。
烧杯法检查崩解时限(中药制剂检验课件)

吊篮法
三. 结果与判定
① 供试品6片,每片均能在规定的时限内全部崩解,判为符 合规定。 ② 初试结果,到规定时限后有1片不能完全崩解,另取6片复 试,各片在规定时限内均能全部崩解,仍判为符合规定。 ③ 初试结果中如有2片或2片以上不能完全崩解;或在复试结 果中有1片或1片以上不能完全崩解,即判为不符合规定
-20-
-5-
吊篮法检查崩解时限
-6-
精诚制药 本草济民
壹 掌握崩解时限测定仪的基本操作 贰 掌握崩解时限检查法-吊篮法的操作 叁 掌握崩解时限检查结果的判定
-7-
吊篮法
大多数药品的崩解时限检查采用此法。 一.仪器及试剂
升降式崩解仪
吊篮装置图
-8-
挡板结构图
吊篮法
二. 操作方法
1、仪器设置: 吊篮位置:下降时筛网距烧杯底部25mm。 水温:37℃±1℃ 水位:使吊篮上升时筛网在水面下15mm处。 挡板方向:V型槽向上。
-18-
烧杯法
仅适用于泡腾片。
一.仪器及试剂
250ml烧杯6个、温度计(分度值1℃)、水等。
-19-
烧杯法
二. 操作方法
取药片6片,分别置6个250ml烧杯(烧杯内各盛 有200ml水,水温为15~25℃)中,有许多气泡放 出,当片剂或碎片周围的气体停止逸出时,片剂应崩 解、溶解或分散在水中,无聚集的颗粒剩留,除另有 规定外,各片均应在5分钟内崩解。如有1片不能完全 崩解,应另取6片复试,均应符合规定。
2、检查意义
在一定程度上可以间接反映药品的生物利用度。
-3-
二、必备知识
3、检查原理
崩解仪、人工模拟胃肠道蠕动、规定溶剂、规定时限内能否崩解或溶散,并 全部通过筛网。
查阅并记录片剂崩解时限检查方法及标准

【主题】查阅并记录片剂崩解时限检查方法及标准一、引言在制药行业中,片剂的崩解时间是一个重要的质量指标,它直接影响着药物的有效性和安全性。
对片剂的崩解时间进行检查是非常必要的。
本文将从深度和广度方面对片剂崩解时间的检查方法及标准进行全面评估,并撰写一篇有价值的文章,以便读者能更深入地理解这一主题。
二、片剂崩解时间检查方法1. 表面法表面法是一种常用的片剂崩解时间检查方法,它通过观察片剂在模拟胃肠道中的崩解情况来判断片剂的崩解时间。
具体操作步骤为将片剂放入模拟胃肠道中,然后记录片剂开始崩解的时间点,直到完全崩解为止。
这种方法简单易行,能够直观地反映片剂的崩解情况。
2. 离体法离体法是另一种常用的片剂崩解时间检查方法,它通过使用离体器官或模拟体液来模拟人体消化道环境,观察片剂在其中的崩解情况。
离体法对片剂崩解时间的检查更加接近真实人体情况,因此具有一定的参考意义。
3. 化学分析法除了直接观察片剂的崩解情况外,化学分析法也是常用的片剂崩解时间检查方法之一。
通过测定片剂中药物成分的溶出速度和量来间接反映片剂的崩解时间。
这种方法能够更加客观地评估片剂的崩解情况,但操作过程较为复杂。
三、片剂崩解时间标准根据《药典》的规定,片剂的崩解时间应当符合相应的标准,一般来说,常用的标准包括15分钟、30分钟和60分钟。
不同类型的药物可能有不同的崩解时间标准,需要根据具体情况进行调整。
四、个人观点和理解对于片剂崩解时间的检查,我认为应该在综合考虑了表面法、离体法和化学分析法的优缺点之后,选择最适合具体情况的检查方法。
标准的制定也应该结合实际情况进行调整,以确保能够更好地评估片剂的崩解情况。
五、总结和回顾通过本文的全面评估,我们对片剂崩解时间的检查方法及标准有了更深入的了解。
在实际的生产和质量控制中,我们应该根据具体情况选择合适的检查方法和标准,并不断优化和完善这一过程。
在本文中,我们深入探讨了片剂崩解时间的检查方法及标准,并共享了个人观点和理解。
崩解时限检查法操作规程
崩解时限检查操作规程 第 1 页/共 1 页
1. 主题内容与适用范围
1.1 本规程规定了片剂崩解时限检查操作的内容与方法与要求。
1.2 本规定适用于片剂崩解时限的检查。
2. 引用标准
2.1 《中华人民共和国药典》(2010年版)二部附录
3. 简述
4.仪器与用具
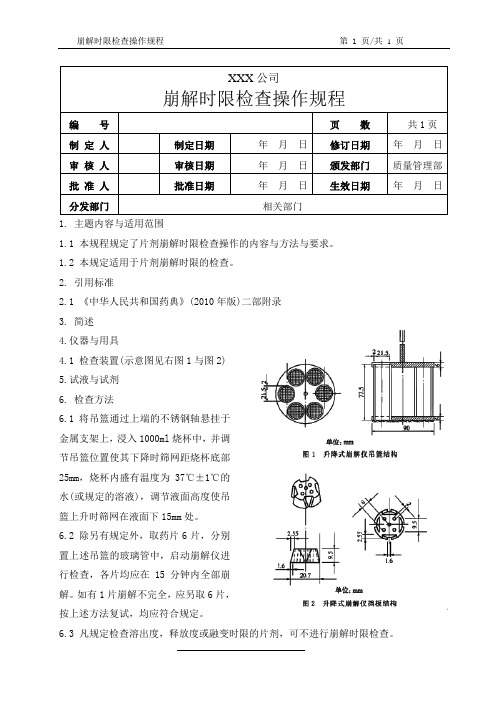
4.1 检查装置(示意图见右图1与图2)
5.试液与试剂
6. 检查方法
6.1 将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml 烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm ,烧杯内盛有温度为37℃±1℃的水(或规定的溶液),调节液面高度使吊篮上升时筛网在液面下15mm 处。
6.2 除另有规定外,取药片6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,各片均应在15分钟内全部崩解。
如有1片崩解不完全,应另取6
片,按上述方法复试,均应符合规定。
6.3 凡规定检查溶出度,释放度或融变时限的片剂,可不进行崩解时限检查。
崩解时限检查法
4.3.1硬胶囊剂或软胶囊剂 ,除另有规定外,取供试品6粒,按上述装置与方法(漂浮在液面的胶囊剂可加挡板)检查。硬胶囊剂应在30分钟内、软胶囊剂应在1小内全部崩解并通过筛网(囊壳碎片除外)。软胶囊剂可改在人工胃液中进行检查。如有1粒不能完全崩解,应另取6粒按上述方法复试,均应符合规定。
4.3.2肠溶胶囊剂,除另有规定外,取供试品6粒,按上述装置与方法(漂浮在液面的胶囊剂 可加挡板)检查。先在盐酸溶液(9→1000)中检查2小时,每粒的囊壳均不得有裂缝或崩解现象;继将吊篮取出,用少量水洗涤后,每管各加挡板一块,再按上述方法在磷酸盐缓冲液(PH6.8)中进行检查,1小内应全部崩解并通过筛网(囊壳碎片除外)。如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
文件名:崩解时限检查法
制定人:
制定日期:
分发份数:3
审核人:
审核日期:
颁发部门:GMP办
批准人:
批准日期:
生效日期:
分发至:质量保证部、质监科、质量检验中心
1.目的:规范崩解时限的检查方法,以保证检验结果的准确性。
2.范围:崩解时限的检查。
3.责任:质量保证部、质监科、质量检验中心、检验操作人员。
4.内容:
4.2.2检查法 将吊篮通过上端不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37℃±1℃的水,调节水位高度使吊篮上升时筛网在水面下15mm处。
4.2.2.1除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,药材原粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片、糖衣片各片均应在1小时内全部崩解。如有1片不能完全崩解,应另取6片复试,均应符合规定。
崩解时限检查法(通则0921)培训试题及答案

依据:中国药典分析检测技术指南(2017年7月)崩解时限检查法(通则0921)培训试题及答案2018.09姓名:成绩:一、单选题(每题4分,共24分)A、取稀盐酸16.4ml,加水约800ml与胃蛋白酶10g,摇匀后,加水稀释成1000ml,即得。
B、取稀盐酸10ml,加水约800ml与胃蛋白酶16.4g,摇匀后,加水稀释成1000ml,即得。
C、取胃蛋白酶10g,加水约800ml,摇匀后,加水稀释成1000ml,即得。
D、取稀盐酸16.4ml,加水约800ml,摇匀后,加水稀释成1000ml,即得。
2、人工肠液是:。
(B)A、稀盐酸B、磷酸盐缓冲液(含胰酶)C、胃蛋白酶水溶液D、磷酸盐缓冲液(不含胰酶)3、介质用量:调节液面高度使吊篮上升时筛网在液面下mm处。
(C)A、5B、10C、15D、20A、30℃±5℃B、30℃±2℃C、20℃±2℃D、20℃±5℃5、在测试过程中,烧杯内的水温应保持在:。
(C)A、20℃±5℃B、30℃±5℃C、37℃±1℃D、37℃±5℃6、在结果判定时,除另有规定外,如有1片(粒)不能完全崩解,应另取片(粒)复式,均应符合规定。
(D)A、3B、4C、5D、6二、多选题(每题4分,共16分)1、崩解时限记录包括:。
(ABCD)A、仪器型号、制剂类型B、测试条件C、介质配制D、崩解或溶散时间2、2015版药典规定了胶囊剂包括:。
(ABC)A、硬胶囊剂B、软胶囊剂C、肠溶胶囊剂D、滴丸剂3、2015版药典规定了片剂包括:。
(ABCD)A、口服普通片、薄膜衣片、糖衣片B、肠溶衣片、肠溶片C、含片、舌下片、可溶片D、泡腾片、口崩片4、在崩解时限检查方法与仪器发展的历史中,出现的检查方法和仪器包括:。
(ABCD)A、手工法B、吊篮式崩解仪C、介质流动的崩解仪D、溶解性总固体崩解仪三、判断题(每题4分,共20 分)1、崩解时限检查法是一项重要的常规检测方法,是注射剂质量监控的重要手段。
查阅并记录片剂崩解时限检查方法及标准

查阅并记录片剂崩解时限检查方法及标准查阅并记录片剂崩解时限检查方法及标准1. 引言片剂崩解时限检查是药品质量控制中不可或缺的一环。
正确而准确地评估片剂崩解时限可以为药品生产企业提供重要的质量保证。
在本文中,我们将深入探讨片剂崩解时限检查的方法和标准,以帮助读者更好地理解这一重要的质量控制指标。
2. 片剂崩解时限的定义和意义片剂崩解时限是指在一定的试验条件下,药物通过崩解释放活性成分所需的时间。
正确评估片剂崩解时限可以验证药物是否按照设计要求释放活性成分。
片剂崩解时限还可以衡量药物的生物利用度和治疗效果。
3. 片剂崩解时限检查方法(1)理论基础片剂崩解时限检查方法主要基于药典规定,其中包括中国药典、美国药典等。
这些药典为片剂崩解时限提供了详细的试验条件和评估指标。
(2)试验条件片剂崩解时限检查通常需要在模拟生理条件下进行。
常见的试验条件包括温度、溶液pH值、搅拌速度等。
这些条件的选择应基于药物的特性和适应对象。
(3)试验设备常用的片剂崩解时限检查设备包括崩解度仪、电子天平、恒温槽等。
这些设备可以提供稳定和准确的试验条件。
(4)试验步骤片剂崩解时限检查的试验步骤包括样品准备、试验条件设定、试验操作、数据记录等。
通过严格按照试验步骤进行操作,可以准确评估片剂崩解时限。
4. 片剂崩解时限的评估标准(1)国家标准不同国家和地区对于片剂崩解时限的评估标准可能存在差异。
中国药典对于常见药物的崩解时限给出了具体的评估标准,生产企业应根据国家标准进行评估。
(2)药企自主标准一些大型药企可能根据自身需求和技术水平制定了更为严格的片剂崩解时限评估标准。
这些标准可以更好地满足企业的质量控制需求。
5. 个人观点和理解片剂崩解时限是药品质量控制过程中非常重要的一项指标。
通过准确评估片剂崩解时限,可以保证药物的质量和疗效。
片剂崩解时限还可以为药企提供重要的质量控制数据和生产指导。
在实际操作中,我认为需灵活运用片剂崩解时限检查方法和标准。
中国药典崩解时限检查方法

中国药典崩解时限检查方法
中国药典崩解时限检查方法是用来评估药物片剂在体内溶解的速度和程度的方法。
以下是一种常用的方法:
1. 准备药物样品:根据药典规定,选择符合要求的药物样品。
2. 准备模拟胃液和模拟肠液:按照规定的配方,准备好模拟胃液和模拟肠液。
这些模拟液中含有类似于胃液和肠液的酸性和碱性成分。
3. 准备试剂和设备:准备好所需的试剂和实验设备,如玻璃容器、搅拌器等。
4. 进行崩解试验:将药物样品放入模拟胃液中,通过搅拌等方式使其充分接触。
然后,将样品转移到模拟肠液中,继续搅拌。
在一定时间内,检测药物溶解的时间和程度。
5. 分析结果:根据药典规定的崩解时限标准和药物溶解的程度,评价样品是否符合要求。
总的来说,中国药典崩解时限检查方法是通过模拟胃液和肠液中的溶解环境来评估药物片剂在体内的溶解速度和程度的方法。
这个方法的目的是确保药物在体内的溶解和吸收能够满足治疗需要,并保证药物质量的稳定性和一致性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
0921崩解时限检查法
本法系用于检查口服固体制剂在规定条件下的崩解情况.
崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶襄壳外,应全部通过筛网。
如有少量不能通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论.
除另有规定外,凡规定检查溶出度、释放度、融变时限或分散均匀性的制剂,不再进行崩解时限检查。
一、片剂
仪器装置采用升降式崩解仪,主要结构为一能升降的金属支架与下端镶有筛网的吊篮,并附有挡板。
升降的金属支架上下移动距离为55mm±2mm,往返频率为每分钟30〜32次。
(1)吊篮玻璃管6根,管长77。
5mm±2.5mm,内径21。
5mm,壁厚2mm;透明塑料板2块,直径90mm,厚6mm,板面有6个孔,孔径26mm;不锈钢板1块(放在上面一块塑料板上),直径90mm ,厚lmm,板面有6个孔,孔径22mm;不锈钢丝筛网1张(放在下面一块塑料板下),直径90mm,筛孔内径2.0mm;以及不锈钢轴1根(固定在上面一块塑料板与不锈钢板上),长80mm。
将上述玻璃管6根垂直置于2块塑料板的孔中,并用3只螺丝将不锈钢板、塑料板和不锈钢丝筛网固定,即得(图1)。
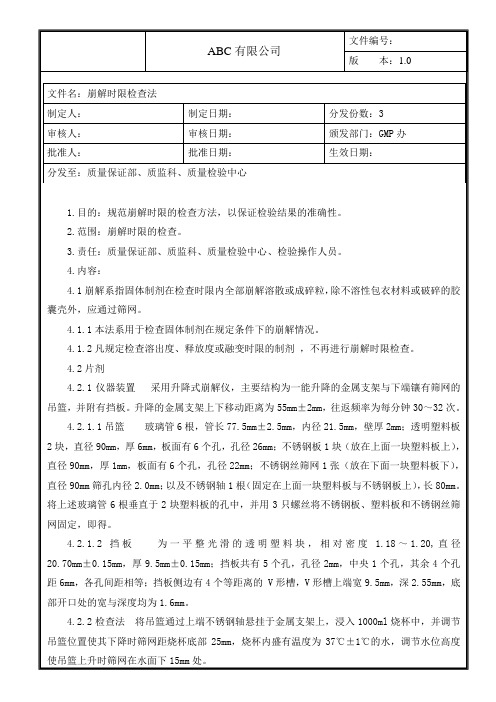
(2) 挡板为一平整光滑的透明塑料块,相对密度1.18〜1.20,直径20。
7mm±0。
15mm,厚9.5mm±0.15mm;挡板共有5个孔,孔径2mm,中央1个孔,其余4个孔距中心6rmn,
各孔间距相等;挡板侧边有4个等距离的V形槽,V形槽上端宽9.5mm,深2.55mm,
底部开口处的宽与深度均为1.6mm(图2)。
检査法将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸人1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C± 1"。
的水,调节水位高度使吊篮上升时筛网在水面下15mm处,调节吊篮顶部不可浸没于溶液中.
除另有规定外,取供试品6片,分别置上述吊篮的玻璃管中,启动崩解仪进行检查,各片均应在15分钟内全部崩解.如有1片不能完全崩解,应另取6片复试,均应符合规定。
中药浸膏片、半浸膏片和全粉片,按上述装置吊篮的玻璃管中,启动崩解仪进行检查,全粉片各片均应在30分钟内全部崩解;浸膏(半浸膏)片各片均应在1个小时内全部崩解。
如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
薄膜衣片,按上述装置与方法检査,并可改在盐酸溶液(9-1000)中进行检查,化药薄膜衣片应在30分钟内全部崩解。
中药薄膜衣片,则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
糖衣片,按上述装置与方法检查,化药糖衣片应在1个小时内全部崩解。
中药糖衣片则每管加挡板1块,各片均应在1个小时内全部崩解,如有供试品黏附挡板,应另取6片,不加挡板按上述方法检查,应符合规定。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
肠溶片,按上述装置与方法,先在盐酸溶液(9—1000)中检査2小时,每片均不得
有裂缝、崩解或软化现象;然后将吊篮取出,用少量水洗涤后,每管加人挡板1块,再按上述方法在磷酸盐缓冲液(PH6.8)中进行检查,1小时内应全部崩解。
如有1片不能完全崩解,应另取6片复试,均应符合规定.
结肠定位肠溶片,除另有规定外,按上述装置照各品种项下规定检查,各片在盐酸溶液(9→1000)及pH6.8以下的磷酸盐缓冲溶液中均应不得有裂缝、崩解或软化现象;在PH7.5~8.0的磷酸盐缓冲液中1小时内应完全崩解。
如有1片不能完全崩解,应另取6片复试,均应符合规定.
含片,除另有规定外,按上述装置和方法检査,各片均不应在10分钟内全部崩解或溶化。
如有1片不符合规定,应另取6片复试,均应符合规定。
舌下片,除另有规定外,按上述装置和方法检査,各片均应在5分钟内全部崩解并溶化。
如有1片不能完全崩解,应另取6片复试,均应符合规定.
可溶片,除另有规定外,水温为20℃±5℃,按上述装置和方法检査,各片均应在3分钟内全部崩解并溶化.如有1片不能完全崩解,应另取6片复试,均应符合规定。
泡腾片,取1片,置250ml烧杯中(内有200ml温度为20℃±5℃的水)中,即有许多气泡放出,当片剂或碎片周围的气体停止逸出时,片剂应溶解或分散在水中,无聚集的颗粒剩留。
除另有规定外,同法检查6片,各片均应在5分钟内崩解。
如有1片不能完全崩解,应另取6片复试,均应符合规定。
口崩片,除另有规定外,照下述方法检查。
仪器装置主要结构为一能升降的支架与下端镶有筛网的不锈钢管。
升降的支架上下移动距离为10mm±1mm,往返频率为每分钟30次。
崩解篮不锈钢管,管长3 0m m ,内径13. 0mm,不锈钢筛网(镶在不锈钢管底部)筛孔内径710微米(图3)。
检查法将不锈钢管固定于支架上,浸入1000ml杯中,杯内盛有温度为3 7 *C ±1*C的水约900ml,调节水位髙度使不锈钢管最低位时筛网在水面下15mm士1m m。
启动仪器。
取本品1 片,置上述不锈钢管中进行检査,应在6 0秒钟内全部崩解并通过筛网,如有少量轻质上漂或黏附于不锈钢管内壁或筛网,但无硬心者,可作符合规定论。
重复测定6片,均应符合规定。
如有1 片不符合规定,应另取6 片复试,均应符合规定。
二、胶囊剂
硬胶囊剂或软胶囊剂,除另有规定外,取供试品6粒,按片剂的装置与方法(如胶囊漂浮于液面,可加挡板)检査。
硬胶囊应在30分钟内全部崩解,软胶囊应在1小时内
全部崩解.软胶囊可改在人工胃液中进行检査。
如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
肠溶胶囊剂,除另有规定外,取供试品6粒,按上述装置与方法,先在盐酸溶液(9—1000)中不加挡板检査2小时,每粒的囊壳均不得有裂缝或崩解现象;继将吊篮取出,用少量水洗涤后,每管加人挡板,再按上述方法,改在人工肠液中进行检查,1小时内应全部崩解。
如有1粒不能完全崩解,应另取6粒复试,均应符合规定。
结肠肠溶胶囊剂,除另有规定外,取供试品6粒,按上述装置与方法,先在盐酸溶液(9—1000)中不加挡板检査2小时,每粒的囊壳均不得有裂缝或崩解现象;将吊篮取出,用少量水洗涤后,再按上述方法,在磷酸盐缓冲液(pH6。
8)中不加挡板检查3小时,每粒的囊壳均不得有裂缝或崩解现象;续将吊篮取出,用少量水洗涤后,每管加人挡板,再按上述方法,改在磷酸盐缓冲液(PH7。
8)中检查,1小时内应全部崩解。
如有1粒不能完全崩解,应另取6粒复试,均应符合规定.
三、滴丸剂
按片剂的装置,但不锈钢丝网的筛孔内径应为0。
425mm;除另有规定外,取供试品6粒,按上述方法检查,应在30分钟内全部溶散,包衣滴丸应在1小时内全部溶散。
如有1粒不能完全溶散,应另取6粒复试,均应符合规定。
以明胶为基质的滴丸,可改在人工胃液中进行检査.
【附注】
人工胃液取稀盐酸16. 4ml,加水约800ml与胃蛋白酶10g ,摇匀后,加水稀
释成1000ml,即得。
人工肠液即磷酸盐缓冲液(含胰酶)(pH 6.8)(通则8004).。
