有机化学第6章立体化学
第六章 对映异构体ppt课件

第六章 立体化学(4学时)
本章基本内容:
1.异构体分类 2.手性和对称性(旋光仪的工作原理、应用) *3.具有一个手性中心的对映异构 **4.构型和命名法 *5.具有两个手性中心的对映异构 6.手性中心的产生 7.不含手性中心化合物的对映异构
精选PPT课件
1
• 本章重点:手性和对称性的基本概念,具 有一个或多个手性碳化合物的构型和命名 法。
l:样品管长度,单位dm;
精选PPT课件
17
对映体举例
镜面
精选PPT课件
18
镜面
CH2CH3
C
H3C
Cl
H
I
CH2CH3
C
Cl
CH3
H
II
精选PPT课件
19
6.4 具有一个手性中心的对映异构
• 6.4.1手性分子的表示方法:
CH2CH3
球 棒 CH2CH3 模 型
H
H
CH3
Cl Cl
CH3
精选PPT课件
C H 3
COOH
CH2CH2CH2CH3
H C O H H3CH2CH2C C CH2CH3
CH3
CH2CH2CH2CH2CH3
精选PPT课件
单 色 光
起偏镜
样品池
检偏镜
精选PPT课件
15
旋光仪 The Polarimeter
精选PPT课件
16
比旋光度
[t
:旋光度;
cl
(+)
表示右旋, (-)
表示左旋
[]:比旋光度;
比旋光度:1mL中
t:温度;
含有1g溶质的溶液
:光波长;
放在1dm长的样品
有机化学第六章立体化学

*
*
2–溴丁烷
*
*
乳酸
*
*
1,2–环氧丙烷
柠檬油精
编辑ppt
含一个手性中 心的分子具有 一对对映体。
19
乳酸
葡萄糖发酵得到 (+)–乳酸
(-)–乳酸
mp : 26 ℃
mp : 26 ℃
(±)–乳酸
mp : 18℃ (S)-(+)-Lactic acid is the compound responsible for the burning sensation felt in muscles during anaerobic exercise,and it is also found in sour milk.
Organic Chemistry 有机化学
第六章 立体化学
编辑ppt
1
内容
立体化学(Stereochemistry) —— 以三维空间研究分子结构和性质的科学
异构体的分类
手性和对称性,对映异构,对映异构体,对称因素
手性分子的性质——光学活性:旋光性与比旋光度
具有一个手性中心的对映体,构型的表示法与标记法
编辑ppt
苏阿糖
(2S,3R)
(苏型)
29
赤型与苏型
(赤型)
(苏型)
编辑ppt
30
6.5.2 具有两个相同手性碳原子的对映异构
(I)
(II)
(III)
对映体
(苏型)
内消旋体
(meso form)
非手性分子
编辑ppt
非对映体
(I)
(III) (II)
31
思考题
这是手性分子吗?为什么? 它的反式异构体是怎样的分子? 它的手性中心的构型是什么?
有机化学习题 第六章 立体化学
第六章
立体化学
(一) 在氯丁烷和氯戊烷的所有异构体中,哪些有手性碳原子? 解:氯丁烷有四种构造异构体,其中 2-氯丁烷中有手性碳:
CH3CH2CH2CH2Cl
CH3CH2
Cl *CHCH3
CH3 CH3 C CH2 Cl CH3
生成白色沉淀。若以 Pt 为催化剂催化氢化,则(A)转变 C6H14 (B),(B)无光学活性。 试推测(A)和(B)的结构式。
H HC
解: (A)
C
CH2CH3 CH3
(B)
ቤተ መጻሕፍቲ ባይዱ
CH3CH2CHCH2 CH3 CH3
(十九)
化合物 C8H12-(A),具有光学活性。(A)在 Pt 催化下加氢生成 C8H18(B),
解:(1) Yes
构体等量混合物无旋光性
(十三)
预测
CH3CH=C=CHCH=CHCH3 有多少立体异构体,指出哪些是对映体、非对
映体和顺反异构体。 解:
CH3CH=C=CHCH=CHCH3 有四种立体异构体:
H C=C=C H3C C=C H H C=C=C C=C H CH3
(D)
H H CH3 H
(十七)
用高锰酸钾处理顺-2-丁烯,生成一个熔点为 32℃的邻二醇,处理反-2-丁烯,生成
熔点为 19℃的邻二醇。它们都无旋光性,但 19℃的邻二醇可拆分为两个旋光度相等、方向相反 的邻二醇。试写出它们的结构式、标出构型以及相应的反应式。
CH3 H C=C CH3
解:
H CH3
KMnO4 H+
H H
《有机化学(第二版)》第6章:立体化学基础

第六章
立体化学基础
19:21
第一节 顺反异构 一、顺式和反式 二、Z—型和E—型 三、顺反异构的性质
19:21
第一节 顺反异构
1、 顺反异构
重点介绍顺反异构体的Z/E标记法。 哪些化合物存在顺反异构体:
(1). 含有 C =C 、 C =N 、 N =N 双键的化合物。
(2). 环状化合物。
顺反异构现象。
顺反异构体的命名方法: 1. 顺/反标记法:
相同的原子或基团位于双键(或环平面)的同侧为“顺 式”; 否则为“反式”。
a C=C b b b a a C=C a b b b b a a a
19:21
b a
_ 顺式 (cis )
_ 反式 (trans )
_ 顺式 (cis )
_ 反式 (trans )
2. Z / E标记法:
该法是1968年IUPAC规定的系统命名法。
规定按“次序规则”,若优先基团位于双键的同侧为 Z
式(德文Zusammen的缩写,中文意为‘在一起’);否
a C=C b (Z)
c d
a c
b d
a C=C b (E)
d c
19:21
应用举例: 含C=C双键的化合物:
H Cl _ C=C H Cl H Cl C=C Cl H
翻 转
CO O H HO H C H3
翻 转
(2) 可以旋转n180。(n>=1),但不能旋转90。或270。。
19:21
CO O H H OH C H3
旋 转180
C H3 。 HO H CO O H
19:21
旋转180 。
CO O H H OH C H3
有机化学上第六章-立体化学

第三十四页,共63页。
注意
• 外消旋体与内消旋体都没有旋光性,但 它们有本质的不同:
• 外消旋体是等量左旋体和右旋体的混合 物,可拆分;
• 内消旋体是分子内有对称面的单一化合 物,不可拆分。
第三十五页,共63页。
(六) 手性中心的产生
• 〔2〕判断分子中有无对称面和对称中心 在立体化学中有重要意义。
第九页,共63页。
(三) 手性分子的性质——光学活性
光学活性:手性分子可以使平面偏振光发生偏转的性质〔旋光性〕
(1) 偏振光
• 光是一种电磁波,光波的振动方向与其前进方向垂直。
• 普通光在所有垂直于其前进方向的平面上振动。
• 偏振光——只在一个平面上振动。
手性中心的产生与手性合成有密切关系。
(1) 第一个手性中心的产生 (自学)
产 生 第 一 手 性 碳
CH3CH2CH2CH3 Cl2
CH3*CHCH2CH3 +其 他 产 物 Cl
前 手 性 碳
外 消 旋 体
当产生第一个手性中心时,两个氢原子被取代的概率
均等,生成的对映体的量相等,产物没有旋光性,是一 个外消旋体。即从非手性反响物合成手性产物时常得到 外消旋体。
HO CH3 赤式
前后
H
H3C
Cl
HO
CH3
H
赤式 前后
前后碳旋转方向不同
前后碳旋转方向相同
“苏式〞、“赤式〞的概念在研究有机反响的立体化 学关系和反响机理时常会遇到。
第三十三页,共63页。
(2) 具有两个相同手性碳原子的对映异构
酒石酸分子中含有2个*C,可能的异构体有:
有机化学中的立体化学

有机化学中的立体化学立体化学是有机化学中的重要分支,研究有机化合物中分子的空间结构和立体构型的相关规律。
随着分析仪器和实验技术的发展,立体化学在有机合成和药物研发等领域中具有重要的应用价值。
一、立体化学的基本概念立体化学关注有机分子中的空间结构和分子的各个部分的排列方式。
在立体化学中,我们关注的主要是手性和立体异构体。
1. 手性:手性是指一个分子无法与其镜像重叠的特性。
具有手性的分子称为手性分子,两个互为镜像的手性分子称为对映异构体。
例如,氨基酸和糖类等有机分子都有手性。
2. 立体异构体:立体异构体是指拥有相同分子式但不同立体结构的化合物。
立体异构体分为构象异构体和对映异构体两种。
构象异构体是由于分子的旋转或扭曲而产生的不同构型,它们在空间结构上有一定的自由度。
例如,环状化合物的立体异构体就是构象异构体,如环己烷的椅式和船式异构体。
对映异构体是由于分子的立体中心存在不对称而产生的异构体。
对映异构体在物理和化学性质上通常非常相似,但与其他对映异构体之间的相互作用却往往存在巨大差异。
拥有对映异构体的有机分子是手性分子,也是立体化学中研究的重点。
二、立体化学的研究方法立体化学的研究方法主要包括实验方法和理论方法。
实验方法主要包括X射线衍射、核磁共振(NMR)光谱、圆二色光谱、旋光度测量和质谱等技术。
这些技术通过测量和分析分子的物理性质来确定其立体结构,为揭示分子构形提供了重要的实验依据。
理论方法主要包括量子化学、分子力学和分子动力学等。
量子化学通过计算分子在不同构型下的能量和性质来预测和解释分子的立体结构、反应机理和性质。
分子力学和分子动力学通过计算机模拟方法模拟和预测分子的构型和动态行为。
三、立体化学的应用立体化学广泛应用于有机合成、药物研发和生物化学等领域,并取得了重要的研究成果。
1. 有机合成:立体化学对于有机合成的研究具有重要的指导意义。
在合成有机化合物的过程中,了解分子的立体结构能够预测和解释反应的立体选择性和对称性。
第六章 立体化学

不具有上述任何一种对称元素的化合物成为不对称化合 物,也就是手性化合物。 注意:1956年前,人们认为的化合物不对称性是构成对 映体的条件,事实上酒石酸就是例外。后来, R. S. Cahn 引 入手性的概念才能准确的区分化合物的不对称性。
有机化学中使用的最多的是对称中心和对称面:
Cl
Cl C C H
平面偏振光
光是一种电磁波,它振动着前 进,振动方向垂直于前进方向。普 通光在所有可能的平面上振动。
普通光
如果使单色光通过Nicol 棱镜 ,只有同棱镜晶轴平行的平面上振 动的光线才可以通过棱镜,因此通 过这种棱镜的光线就只在一个平面 上振动,这种光就是平面偏振光。
平面偏振光
旋光仪示意图 在盛液管中放入旋 光性物质后,偏振光将发生 偏转。能使偏振光向右旋转的,称为右旋化合物,用 (+) 表示; 能使偏振光向左旋转的,称为左旋化合物 ,用(-) 表示。
第六章 立体化学
一、手性和对称性 二、具有一个手性中心的对映异构 三、 构型和命名法 四、 具有两个手性中心的对映异构 五、 手性中心的产生 六、 不含手性中心化合物的对映异构
七、 立体化学的应用
一、手性和对称性
同分异构体
碳架异构
同 分 异 构 体
构造异构
位置异构
官能团异构 顺反异构
立体异构 光学异构 构象异构
偏振光旋转的角度α称为旋光度。旋光度 α与盛液管的长度、溶液的浓度、光源的波长 、测定时的温度、所用的溶剂的关系。通常用 比旋光度[α]来表示物质的旋光属性。公式如 下:
t
B l
α: 旋光仪的旋光度 ρB: 质量浓度(g/ml) l: 盛液管的长度 Tt: 测定时的温度 λ: 光源的波长
有机化学立体化学课件
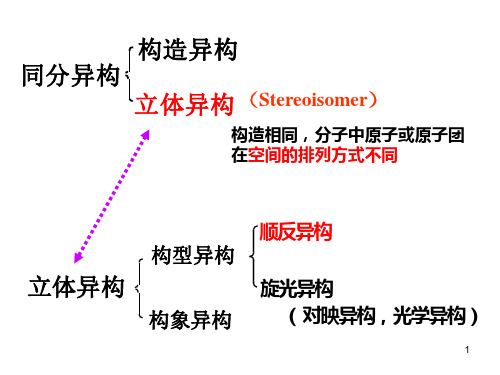
(c)和(d)之间是何种关系?
30
将 (d) 在纸平面上旋转180,就和 (c) 完全相同。
CCOOOOHH
COCOOHOH
COOH
HH OOHH HHOO H H
H OH H
HHO OHH
HHO OHH
H OH H
CCOOOOHH
COCOOHOH
COOH
(c)
(d)
象 (c) 这种构型的分子, 虽然有两个手性中心, 但作 为分子整体来说是非手性的。 (c) 称为内消旋化合 物 (meso compound)。
8
问题:下列化合物哪些含手性碳原子?
1. CH3CHCH2CH3
*CH3
2.CH3CHClCH2CH3
**
3. CH3-CH-CH-CH2CH3 OH OH
有对称因素的分
有手性碳就一定有手性吗?
子没有手性
三、对称面和非手性分子
有对称面的分子与它的镜像能重合,因此没有对 映异构现象,称为非手性分子
对称因素
透视式是书写立体结构式常见的方法之一。
应注意它的书写方法,通常实线 “” 代表位 于纸平面上的键;虚线 “ ” (或“ ”) 代表 伸向纸平面后方的键,楔形线 “ ” 代表伸 向纸平面前方的键。
CO2H
CO2H
Cl
Cl
CH HC
I C Br Br C I
H3C OH
HO
CH3
H
H
13
(三) 费歇尔投影式 横前竖后
纯液体为密度 通常还要注明溶剂
比例常数 [α] 称为比旋光度。它是单位长度和单 位浓度下的旋光度。
如:[α]D20 = +98.3o (C, 0.05, CH3OH)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
型为R(R是拉丁文Rectus的字头,是右的意思),若是反时
针方向,则构型为S(Sinister,左的意思)。
快速判断Fischer投影式构型的方法:概括地说,“横变竖不变” 1°当最小基团位于横线时,若其余三个基团由大→中→小为顺时针方向,
则此投影式的构型为S,反之为R。
2°当最小基团位于竖线时,若其余三个基团由大→中→小为顺时针方向, 则此投影式的构型为R,反之为S。 实例:
小结:
1、如何判断一个分子是手性分子 2、对称因素手性分子对映体外消旋体内消旋体 旋光性之间的关系,它们的性质是否相同。 3、旋光度的概念,比旋光度的意义。
4、菲舍尔投影式、透视式的书写及相互转换。
5、用D/L和R/S标记法命名 作业:1(2,3)、2(2)、4(1,2)、6(1,2,3,4)、11 预习:第7章 卤代烃
6.4几类常见类型有机物的对映异构和非对映异构
6.4.1含一个手性碳原子化合物的对映异构
•6.4.1.1对映体
对映体——互为物体与镜象关系的立体异构体 对映异构体都有旋光性,其中一个是左旋的, 一个是右旋的。所以对映异构体又称为旋光异构体。
对映体之间的异同点:
(1)、物理性质和化学性质一般都相同,比旋光度的 数值相等,仅旋光方向相反。 (2)、在手性环境条件下,对映体会表现出某些不同 的性质,如反应速度有差异,生理作用的不同等。
非手性分子:不具有手性的分子称为非手性分子。
手性碳:连有四个不同基团的碳原子
6.2.2对称因素 •6.2.2.1对称轴
Cn的对称操作是旋转
•6.2.2.2对称面
对称面的对称操作是反映(即照镜子) 具有对称面的分子是非手性分子。
6.2.2.3对称中心
对称中心的对称操作是反演。有对称中心的分子无手性。
做左旋物质,用“ι”或“-”表示左旋。
一个手性分子和其镜像称做一对对映体。一对对映体的 旋光能力是相同的,但旋光方向是相反的。一个是右旋, 另一个是左旋。 影响旋光度的因素:(a)被测物质; (b) 溶液的浓度;
(c) 盛液管长度; (d) 测定温度; (e) 所用光的波长。
因此不能做为一个特定的物理常数。
具有旋光性的物质称为旋光性物质(也称为光活性物质)。
结论: 物质有两类: (1)旋光性物质——能使偏振光振动面旋转的性质, 叫做旋光性;具有旋光性的物质,叫做旋光性物质。 (2)非旋光性物质——不具有旋光性的物质,叫做
非旋光性物质。
(3)凡是手性分子都具有旋光性;非手性分子则没 有旋光性
旋光度:旋光性物质使偏振光偏振面旋转的角度,称为 旋光度,以“”表示。 旋光方向:有的旋光性物质能使偏振光偏振面向右旋转 (顺时针),这种物质称做右旋物质,用“d”或“+”表示 右旋。能使偏振光偏振面向左旋转(逆时针)的物质称
•6.3.2旋光仪与比旋光度 •6.3.2.1旋光仪
6.3.2.2比旋光度
将可变因素固定后测得的旋光度才是物质的特征常数
叫比旋光度。 比旋光度:表示化合物旋光性的物理常数,物理意义指在 10cm长的样品池中,浓度为1g/ml化合物的旋光度。化
合物不同,比旋光度也不同。当溶剂、t、 固定时,比
旋光度只与物质的结构有关,可做为物质特定的物理常
投影原则:
a.横、竖两条直线的交叉点代表手性
碳原子,位于纸平面。 b.横线表示与C*相连的两个键指向纸
平面的前面,竖线表示指向纸平面的
后面。 c.将含有碳原子的基团写在竖线上,
编号最小的碳原子写在竖线上端。
使用费歇尔投影式应注意的问题:
a.基团的位置关系是“横前竖后” b.不能离开纸平面翻转180°;也不能在纸平面上旋转90° 或270°与原构型相反。 c.将投影式在纸平面上旋转180°,仍为原构型。
第6章
主要内容 6.1同分异构现象
立体化学
6.2分子的手性和对称因素
6.3物质的旋光性 6.4几类常见类型有机物的对映异构和非对映异构 6.5旋光异构体的性质
6.1同分异构现象
对映异构:
•6.2分子的手性和对称因素
6.2.1分子的手性
手性(chirality):实物和其镜像 不能重叠的现象
手性分子:与其镜像不能重迭的化合物 分子叫手性分子
若手性碳组成相同,数目有所减少。
3.观察分子的有无对称性 若分子含有对称面或对称中心,为非手性分子
课堂作业:判断下列化合物是同一物还是对映体或非对映体,
•6.5旋光异构体的性质
1.相同的非手性条件下,旋光异构体的物理性质与化学性质相同
2.旋光异构体在手性条件下(如手性试剂、手性催化剂等) 其反应速率不同。
非对映异构体的特征:
1° 物理性质不同(熔点、沸点、溶解度等)。 2° 比旋光度不同。 3° 旋光方向可能相同也可能不同。 4° 化学性质相似,但反应速度有差异。
•6.4.3.2含两个相同手性碳原子的化合物
内消旋体(meso):分子Fra bibliotek部形成对映两半的化合物。(有平面
对称因数,对称中心)。
内消旋体无旋光性 (两个相同取代、构型相反的手性碳原子,
处于同一分子中,旋光性抵消)。
内消旋体与外消旋体的异同: 相同点:都不旋光 不同点:内消旋体是一种纯物质,外消旋体是两个对映体的等
量混合物,可拆分开来。
内消旋体的特性: 内消旋体和左旋体、右旋体之间的关系是非对映体关系,因此, 内消旋体的物理性质与 左旋体、右旋体、外消旋体都不相同。
提问:苯、二氯甲烷均无旋光性,能否说它们也是内消旋体化
6.4.1.2外消旋体
等量的左旋体和右旋体的混合物称为外消旋体,一般用 (±)来表示。 外消旋体与对映体的比较(以乳酸为例): 旋光性 物理性质
外消旋体
对映体
不旋光
旋光(左和右)
mp
mp
18℃
53℃
6.4.2对映体构型的表示方法 •6.4.2.1构型的表示方法 (1)、立体结构式 2-丁醇
(2)Fischer投影式
结论:判别手性分子的依据 对称元素 对称面 有无 有 判断结果 分子无手性
对称中心
有
分子无手性
注意:对称轴不能做为判断分子是否具有手性的依据。
6.3物质的旋光性
6.3.1平面偏振光和物质的旋光性 •6.3.1.1平面偏振光
只在一个平面上振动的光, 称为平面偏振光。
6.3.1.2物质的旋光性
能使平面偏振光振动平面旋转的物质称为物质的旋光性,
6.4.2.2构型的标记 1. D-L标记法
CHO H OH CH2OH D-(+)-甘油醛 CHO HO H CH2OH L-()-甘油醛 CO2H H OH CH3 D-()-乳酸
2.R-S标记法 R、S命名规则: a.按次序规则将手性碳原子上的四个基团排序。 b.把排序最小的基团放在离观察者眼睛最远的位置,观察其 余三个基团由大→中→小的顺序,若是顺时针方向,则其构
•6.4.4环状化合物的立体异构
如何判断一个分子是否有手性:
1.最直接法: 画其对映体,看是否重合
2.观察有无手性碳: 若分子只含有一个手性碳,即为手性分子
分子含有二个以上手性碳,情况较为复杂
手性碳与立体异构体数目的关系: 若分子有 n 个手性碳,理论上有 2n 个立体异构体(2n / 2对 对映体。
判断不同投影式是否同一构型的方法:
a. Fischer 投影式在纸面上旋转 90°则得到另外一个异构体,
旋转 180°则构型不变。
b.离开纸平面翻转 180°则得到另一个异构体。
c.任意固定一个基团不动,依次顺时针或反时针调换另三个基
团的位置,不会改变原构型。 d.对调任意两个基团的位置,对调偶数次构型不变,对调奇数 次则为原构型的对映体。例如:
数。用[]t表示。
a :实验观察到的选光度 L : 样品管长度(dm, 分米) c : 样品浓度(g / cm3) t :测试时温度 :波长
思考:如何确定一个活性物质是+60o的右旋体还是-300o的左旋体?
两次测定:第一次测定后,第二次测量将盛液管长度减 半获奖浓度减半。若测出的数值比第一次小,则为右旋; 比第一次大,则为左旋。
合物呢?
判断下列的阐述哪些是正确的?哪些是错误的? (1)所有手性分子都有非对映体。 (2)所有具有手性碳的化合物都是手性分子。
(3)一对对映体总有实物和镜像的关系。
(4)对映异构体可以通过单键旋转相互重合。 (5)如果一个化合物没有对称面,它必然是手性的。 (6)具有 R-构型的手性化合物必定有右旋的旋光方向。
判断下列化合物手性中心的构型:
6.4.3含两个手性碳原子化合物的对映异构
6.4.3.1含两个不同手性碳原子的化合物
对映关系: 1与2; 3与4 非对映关系: 1与3、1与4、2与3、2与4 对映异构体的数目: 含n个不同手性碳原子的化合物,对映体的数目有2n个,外消旋体的数目2n-1 个。 非对映体: 不呈物体与镜象关系的立体异构体叫做非对映体。分子中有两个以上手性 中 心时,就有非对映异构现象。
