腺病毒的包装步骤 自己总结 很详细
病毒包装实验整体流程及原理

病毒感染细胞实验整体流程及原理目的基因不能直接整合到大多数真核细胞,常用的手段是将目的基因包装成病毒来感染细胞,从而得到表达满足实验需求。
1、病毒的种类病毒有很多种,常见的有慢病毒和腺病毒1.1慢病毒1.1.1原理慢病毒(Lentivirus)是逆转录病毒的一种。
构建的siRNA / miRNA慢病毒载体,与化学合成的siRNA 和基于瞬时表达载体构建的普通siRNA 载体相比,一方面可以扩增替代瞬时表达载体使用,另一方面,Lentivirus-siRNA 克隆经过慢病毒包装系统包装后,可用于感染依靠传统转染试剂难于转染的细胞系如原代细胞、悬浮细胞和处于非分裂状态的细胞,并且在感染后可以整合到受感染细胞的基因组,进行长时间的稳定表达。
1.1.2特点1)直接包装成为假病毒颗粒,对分裂和非分裂细胞均有感染作用,适合RNAi 研究和体内实验中难以转染的细胞(比如神经元细胞、干细胞或其它原代细胞)。
2)可以通过简单方式,在短时间内获得稳定表达特定基因的多种细胞株。
3)可用于基因敲除、基因治疗和转基因动物研究。
4)无需任何转染试剂,操作简便。
5)可以根据客户需要制备多种标记。
1.1.3慢病毒包装简要流程:1)含有目的基因的慢病毒RNAi 干扰载体的构建和质粒纯化提取。
2)慢病毒载体,包装系统共转染病毒包装细胞293T等。
3)培养48hrs - 72hrs 左右,收集含有病毒的上清培养液。
4)病毒的纯化和浓缩。
5)分装、- 80 ℃保存。
6)滴度测定目的基因检定,并出具检测报告。
1.2、腺病毒1.2.1原理腺病毒(Adenovirus,Ad)是一种无包膜的线状双链DNA病毒,其复制不依赖于宿主细胞的分裂。
有近50个血清型,大多数Ad载体都是基于血清型2和5,通过转基因的方式取代E1和E3基因,降低病毒的复制能力。
这些重组病毒仅在高水平表达E1和E3基因的细胞中复制,因此是一种适用于治疗的高效控制系统。
1.2.2特点1)几乎可以感染所有类型的细胞2)可以获得复制缺陷型(E1 和E3 缺失) 的腺病毒3)病毒滴度高,产生病毒经过浓缩后可以达到1012 PFU/mL,能有效的进行增殖。
病毒包装相关资料docsiRNA化学合成

(1)转染范围广,可以感染各种细胞类型,如淋巴细胞或肝细胞、肌细胞等;
(2)转入的外源基因可完全整合;
(3)对细胞感染率高,到达100%;
(4)感染细胞不发生病变,可树立细胞系临时继续表达外源基因。
逆转录病毒载体的缺乏之处,如:
(1)只能整合至分裂期细胞;
(2)可拔出外源基因片断小〔<10kb〕,难以满足较大基因的拔出;
1)重组后的慢病毒载体质粒以及测序图谱。
2)产品无菌检测结果。
3)慢病毒储液及相应的病毒滴度。
我们保证:1)制备的病毒颗粒携带片段的正确性2)病毒颗粒的总数和病毒滴度:如无特殊要求我们提供1mL滴度为1×107-1×108/mL的病毒储液。
3.3其他类型病毒载体包装
病毒包装的siRNA基因能否对目的靶基因停止有效基因缄默,依赖于外源基因在受体中高效、动摇的表达,而这在很大水平上取决所采用的载体系统。
与其他载体病毒相比,腺相关病毒的特点:
(1)AAV无致病性,并且在受染体上不会引发免疫反响;
(2)宿主范围广,并可感染非分裂细胞;
(3)AAV载体可将外源基因定点整合到人类19号染色体长臂,基因表达动摇;
(4)AAV是一种无包膜病毒,对各种理化处置动摇,易于分别纯化。
腺相关病毒也有一些缺陷,如病毒滴度低,感染效率低,外源基因容量小及病毒对细胞毒性。
3.1.2原理:
腺病毒(Adenovirus,Ad)是一种无包膜的线状双链DNA病毒,其复制不依赖于宿主细胞的分裂。有近50个血清型,大少数Ad载体都是基于血清型2和5,经过转基因的方式取代E1和E3基因,降低病毒的复制才干。这些重组病毒仅在高水平表达E1和E3基因的细胞中复制,因此是一种适用于治疗的高效控制系统。
轮状病毒、腺病毒二合一抗原检测试剂盒(乳胶法)说明书

轮状病毒、腺病毒抗原检测试剂盒(乳胶法)说明书【产品名称】通用名称:康珠生物轮状病毒、腺病毒抗原检测试剂盒(乳胶法)【包装规格】1人份/袋,20袋/盒。
【预期用途】本产品用于体外定性检测婴幼儿腹泻患者粪便中的A群轮状病毒和腺病毒抗原。
人类轮状病毒(Human RotaVirus,HRV)感染是婴儿和小孩重度脱水性胃肠炎最常见的原因,3月龄后的婴儿最可能发生重度腹泻和脱水,几乎所有人在其3~5岁时都感染过HRV。
轮状病毒于1973年被人类认识,Bishop等于在澳大利亚墨尔本腹泻儿童的十二指肠活检物通过电镜检出该病毒。
轮状病毒属于呼肠孤病毒科,为球型无包膜的双股RNA病毒。
腺病毒(adenovirus)是一种没有包膜的直径为70~90 nm的颗粒,由252个壳粒呈廿面体排列构成。
腺病毒是DNA 病毒,主要在细胞核内繁殖,耐温、耐酸、耐脂溶剂的能力较强,一般通过呼吸道传染。
【检验原理】本检测试纸条采用高度特异性的双抗体夹心反应原理及免疫层析分析技术,试纸卡为两窗试纸卡,在试纸卡左边的窗口的试纸条上含有被预先固定于膜上测试区(T)抗A群轮状病毒抗体和质控区(C)的羊抗鼠抗体,乳胶标记垫上包被有乳胶颗粒标记的抗A群轮状病毒单克隆抗体;右边的窗口的试纸条上含有被预先固定于膜上测试区(T)抗腺病毒抗体和质控区(C)的羊抗鼠抗体,乳胶标记垫上包被有乳胶颗粒标记的抗腺病毒单克隆抗体,测试时,标本与预包被在左边的试纸条上的乳胶颗粒标记的抗A群轮状病毒单克隆抗体(或者与预包被在右边的试纸条上的乳胶颗粒标记的抗腺病毒单克隆抗体)混合,并在毛细效应下向上层析。
如是A群轮状病毒阳性,左边试纸条上的乳胶标记抗体在层析过程中先与标本中的A群轮状病毒结合,随后结合物会与固定在膜上的抗A群轮状病毒抗体结合,在测试区(T)内会出现一条红色条带。
这条带是特异性的抗体-抗原-乳胶标记抗体复合物在膜上结合形成的。
如是阴性,则测试区(T)内将没有红色条带。
腺病毒疫苗制作流程

腺病毒疫苗制作流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!腺病毒疫苗是一种以腺病毒为载体的基因工程疫苗,其制作流程主要包括以下几个步骤:1. 腺病毒载体的构建。
病毒包装
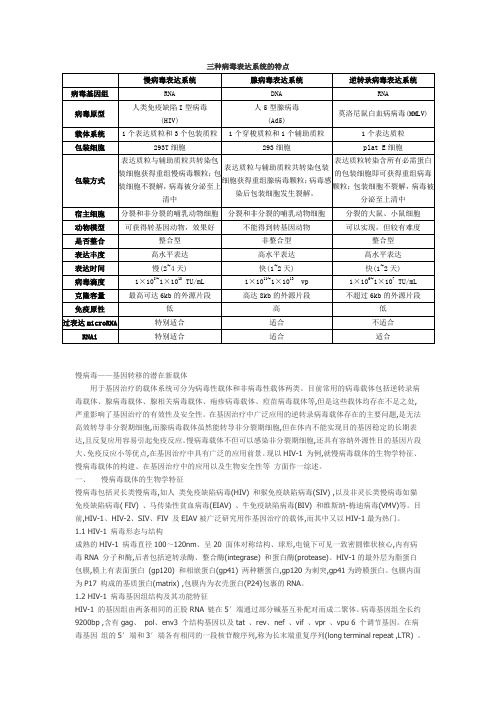
基因编码p55的蛋白前体,经蛋白酶裂解而形成病毒的核衣壳蛋白(p7) 、内膜蛋白(p17) 和衣壳蛋白(p24) 。
pol 基因编码病毒复制所需的酶类,env编码gp120 和gp41 两种包膜糖蛋白,决定病毒感染宿主的靶向性。
tat 基因编码的gp14 是一种反式激活的转录因子,与LTR 结合后能促进病毒所有基因的转录。
rev 基因编码的产物gp19 能促进未经拼接的大mRNA 分子从细胞核向胞浆转运,并相对减少拼接后小mRNA 分子的数量。
nef基因编码负调节蛋白,对病毒的结构蛋白和调节蛋白的表达均有下调作用。
vif编码产物与病毒体的感染性有关,vpu产物与病毒的装配、成熟和释放有关,而vpr编码产物的功能尚不清楚。
1.3 HIV-1 生活史HIV-1 病毒通过gp120 与宿主细胞的CD4 分子和趋化因子受体结合,然后将病毒的基因(RNA) 、蛋白及酶等释放到宿主细胞内;随后,逆转录酶将病毒RNA 转录成DNA,病毒DNA 在整合酶的作用下插入宿主细胞核的基因组中,此时的病毒DNA 也称为原病毒;紧接着,原病毒转录成mRNA ,mRNA 从细胞核进入细胞质,并利用宿主细胞的原料合成病毒的各种成分(蛋白质) ,新合成的各种蛋白、酶及RNA 等聚集在宿主细胞的膜下,病毒的包膜蛋白(gp120 ,gp41) 插入宿主细胞的细胞膜并形成一种未成熟的病毒(此时病毒无传染性) ;最后蛋白酶将病毒核心中的许多过长的蛋白及酶切短,便形成成熟的病毒。
病毒利用宿主细胞的细胞膜将自己包被起来,离开该细胞去寻找新的宿主。
1.4 慢病毒载体转导非分裂期细胞的分子机制慢病毒载体能转导非分裂期细胞,3 种分子元件决定了这种能力:MAN、IN 和vpr。
这3 类蛋白利用细胞核的输入机制,靶向作用于细胞核的前整合复合物( PIC)。
细胞核的输入系统包括: 胞质蛋白、importin-a 、importin-b 及核孔蛋白。
腺病毒载体构建的基本原理与应用

腺病毒载体构建的基本原理与应用1. 简介腺病毒(Adenovirus)是一类非常常见的病毒,它可引起呼吸道、眼部和肠道感染等问题。
在基因工程领域,腺病毒被广泛应用作为基因传递载体。
通过对腺病毒进行适当的改造,可以将外源基因有效地传递到目标细胞中,并实现基因的高表达。
本文将介绍腺病毒载体构建的基本原理以及其在实际应用中的主要用途。
2. 腺病毒载体构建的基本原理腺病毒载体构建的基本原理主要包括以下几个步骤:2.1 选择适当的腺病毒亚型腺病毒有多个亚型,其中最常用的是腺病毒2(Ad2)和腺病毒5(Ad5)。
选择适当的腺病毒亚型取决于目标细胞的特点以及需要传递的基因。
2.2 构建质粒载体构建质粒载体是腺病毒载体构建的第一步。
质粒载体通常由多个部分组成,包括腺病毒的核心序列、外源基因表达的启动子和终止子等。
通过合成或PCR扩增等方法,可以将这些部分组装到一起构建质粒载体。
2.3 建立包装细胞系在构建过程中,需要建立一个能够产生包装腺病毒的细胞系。
这些细胞系通常包括两种类型的细胞:一种是质粒携带者,将质粒转染进细胞内;另一种是包装细胞,它们能够提供所需的腺病毒包装蛋白和其他辅助蛋白。
2.4 转染质粒载体将质粒载体转染到包装细胞系中,使其进入细胞内。
转染的方法可以采用常规的化学方法,如钙磷共沉淀法或使用商业化学试剂。
2.5 腺病毒产生与包装质粒载体进入到包装细胞中后,通过转染和转座等过程,腺病毒基因组会产生复制和转录。
最终,腺病毒包装蛋白和基因组会组装成腺病毒颗粒,从而完成腺病毒载体的构建。
3. 腺病毒载体的应用腺病毒载体在基因治疗、疫苗开发、基因功能研究等方面具有广泛的应用。
以下是腺病毒载体的主要应用领域的列点介绍:•基因治疗:腺病毒载体可以用于治疗多种遗传性疾病,如囊性纤维化、遗传性视网膜疾病等。
通过将治疗基因成功地传递到患者细胞中,可以恢复或增强正常基因的功能,从而治疗相关疾病。
•疫苗开发:腺病毒载体在疫苗开发中具有重要的作用。
病毒包装原理

病毒包装原理病毒包装是指病毒在宿主细胞内的组装和释放过程。
病毒包装原理是病毒利用宿主细胞的生物合成机制来合成病毒颗粒的过程。
病毒包装是病毒生命周期中至关重要的一环,也是病毒传播和感染宿主细胞的关键步骤。
病毒包装的原理主要包括以下几个步骤,首先,病毒侵入宿主细胞后,病毒基因组会被释放出来,然后利用宿主细胞的生物合成机制来合成病毒颗粒的各种构成蛋白。
接着,这些构成蛋白会被组装成完整的病毒颗粒,然后通过宿主细胞的分泌途径释放到细胞外。
最后,这些新合成的病毒颗粒会继续感染其他宿主细胞,完成病毒的传播和复制过程。
病毒包装原理的核心是依赖于宿主细胞的生物合成机制。
病毒利用宿主细胞的蛋白质合成机器来合成自己的蛋白质,然后利用宿主细胞的组装和分泌机制来组装和释放病毒颗粒。
这种依赖性使得病毒对宿主细胞的侵染和利用变得更加有效和高效。
病毒包装原理的研究不仅有助于深入理解病毒的生命周期和传播机制,还为病毒感染的防治提供了重要的理论基础。
通过深入研究病毒包装原理,可以为病毒感染的防治提供新的思路和方法。
例如,可以针对病毒包装过程中的关键环节开发新的抗病毒药物,从而阻断病毒的传播和复制。
此外,病毒包装原理的研究还可以为病毒疫苗的研发提供重要参考,有助于加速病毒疫苗的研制和应用。
总之,病毒包装原理是病毒生命周期中至关重要的一环,其研究不仅有助于深入理解病毒的生命周期和传播机制,还为病毒感染的防治提供了重要的理论基础。
随着病毒包装原理研究的不断深入,相信将会为病毒感染的防治提供新的思路和方法,为人类健康做出更大的贡献。
腺病毒载体操作手册1407

腺病毒载体操作手册一、实验流程制备腺病毒穿梭质粒,分别高纯度无内毒素抽提腺病毒穿梭质粒和骨架质粒,共转染293A细胞,转染后6h更换为完全培养基,培养十几天,在中间四五天左右更换一次新鲜培养基,然后收集细胞和1ml培液置于15ml离心管后,液氮/37度冻融三次(冻-融要彻底),2000rpm离心5分钟,取上清即为病毒液初代原液。
连续三代反复扩增收集病毒后,行病毒的大量扩增,然后通过CsCl密度梯度离心-透析联用法纯化病毒。
二、实验材料(一)腺病毒载体、包装细胞和菌株该病毒包装系统为两质粒系统,组成为穿梭质粒(包括pHBAd-CMV-IRES-GFP,pHBAd-CMV-IRES-RFP,pHBAd-U6-GFP, pHBAd-U6-RFP)和骨架质粒pBHGlox(delta)E1,3Cre。
其中穿梭质粒pHBAd-CMV-IRES-GFP和pHBAd-U6-GFP能表达绿色荧光蛋白(GFP)。
pHBAd-CMV-IRES-RFP和pHBAd-U6-RFP能表达红色荧光蛋白(RFP)。
1、载体信息1) 腺病毒克隆载体图谱如下:各载体用途如下表:2)骨架质粒信息如下:2、细胞株293A,腺病毒的包装细胞,为贴壁依赖型成上皮样细胞,经培养生长增殖形成单层细胞,生长培养基为DMEM(含10% FBS)。
3、菌株大肠杆菌菌株DH5α。
用于扩增腺病毒载体和腺病毒骨架载体质粒。
三、包装细胞293A细胞的培养(一)293A细胞的冻存293A细胞来源于一个用作空斑测定的亚克隆,具有易使用和易转染的特性。
该细胞株对于高细胞密度很敏感,当细胞超过70%汇合时,一些细胞可能会丢失它们的表型。
若细胞密度持续在70%以下,QBI-293A细胞则能连续培养3~4个月维持原有细胞特性。
若以购买得到的293A作为第一代,则30代内能得到最佳结果。
随着传代的次数增加,293A细胞会出现生长状态下降、突变等。
为了防止此类现象的出现,我们需要在开始就对细胞进行大量冻存,以保证实验的稳定性和持续性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Adenoviruses Expression System
1、 从NCBI网站上查找相应基因(如小鼠KL14基因)的编码区,即CDS序列。
2、 根据KLF14 CDS设计相应的引物,PCR来扩增KLF14的编码序列,即KLF14的cDNA
3、 将扩增出来的cDNA序列连接到PGEM-Teasy载体,蓝白斑筛选,挑取白斑摇菌,提质
粒,EcoR I 酶切鉴定,然后送测序
4、 测序正确后用限制性内切酶把cDNA切下来连接到pcDNA3.1载体(很重要的一种表达载
体)上,做报告基因实验。
5、 双荧光报告基因检测其对下游的靶基因启动子有作用以后,用合适(HindIII和XhoI)的
限制性内切酶将连接到pcDNA3.1上的KLF14 cDNA切下来,凝胶回收,同时也切pAdTrack-
CMV 回收。把KLF14 cDNA连接到pAdTrack-CMV载体上。
6、 在包装腺病毒之前要先用western检测一下连接到pAdTrack-CMV的KLF14的cDNA能否
表达出蛋白。把第5步连接好的质粒用转染试剂转染293A细胞,然后收细胞(RAPI裂
解液,加蛋白酶抑制剂),提取蛋白,做western,杂标签抗体(Myc或Flag)。只有在
293A细胞有表达之后才可以继续包装。
7、 在第5步最好多提取一些连接好的KLF14 cDNA-CMV质粒,浓度高点。然后用PmeI酶
切,让这个质粒线性化(大概要切10ug左右,50ul的体系)。然后跑胶回收切开的质粒,
一般PmeI都可以完全切开,大概要回收3-4ug。
8、 将回收的线性化产物加入到BJ5183感受态细菌中(该细菌中已经含有pAdEasy-1质粒),
电转化让其发生重组。然后在kanamycin抗性的平板上筛选,就按一般的热激,涂板的
方法转化就可以。因为重组后的pAdTrack-CMV-KLF9+ pAdEasy-1非常大,大约41.5kb,
所以要差不多在37度细菌孵箱中生长16-20h才可以,即使长出菌落,也是非常小的那
种。非常大的菌落肯定不是重组上的。
在kanamycin抗性平板上筛选,是因为pAdTrack-CMV质粒上有Kan抗性,而pAdEasy-1
则没有任何抗性。理论上讲只有重组上的质粒才有可能在有Kan抗性的平板上长出菌落。
9、 挑取小菌落,提取质粒,然后用PacI酶切,鉴定是不是重组的质粒。
酶切鉴定时要设置两个对照,一个pAdTrack-CMV-KLF9(约11kb),另一个是pAdEasy-1
(约34.4kb),重组质粒大约41.5kb。将这三个质粒都用PacI酶切。
① pAdTrack-CMV-KLF9含有两个PacI酶切位点,会切出3kb和8kb两条带
② pAdEasy-1只含有一个PacI酶切位点,跑胶时只会有一条比较大的带34.4kb
③ 重组的质粒也有2个PacI酶切位点,切开后会有两条带,一条和①中的一样3kb左
右,另一条则是非常大的一条带,比②中的条带还大,或者差不多大
10、 鉴定正确以后,将从BJ5183菌株中提取的质粒,转化到DH5a感受态中大量扩增。
然后提取质粒,浓度也不会太高。(电转以后的BJ5183菌株不能保存菌种的)。
将提取的重组质粒用PacI切,让它线性化,一般要切10ug,50ug体系37度酶切8h以
上。然后加3倍体积的无水乙醇-80℃沉淀过夜。之后12000rpm,4℃,离心15min,
弃去上清液,再用75%的乙醇清洗一次,晾干后用ddH2O溶解,不要加水太多,然后
测回收的浓度。
11、 把回收到的线性化重组质粒用lipo2000转染293A细胞(脂质体的转染效率强),
转染的时候液体都要用无血清的DMEM培养基,转染完6h以后换液。转染的时候293A
状态要很好,密度在百分之七八十。(用细胞培养瓶,不能用培养皿)
转染之后的3-4天不要动,之后每天可以观察一次有没有出现绿的噬菌斑,在此期间不
能换液,只能一点一点的补加DMEM,直到细胞变的全部绿,有50 %左右漂。
12、等到细胞全绿以后,把培养瓶的细胞冲匀,离心,这是第一轮的病毒,利心丸的上清也
要好好保留,细胞沉淀用PBS溶,然后液氮反复冻融3次,让病毒释放。用第一轮裂解的
病毒上清感染293A得到第2轮的病毒。
