石灰石-石膏湿法烟气脱硫工艺的化学原理
石灰石石膏湿法脱硫原理 (2)

石灰石-石膏湿法烟气脱硫工艺石灰石(石灰)-石膏湿法脱硫工艺是湿法脱硫的一种,是目前世界上应用范围最广、工艺技术最成熟的标准脱硫工艺技术。
是当前国际上通行的大机组火电厂烟气脱硫的基本工艺。
它采用价廉易得的石灰石或石灰作脱硫吸收剂,石灰石经破碎磨细成粉状与水混合搅拌成吸收浆液,当采用石灰为吸收剂时,石灰粉经消化处理后加水制成吸收剂浆液。
在吸收塔内,吸收浆液与烟气接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的氧化空气进行化学反应被脱除,最终反应产物为石膏。
脱硫后的烟气经除雾器除去带出的细小液滴,经换热器加热升温后排入烟囱。
脱硫石膏浆经脱水装置脱水后回收。
由于吸收浆液循环利用,脱硫吸收剂的利用率很高。
最初这一技术是为发电容量在100MW以上、要求脱硫效率较高的矿物燃料发电设备配套的,但近几年来,这一脱硫工艺也在工业锅炉和垃圾电站上得到了应用.根据美国EPRI统计,目前已经开发的脱硫工艺大约有近百种,但真正实现工业应用的仅10多种。
已经投运或正在计划建设的脱硫系统中,湿法烟气脱硫技术占80%左右。
在湿法烟气脱硫技术中,石灰石/石灰—石膏湿法烟气脱流技术是最主要的技术,其优点是:1、技术成熟,脱硫效率高,可达95%以上。
2、原料来源广泛、易取得、价格优惠3、大型化技术成熟,容量可大可小,应用范围广4、系统运行稳定,变负荷运行特性优良5、副产品可充分利用,是良好的建筑材料6、只有少量的废物排放,并且可实现无废物排放7、技术进步快。
石灰石/石灰—石膏湿法烟气脱硫工艺,一般布置在锅炉除尘器后尾部烟道,主要有:工艺系统、DCS控制系统、电气系统三个分统。
基本工艺过程在石灰石一石膏湿法烟气脱硫工艺中,俘获二氧化硫(SO2)的基本工艺过程:烟气进入吸收塔后,与吸收剂浆液接触、进行物理、化学反应,最后产生固化二氧化硫的石膏副产品。
基本工艺过程为:(1)气态SO2与吸收浆液混合、溶解(2) SO2进行反应生成亚硫根(3)亚硫根氧化生成硫酸根(4)硫酸根与吸收剂反应生成硫酸盐(5)硫酸盐从吸收剂中分离用石灰石作吸收剂时,SO2在吸收塔中转化,其反应简式式如下: CaCO3+2 SO2+H2O ←→Ca(HSO3)2+CO2在此,含CaCO3的浆液被称为洗涤悬浮液,它从吸收塔的上部喷入到烟气中。
石灰石-石膏湿法烟气脱硫废水处理技术探讨

石灰石-石膏湿法烟气脱硫废水处理技术探讨摘要:石灰石-石膏湿法烟气脱硫技术以其技术成熟、使用煤种广、脱硫效率高和对机组的适应性好而成为应用最为广泛的脱硫技术。
但是石灰石-石膏湿法脱硫技术不可避免的会有脱硫废水产生,由于该废水性质较特殊,与电厂的其他废水性质差别较大,如何对这些脱硫废水进行经济有效地处理以及如何回用,成为了一道难题。
关键词:石膏湿法;烟气脱硫;废水处理技术1脱硫废水水质特点pH值较低(一般为4~6);悬浮物含量很高,质量浓度可达几万mg/L;氟化物、COD和重金属超标,其中包括我国严格限制排放的第1类污染物,如Hg、As、Pb等;盐分极高,含有大量的Cl_、SO42-等离子,其中Cl_的质量分数可达到0.04左右,远大于标准海水的Cl_质量分数。
脱硫废水的具体水质与燃煤的种类、电除尘器的极数、脱硫工艺用水的水质情况等因素有关。
2石灰石-石膏湿法烟气脱硫废水处理技术的原理在石灰石-石膏湿法烟气脱硫废水处理技术中脱硫废水的液体是呈酸性的,主要是利用物理和化学沉淀物质和分离重金属的机械方法来进行污染物脱硫废水处理。
通过对脱硫废水的水质特点进行研究分析,可以确定石灰石-石膏湿法烟气脱硫废水处理技术是由中和、沉淀、絮凝及澄清等工艺技术组成的,在对废水进行脱硫处理时,先要将氢氧化钠加入到废水中,使废水中的金属离子发生化学反应,生成氢氧化物沉淀,再在废水中加入有机硫溶液,形成硫化物沉淀,在加入絮凝剂之后,这些絮体会发挥出吸附功能,在硫化物沉淀的过程中,可以将这些沉淀进行吸附,为增大絮体的体积,可再往废水中加入絮凝助剂,减少细小絮体的残留,加快沉淀速度,将废水进行分离沉淀达到标准之后再排放。
3我国脱硫废水常规处理方法3.1排至水力除灰系统这种处理方式只适用于存在水力除灰系统的电厂,其基本原理是将脱硫废水不进行处理直接排放至水力除灰系统,废水中的酸性物质和重金属离子跟石灰中的CaO发生反应,生成固体物质而被去除。
石灰石-石膏湿法烟气脱硫原理及工艺流程

石灰石-石膏湿法烟气脱硫原理及工艺流程摘要:文中主要对目前火力发电厂普遍使用的石灰石-石膏湿法烟气脱硫工艺的化学反应原理及工艺流程进行了阐述。
为运行及检修提供理论基础。
关键词:火力发电厂石膏湿法烟气脱硫目前,我国的电力供应仍以燃煤的火力发电厂为主,并因此产生的大量SO2的排放而产生的酸雨对我国的生态环境造成了极大的危害,因此,减少SO2的排放是我国大气治理的一个重要方面。
当前,我国火力发电厂减少SO2排放主要采用的为烟气脱硫技术,其中石灰石—石膏湿法FGD技术由于最为成熟、可靠而被广泛采用。
一、石灰石-石膏湿法烟气脱硫工艺介绍石灰石-石膏湿法烟气脱硫工艺属于煤燃烧后脱硫,脱硫系统位于除尘器之后,脱硫过程在溶液中进行,脱硫剂及脱硫生成物均为湿态,脱硫过程的反应温度低于露点,故脱硫后的烟气一般需要经再加热后排出,或提高烟囱的防腐等级。
1 工艺流程介绍其工艺流程为:从锅炉出来的烟气首先经过电除尘器进行除尘,去除烟气中的大部分粉尘颗粒,经除尘后的烟气进入到吸收塔中,同时,浆液循环泵由吸收塔下部抽取浆液并提升到一定高度后,通过喷淋层内设置的喷嘴喷射到吸收塔中。
在吸收塔内烟气向上流动,浆液向下流动,两种物料在吸收塔内进行逆流接触混合,此时,SO2与浆液中的碳酸钙相接触,在空气作用下进行化学反应,并最终形成石膏(CaSO4•2H2O)。
为保证有足量空气使亚硫酸根离子的充分氧化,还需设置氧化风机进行强制氧化。
整个过程中,吸收塔内浆液被循环泵连续不断的向上输送到喷淋层,浆液通过喷嘴喷出,在喷嘴的雾化作用下,气液两相物质充分混合。
每个循环泵与各自的喷淋层相连接,形成多层浆液喷嘴,根据锅炉烟气量及烟气含硫量开启相应的喷嘴层数。
随着烟气中SO2的不断被吸收,在吸收塔中不断的产生石膏,因此必须将石膏排出,以维持物料平衡,故在吸收塔底部设置石膏浆液泵,将二氧化硫与石灰石浆液反应生成的石膏浆液输送至石膏脱水系统,形成可被利用的工业石膏。
石灰石—石膏湿法 烟气脱硫工艺影响因素

石灰石—石膏湿法烟气脱硫工艺的影响因素分析摘要:本文主要讲述了工业石灰石—石膏湿法低浓度二氧化硫烟气脱硫工艺的影响因素分析,通过对石灰石—石膏法分析开辟了新运用前景。
0前言二氧化硫是主要大气污染物之一,严重影响环境,威胁人们的生活健康。
削减二氧化硫的排放量,保护大气环境质量,是目前及未来相当长时间内我国环境保护的重要课题之一。
目前,国内外处理低浓度SO2烟气的方法有许多,钙法是采用石灰石水或石灰石乳洗涤含二氧化硫的烟气,技术成熟,生产成本低,但吸收速率慢、吸收能力小、装置运行周期短。
针对传统脱硫方法存在的缺陷,本文阐述了主要钙法在处理低浓度二氧化硫烟气脱硫工艺的影响因素分析,这些影响因素分析解决资源合理利用问题。
获得了良好的社会效益和经济效益。
1常用湿法烟气脱硫技术介绍1.1石灰石—石膏湿法烟气脱硫工艺原理该法是将石灰石粉磨成小于250目的细粉,配成料浆作SO2吸收剂。
在吸收塔中,烟气与石灰石浆并流而下,烟气中的SO2与石灰石发生化学反应生成亚硫酸钙和硫酸钙,在吸收塔低槽内鼓入大量空气,使亚硫酸钙氧化成硫酸钙,结晶分离得副产品石膏。
因此过程主要分为吸收和氧化两个步骤:(1)SO2的吸收石灰石料降在吸收塔内生成石膏降,主要反应如下:CaCO3+SO2+1/2H2O=CaSO3·1/2H2O+CO2CaSO3·1/2H2O +SO2+1/2H2O=Ca(HSO3)2(2)亚硫酸钙氧化由于烟气中含有O2,因此在吸收过程中会有氧化副反应发生。
在氧化过程中,主要是将吸收过程中所生成的CaSO3·1/2H2O氧化生成CaSO4·2H2O。
2CaSO3·1/2H2O+ O2+3H2O =2CaSO4·2H2O由于在吸收过程中生成了部分Ca(HSO3)2,在氧化过程中,亚硫酸氢钙也被氧化,分解出少量的SO2:Ca(HSO3)2+1/2O2+ H2O=CaSO4·2H2O+ SO2亚硫酸钙氧化时,其离子反应可表达为:CaSO3·1/2H2O+H+ Ca2++ HSO3—+1/2H2OHSO3—+1/2O2 SO42—+H+Ca2++ SO42—+2H2O CaSO4·2H2O由以上反应可见,氧化反应必须有H+存在,浆液的PH值在6以上时,反应就不能进行。
石灰石-石膏湿法脱硫技术的工艺流程、反应原理及主要系统
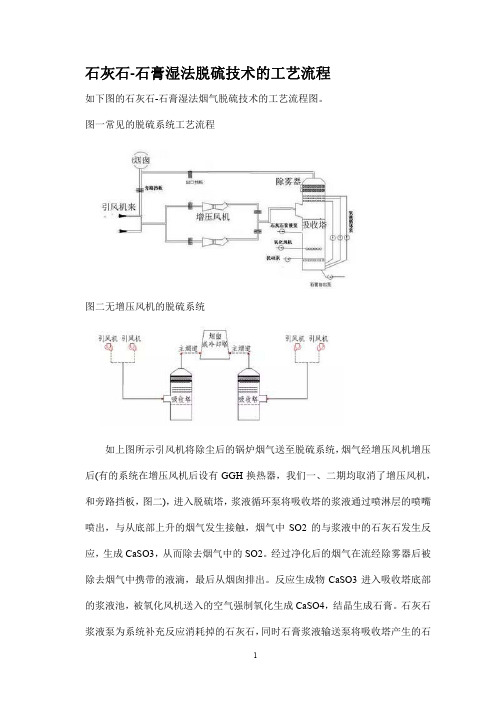
石灰石-石膏湿法脱硫技术的工艺流程如下图的石灰石-石膏湿法烟气脱硫技术的工艺流程图。
图一常见的脱硫系统工艺流程图二无增压风机的脱硫系统如上图所示引风机将除尘后的锅炉烟气送至脱硫系统,烟气经增压风机增压后(有的系统在增压风机后设有GGH换热器,我们一、二期均取消了增压风机,和旁路挡板,图二),进入脱硫塔,浆液循环泵将吸收塔的浆液通过喷淋层的喷嘴喷出,与从底部上升的烟气发生接触,烟气中SO2的与浆液中的石灰石发生反应,生成CaSO3,从而除去烟气中的SO2。
经过净化后的烟气在流经除雾器后被除去烟气中携带的液滴,最后从烟囱排出。
反应生成物CaSO3进入吸收塔底部的浆液池,被氧化风机送入的空气强制氧化生成CaSO4,结晶生成石膏。
石灰石浆液泵为系统补充反应消耗掉的石灰石,同时石膏浆液输送泵将吸收塔产生的石膏外排至石膏脱水系统将石膏脱水或直接抛弃。
同时为了防止吸收塔内浆液沉淀在底部设有浆液搅拌系统,一期采用扰动泵,二期采用搅拌器。
石灰石-石膏湿法脱硫反应原理在烟气脱硫过程中,物理反应和化学反应的过程相对复杂,吸收塔由吸收区、氧化区和结晶区三部分组成,在吸收塔浆池(氧化区和结晶区组成)和吸收区,不同的层存在不同的边界条件,现将最重要的物理和化学过程原理描述如下:(1)SO2溶于液体在吸收区,烟气和液体强烈接触,传质在接触面发生,烟气中的SO2溶解并转化成亚硫酸。
SO2+H2O<===>H2SO3除了SO2外烟气中的其他酸性成份,如HCL和HF也被喷入烟气中的浆液脱除。
装置脱硫效率受如下因素影响,烟气与液体接触程度,液气比、雾滴大小、SO2含量、PH值、在吸收区的相对速度和接触时间。
(2)酸的离解当SO2溶解时,产生亚硫酸,同时根据PH值离解:H2SO3<===>H++HSO3-对低pH值HSO3-<===>H++SO32-对高pH值从烟气中洗涤下来的HCL和HF,也同时离解:HCl<===>H++Cl-F<===>H++F-根据上面反应,在离解过程中,H+离子成为游离态,导致PH值降低。
1-2-2 石灰石石膏湿法烟气脱硫技术工艺原理及特点课件ppt

2021/3/10
6
三、脱除SO2的化学反应机理
• 1、过程阶段: • (1)气态反应物从气相内部迁移到气-液界面。 • (2)气态反应物穿过气-液界面进入液相,并发生化学反应。 • (3)反应组分从液相界面迁移到液相内部。 • (4)进入也想的反应组分与液相组分发生反应。 • (5)已溶解的反应物的迁移和由反应引起的浓度梯度产生的
3
典型的工程全景
2021/3/10
4
2021/3/10
5
二、石灰石湿法烟气脱硫工艺过程的描述
• 该工艺采用石灰石作为脱硫吸收剂,石灰石经破碎磨细 成粉状与水混合搅拌制成吸收浆液。在吸收塔内,吸收 浆液与烟气接触混合,烟气中的二氧化硫与浆液中的碳 酸钙以及鼓入的氧化空气进行化学反应吸收脱除二氧化 硫,最终产物为石膏。脱硫后的洁净烟气通过除雾器除 去雾滴经烟囱排放,脱硫渣石膏可以综合利用。
2021/3/10
20
4、吸收塔浆液的PH值
pH值—酸与碱
定义:
酸 = pH < 7
碱 = pH > 7
胃酸 亚硫酸 醋 典型洗涤塔 水 石灰石
石灰
硫酸 可口可乐
二元酸 血
pH
1
7
2021/3/10
碱液
14
21
pH对HSO3-氧化速率的影响
• pH值太高,则容易造成设备的堵塞和结垢,同时使得脱 硫剂的利用率降低,脱硫产物的品位下降。
• 而pH值太低,则影响了脱硫效率。
• 所以必须选择合适的pH值,使得保证脱硫效率,同时保 证脱硫剂的利用率和脱硫产物的品位。
2021/3/10
22
5、钙硫比
•脱硫塔内脱硫剂所含钙的摩尔数与烟气中所含二氧化硫摩尔 数的比例。
石灰石浆液在湿法脱硫中的作用
石灰石浆液在湿法脱硫中的作用
石灰石浆液在湿法脱硫中起着重要作用。
湿法脱硫是一种常用的
烟气脱硫技术,其原理是通过将石灰石浆液喷洒或喷雾到烟气中,与
废气中的二氧化硫进行反应,从而将其转化为石膏或其他硫酸盐产物。
石灰石浆液中的主要成分是石灰石(即氢氧化钙,Ca(OH)2)溶
于水中形成的悬浮液。
当石灰石浆液与二氧化硫接触时,发生以下反应:Ca(OH)2 + SO2 → CaSO3·H2O。
在反应中,二氧化硫被转化为硫亚硫酸钙(CaSO3·H2O),其可
进一步与空气中的氧气反应,生成石膏(硫酸钙,CaSO4·2H2O)。
石灰石浆液中的石灰石颗粒能够提供大量的碱性离子攻击二氧化
硫分子,使其在气液界面处发生反应。
由于石灰石浆液具有良好的分
散性和可湿性,能够有效地与烟气充分接触,增加了反应的速率和效率。
此外,石灰石浆液在湿法脱硫过程中还具有降低燃烧过程中产生
的氮氧化物(NOx)和悬浮颗粒物(PM)的能力。
石灰石浆液中的石灰
石颗粒能捕捉和吸附废气中的这些污染物,减少其排放量,达到净化
废气的效果。
通过使用石灰石浆液进行湿法脱硫,能够有效地去除烟气中的二
氧化硫,减少排放的空气污染物,保护大气环境。
因此,石灰石浆液
在湿法脱硫中扮演着重要的角色。
燃煤电站锅炉湿法烟气脱硫技术及应用案例
燃煤电站锅炉湿法烟气脱硫技术及应用案例燃煤电站锅炉石灰石/石灰-石膏湿法烟气脱硫技术,采用石灰石或石灰作为脱硫吸收剂,在吸收塔内,吸收剂浆液与烟气充分接触混合,烟气中的二氧化硫与浆液中的碳酸钙(或氢氧化钙)以及鼓入的氧化空气开展化学反应从而被脱除,最终脱硫副产物为二水硫酸钙即石膏。
该技术的脱硫效率一般大于95%,可达98%以上;S02排放浓度一般小于100mg∕m3,可达50mg∕m3以下。
单位投资大致为150~250元∕kW;运行成本一般低于1.5分/kWh。
[适用范围]燃煤电站锅炉图1典型石灰石-石膏湿法脱硫技术工艺流程图图2石灰石-石膏湿法烟气脱硫系统示意图典型案例[案例名称]2X1000MW超超临界机组湿法烟气脱硫工程[项目概况]本项目于20**年5月脱硫项目开工建设,20**年6月首套脱硫装置与7#主机同步完成168试运行,第2套脱硫装置与8#主机组于20**年10月同步完成168试运行。
本项目于20**年11月25日获中国施工企业管理企业颁发的20**-20**年度国家优质工程奖。
[主要工艺原理]本项目采用带托盘的喷淋式石灰石-石膏湿法烟气脱硫技术,主要工艺原理如下:烟气经除尘后,通过吸收塔入口区从浆液池上部进入塔体,在吸收塔内,热烟气逆流向上与自上而下的循环浆液接触发生化学吸收反应。
添加的石灰石浆液由石灰石浆液泵输送至吸收塔,与吸收塔内的浆液混合,混合浆液通过循环泵向上输送由多层喷淋层的喷嘴喷出。
浆液吸收烟气中二氧化硫以及其它酸性物质,在液相中二氧化硫与碳酸钙反应,形成亚硫酸钙。
在吸收塔内通过搅拌器和氧化风机将亚硫酸钙强制氧化成二水硫酸钙(石膏)。
从吸收塔排出的石膏浆液经浓缩、脱水,使其含水量小于10%,形成石膏。
脱硫后的烟气经除雾器除去雾滴后由烟囱排入大气。
[关键技术或设计创新特色]0采用先进的托盘喷淋塔工艺,气流分布均匀,吸收塔直接越大,优势越明显。
0吸收塔喷嘴采用空心锥喷嘴,增加了浆液与烟气的接触面积,进一步提高脱硫效率。
脱硫脱硝工艺概述
石灰石-石膏湿法脱硫工艺概述烟气脱硫采用技术为石灰石-石膏湿法烟气脱硫工艺。
脱硫剂采用石灰石粉(CaCO3), 石灰石由于其良好的化学活性及低廉的价格因素而成为目前世界上湿法脱硫广泛采用的脱硫剂制备原料。
SO2与石灰石浆液反应后生成的亚硫酸钙, 就地强制氧化为石膏,石膏经二级脱水处理可作为副产品外售。
本设计方案采用传统的单回路喷淋塔工艺,将含有氧化空气管道的浆池直接布置在吸收塔底部, 塔内上部设置三层喷淋层和二级除雾器。
从锅炉来的原烟气中所含的SO2与塔顶喷淋下来的石灰石浆液进行充分的逆流接触反应,从而将烟气中所含的SO2去除,生成亚硫酸钙悬浮。
在浆液池中通过鼓入氧化空气,并在搅拌器的不断搅动下,将亚硫酸钙强制氧化生成石膏颗粒。
脱硫效率按照不小于90%设计。
其他同样有害的物质如飞灰,SO3,HCI 和HF也大部分得到去除。
该脱硫工艺技术经广泛应用证明是十分成熟可靠的。
工艺布置采用一炉一塔方案,石灰石制浆、石膏脱水、工艺水、事故浆液系统等两塔公用。
#1锅炉来的原烟气由烟道引出,经升压风机(两台静叶可调轴流风机) 增压后, 送至吸收塔,进行脱硫。
脱硫后的净烟气经塔顶除雾器除雾后通过烟囱排放至大气。
#2炉的烟道系统流程与#1炉相同,布置上与#1炉为对称布置。
脱硫剂采用外购石灰石粉,用滤液水制成30%的浆液后在石灰石浆液箱中贮存,通过石灰石浆液泵不断地补充到吸收塔内。
脱硫副产品石膏通过石膏排出泵,从吸收塔浆液池抽出,输送至石膏旋流站(一级脱水系统),经过一级脱水后的底流石膏浆液其含水率约为50%左右,直接送至真空皮带过滤机进行二级过滤脱水。
石膏被脱水后含水量降到10%以下。
石膏产品的产量为20.42t/h(#1、#2炉设计煤种,石膏含≤10%的水分)。
脱硫装置产生的废水经脱硫岛设置的废水处理装置处理后达标排放或回收利用。
脱硝工艺系统描述3.1 脱硝工艺的原理和流程本工程采用选择性催化还原法(SCR)脱硝技术。
石灰石/石膏湿法烟气脱硫技术概述
石灰石/石膏湿法烟气脱硫技术概述摘要:本文主要对烟气脱硫工艺中的石灰石/石膏湿法烟气脱硫技术进行介绍。
首先介绍其工艺原理,烟气中的二氧化硫与浆液中的碳酸钙以及从塔下部浆池鼓入的氧化空气进行反应生成硫酸钙,硫酸钙达到一定饱和度后,结晶形成二水石膏。
关键词:FGD;石灰石/石膏湿法;烟气系统;吸收系统1 烟气脱硫工艺概述烟气脱硫(FGD)是目前燃煤电厂控制气体排放最有效和应用最广的技术。
20世纪60年代后期以来,烟气脱硫技术发展迅速,根据美国电力研究院的统计,大约有200种不同流程的FGD工艺进行了小试或工业性试验,但最终被证实在技术上可行、经济上合理并且在燃煤电厂得到采用的成熟技术仅有十多种。
2. 石灰石/石膏湿法烟气脱硫工艺石灰石/石膏湿法脱硫工艺是目前世界上应用最广泛、技术最为成熟的脱除技术,约占全部安装FGD 容量的70%。
它是以石灰石为脱硫吸收剂,通过向吸收塔内喷入吸收剂浆液,使之与烟气充分接触、混合,并对烟气进行洗涤,使得烟气中的与浆液中的碳酸钙以及鼓入的强制氧化空气发生化学反应,最后生成石膏,从而达到脱除的目的。
2.1 工艺原理石灰石粉加水制成重量浓度约为30%的浆液作为脱硫吸收剂,泵入吸收塔与烟气充分接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及从塔下部浆池鼓入的氧化空气进行反应生成硫酸钙,硫酸钙达到一定饱和度后,结晶形成二水石膏。
脱硫后的烟气依次经过除雾器除去雾滴,再经过加热器升温至大于80℃后,由烟囱排入大气。
2.2.1工艺流程采用价廉易得的石灰石或石灰做脱硫吸收剂,石灰石经破碎磨成粉状与水混合搅拌成吸收浆液。
当采用石灰为吸收剂时,石灰经消化处理加水搅拌成吸收浆液。
锅炉的烟气从电除尘器或布袋除尘后(除尘效率大于97%),经烟气换热器降温后从吸收塔下部进入吸收塔(经过气-气换热器后的烟气温度下降到100℃左右)。
脱硫净化后的烟气依次经过除雾器除去雾滴然后再经气-气换热器升温后,从烟囱排放到大气空中。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
. .. 石灰石-石膏湿法烟气脱硫工艺的化学原理 一、概述:脱硫过程就是吸收,吸附,催化氧化和催化还原,石灰石浆液洗涤含SO2烟气,产生化学反应分离出脱硫副产物,化学吸收速率较快与扩散速率有关,又与化学反应速度有关,在吸收过程中被吸收组分的气液平衡关系,既服从于相平衡(液气比L/G,烟气和石灰石浆液的比),又服从于化学平衡(钙硫比Ca/S,二氧化硫与炭酸钙的化学反应)。
1、气相:烟气压力,烟气浊度,烟气中的二氧化硫含量,烟尘含量,烟气中的氧含量,烟气温度,烟气总量
2、液相:石灰石粉粒度,炭酸钙含量,黏土含量,与水的排比密度, 3、气液界面处:参加反应的主要是SO2和HSO3-,它们与溶解了的CaCO3的反应是瞬间进行的。
二、脱硫系统整个化学反应的过程简述: 1、 SO2在气流中的扩散, 2、 扩散通过气膜 3、 SO2被水吸收,由气态转入溶液态,生成水化合物 4、 SO2水化合物和离子在液膜中扩散 5、 石灰石的颗粒表面溶解,由固相转入液相 6、 中和(SO2水化合物与溶解的石灰石粉发生反应) 7、 氧化反应 8、 结晶分离,沉淀析出石膏, 三、烟气的成份:火力发电厂煤燃烧产生的污染物主要是飞灰、氮氧化物和二氧化硫,使用静电除尘器可控制99%的飞灰污染。
四、二氧化硫的物理、化学性质: ①. 二氧化硫SO2的物理、化学性质:无色有刺激性气味的有毒气体。密度比空气大,易液化(沸点-10℃),易溶于水,在常温、常压下,1体积水大约能溶解40体积的二氧化硫,成弱酸性。SO2为酸性氧化物,具有酸性氧化物的通性、. .. 还原性、氧化性、漂白性。还原性更为突出,在潮湿的环境中对金属材料有腐蚀性,液体SO2无色透明,是良好的制冷剂和溶剂,还可作防腐剂和消毒剂及还原剂。
②. 三氧化硫SO3的物理、化学性质:由二氧化硫SO2催化氧化而得,无色易挥发晶体,熔点16.8℃,沸点44.8℃。SO3为酸性氧化物,SO3极易溶于水,溶于水生成硫酸H2SO4,同时放出大量的热,
③. 硫酸H2SO4的物理、化学性质:二元强酸,纯硫酸为无色油状液体,凝固点为10.4℃,沸点338℃,密度为1.84g/cm3,浓硫酸溶于水会放出大量的热,具有强氧化性(是强氧化剂)和吸水性,具有很强的腐蚀性和破坏性,
五、石灰石湿-石膏法脱硫化学反应的主要动力过程: 1、气相SO2被液相吸收的反应:SO2经扩散作用从气相溶入液相中与水生成亚硫酸H2SO3 亚硫酸迅速离解成亚硫酸氢根离子HSO3-和氢离子H+,当PH值较高时,HSO3二级电离才会生成较高浓度的SO32-,要使SO2吸收不断进行下去,必须中和电离产生的H+,即降低吸收剂的酸度,碱性吸收剂的作用就是中和氢离子H+当吸收液中的吸收剂反应完后,如果不添加新的吸收剂或添加量不足,吸收液的酸度迅速提高,PH值迅速下降,当SO2溶解达到饱和后,SO2的吸收就告停止,脱硫效率迅速下降
2、吸收剂溶解和中和反应:固体CaCO3 的溶解和进入液相中的CaCO3的分解,固体石灰石的溶解速度,反应活性以及液相中的H+浓度(PH值)影响中和反应速度和Ca2+的氧化反应,以及其它一些化合物也会影响中和反应速度。Ca2+的形成是一个关键步骤,因为SO2正是通过Ca2+与SO32- 或与SO42-化合而得以从溶液中除去,
3、氧化反应:亚硫酸的氧化,SO32-和HSO3-都是较强的还原剂,在痕量过渡金属离子(如锰离子Mn2+)的催化作用下,液相中的溶解氧将它们氧化成SO42-。反应的氧气来源于烟气中的过剩空气和喷入浆液池的氧化空气,烟气中洗脱的飞灰和石灰石的杂质提供了起催化作用的金属离子。
4、结晶析出:当中和反应产生的Ca2+、SO32- 以及氧化反应产生的SO42-,达到一定浓度时这三种离子组成的难溶性化合物就将从溶液中沉淀析出。
沉淀产物: ①. 或者是半水亚硫酸钙CaSO3·1/2H2O、亚硫酸钙和硫酸钙相结合的半水固溶体、二水硫酸钙CaSO4·2H2O。这是由于氧化不足而造成的,系统易产生硬垢。 . .. ②. 或者是固溶体和石膏的混合物。氧化充足的硫酸钙饱和溶液,不会形成二水硫酸钙硬垢
石灰石湿法工艺过程的脱硫反应速率取决于上述四个控制步骤: 七、吸收塔内的化学反应 化学总反应式:CaCO3+2SO2+H2O Ca(HSO3)2+CO2 (吸收反应) Ca(HSO3)2+O2+CaCO3+3H2O 2CaSO4·2H2O+CO2(氧化中和结晶) 1. 吸收区的吸收反应: 1) 在吸收区主要发生的化学反应为: SO2+H2O→H2SO3 H2SO3-→H++HSO3- 部分发生的化学反应为: H++HSO3-+1/2O2→2H++SO42- 2H++SO42-+CaCO3+ H2O→CaSO4·2H2O+CO2 2) 气态二氧化硫SO2溶解于水H2O中发生反应生成液态亚硫酸H2SO3溶液, H2SO3
迅速离解生成氢离子和亚硫酸氢根离子H+、HSO3-,部分H+、HSO3-与烟气中的过
剩氧和水中的溶解氧发生氧化反应,生成氢离子2H+和硫酸根离子SO42-,由于喷淋的石灰石浆液在吸收区停留的时间很短,约5S左右,只有部分固态石灰石颗粒溶解形成的CaCO3溶液,分解出钙离子Ca2+与氢离子2H+,它们和硫酸根离子SO42-发生中和反应,中和了H+离子,生成硫酸钙CaSO4,相对过饱和结晶析出二水石膏CaSO4·2H2O。
3)在上述同时进行的化学反应过程中,在吸收区上部(PH值高),逆流上升被吸收的SO2基本被吸收,烟气中的过剩氧和水中的溶解氧也逐渐降低,H+、HSO3
-与烟气中的过剩氧和水中的溶解氧发生的氧化反应,在生成硫酸根离子SO42-的
同时,由于氧量的减少生成了大量的亚硫酸根离子SO32-,它与石灰石浆液中的钙离子Ca2+中和反应生成亚硫酸钙CaSO3,若在氧化区内不能充分氧化,在中和区易析出难以溶解的半水石膏CaSO3·1/2H2O。 . .. 4)烟气中的SO2溶入石灰石吸收浆液的过程几乎全部发生在吸收区,但由于石灰石浆液和烟气在吸收区的接触时间仅数秒钟,浆液中的CaCO3仅中和了部分已氧化的亚硫酸H2SO3(以及少量被烟气中的过剩氧O2氧化的硫酸H2SO4)。即在吸收区内,石灰石浆液只有少量的CaCO3参与了化学反应。
5)吸收区吸收SO2的控制: ①.控制石灰石的品质、纯度和粒度: 1. 石灰石中的杂质对石灰石颗粒的消溶起阻碍作用,石灰石品质高,石灰石颗粒的消溶性越好。
2. 石灰石颗粒的粒度越小,质量比面积就越大,石灰石的消溶性越好; 3. 增强石灰石的消溶速率,浆液吸收SO2的反应速率越快,即提高了脱硫效率,也提升了石灰石粉的利用率;
②.控制进入吸收塔的烟气的飞灰:飞灰阻碍石灰石的消溶,降低石灰石的消溶速率,导致脱硫效率下降。PH值降低而无法调高,一般经过静电除尘器后,烟气飞灰浓度在100~300mg/Nm3。电除尘电场退出超过规定,FGD保护退出运行。
③.根据进入FGD的SO2浓度,控制Ca/S比和L/G比:进入FGD的SO2浓度降低,应向吸收塔送入较低密度的石灰石浆液,而在进入FGD的SO2浓度很高时,应向吸收塔送入较高密度的石灰石浆液。如果进入FGD的SO2浓度很高,石灰石浆液供浆流量已达到最大,PH值仍然下降,净烟气浓度超过设计保证值,脱硫效率下降,应加开备用循环泵增加液气比,
2. 氧化区的氧化反应: 1) 发生在氧化区的主要化学反应: H++HSO3-+1/2O2→2H++ SO42- CaSO3+ 2H+→ Ca2++H2O+CO2 Ca2++SO42-+ H2O→CaSO4·2H2O 2) 氧化区的范围大致从浆液池液面至固定管网氧化装置喷咀下方300mm处,即吸收塔约10米以上的液位,在氧化区氧化池内,从吸收区吸收SO2后喷淋落下的浆液,主要是大量未被氧化的亚硫酸氢根离子HSO3-溶液。氧化风机将大量氧化空气沿吸收塔径向圆周均匀的喷入氧化区下部,将HSO3-氧化成氢离子H+和硫. .. 酸根SO42-,迅速中和洗涤浆液中剩余的CaCO3,以及在吸收区由于氧量不足而生成的亚硫酸钙CaSO3,最终生成溶解状态的硫酸钙CaSO4,当钙离子Ca2+和硫酸根SO42-浓度达到一定饱和时,结晶生成二水硫酸钙CaSO4·2H2O(二水石膏)。
3) 氧化控制:保证氧化区的液位,保证氧化风机的正常运行和供风量。HSO3-
离子在PH值为4.5时氧化速率最大,通过增加强制氧化控制PH值可控制在4.5-5.5之间,可将大量的HSO3-离子强制氧化成硫酸根SO42-,而SO42-与钙离子Ca2+发生反应生成硫酸钙CaSO4,
氧化量 反应式 生成物中文名称 强制氧化严重不足 Ca2++2HSO3-→Ca(HSO3)2 亚硫酸氢钙 强制氧化不足: Ca2++SO32-→CaSO3 亚硫酸钙 强制氧化充足 Ca2++SO42-→CaSO4 硫酸钙
亚硫酸氢钙的危害性:无色或微黄色固体或液体,有强烈的二氧化硫气味。具有还原性。接触酸或酸气能产生有毒气体。(如硫化氢是一种有毒气体,人吸入后会引起昏迷甚至于死亡)受高热分解放出有毒的气体。具有腐蚀性、刺激性。有毒。误服会中毒。蒸气刺激眼睛和粘膜。液体能腐蚀眼睛、皮肤和粘膜。对环境可能有危害,对水体可造成污染。高浓度可致人体灼伤。空气中浓度超标时,必须佩戴自吸过滤式防毒面具(半面罩)。应该佩戴空气呼吸器。戴化学安全防护眼镜。直接接触者应穿橡胶耐酸碱服。戴橡胶耐酸碱手套。吸收塔氧化空气严重不足,浆液会携带大量的有毒气体从脱水系统中分解出来。
4) 吸收塔浆液获得氧的途径主要是:烟气中的过剩氧气,水中的溶解氧和主要由氧化风机强制喷入浆液池的氧化空气。另外烟气飞灰中和石灰石杂质中,对吸收的氧化反应也提供了起催化作用的金属离子,如:?
5) 避免过多的新鲜石灰石浆液进入氧化区。这将不利于HSO3-的氧化,存在过量的CaSO3有助于形成CaSO3·1/2H2O,而溶解氧很难氧化CaSO3·1/2H2O。除非有过量的H+才能使其重新溶解为HSO3-。
3. 中和区的中和反应: 1) 吸收浆液落入浆液池,缓缓经过氧化区,进入中和区,氧化区的下面一般视为中和区,循环泵入口至吸收塔喷淋层喷咀之间的管道、泵体空间也是中和区的一部分。经过强制氧化,浆液中过剩的亚硫酸钙CaSO3浓度降至最低值,此时浆液中结晶生成二水硫酸钙CaSO4·2H2O的浓度最高,从吸收塔底部一侧排出浆液至脱水系统。即可获得较高品位的石膏。
