鼠伤寒沙门氏菌/回复突变试验
附表2特殊用途化妆品检测项目
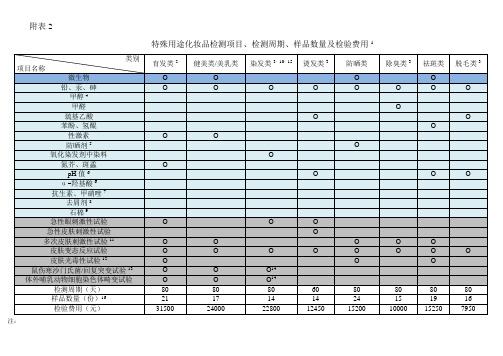
附表2特殊用途化妆品检测项目、检测周期、样品数量及检验费用1注:1、一个样品包装内有两个以上独立小包装或分隔(如粉饼、眼影、腮红等),且只有一个产品名称,原料成分不同的样品,应当分别检验相应项目;非独立小包装或无分隔部分,且各部分除着色剂以外的其他原料成分相同的样品,应当按说明书使用方法确定是否分别进行检验。
2、乙醇含量≥75%(w/w)者不需要测微生物项目。
3、产品配方中没有微生物抑制作用成分的产品(如物理脱毛类产品、纯植物染发类产品等)需测微生物指标。
4、乙醇、异丙醇含量之和≥10%(w/w)的产品需要测甲醇项目。
5、除防晒产品外,防晒剂(二氧化钛和氧化锌除外)含量≥0.5%(w/w)的其他产品也应当加测防晒剂项目。
6、宣称含α-羟基酸或虽不宣称含α-羟基酸,但其总量≥3%(w/w)的产品需要测α-羟基酸项目,同时测pH值。
7、宣称祛痘、除螨、抗粉刺等用途的产品需要测抗生素和甲硝唑项目。
8、宣称去屑用途的产品需要测去屑剂项目。
9、凡含滑石粉的产品,需加测石棉。
10、染发类产品为两剂或两剂以上配合使用的产品,应当按剂型分别检测相应的卫生化学项目。
11、即洗类产品不需要进行多次皮肤刺激性试验,只进行急性皮肤刺激性试验。
12、除育发类、防晒类和祛斑类产品外,防晒剂(二氧化钛和氧化锌除外)含量≥0.5%(w/w)的产品还应进行皮肤光毒性试验。
13、进行鼠伤寒沙门氏菌/回复突变试验或选用体外哺乳动物细胞基因突变试验。
14、涂染型暂时性染发产品不进行鼠伤寒沙门氏菌/回复突变试验和体外哺乳动物细胞染色体畸变试验。
15、染发类产品为两剂或两剂以上配合使用的产品,应按说明书中使用方法进行毒理学试验。
16、检验数量是针对每包装净重大于25克的产品而言,不满25克者,需增加样品数量。
此数量包括进口化妆品在药监局审批时提供的封样样品,封样与检验报告同时领取。
国产特殊用途化妆品不用。
毒理复习资料

名解:1.蓄积作用:指毒物逐次进入生物体,而在靶器官内积和/或毒物对生物体所致效应的累加现象。
当较长时间连续、反复给药,或者说给药的时间间隔和剂量超过机体消除药物的能力时,出现药物进入机体的速度(或总量)超过排除的速度(或总量)的现象,这时药物就有可能在体内逐渐增加并贮存起来,也就是说出现了蓄积作用。
蓄积作用可以分为药物积蓄和功能性积蓄。
2.近似致死量:近似致死量(Approximatal Lethal Dose,ALD)是介于最小致死量(Minimum Lethal Dose, MLD)与最大非致死量(Maximum Non-Lethal Dose, MNLD)之间的剂量。
MLD是指药物在最低剂量组的一群实验动物中仅引起个别动物死亡的剂量,在急性毒性试验中可表示为LD10或LD5;MNLD实际上是急性毒性试验中以死亡为毒效应时的一种最大耐受量,指药物不引起实验动物死亡的最大剂量,可表示为LD0。
3.染色体畸变:药物或化合物对遗传物质的影响涉及到整个染色体,表现为染色体结构或数目的变化称为染色体畸变。
4.S9:肝脏微粒体酶。
指1经酶诱导剂处理后制备的肝匀浆,2再经离心分离所得上清液,3再加上适当的缓冲液和辅助因子。
/ 它主要含有混合功能氧化酶(MFO),是国内常规应用于体外致突变实验的代谢活化系统。
其缺点是S9随实验动物种属或器官不同而有差异;S9含有的大量亲核物质有可能影响实验的敏感性。
选用200g左右的雄性大鼠,ip多氯联苯,500mg/kg。
杀死12小时前开始禁食。
诱导处理后d5断头法处死大鼠,无菌条件下取出肝脏,用冷KCL溶液洗涤后称重。
剪碎肝脏,制备肝匀浆。
肝匀浆以9000xg速度离心,取上清液分装小试管。
置液氮罐内速冻,-80或-20度保存备用,此即S9上清液,简称S9。
5.微核:染色体发生畸变导致断裂,断裂的碎片在分裂间期留在子代细胞中形成的规则的圆形或椭圆形结构的小块物质,又与他比普细胞核小,故称微核。
中药毒理学研究1

皮肤吸收定量试验
脱毛并罩上玻璃钟罩——加入定量药物——药 物与皮肤接触2~6小时——观察 脱毛:化学法和机械法
二、局部刺激性试验
血管
肌肉
红肿、充血、渗出、变性或坏死
皮肤
粘膜
注意:不宜进行局部刺激性试验的情况
pH≤ 2
pH≥ 11.2
血管刺激性试验
家兔——耳背血管注射药物——观察局部血管 及周围组织反应(48-96小时) 肉眼观察、显微镜检查、组织病理学检查。
急性毒性试验 长期毒性试验 局部毒性试验
致畸试验 致癌试验 致突变试验 药物依赖试验
研究方法
体内试验——利用整体动物进行的试验。
体外试验——利用离体脏器、培养细胞
进行的试验。
中
中药毒理学 药政管理学 中药药动学 分子生物学
药 安 全
细胞生物学
性
统计学
评
价
药理学 生理学 病理学 遗传学 动物学 组胚学 临床医学
定义
溶血性试验:考察中药注射剂是否具有溶血和 红细胞凝聚等反应。
分类
免疫性溶血——免疫反应——抗体——溶血 非免疫性溶血——药物诱导——溶血
必要性
中药 1、含有溶血成分 2、含有杂质成分 3、免疫性溶血
常见方法
一、常规体外试管法(肉眼观察法) 红细胞悬液——加入受试物——温育——观察 溶血或凝集反应情况。
急性毒性试验
概念
急性毒性试验:中药一次或24小时内多次给予 试验动物,观察在短时间内对动物所引起的快 速而剧烈的中毒效应的试验方法。
意义
1.了解中药急性毒性的强弱 2.为长期毒性试验及特殊毒性试验选择
剂量提供依据 3.获取毒性反应信息
实验设计
化妆品申报时毒理检验的审查要点及评价(2)皮肤变态反应、皮肤光毒、Ames

化妆品备案毒理学检验的审查要点及评价(二)在化妆品备案申报时,产品都要在国家认可的检验机构按照《化妆品卫生规范》的要求进行检验。
虽然这些试验的具体操作都由检验机构来完成,但如果申请企业的研发申报人员能够对主要试验方法、审查要点和评价标准有一个大致的了解,对研究产品配方、调整产品工艺及把控产品质量都会有所帮助。
下面北京天健华成国际投资顾问有限公司化妆品注册部就主要的毒理试验帮大家进行简单的梳理,供您参考。
化妆品备案毒理学检验之皮肤变态反应试验实验方法◆ 动物数试验组至少20只,对照组至少10只。
◆ 剂量水平诱导接触受试物浓度为能引起皮肤轻度刺激反应的最高浓度激发接触受试物浓度为不能引起皮肤刺激反应的最高浓度。
试验浓度水平可以通过少量动物(2-3只)的预试验获得。
◆ 对于化妆品产品而言,一般使用原霜或原液◆试验方法可靠性的检查使用已知的能引起轻度/中度致敏的阳性物每隔半年检查一次。
局部封闭涂皮法至少有30% 动物出现皮肤过敏反应。
阳性物一般采用2,4-二硝基氯代苯。
试验步骤(1)试验前约24 h ,将豚鼠背部左侧去毛,去毛范围为4cm2-6cm2。
(2)诱导接触:将受试物约0.2mL(g)涂在实验动物左侧去毛区皮肤上,以二层纱布和一层玻璃纸覆盖,再以无刺激胶布封闭固定6 h。
第7d和第14d以同样方法重复一次。
(3)激发接触:末次诱导后14-28d,将约0.2mL的受试物涂于豚鼠背部右侧2cm×2cm 去毛区(接触前24h脱毛),然后用二层纱布和一层玻璃纸覆盖,再以无刺激胶布固定6h。
(4)激发接触后24h和48h观察皮肤反应,按表1评分(5)试验中需设阴性对照组,使用(2)和(3)的方法,在诱导接触时仅涂以溶剂作为对照,在激发接触时涂以受试物。
对照组动物必须和受试物组动物为同一批。
在实验室开展变态反应试验初期,或使用新的动物种属或品系时,需同时设阳性对照组结果判定(1)当受试物组动物出现皮肤反应积分≥1时,按表2判为该动物出现皮肤变态反应阳性,按表3判定受试物的致敏强度。
牡丹籽油软胶囊回复突变试验的研究

牡丹籽油软胶囊回复突变试验的研究张爽;童琳;许勇;李舜;叶红【期刊名称】《安徽农业科学》【年(卷),期】2017(045)033【摘要】[目的]采用鼠伤寒沙门氏菌/哺乳动物微粒体酶试验(Ames)对牡丹籽油软胶囊进行安全性毒理学试验.[方法]试验选用鼠伤寒沙门菌TA97、TA98、TA100和TA102菌株,将牡丹籽油软胶囊配制成浓度为5.0、1.0、0.2、0.04 mg/皿4个剂量,和阳性对照组(叠氮钠、2-氨基芴、敌克松)进行比较,观察各菌株的回变菌落数.[结果]牡丹籽油对4个菌株诱发的回变菌落数均未超过对照组2倍,为阴性结果.[结论]牡丹籽油对鼠伤寒沙门氏菌无直接致突变作用.【总页数】2页(P79-80)【作者】张爽;童琳;许勇;李舜;叶红【作者单位】安徽省医学科学研究院,安徽合肥230061;安徽省医学科学研究院,安徽合肥230061;安徽省医学科学研究院,安徽合肥230061;安徽省医学科学研究院,安徽合肥230061;安徽省医学科学研究院,安徽合肥230061【正文语种】中文【中图分类】TS225.1【相关文献】1.乙交酯一L-丙交酯一己内酯三元无规共聚物(PGLC)鼠伤寒沙门氏菌基因回复突变试验(Ames试验) [J], 张强;朱燕;周玲;张秀芹2.牡丹籽油自微乳化软胶囊内容物的制备工艺研究 [J], 罗国平;曹斌;闫梦茹;孟会宁;张存劳;陈程;王小宁3.细菌回复突变试验研究薏苡仁油的遗传毒性作用 [J], 黄宗锈; 林云; 钟礼云4.牡丹籽油复方软胶囊增强免疫力的功能研究 [J], 张梦兰; 杨琴; 张冰洁; 王洪新; 马朝阳5.鼠伤寒沙门氏菌回复突变试验中通过吸光度值测定菌液浓度的方法研究 [J], 周谡; 李睿; 朱鸿雁; 张志超; 方静; 唐黎明因版权原因,仅展示原文概要,查看原文内容请购买。
番泻叶提取物长期食用安全性研究

番泻叶提取物长期食用安全性研究摘要:目的研究番泻叶提取物长期食用的安全性。
方法通过动物急性经口毒性试验、三项遗传毒性试验、90天经口毒性试验对番泻叶提取物长期食用安全性进行研究。
结果番泻叶提取物小鼠急性经口LD50大于10.0 g/kg,属实际无毒级。
三项遗传毒性试验(细菌回复突变试验、哺乳动物红细胞微核试验、小鼠精母细胞染色体畸变试验)均为阴性结果,番泻叶提取物无遗传毒性。
90天经口毒性试验观察期间,大鼠一般临床观察情况良好,各剂量番泻叶提取物组大鼠体重、进食量、食物利用率、血液学和血生化学指标、脏器重量及脏器/体重比值与对照组比较无明显变化,差异无显著性(P>0.05);大鼠尿液检查、眼部检查、大体解剖及组织病理学检查未见明显与番泻叶提取物有关的异常改变。
结论动物安全性试验研究证明番泻叶提取物长期食用安全。
关键词:番泻叶提取物;急性经口毒性;遗传毒性;亚慢性毒性中药材番泻叶收载于《中华人民共和国药典》,为豆科植物狭叶番泻Cassia angustifoliaVahl或尖叶番泻Cassia acutifolia Delile的干燥小叶,味甘、苦,性寒,归大肠经。
具有泻热行滞,通便,利水的功能,用于热结积滞,便秘腹痛,水肿胀满[1]。
美国药典、英国药典均收载了番泻叶流浸膏、总番泻苷片等番泻叶制剂,主要用作清洁肠道和便秘的治疗[2]。
在卫法监发[2002]51号《卫生部关于进一步规范保健食品原料管理的通知》中,将番泻叶列入到附件2“可用于保健食品的物品名单”中,即番泻叶可应用于医药、保健食品中。
番泻叶是全世界范围内应用最广的导泻剂,在国外应用已有千余年历史。
其主要活性成分为番泻苷A、番泻苷B。
由于人体消化酶不能分解具有β-葡萄糖键连接的番泻苷,使其在肠道上部既不被吸收,也不被弱酸环境(空腹)所破坏,可直接到达大肠,由细菌分解转化为大黄酸蒽酮刺激肠道强烈蠕动,使蠕动频率增加,肠道内容物的运输及大肠的排空运动加速;另一方面,番泻苷可使肠道水、电解质的净吸收明显减少,服用后可明显增加体液向肠腔的分泌,使肠腔容积增大,进而使肠蠕动增加,产生攻里通下作用[2]。
食品毒理学总结(山农大,全)
名词解释:1.毒物:指在一定条件下,以较小剂量进入机体能干扰正常的生化过程或生理功能,引起暂时的或永久性的病理改变,甚至危及生命的化学物质。
2.中毒:指生物体受到毒物作用而引起的功能性或器质性的疾病状态。
3.毒性:化学物质能够造成机体损失的能力。
4.选择毒性:指一种化学物质只对某种生物产生损害作用,而对其他种类生物无害;或只对机体内某一组织器官发挥毒性,而对其他组织器官无毒作用。
5.毒作用:是化学作用对生物体的损害作用,又称毒性作用。
6.毒效应谱:指机体接触外源化学物后,由于外源化合物的性质和剂量不同可引起机体多种变化。
7.(1)损害作用:是指影响机体行为的生物化学变化,功能紊乱或病理损害或降低对外界环境应激的反应能力。
(2)非损害作用:机体所发生的一切生物学变化应在机体的代偿能力范围内,机体对其他外界不利因素的影响易感性也不改变。
8.靶器官:外源化合物可以直接发挥毒作用的器官称为该物质的靶器官。
9.生物学标志:指针对通过生物学屏障进入组织或体内的化学物质及其代谢产物以及它们所引起的生物学效应而采用的检测指标。
可分为:接触生物学标志、效应生物学标志、易感性生物学标志。
10.吸收:指外源化合物从机体接触部位透过生物膜进入血液的过程。
11.分布:指外源化合物吸收后,随血液或淋巴液流动分散到全身组织细胞的过程。
12.肝脏的首过效应:是指经胃肠道吸收的外源化合物都要汇入肝门静脉到达肝脏之后再进入体循环,由于肝脏具有代谢外源化合物的功能,未被代谢的原型和代谢产物离开肝脏随体循环分布到全身,这种未到体循环就被肝脏代谢的现象称为首过效应。
13.血脑屏障:是由毛细血管内皮细胞和聚集包围毛细血管的星形角质细胞的软脑膜组成的一种特殊的功能结构。
14.胎盘屏障:由分割母体和胎儿血液循环的一层或几层细胞构成。
15.结合反应(二相反应):进入机体的外源化学物在代谢过程中与其他内源性化学物或基因发生的生物结合反应。
16.蓄积作用:当化学毒物与机体发生多次接触,将反复进入机体,而且当进入机体的速度或总量超过代谢转化的速度和派出的速度或总量时,化学毒物或其代谢产物就有可能在机体内逐渐增加并贮存,这种现象称化学毒物的蓄积作用。
毒理复习资料
名解近似致死量:近似致死量(Approximatal Lethal Dose,ALD)是介于最小致死量(Minimum Lethal Dose, MLD)与最大非致死量(Maximum Non-Lethal Dose, MNLD)之间的剂量。
MLD是指药物在最低剂量组的一群实验动物中仅引起个别动物死亡的剂量,在急性毒性试验中可表示为LD10或LD5;MNLD实际上是急性毒性试验中以死亡为毒效应时的一种最大耐受量,指药物不引起实验动物死亡的最大剂量,可表示为LD0。
染色体畸变:药物或化合物对遗传物质的影响涉及到整个染色体,表现为染色体结构或数目的变化称为染色体畸变。
S9:肝脏微粒体酶。
指1经酶诱导剂处理后制备的肝匀浆,2再经离心分离所得上清液,3再加上适当的缓冲液和辅助因子。
/ 它主要含有混合功能氧化酶(MFO),是国内常规应用于体外致突变实验的代谢活化系统。
其缺点是S9随实验动物种属或器官不同而有差异;S9含有的大量亲核物质有可能影响实验的敏感性。
选用200g左右的雄性大鼠,ip多氯联苯,500mg/kg。
杀死12小时前开始禁食。
诱导处理后d5断头法处死大鼠,无菌条件下取出肝脏,用冷KCL溶液洗涤后称重。
剪碎肝脏,制备肝匀浆。
肝匀浆以9000xg速度离心,取上清液分装小试管。
置液氮罐内速冻,-80或-20度保存备用,此即S9上清液,简称S9。
促长剂(promoter of carcinoma):本身并没有致癌性,但可使化学物诱发突变细胞的克隆扩增,与致癌物共同作用or 在致癌物作用之后,这类物质反复作用于细胞,具有促进癌的发生or加速癌细胞发展成为癌瘤的间接致癌作用。
常见的促癌物有佛波酯(TPA),巴豆油(croton oil),煤焦油中的酚类、卤代烃、烟草中的某些成分等。
完全致癌物(complete carcinogen):指同时具有引发、促长和恶性进展作用的化学致癌物。
致畸指数(teratogeic index):指药物对母体的LD50与最小致畸剂量之比。
毒理学,名词解释,简答题
1、化学致癌三个阶段特点:引发阶段:不可逆;所引发的“干细胞”在形态学上无法识别;需要通过细胞分裂“固定突变”;剂量-反应关系良好,但很难测定的阈值,无可测定的最大反应;存在自发启动的引发作用(内源性);对外源性化学物质和其他化学因素敏感;引发剂的强度以经一定的促长阶段后发生的癌前病变来定量。
促长阶段:可逆(基因表达、细胞水平);促长剂的有效性仅出现在引发作用之后;促长细胞群的存在取决于促长剂的持续存在;内源性促长剂可起“自发”促长作用;剂量-反应显示有可测定的阈值,有可测定的最大效应;对饮食和激素等因素敏感;以能否有效的扩大引发细胞群来确定促长剂的相对强度。
进展阶段:不可逆;核型不稳性性导致细胞基因组结构的形态学改变;有可测定的和/或形态学可描述的细胞基因组的改变;进展的早期阶段,已改变的细胞对环境因素敏感;可见良性和/或恶性肿瘤;促进展剂可使已促长的细胞进入该阶段;可以发生自发的进展作用。
2、影响外源化学物质活性化学物因素:化学结构取代基的影响:取代基的影响、异构体和立体构型、同系物的碳原子数和结构的影响、分子饱和度化合物的联合作用(joint action ):两种或两种以上毒物同时或先后作用于机体时产生的交互毒性作用。
非交互作用:相加作用、独立作用;交互作用:协同作用、加强作用、拮抗作用3、影响外源化学物毒性因素:化学物因素:化学结构,理化性质,不纯物和外源化学物的稳定性机体因素:物种个体遗传学差异,宿主其它因素对于毒作用敏感影响环境因素:气象条件,季节和昼夜节律动物笼养方式,外源化合物的接触特征和赋形剂化合物联合作用:4、影响外源化学物生物转化的因素化学因素:化学结构影响:取代基不同毒性不同,异构体和立体构型的影响,同系物的碳原子数和结构的影响,理化性质:脂水分配系数,分子量大小,挥发性,气态物质血气非配系数比重,电离度和荷电性、不纯物和外源化学物的稳定性二是机体因素5、安全性评价的四个阶段的试验项目:第一阶段:包括急性毒性试验和局部毒性试验。
微生物学遗传变异习题
遗传变异一、名词解释1、基因型2、表型3、突变4、突变型5、饰变6、普遍性转导7、转化8、细菌素9、抗生素10、突变率11、光复活作用12、准性生殖13、野生型14、原养型15、营养缺陷型菌株16、完全培养基17、补充培养基18、F+菌株19、F-菌株20、Hfr菌株21、F'菌株22、接合中断法二、填空题1、、和是证明核酸是遗传物质的三个经典实验。
2、细菌的质粒的种类很多,其中接合性质粒如,抗药性质粒如,产细菌素质粒如,诱癌质粒如,诱生不定根的质粒如,执行固氮功能的质粒如,降解性质粒如等。
3、细胞的平均突变率是。
4、选择性突变株可包括、和等,而非选择性突变株则可包括、和等。
5、、、、、和是基因突变的六个特点。
6、基因突变的自发性和不对应性曾有三个著名的实验予以证明,它们是、和。
7、点突变是由于碱基置换而引起的,和是两种具体机制。
8、诱发突变可分为三类,即、和。
9、紫外线对微生物的损伤,主要是产生,主要通过两种方式修复DNA的损伤,即和。
10、、、和是在DNA的切除修复中参与的四种酶;参与光复活作用的酶则仅有一种。
11、若利用紫外线诱变微生物,应在条件下进行操作,并在条件下培养。
12、常见的“三致”是指、和作用,是目前检出某试样是否有“三致”的简便快速高效的试验。
13、艾姆斯试验中用的菌种是,通过回复突变可以检测待测样品中的存在。
14、、和是与筛选营养缺陷型突变株有关的三类培养基。
15、与营养缺陷型有关的菌株有三种:从自然界分离到的任何菌种的原始菌株称为,该菌株经诱变剂处理后所发生的丧失某酶合成能力的菌株称为,若再经回复突变或重组后的菌株称为。
16、、、和是筛选营养缺陷型菌株的四个环节。
17、、、和是四种从混合菌液中检出营养缺陷型菌株方法。
18、普遍转导与局限转导的主要区别在于:第一,普遍转导噬菌体是属于噬菌体,而局限转导噬菌体属于噬菌体;第二,普遍转导噬菌体能转移供体菌的基因,而局限转导噬菌体只能转移供体菌的基因。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
107 八、鼠伤寒沙门氏菌/回复突变试验 Salmonella Typhimurium / Reverse Mutation Assay
1 范围 本规范确定了鼠伤寒沙门氏菌/回复突变试验的基本原则、要求和方法。 本规范适用于化妆品原料及其产品的基因突变检测。
2 规范性引用文件 OECD Guidelines for Testing of Chemicals (No.471,Adopted:21,July 1997)。
3 定义 3.1 回复突变(Reverse mutation) 细菌在化学致突变物作用下由营养缺陷型回变到原养型(prototroph)。 3.2 基因突变 (Gene mutation) 在化学致突变物作用下细胞DNA中碱基对的排列顺序发生变化。 3.3 碱基置换突变 (Base substitution mutation) 引起DNA链上一个或几个碱基对的置换。 碱基置换有转换(transition)和颠换(transversion)两种形式。 转换是DNA链上的一个嘧啶被另一嘧啶所替代,或一个嘌呤被另一嘌呤所代替。 颠换是DNA链上的一个嘧啶被另一嘌呤所替代,或一个嘌呤被另一嘧啶所代替。 3.4 移码突变( Frameshift mutation) 引起DNA链上增加或缺失一个或多个碱基对。 3.5 鼠伤寒沙门氏菌/回复突变试验( Salmonella typhimurium/reverse mutation assay) 利用一组鼠伤寒沙门氏组氨酸缺陷型试验菌株测定引起沙门氏菌碱基置换或移码突变的化学物质所诱发的组氨酸缺陷型(his-)→原养型(his+)回复突变的试验方法。 3.6 S9 经多氯联苯(PCB混合物)或苯巴比妥钠和β-萘黄酮结合诱导的大鼠制备肝匀浆,在9000g下离心10min后的肝匀浆上清液。
4 原理 鼠伤寒沙门氏组氨酸营养缺陷型菌株不能合成组氨酸,故在缺乏组氨酸的培养基上,仅少数自发回复突变的细菌生长。假如有致突变物存在,则营养缺陷型的细菌回复突变成原养型,因而能生长形成菌落,据此判断受试物是否为致突变物。 某些致突变物需要代谢活化后才能引起回复突变, 故需加入经诱导剂诱导的大鼠肝制备的S9混合液。
5 仪器和设备 培养箱、恒温水浴、振荡水浴摇床、压力蒸汽消毒器、干热烤箱、低温冰箱(-80℃) 或液氮生物容器、普通冰箱、天平(精密度0.1g和0.0001g)、混匀振荡器、匀浆器、菌落计数器、低温高速离心机,玻璃器皿等。 108
6 培养基和试剂 6.1 0.5mmol/L组氨酸-0.5mmol/L生物素溶液 成分: L-组氨酸(MW 155) 78mg D-生物素(MW 244) 122mg 加蒸馏水至 1000mL 配制:将上述成分加热,以溶解生物素,然后在0.068MPa下高压灭菌20min。贮于4℃冰箱。 6.2 顶层琼脂培养基 成分: 琼脂粉 1.2g 氯化钠 1.0g 加蒸馏水至 200mL 配制:上述成分混合后,于0.103MPa下高压灭菌30min。实验时,加入0.5mmol/L组氨酸—0.5mmol/L生物素溶液20mL。 6.3 Vogel-Bonner (V-B) 培养基E 成分:枸椽酸(C6H8O7·H2O) 100g 磷酸氢二钾(K2HPO4) 500g 磷酸氢铵钠(NaNH4HPO4·4H2O) 175g 硫酸镁(MgSO4·7H2O) 10g 加蒸馏水至 1000mL 配制:先将前三种成分加热溶解后,再将溶解的硫酸镁缓缓倒入容量瓶中,加蒸馏水至1000mL。于0.103MPa下高压灭菌30min。储于4℃冰箱。 6.4 20%葡萄糖溶液 成分:葡萄糖 200g 加蒸馏水至 1000mL 配制:加少量蒸馏水加温溶解葡萄糖,再加蒸馏水至1000mL。于0.068MPa下高压灭菌20min。储于4℃冰箱。 6.5 底层琼脂培养基 成分:琼脂粉 7.5g 蒸馏水 480mL V-B培养基E 10mL 20%葡萄糖溶液 10mL 配制:首先将前两种成分于0.103MPa下高压灭菌30min后,再加入后两种成分,充分混匀倒底层平板。按每皿25mL制备平板,冷凝固化后倒置于37℃培养箱中24h,备用。 6.6 营养肉汤培养基 成分:牛肉膏 2.5g 胰 胨 5.0g 磷酸氢二钾(K2HPO4) 1.0g 加蒸馏水至 500mL 配制:将上述成分混合后,于0.103MPa下高压灭菌30min。储于4℃冰箱。 6.7 盐溶液(1.65mol/L KCl+0.4mol/L MgCl2) 成分:氯化钾(KCl) 61.5g 氯化镁(MgCl2·6H2O) 40.7g 加蒸馏水至 500mL 109
配制:在水中溶解上述成分后,于0.103MPa下高压灭菌30min。储于4℃冰箱。 6.8 0.2mol/L磷酸盐缓冲液(pH7.4) 成分:磷酸二氢钠(NaH2PO4·2H2O) 2.965g 磷酸氢二钠(Na2HPO4·12H2O) 29.015g 加蒸馏水至 500mL 配制:溶解上述成分后,于0.103MPa下高压灭菌30min。储于4℃冰箱。 6.9 S9混合液 成分 每毫升S9混合液 肝S9 100l 盐溶液 20l 灭菌蒸馏水 380l 0.2mol/L磷酸盐缓冲液 500l 辅酶II(NADP) 4mol 6-磷酸葡萄糖(G-6-P) 5mol 配制:将辅酶II和6-磷酸葡萄糖置于灭菌三角瓶内称重,然后按上述相反的次序加入各种成分, 使肝S9加到已有缓冲液的溶液中。该混合液必须临用现配,并保存于冰水浴中。实验结束,剩余S9混合液应该丢弃。 6.10 菌株鉴定用和特殊用途试剂 6.10.1 组氨酸—生物素平板 成分:琼脂粉 15g 蒸馏水 944mL (V-B)培养基E 20mL 20%葡萄糖 20mL 灭菌盐酸组氨酸水溶液(0.5g/100mL) 10mL 灭菌0.5mmol/L生物素溶液 6mL 配制:高压灭菌琼脂和水后,将灭菌20%葡萄糖,V-B培养基和组氨酸溶液加进热的琼脂溶液中。待溶液稍为冷却后,加入灭菌生物素,混匀,浇制平板。 6.10.2 氨苄青霉素平板和氨苄青霉素/四环素平板 成分:琼脂粉 15g 蒸馏水 940mL (V-B)盐溶液 20mL 20%葡萄糖 20mL 灭菌盐酸组氨酸溶液(0.5g/100mL) 10mL 灭菌0.5mmol/L生物素溶液 6mL 氨苄青霉素溶液(8mg/mL于0.02mol/LNaOH中) 3.15mL 四环素溶液(8mg/mL于0.02mol/L HCl中) 0.25mL 配制:琼脂和水高压灭菌20min,将无菌的葡萄糖、VB盐溶液和组氨酸—生物素溶液加进热的溶液中去,混匀。冷却至大约50℃,无菌条件下加入四环素溶液和/或氨苄青霉素溶液。 应该在倾注琼脂平板后几天内,制备主平板。 6.10.3 营养琼脂平板 成份:琼脂粉 7.5g 营养肉汤培养基 500mL 110
配制:于0.103MPa下高压灭菌30min后倾注平板。 7 试验菌株及其生物学特性鉴定 7.1 试验菌株 采用TA97、TA98、TA100和TA102一组标准测试菌株。 7.2 生物学特性鉴定 新获得的或长期保存的菌种,在试验前必须进行菌株的生物特性鉴定。菌株鉴定的判断标准,如表1所示。 表1 试验菌株鉴定的判断标准
菌株 组氨酸 缺陷 脂多糖屏障缺损 氨苄青霉素抗性 切除修复缺损 四环素 抗性 自发回变菌落数*
TA97 TA98 TA100 TA102 + + + + + + + + + + + + + + + - - - - + 90-180 30-50 100-200 240-320
注 “+”表示需要组氨酸 “+”表示具有rfa突变 “+”表示具有R因子 “+”表示具有△uvrB突变 “+”表示具有pAQ1质粒 *在体外代谢活化条件下自发回变菌落数略增
7.2.1 组氨酸缺陷 原理:组氨酸缺陷型试验菌株本身不能合成组氨酸,只能在补充组氨酸的培养基上生长,而在缺乏组氨酸的培养基上,则不能生长。 鉴定方法:将测试菌株增菌液分别于含组氨酸培养基平板和无组氨酸平板上划线,于37℃下培养24h后观察结果。 结果判断:组氨酸缺陷型菌株在含组氨酸平板上生长,而在无组氨酸平板上则不能生长。 7.2.2 脂多糖屏障缺损 原理:具有深粗糙(rfa)的菌株,其表面一层脂多糖屏障缺损,因此一些大分子物质如结晶紫能穿透菌膜进入菌体,从而抑制其生长,而野生型菌株则不受其影响。 鉴定方法:吸取待测菌株增菌液0.1mL于营养琼脂平板上划线,然后将浸湿的0.1%结晶紫溶液滤纸条与划线处交叉放置。37℃下培养24h后观察结果。 结果判断:假若待测菌在滤纸条与划线交叉处出现一透明菌带,说明该待测菌株具有rfa突变。 7.2.3 氨苄青霉素抗性 原理:含R因子的试验菌株对氨苄青霉素有抗性。因为R因子不太稳定,容易丢失,故用氨苄青霉素确定该质粒存在与否。 鉴定方法:吸取待测菌株增菌液0.1mL,在氨苄青霉素平板上划线,37℃下培养24h后观察结果。 结果判断;假若测试菌在氨苄青霉素平板上生长,说明该测试菌具有抗氨苄青霉素作用,表示含R因子,否则,表示测试菌不含R因子或R因子丢失。 7.2.4 紫外线敏感性 原理:具有△uvrB突变的菌株对紫外线敏感,当受到紫外线照射后,不能生长,而具有野生型切除修复酶的菌株,则能照常生长。
