碱金属原子双线结构的原因
§21碱金属双线

式中 l r me
电子的轨道角动量 电子的静止能量
U 电子磁矩(内禀磁矩)s在磁场中的势能: s B
E0=mec2
1 s s( s 1), s ; s g s B s s s(s 1) gs B ; 2 1 Zg s B e s l 所以,在电子坐标系中 U 3 4 0 E0 r
钠的黄色D线
但要计算钠3P能级的分裂 却不很容易,(5)式不能直 接用.因为钠的原子核外 有10个电子屏蔽着,使最 后一个单电子感受到的Ze 并非核的电荷,而是有效 电荷z有效e。Z有效=3.5
需要指出,对原子的自旋角动量、轨道角动量和 总角动量有贡献的电子数目不止一个时,理论上 可以证明自旋轨道相互作用引起的附加能量U也 正比于 S L,但公式(5)有的可用,但(6)不能。
(4)
把式(4)和(3)代入式(2),得到自旋一轨道耦合 项: ( Z )4 E [ j ( j 1) s( s 1) l (l 1)] 0 U , l 0 (5) 3 1
4n
对于单电子:
l (l )(l 1) 2
( Z )4 E0 U 3 ; 2n (2l 1)(l 1) ( Z )4 E0 U 3 ; 2n l (2l 1)
假设是圆轨道;可证明,对任意形状的轨道都适用 电流i在中心处(电子所在位置)产生的磁场大小为: 1 2i 1 Ze B 2 4 0 c r 4 0 c 2 r 2
B Ze 1 Ze ( ) r l 2 3 3 4 0 c r 4 0 E0 r 1
1 当j l , l 0 2 1 当j l , l 0 2
双能级差值
4.4 碱金属双线

对于同一个n,碱金属能级分裂成n个,这可以 从原子实的极化和轨道贯穿加以解释。
3、斯特恩—盖拉赫实验
证实了:
L l(l 1) h 原子的空间量子化
2 电子自旋假设的正确性
l 0,1,…,(n- 1)
量子力学关于l 的取值的正确性即
4、碱金属原子状态的描述
(1)描述电子运动状态的量子数 主量子数n:决定了原子能量的主要部分。n=1、2、3… 轨道角量子数l:决定了轨道的角动量,并由于轨道形状的 不同而影响能级,同一n分成不同l 的能级。
一辅系和柏格曼系由三条组成,主线系和二辅助系由两 条组成。 由于电子自旋和轨道运动的相互作用,碱金属原子能级除 S能级外都分裂成两个,称为双重能级。 考虑能级的分裂后,根据跃迁选择定则,可解释光谱的双 线结构。
3.5为什么谱项的S项的精细结构总是单层的?试从电子 自旋与轨道相互作用的物理概念说明。
当 n=2,s=1/2,l=1时,总角量子数 j=1/2或 j=3/2,而题 中 j=5/2,不符合量子数的取值规律,所以不是。
当 n=3时,l=0、1、2,而题中 l=3,不符合量子数的取 值规律,所以不是。
碱金属原子态的符号
碱金属无 此原子态
二、对碱金属光谱双线结构的解释
l 1、单电子辐射跃迁定则: 1, j 0, 1
1 l
2
2
1 2
(l
1)
2
1 jl
2 jl1
2
l≠0
1、所以自旋轨道相互作用能为
0
Els
AL
S
Al 2 2
A (l 2
碱金属原子光谱的精细结构
l
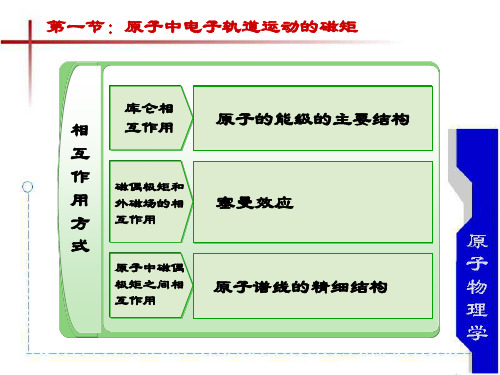
分量,与j垂直的分量对外的平均效 果抵消了(由于绕j转动的缘故)。
j
对外起作用的是它沿j的延线的分量, j
这就是电子的总磁矩
单电子磁矩与角动量的关系
对图示进行分析,利用三角形的余弦定理
可求出 j
lˆ l(l 1)
l
sˆ s(s 1)
ˆj
j( j 1)
1、载流闭合回路的磁矩 μ (IS)n 对应力矩: τ μ B
经典物理:封闭矩形线圈
1、载流闭合回路的磁矩 (IS)n 力矩τ μ B
2、回转运动电子的角动量与磁矩 μ e L L
2m
1、载流闭合回路的磁矩 (IS)n 力矩τ μ B
观察到两个取向;
难道是轨道角动量矢量合成?
第四章:原子的精细结构:电子的自旋
第一节 原子中电子轨道运动磁矩 第二节 史特恩—盖拉赫实验 第三节 电子自旋的假设 第四节 碱金属双线 第五节 塞曼效应 第六节 氢原子能谱研究进展
埃伦费斯特和他的学生,1924年,莱顿. 左起: 第开, 古兹密特, 汀柏根, 埃 伦费斯特, 克罗尼格, 和费米。
原子处于基态。
沿着-x方向观察:
沿X水平方向运动的氢原子束,其速度:v
3kT m
为了使进入磁场的氢原子 束受到力的作用,这个磁 场必须是不均匀的磁场区 (0.1nm的线度范围内)。
N
S
磁场沿Z 方向是变化的,即
Bz 0, Bz Bz 0
z
x y
在磁场中,磁矩在磁场中的势能:
ˆj2 lˆ2 sˆ2
ˆj2 sˆ2 lˆ2
g j gl
钠金属光谱

碱金属原子光谱碱金属原子光谱,特指碱金属锂、钠、钾、铷、铯等元素的光谱。
它们具有相似的结构,明显地分成几个线系。
通常观察到的有主线系、第一辅线系(漫线系)、第二辅线系(锐线系)和伯格曼线系(基线系)。
众所熟知的钠黄光波长为589.3纳米,就是钠光谱主线系的第一条谱线。
碱金属原子都具有相似的结碱金属原子光谱构,内层的z-1 个电子与原子核组成原子实,最外层只有一个价电子,与氢原子有些类似,不同的是电子运动对原子实有极化和贯穿作用,引起不同轨道的电子能态的较大分裂,能级对l的简并解除。
另外由于电子自旋取向不同,引起自旋轨道耦合的能量微小分裂,因此碱金属原子的能级除S态是单层的外,其他P、D、F态都是双层的。
根据单价原子光谱的选择定则,可得出,主线系和锐线系是双线结碱金属原子光谱构,漫线系和基线系为三线结构。
观察结果图1画出了锂原子光谱的四个线系。
从图中可以看到主线系的波长范围最宽、第一条是红色的,碱金属原子光谱其余的都在紫外。
线系限是229.97nm;第一辅线系在可见光区部分;第二辅线系的第一条在红外区,其余在可见光区,这二线系有同一线系限,伯格曼线系在红外区,其他碱金属原子也有相似的光谱线系,只是波长不同,例如钠的主线系的第一条线是大家熟悉的黄色光,波长为589.3nm。
原子结构碱金属原子与氢原子光谱规律相似,是由于它们的原子结构相似,虽然碱金属元素与氢元素的性质极不相同,但它们都只有一个外层电子,称为价电子。
内满充壳层电子与原子核组成原子实,价电子即处于原子实的中心势场中。
按锂、钠、钾、铷、铯的次序原子实内的电子数分别是2、10、18、36、54、86,价电子所在的轨道的主量子数分别为n≥2、n≥3、n≥4、n≥5、n≥6。
能级公式碱金属原子的能级公式与氢原子相似公式式中墹l为量子亏损,是一个与角动量量子数l有关的正数,R是碱金属的里德伯常数。
显然,碱金属的能级不但与n有关,而且与l有关。
上式还可写为Z*称为有效核电荷数。
最新原子物理学——碱金属原子光谱的精细结构
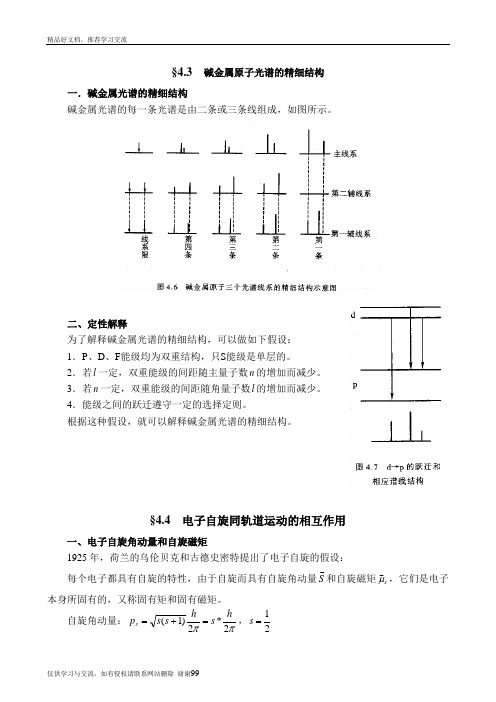
§4.3 碱金属原子光谱的精细结构一.碱金属光谱的精细结构碱金属光谱的每一条光谱是由二条或三条线组成,如图所示。
二、定性解释为了解释碱金属光谱的精细结构,可以做如下假设:1.P 、D 、F 能级均为双重结构,只S 能级是单层的。
2.若l 一定,双重能级的间距随主量子数n 的增加而减少。
3.若n 一定,双重能级的间距随角量子数l 的增加而减少。
4.能级之间的跃迁遵守一定的选择定则。
根据这种假设,就可以解释碱金属光谱的精细结构。
§4.4 电子自旋同轨道运动的相互作用一、电子自旋角动量和自旋磁矩1925年,荷兰的乌伦贝克和古德史密特提出了电子自旋的假设:每个电子都具有自旋的特性,由于自旋而具有自旋角动量S 和自旋磁矩s μ ,它们是电子本身所固有的,又称固有矩和固有磁矩。
自旋角动量:ππ2*2)1(h s h s s p s =+=,21=s外场方向投影:π2h m S s z =, 21±=s m 共2个, 自旋磁矩:s s p me -=μ Bs s h s s m e p m e μπμ32)1(-=+-=-= 外场方向投影:B z z S me μμ±=-= 共两个⇒偶数,与实验结果相符。
1928年,Dirac 从量子力学的基本方程出发,很自然地导出了电子自旋的性质,为这个假设提供了理论依据。
二、电子的总角动量电子的运动=轨道运动+自旋运动轨道角动量:ππ2*2)1(h l h l l p l =+= 12,1,0-=n l 自旋角动量:ππ2*2)1(h s h s s p s =+= 21=s 总角动量: s l j p p p += ππ2*2)1(h j h j j p j =+= s l j +=,1-+s l ,……s l -当s l >时,共12+s 个值当s l <时,共12+l 个值由于 21=s 当0=l 时,21==s j ,一个值。
第四章 原子的精细结构 21节 碱金属双线1

§21 碱金属双线
掌握碱金属双线产生的原因
掌握旋-轨相互作用导致的能级分裂的计算方法
① 自旋角动量与旋-轨相互作用;
② 碱金属双线中能量与光谱的计算。
理论讲授
2学时
第三章 原子的精细结构:电子的自旋
§21 碱金属双线
一、碱金属原子谱线的精细结构:定性考虑
Li 原子的光谱精细结构:在高分辨率光谱仪下为双线或三线结构。
其中,主线 系、二辅系为双线结构,一辅系、柏格曼系为三线结构。
主线系: S nP 2→ ,3,2=n 二辅系(锐线系)P nS 2→ ,4,3=n 一辅系(漫线系)P nD 2→ ,4,3=n 柏格曼系(基线系)D nF 3→ ,5,4=n
前项为动项,后项为固定项。
推想:①有主线、二辅系,S 能级为单层的,l 能级为双层的;
②随l 增加,能级分裂越来越小;
③遵从一定的选择定则。
4[1].3 4.4 碱金属原子光谱的精细结构
p j = pl + ps或p j = pl + ps
h h +s 或pj = l 2π 2π h h = (l + s ) 或 (l s ) 2π 2π h = j , j = l + s或 l s 2π
j:电子的总角动量量子数
h pj = l 2π
h s 2π
由电磁学理论,考虑电子的自旋磁距后附加的能量为
1 3 1 1 如l = 1,j = 1 + = 或1 - = 2 2 2 2
h h pl = 2 = 1.41 2π 2π 1 3 h h ps = × = 0.87 2 2 2π 2π
3 5 h h pj = × = 1.94 2 2 2π 2π h 1 3 h 或= × = 0.87 2 2 2π 2π
附加光谱项和精细结构裂距
T
T
j =l +
1 2
l = a 2
l +1 =a 2
Tls上=-a l 2
j =l
1 2
T0
nl
Tls下=a
l +1 2
双层能级间隔用波数表示
1 Rα 2 z 4 ~ v = T1 T2 = a (l + ) = 3 米 1 2 n l (l + 1)
~ v 与n 3和l (l + 1)成反比,与z 4成正比
对电子: 可得:
0 z ev B= sin α 2 4π r
mrv sin α = pl
ze 1 1 B= 3 pl (ε 0 0 = 2 ) 2 4πε 0 mc r c 1
3, θ 的取值 cos
p j = pl + ps 2 pl ps cos θ
8.4碱金属原子光谱的双线结构和反常Zeeman效应
(17)
22
17
利用8.3节的结果,可得:
L l j mj | Sz | l j mj L
mj 2 j , j l 1/ 2
(18)
mj (2 j 2) , j l 1/ 2
(l 0)
按照简并态一级微扰近似,在弱磁场中,电子
的能量本征值可以相当好地近似表示成:
Enljm j
Enlj
(1 (1
L
p2
2 V (r) (r)S L eB 2c
jz
eB
2c
Sz
(14)
要严格处理上式最后一项,是很麻烦的。为此先
不考虑最后一项,则H本征值问题与处理碱金属光谱
双线分裂相同。此时 (l 2 , j2 , jz ) 仍为守恒量,H的本
征态仍然可以表示成
nljmj (r,,, Sz ) Rnlj (r)nljmj (,, Sz ) (15)
数可表示为 (H ,l2 ,lz , Sz ) 的共同本征函数 ljmj (r,,)ms (Sz )
本征值则为
eB
Enlmms
Enl
2c
(m 2ms )
(ms 1 2)
Enl
eB
2c
(m 1)
(13)
考虑到光辐射跃迁定则,ms 0 ,跃迁只能分别在
ms 1 2及 ms 1 2 两组能级内部进行,因此尽管 能级有所改变,比较13式与11式,对谱线分裂却没
该现象在1896年被Zeeman首先观察到.
(1)简单(正常)塞曼效应:在强磁场中, 原子光谱发生分裂(一般为3条)称为正常 Zeeman效应。 。
(2)复杂(反常)塞曼效应:当外磁场较弱,
轨道-自旋相互作用不能忽略时,将产生复杂
第四章碱金属原子
第四章碱金属原子习题解答4.1已知锂原子光谱主线系最长波长nm 7.670=λ,辅线系系限波长nm 9.351=∞λ,求锂原子第一激发电势和电离电势。
解:主线系最长波长的谱线对应跃迁为2p 2s ,有:22)2/()2/(/1p R s R ∆--∆-=λ而辅线系系限对应2)2/(/1p R ∆-=∞λ,所以)m (10333.4109.351/1107.670/1/1/1)2/(16992---∞⨯=⨯+⨯=+=∆-λλs R得:第一激发电势为V)(853.1107.670106.11031063.6])2()2([91983422121=⨯⨯⨯⨯⨯⨯=⋅=∆--∆-=∆=---λe hc R R e hc e E u p s电离电势为V)(386.5106.11031063.610333.4)2(19834621=⨯⨯⨯⨯⨯⨯=∆-=-=--∞∞s e hcR e E E u4.2 钠原子基态为3s ,已知其主线系第一条线(共振线)波长为589.6nm ,漫线系第一条线的波长为819.3nm ,基线系第一条线的波长为1845.9nm ,主线系的系限波长为241.3nm ,试求3S,3P,3D,4F 各谱项的项值。
解:由题意知:)m (10144.4nm 3.241/1/1S 316-∞⨯===λ由)m (10696.1nm 6.589/1/1P 3S 3161-⨯===-λ得: )m (10448.2P316-⨯= 由)m (10221.1nm 3.819/1/1D 3P 3162-⨯===-λ得: )m (10227.1D 316-⨯=又由)m (10542.0nm 9.1845/1/1F 4D 3163-⨯===-λ得:)m (10685.0F 416-⨯=4.3 钾原子共振线波长为766.5nm ,主线系系线波长为285.8nm ,已知钾原子基态为4s ,试求4S ,4P 谱项的量子数亏损s ∆、p ∆各为多少? 解:由∞=∆-λ/1)4/(2s R 得:229.2108.28510973731449=⨯⨯-=-=∆-∞λR s又由1221)4()4(λ=∆--∆-p R s R 得:)m (10194.2nm5.7661nm 8.285111)4(1612-∞⨯=-=-=∆-λλp R 76355.110194.2/46=⨯-=∆R p4.4 处于3D 激发态的锂原子,向低能级跃迁时可产生哪些光谱线?在能级图上表示出来:(1)不考虑精细结构;(2)考虑精细结构。
徐州工程学院原子物理复习学习
徐州⼯程学院原⼦物理复习学习11光伏原⼦物理75分范围及参考答案注:此份试卷是由11测试班原⼦物理⽼师腾绍勇⽼师给的纸质稿,后经孟祥龙同学编辑⽽成的。
答案出⾃11光伏、11测试两个班多位⼤神之⼿,由于时间仓促,内中错误难免会有很多,在此,此份材料只作为参考材料,若考试考不到,本⼈不负任何责任。
⼀、选择题(共10⼩题,每题2分,共计20分)1、原⼦半径的数量级是:(B )A 、cm 1010- B.m 1010- C.m 108- D.m 1310-2、根据波尔理论,若将氢原⼦激发到n=5的状态,则:(A )A.可能出现10条谱线,分属4个线系B.可能出现9个谱线,分属3个线系C.可能出现11条谱线,分属5个线系D.可能出现⼀条谱线,属莱曼系3、碱⾦属原⼦能级的双重结构是由于下⾯的原因产⽣:(A )A.价电⼦⾃旋与轨道⾓动量相互作⽤B.原⼦实极化C.价电⼦的轨道贯穿D.相对论效应4、氦原⼦有单态和三重态两套能级,从⽽它们产⽣的光谱特点是:(D )A.单能级各线系皆为单线,三重能级各线皆为三线B.单能级各线系皆为单线,三重能级各线系皆为双线C.单能级各线系皆为双线,三重能级各线系皆为三线D.单能级各线系皆为单线,三重能级各线系较为复杂,不⼀定是三线5、原⼦中轨道磁矩µL 和轨道⾓动量L 的关系应为:(B ) A.L m e L 2e -=µ B.L m e L 2e =µ C.L m e L e =µ D.L m eL e -=µ 6、我们说可以⽤描写碱⾦属原⼦中价电⼦的量⼦数n ,l,j 来描写伦琴射线光谱对应的状态,确切地说应该是描写:(A )A.内壳层具有空位的状态B.内壳层某个电⼦的状态C.K 壳层电⼦的状态D.最外壳层价电⼦的状态7、在LS 耦合下,两个⾮同科p 电⼦能形成的原⼦态是:(D )A. D 1,D 3B.S P D 131,,C. D P D P 3311,,,D.S S P P D D 31313,1,,,,8、镁原⼦(Z=12)处于基态时价电⼦的原⼦组态及基态原⼦应是:(A )A. 013s 3S sB. 032s 2P p C 012s 2S s .D.0333P p s 9、电⼦填充外层原⼦轨道是,先填4s 轨道后填3d 轨道,是由于:(A )A.n 内层电⼦对4s 电⼦的屏蔽作⽤不如3d 电⼦的屏蔽作⽤强B.3d 电⼦的⾃旋-⾃旋作⽤⽐4s 电⼦的强C.3d 电⼦与核的库伦作⽤⽐4s 电⼦的更强D.两电⼦间的⾃旋轨道作⽤使4s 能级低于3d 能级10、通过测量β衰变的β离⼦能谱,可得出正确的结论:(B )A.为连续谱,最⼤值不确定,与核具有能级相⽭盾B.为连续谱,有确定的最⼤值,与核具有能级不⽭盾C.为连续谱,有确定的最⼤值,与核具有能级相同D.为连续谱,没有确定的最⼤值,故仍可确定核能级。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碱金属原子双线结构的原因
碱金属原子(例如钠、钾等)的双线结构主要是由于光谱学的现象,具体来说,是由于电子的激发和跃迁导致的。
这一现象被称为碱金属的双线结构或双黄线。
在碱金属的光谱中,通常有两条特征性的黄色线,即D线。
以钠为例,这两条线的波长分别为589.0纳米和589.6纳米。
这种现象的原因可以追溯到碱金属原子的电子结构和能级跃迁。
* 电子结构:碱金属的原子结构中,最外层只有一个s电子。
这个s电子相对较远离原子核,因此它的激发和跃迁可以产生较低能级的光谱线。
* 激发和跃迁:当碱金属原子受到能量激发时,电子会从基态跃迁到一个较高的激发态。
当电子返回基态时,会释放能量,并且这个能量以光的形式发出。
由于电子结构的特殊性,碱金属的D线非常显著,产生两条主要的谱线。
这两条谱线的存在和相对位置是由于碱金属原子的电子结构,这也使得它们在光谱学和光谱分析中具有很高的重要性。
这种现象在光谱学和原子物理学的研究中有广泛的应用。
1。
