常用标液的配置与标定
EDTA标准溶液的配制与标定

EDTA标准溶液的配制与标定实验⼀EDTA标准溶液的配制与标定⼀、实验⽬的1. 掌握络合滴定的原理,了解络合滴定的特点。
2. 学习EDTA标准溶液的配制和标定⽅法3. 了解⾦属指⽰剂的特点,熟悉⼆甲酚橙、钙指⽰剂的使⽤及其终点颜⾊的变化。
⼆、实验原理⼄⼆胺四⼄酸(简称EDTA)难溶于⽔,其标准溶液常⽤其⼆钠盐(EDTA·2Na·H2O,分⼦量M=392.28)采⽤间接法配制。
标定EDTA溶液的基准物质有Zn、ZnO、CaCO3、Cu、MgSO4·7H2O、Hg、Ni、Pb等。
⽤于测定Pb2+、Bi3+含量的EDTA溶液可⽤ZnO或⾦属Zn作基准物进⾏标定。
以⼆甲酚橙为指⽰剂,在pH=5-6的溶液中,⼆甲酚橙指⽰剂(XO)本⾝显黄⾊,⽽与Zn2+的络合物显紫红⾊。
EDTA能与Zn2+形成更稳定的络合物,当使⽤EDTA 溶液滴定⾄近终点时,EDTA会把与⼆甲酚橙络合的Zn置换出来,⽽使⼆甲酚橙游离,因此溶液由紫红⾊变为黄⾊。
其变⾊原理可表达如下:XO(黄⾊)+Zn2+ZnXO(紫红⾊)ZnXO(紫红⾊)+EDTA Zn-EDTA(⽆⾊) +XO(黄⾊)EDTA溶液若⽤于测定⽯灰⽯或⽩云⽯中的CaO、MgO的含量及测定⽔的硬度,最好选⽤CaCO3为基准物质进⾏标定。
这样基准物质和被测组分含有相同的成分,使得滴定条件⼀致,可以减⼩误差。
⾸先将CaCO3⽤HCl溶解后,制成Ca标准溶液,调节酸度⾄pH≥12,以钙指⽰剂作指⽰剂,⽤EDTA滴⾄溶液由酒红⾊变为纯蓝⾊。
三、仪器和药品仪器:电⼦分析天平、酸式滴定管、移液管、锥形瓶、容量瓶、烧杯、试剂瓶。
药品:(1)以ZnO为基准物时所⽤试剂:⼄⼆胺四⼄酸⼆钠(AR)、ZnO(AR)、六次甲基四胺(20%)、⼆甲酚橙指⽰剂(0.2%)、HCl(1:1)。
(2)以CaCO3为基准物质时所⽤试剂:CaCO3(AR)、氨⽔(1:1)、NaOH溶液(10%)、1%钙指⽰剂(固体指⽰剂)、⼄⼆胺四⼄酸⼆钠(AR)、Mg溶液(溶解1gMgSO4·7H2O于⽔中,稀释⾄200mL)。
氢氧化钠标准溶液的配制和标定

氢氧化钠标准溶液的配制和标定氢氧化钠(NaOH)是一种常用的化学试剂,广泛应用于实验室中。
在实验室工作中,我们经常需要配制和标定氢氧化钠标准溶液,以确保实验的准确性和可靠性。
本文将介绍氢氧化钠标准溶液的配制和标定方法,希望能对您的实验工作有所帮助。
一、氢氧化钠标准溶液的配制。
1. 实验室常用的氢氧化钠标准溶液浓度一般为0.1mol/L,配制方法如下:a. 取一定质量的氢氧化钠固体,加入适量的去离子水中,用玻璃棒搅拌均匀,直至固体完全溶解;b. 将溶液转移至容量瓶中,用去离子水稀释至刻度线,摇匀即得到0.1mol/L的氢氧化钠标准溶液。
2. 配制好的标准溶液应密封保存,在室温下避光保存,避免碳酸气体的吸收,以确保溶液浓度的稳定性。
二、氢氧化钠标准溶液的标定。
1. 准备一定浓度的盐酸标准溶液,用天平称取一定质量的氢氧化钠固体,溶解于适量的去离子水中,转移至容量瓶中,用去离子水稀释至刻度线,摇匀即得到盐酸标准溶液。
2. 取一定体积的氢氧化钠标准溶液,加入几滴酚酞指示剂,用盐酸标准溶液滴定至颜色由粉红色变为无色,记录所耗盐酸标准溶液的体积V1。
3. 重复上述步骤,至少进行3次滴定,取平均值计算氢氧化钠标准溶液的浓度C。
三、注意事项。
1. 在配制和标定氢氧化钠标准溶液时,要注意实验操作的精确性,尽量减小误差,保证实验结果的准确性。
2. 配制好的标准溶液应进行标签标注,包括浓度、配制日期等信息,以便日后使用和识别。
3. 实验操作中要注意安全,避免氢氧化钠溶液的溅洒和吸入,避免对皮肤和粘膜的刺激。
通过本文的介绍,相信您对氢氧化钠标准溶液的配制和标定有了更清晰的认识。
希望您在实验工作中能够严格按照操作规程进行操作,确保实验结果的准确性和可靠性。
祝您实验顺利!。
标准溶液的配制与标定

标准溶液的配制与标定标准溶液的配制与标定的一般规定:1.配制及分析中所用的水及稀释液,在没有注明其它要求时,系指其纯度能满足分析要求的蒸馏水或离子交换水。
2.工作中使用的分析天平砝码,滴管,容量瓶及移液管均需较正。
3.标准溶液规定为20℃时,标定的浓度为准(否则应进行换算)。
4.在标准溶液的配制中规定用“标定”和“比较”两种方法测定时,不要略去其中任何一种,而且两种方法测得的浓度值之相对误差不得大于0.2%,以标定所得数字为准。
5.标定时所用基准试剂应符合要求,含量为99.95-100.05%,换批号时,应做对照后再使用。
6.配制标准溶液所用药品应符合化学试剂分析纯级。
7.配制0.02(M)或更稀的标准溶液时,应于临用前将浓度较高的标准溶液,用煮沸并冷却水稀释,必要时重新标定。
8.碘量法的反应温度在15-20℃之间。
(一)3N硫酸标准溶液配制1.配制0.1N硫酸标准溶液,量取3mLH2SO4注入1000mL水中,冷却摇匀。
0.5N硫酸标准溶液,量取15mL H2SO4注入1000mL水中,冷却摇匀。
1N硫酸标液量取30mL H2SO4注入1000mL水中,冷却摇匀。
3N硫酸标液量取90mL H2SO4注入1000mL水中,冷却摇匀。
切记一定是将浓硫酸往水里慢慢加。
2.标定(1)反应原理:Na2CO3+H2SO4→Na2SO4+H2O+CO2↑混合指示剂变色情况参见1N盐酸标准溶液的“标定”项下(2)仪器:滴定管50mL;锥形瓶250mL;125mL;磁坩埚;称量瓶。
(3)标定过程:基准物处理:取预先在玛瑙乳钵中研细之无水碳酸钠适量,置入洁净的磁坩埚中,在沙浴上加热,注意使运动坩埚中的无水碳酸钠面低于沙浴面,坩埚用磁盖半掩之,沙浴中插一支360℃温度计,温度计的水银球与坩埚底平,开始加热,保持270-300℃1小时,加热期间缓缓加以搅拌,防止无水碳酸钠结块,加热完毕后,稍冷,将碳酸钠移入干燥好的称量瓶中,于干燥器中冷却后称量。
EDTA标准溶液的配制与的标定

EDTA标准溶液的配制与的标定一、实验目的1、了解EDTA标液的配制和标定原理;2、掌握常用的标定EDTA的方法。
二、实验原理1、EDTA:乙二胺四乙酸H4Y(本身是四元酸),由于在水中的溶解度很小,通常把它制成二钠盐(Na2H2Y·2H2O),也称为EDTA或EDTA二钠盐。
EDTA相当于六元酸,在水中有六级离解平衡。
与金属离子形成螯合物时,络合比皆为1:1。
EDTA因常吸附0.3%的水分且其中含有少量杂质而不能直接配制标准溶液,通常采用标定法制备EDTA标准溶液。
标定EDTA的基准物质有纯的金属:如Cu、Zn、Ni、Pb,以及它们的氧化物。
某些盐类:如CaCO3、ZnSO4.7H2O、MgSO4.7H2O。
2、金属离子指示剂:在络合滴定时,与金属离子生成有色络合物来指示滴定过程中金属离子浓度的变化。
M+In←→MIn颜色甲颜色乙滴入EDTA后,金属离子逐步被络合,当达到反应化学计量点时,已与指示剂络合的金属离子被EDTA夺出,释放出指示剂的颜色:MIn+Y←→MY +In颜色乙颜色甲指示剂变化的pMep应尽量与化学计量点的pMsp一致。
金属离子指示剂一般为有机弱酸,存在着酸效应,要求显色灵敏,迅速,稳定。
常用金属离子指示剂:铬黑T(EBT):pH=10时,用于Mg2+,Zn2+,Cd2+,Pb2+,Hg2+,In3+,二甲酚橙(XO):pH5~6时,Zn2+K-B指示剂(酸性铬蓝(K)-荼酚绿(B)混合指示剂):pH=10时,用于Mg2+,Zn2+,Mn2+。
pH=12时,用于Ca2+。
三、实验步骤1、标准溶液和EDTA溶液的配制(1)、Ca2+标准溶液差减法称取计算量的CaCO3于150ml小烧杯中→溶解(少量水润湿,盖上表面皿,用滴管从烧杯嘴处滴加HCl至CaCO3完全溶解→冷却→定量转移至250ml容量瓶中→定容→计算Ca2+的浓度。
(2)、EDTA溶液的配制天平称取计算量的EDTA二钠盐于200ml烧杯中→温热溶解→冷却。
标准溶液的配制与标定
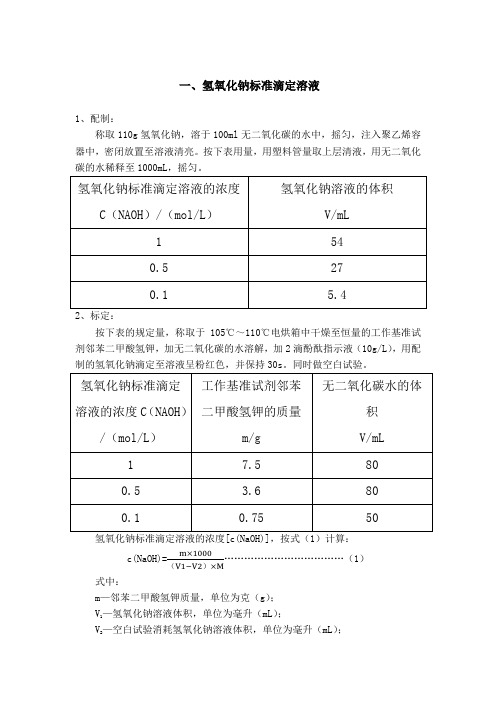
一、氢氧化钠标准滴定溶液1、配制:称取110g氢氧化钠,溶于100ml无二氧化碳的水中,摇匀,注入聚乙烯容器中,密闭放置至溶液清亮。
按下表用量,用塑料管量取上层清液,用无二氧化碳的水稀释至1000mL,摇匀。
2、标定:按下表的规定量,称取于105℃~110℃电烘箱中干燥至恒量的工作基准试剂邻苯二甲酸氢钾,加无二氧化碳的水溶解,加2滴酚酞指示液(10g/L),用配制的氢氧化钠滴定至溶液呈粉红色,并保持30s。
同时做空白试验。
氢氧化钠标准滴定溶液的浓度[c(NaOH)],按式(1)计算:c(NaOH)= (1)()式中:m—邻苯二甲酸氢钾质量,单位为克(g);—氢氧化钠溶液体积,单位为毫升(mL);V1—空白试验消耗氢氧化钠溶液体积,单位为毫升(mL);V2M—邻苯二甲酸氢钾的摩尔质量,单位为克每摩尔(g/mol)[M(KHC8H4O4)=204.22]二、盐酸标准滴定溶液1、配制:按下表规定量,量取盐酸,注入1000mL水中,摇匀。
2、标定按下表规定量,称取于270℃~300℃高温炉中灼烧至恒量的工作基准试剂无水碳酸钠,溶于50mL水中,加10滴溴甲酚绿-甲基红指示液,用配制的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,加盖具钠石灰管的橡胶塞,冷却,继续滴定至溶液再呈暗红色。
同时做空白试验。
盐酸标准滴定溶液的浓度c[HCl],按式(2)计算:c(HCl)=() (2)式中:m—无水碳酸钠质量,单位为克(g);V1—盐酸溶液体积,单位为毫升(mL);V2—空白试验消耗盐酸溶液体积,单位为毫升(mL);M—无水碳酸钠的摩尔质量,单位为克每摩尔(g/mol)[M(1/2Na2CO3)=52.994]三、硫酸标准滴定溶液1、配制:按下表规定量,量取硫酸,缓缓注入1000mL水中,冷却,摇匀。
2、标定按下表规定量,称取于270℃~300℃高温炉中灼烧至恒量的工作基准试剂无水碳酸钠,溶于50mL水中,加10滴溴甲酚绿-甲基红指示液,用配制的硫酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,加盖具钠石灰管的橡胶塞,冷却,继续滴定至溶液再呈暗红色。
标液配置

标准溶液的配制和标定规程甲:一般要求:以知其准确浓度的溶液叫做标准溶液,标准溶液的配制一般有直接法和标定法两种。
1、直接法:直接法指准确的称取一定量的高纯度试剂,溶解后,制成一定体积的溶液,根据其基准物质的重量和溶液的体积即可称出此准确浓度。
用此法配制的标准溶液不需要进行标定。
例如:称取4.9035g固体重铬酸钾,溶于水中后,稀释到1000ml容量瓶中,此溶液用于氧化还原滴定时,它的当量溶度是0.1000N2、标定法:标定法指先配制一种接近此需溶度的溶液,然后用基准物质(或以用基准物质标定的标准溶液)来确定它的准确浓度。
例如:欲配制0.1N盐酸溶液时,先配制成浓度接近于0.1N的盐酸溶液,然后称取一定量的基准物质碳酸钠进行标定,或用已知准确浓度的NAOH标准溶液进行标定。
这样即可求得盐酸溶液的准确浓度。
注:溶液的标定一般应平行操作2—3份,要求相对偏差不大于0.2%,然后取它的平均值,配制和标定的量器必要时进行校正,能用的水应是蒸馏水或交换水,有时甚至二次蒸馏水或二次交换水。
配制和标定好的标准溶液的贮瓶上,必须贴上标签,在标签上要写明:溶液的名称,准确浓度,配制日期,标定日期和配制及标定者的姓名。
乙:常用的标准溶液的配制和标定一、高锰酸钾分子量158.04 分子式:KMnO4因为固体的KMnO4常含有少量的MnO2等杂质,配溶液的蒸馏水中,常含有少量的有机物,能与KMnO4缓慢的反应,析出水合MnO2沉淀使其浓度降低,所以,即使是一级试剂也不宜用直接法配制KMnO4标准溶液。
1、配制:称取KMnO43.2—3.4g,溶于少量水中,然后以水稀释至1000ml,加热至沸保持微沸约1小时,以后放在暗处2—3天,用砂芯漏斗过滤除去沉淀,放在棕色瓶中,保持于暗处,此溶液的浓度用于Mn2+氧化还原反应时约0.1N. 2、标定:O40.2g,于准确称取在105--110℃烘干2小时,并冷却至室温的基准级NaC2SO450 ml摇溶,加热至75--80℃,用高锰酸钾溶250ml三角瓶中,用1N的H2液滴定,开始时,每滴加一滴KMnO4溶液都应充分摇动,待溶液中红色退去后,在滴加。
标准溶液的配制与标定
• 三、标准溶液
• 所谓标准溶液,是一种已知准确浓度的溶液。
(一)基准物质 用来直接配制标准溶液或标定溶液浓度的物质称为 基准物质。 作为基准物质应符合下列要求: 1.物质的组成应与化学式完全相符。若含结晶水,其结 晶水的含量也应与化学式相符。如草酸 H2C2O4·2H2O,硼砂Na2B4O7∙ 10H2O等。 2.试剂的纯度要足够高,一般要求其纯度应在99.9%以 上,而杂质含量应少到不致于影响分析的准确度。 3.试剂在一般情况下应该很稳定。例如不易吸收空气中 的水分和CO2,也不易被空气所氧化等。 4.试剂最好有比较大的摩尔质量。这样一来,对相同摩 尔数而言,称量时取量较多,而使称量相对误差减小。 5.试剂参加反应时,应按反应方程式定量进行而没有副 反应。
(二)基准物应具备的条件: ①纯度高 ②组成与化学式相符 ③性质稳定 ④使用时易溶解 ⑤最好的摩尔质量较大
(三)标定的两种方法
(1)直接标定:准确称取一定量的基准物,溶 于水后用待标定的溶液滴定,至反应完全。根 据所消耗待标定溶液的体积和基准物的质量, 计算出待标定溶液的准确浓度。 (2)间接标定:有一部分标准溶液,没有合适 的用以标定的基准试剂,只能用另一已知浓度 的标准溶液来标定。 如:乙酸溶液用NaOH标准溶液来标定,草酸 溶液用KMnO4标准液来标定等,当然,间接 标定的系统误差比直接标定要大些。
(五)标准溶液的标定要求
1.根据《化学试剂标准滴定溶液的制备》的规 定,标定准滴定溶液浓度时,须两人进行试 验,分别做 四 平行,每人平行测定结果极差 的相对值不大于 重复性临界极差的相对值 0.15% 。两人八行,测定结果 极差的相对值 不大于重复性临界极差的相对值 0.18% 2.结果取平均值 3.浓度值取四位有效数值 4.滴定分析标准溶液在常温(1525度)下,保 存时间一般不超过两个月。
hcl标准溶液的配制与标定
hcl标准溶液的配制与标定HCl标准溶液的配制与标定。
HCl标准溶液是化学实验室中常用的一种溶液,通常用于酸度测定、pH值调节等实验中。
正确的配制和标定HCl标准溶液对实验结果的准确性至关重要。
本文将详细介绍HCl标准溶液的配制和标定方法,希望能对大家有所帮助。
首先,我们需要准备一定浓度的盐酸溶液作为原料。
一般来说,实验室中常用的是浓度为37%的盐酸溶液,我们可以根据需要将其稀释至所需浓度。
在进行稀释时,需要注意将盐酸缓慢加入水中,并且要注意避免溅出和产生大量热量。
在搅拌均匀后,可以用PH试纸或PH计检测溶液的酸度,确保其达到所需的浓度。
接下来,我们需要准备所需浓度的NaOH溶液和酚酞指示剂。
NaOH溶液的浓度应该略高于HCl标准溶液的浓度,以确保标定的准确性。
酚酞指示剂是一种常用的酸碱指示剂,能够在酸性溶液中呈现无色,在碱性溶液中呈现粉红色。
在标定过程中,酚酞指示剂可以帮助我们准确地判断中和点。
接下来,我们将进行HCl标准溶液的标定。
首先,在酸碱中和瓶中取一定量的NaOH溶液,然后加入几滴酚酞指示剂。
随后,用瓶口滴定管从容器中取出一定量的HCl标准溶液,滴定至溶液由粉红色转变为无色。
记录下滴定所需的HCl标准溶液的体积,根据NaOH和HCl的摩尔浓度的关系,可以计算出HCl标准溶液的准确浓度。
在标定过程中,需要注意滴定管的使用方法,确保每滴溶液的体积尽可能准确。
此外,为了提高实验的准确性,可以进行多次重复标定,取平均值作为最终结果。
最后,标定完成后,我们需要将HCl标准溶液保存在干燥、避光的环境中,以确保其稳定性和准确性。
在使用时,需要注意密封瓶口,避免溶液浓度的变化。
总之,正确的HCl标准溶液的配制和标定对化学实验的准确性至关重要。
通过本文介绍的方法,希望能帮助大家正确、准确地进行HCl标准溶液的配制和标定,为实验结果的准确性提供保障。
氢氧化钾标准溶液的配制和标定
氢氧化钾标准溶液的配制和标定氢氧化钾(KOH)是一种常用的化学试剂,广泛应用于实验室中。
在实验室中,我们经常需要配制氢氧化钾标准溶液,并对其进行标定,以确保实验数据的准确性。
本文将介绍氢氧化钾标准溶液的配制和标定方法,希望能对大家有所帮助。
一、氢氧化钾标准溶液的配制。
1. 配制氢氧化钾标准溶液的原理。
氢氧化钾标准溶液通常用于酸碱中和实验中,其浓度通常为0.1mol/L。
配制氢氧化钾标准溶液的关键是控制其浓度,以确保实验结果的准确性。
2. 配制氢氧化钾标准溶液的步骤。
(1)称取适量的氢氧化钾固体,加入一定量的去离子水中,并用玻璃棒搅拌,直至完全溶解;(2)将溶液转移至容量瓶中,加入去离子水至刻度线,摇匀即可。
3. 配制氢氧化钾标准溶液的注意事项。
(1)在称取氢氧化钾固体时,应使用干燥的量筒或烧杯;(2)溶解氢氧化钾固体时,应搅拌均匀,以确保其完全溶解;(3)转移溶液至容量瓶时,应使用移液管,并注意避免溶液的挥发。
二、氢氧化钾标准溶液的标定。
1. 氢氧化钾标准溶液的标定原理。
标定氢氧化钾标准溶液的目的是确定其准确浓度,常用酸碱滴定法进行标定。
常用的标定试剂有盐酸、硫酸等。
2. 氢氧化钾标准溶液的标定步骤。
(1)取一定量的氢氧化钾标准溶液,加入酸性指示剂,如酚酞,使其呈粉红色;(2)用盐酸标准溶液滴定氢氧化钾标准溶液,直至溶液颜色变为无色为止;(3)记录滴定所需的盐酸标准溶液的体积,根据滴定反应计算氢氧化钾标准溶液的浓度。
3. 氢氧化钾标准溶液的标定注意事项。
(1)在滴定过程中,应缓慢加入标定试剂,直至颜色变化终点;(2)标定试剂的浓度应事先确定,并在实验中保持稳定;(3)记录滴定所需的标定试剂体积时,应注意准确读数,避免误差。
总结,氢氧化钾标准溶液的配制和标定是实验室常见的操作,正确的配制和标定方法能够保证实验数据的准确性。
在进行配制和标定时,应严格按照操作步骤进行,并注意实验中的细节问题,以确保实验结果的可靠性。
edta标准溶液的配制与标定
edta标准溶液的配制与标定介绍EDTA(乙二胺四乙酸)是一种常用的络合剂,常用于配制标准溶液和金属离子的定量分析中。
本文将介绍如何配制和标定EDTA标准溶液。
配制EDTA标准溶液步骤一:准备实验室试剂准备以下试剂:•EDTA粉末•点滴瓶•蒸馏水或去离子水步骤二:准备容器使用蒸馏水或去离子水清洗一个容器,确保容器干净无杂质。
步骤三:称取EDTA粉末称取适量的EDTA粉末,并将其转移到容器中。
根据所需的浓度和体积,确定EDTA的质量。
步骤四:加入蒸馏水或去离子水向容器中加入适量的蒸馏水或去离子水,使EDTA完全溶解。
搅拌溶液,直到EDTA完全溶解。
步骤五:调整pH值根据所需的实验条件,使用酸或碱调整溶液的pH值。
使用pH计测量溶液的pH值,并进行调整,直到达到预期的pH范围。
步骤六:调整溶液体积使用蒸馏水或去离子水将溶液体积调整至所需的体积。
使用容量瓶或移液管测量溶液的体积,并进行调整。
步骤七:保存溶液将配制好的EDTA标准溶液倒入一个干净的容器中,并标注溶液的浓度、配制日期和其他必要信息。
存储溶液在冷暗处,避免光照和高温。
标定EDTA标准溶液步骤一:准备样品选择需要测定的金属离子样品,并将其准备好。
确保样品干净,无杂质。
步骤二:配制配位反应液配制配位反应液,一般是使用NH4Cl和NH4OH配制的缓冲溶液。
确保配位反应液的pH值在指定的范围内。
步骤三:加入指示剂向配位反应液中加入适量的指示剂。
Y锌指示剂是常用的指示剂,它能与金属离子(如铜和镍)形成明显的变色反应。
步骤四:滴定EDTA标准溶液取一定体积的样品,加入配位反应液,并滴加EDTA标准溶液。
在滴加EDTA溶液的过程中,观察指示剂颜色的变化。
当指示剂颜色完全转变时,滴定结束。
步骤五:计算样品中金属离子的浓度根据滴定过程中EDTA标准溶液的用量,计算样品中金属离子的浓度。
根据滴定的终点和指示剂的变色反应,确定金属离子的浓度。
步骤六:记录实验数据将滴定过程中使用的试剂用量、滴定数据和计算结果等实验数据记录下来,并制作结果报告。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常用标液的配置与标定 硫代硫酸钠标准溶液的配制和标定: (依据国标GB/T5009.1-2003) C(Na2S2O3)=0.1 mol/L
1. 配制:称取26g 硫代硫酸钠(Na2S2O3·5H2O)
或16 g无水硫代硫酸 钠,及0.2 g无水碳酸钠,加入适量新煮沸过的冷水使之溶解,并稀释至1000ml,混匀,放置一个月后过滤备用。 2. .标定:准确称取0.18±0.01g在120℃干燥
至恒量的基准重铬酸钾,置于 碘量瓶中,加入25ml水使之溶解。加入2g碘化钾及20ml20%硫酸溶液(1+8),密塞,摇匀,放置暗处10 min后用150ml水稀释。用硫代硫酸钠溶液滴定至溶液呈浅黄绿色,再加2ml淀粉指示剂(称取0.5g可溶性淀粉,加入约5mL水,搅匀后缓缓倾入100mL沸水中,随加随搅拌,煮沸2min,放冷,备用。此指示液应临用时配制。),继续滴定至溶液由蓝色消失而显亮绿色。反应液及稀释用水的温度不应超过20℃。同时做空白试验。 3. 计算:硫代硫酸钠标准溶液的浓度按下式计
算: M
C(Na2S2O3)= --------------------------- (V1- V0)×0.04903
式中:C(Na2S2O3)——硫代硫酸钠标准溶液的物质的浓度, mol/L; M——重铬酸钾的质量,g; V1——硫代硫酸钠标准溶液之用量,ml; V0——空白试验用硫代硫酸钠标准溶液之用量,ml; 0.04903——重铬酸钾的摩尔质量,Kg/mol。1/6(K2CrO7) 标定原理 上述反应分两步进行: 第一步反应: Cr 2O72-+6I- +14H+ =2Cr3+ +3I2 +7H2O 反应后产生定量的I2,加水稀释后用硫代硫酸钠标准溶液滴定。 第二步反应: 2Na2S2O3+I2= Na2S4O6 +2NaI 以淀粉为指示剂,当溶液变为亮绿色即为终点。 两步反应所需要的条件如下: 第一,反应进行要加入过量的KI和H2SO4,摇匀后在暗处放置10min。实验证明:这一反应速度较慢,需要放置10min后反应才能定量完成,加入过量的KI和H2SO4,不仅为了加快反应速度,也为了防止I2 的挥发,此时生成I3- 络离子,由于I- 在酸性溶液中易被空气中的氧氧化,I2 易被日光照射分解,故需要置于暗处避免见光。 第二,第一步反应后,用硫代硫酸钠标准溶液滴定前要加入大量水稀释。由于第一步反应要求在强酸性溶液中进行,而Na2S2O3 与I2 的反应必须在弱酸性或中性溶液中进行,因此需要加水稀释以降低酸度,防止Na2S2O3 分解。此外由于Cr 2O72- 还原产物是Cr3+ 显墨绿色,妨碍终点的观察,稀释后使溶液中Cr3+ 浓度降低,墨绿色变浅,使终点易于观察。 滴定至终点后,经过5分钟以上,溶液又出现蓝色,这是由于空气氧化I- 所引起的,不影响分析结果;但如果到终点后溶液又迅速变蓝,表示Cr2O72- 与I- 的反应不完全,也可能是由于放置时间不够或溶液稀释过早,遇此情况应另取一份重新标定。 发生反应时溶液的温度不能高,一般在室温下进行 滴定时不要剧烈摇动溶液,使用带有玻璃塞的锥形瓶。 析出I2 后不能让溶液放置过久。 滴定速度宜适当地快些。 淀粉指示液应在滴定近终点时加入,如果过早地加入,淀粉会吸附较多的I2,使滴定结果产生误差。 所用KI溶液中不应含有KIO3 或I2,如果KI溶液显黄色或将溶液酸化后加入淀粉指示液显蓝色,则应事先用Na2S2O3溶液滴定至无色后再使用。 需要说明的是,进行空白试验时有时空白值过大,正常的空白值为1-2滴,若超过此数表明蒸馏水制备过久,可能其中溶解了较多的氧,KI会与氧发生反应产生I2,同时蒸馏水中的氧本身也会和硫代硫酸钠标准溶液发生反应,这两方面都会增加硫代硫酸钠标准溶液消耗量使空白值过大: 4I- + 4H+ + 4 O2 = 2 I2 + 2H2O 2S2O32- + O2 = 2SO42- +2S↓ 因此每次标定时均应使用新鲜制备的蒸馏水或将蒸馏水重新煮沸10min,冷却后使用,这样可有效避免上述情况的发生。
乙二胺四乙酸二钠(EDTA)标准溶液的配制与标定 [CEDTA=0.02mol/L] 一、配制: 称取乙二胺四乙酸二钠8g,加1000毫升水,加热溶解,冷却,摇匀,备用。 二、标定: (一)以基准氧化锌(ZnO)标定(指示剂:0.5%铬黑T指示剂) 标定流程:准称于800±500C度高温炉中灼烧至恒重的工作基准试剂氧化锌(0.3~0.4g)于100mL烧杯中 ↓←少量水湿润,盖上表面皿 滴加盐酸溶液(20%)使之刚好完全溶解 ↓ 转移入250毫升容量瓶中,加水至刻度,混匀 ↓ 准确移取25.00毫升(含Zn2+溶液)于锥形瓶 ↓←加甲基红指示剂一滴 滴加氨水(10%)至微黄色(此时PH=7~8) ↓←加蒸溜水25mL 加10毫升氨~氯化铵缓冲溶液(PH≈10) ↓←加5滴铬黑T指示液(0.5%) 用EDTA溶液滴定至溶液由紫红色变为纯蓝色,即为终点。 ↓ 记录EDTA溶液消耗的体积 ↓ 同时做空白实验 计算:CEDTA=[mX(V1/250)X1000]/[(V2-V0)XMZnO] 式中: m--------氧化锌的质量,g V1---------含Zn2+标准溶液所取的体积 V2----------------滴定时,EDTA标准溶液所消耗的体积,mL V0-----------------空白滴定时,EDTA标准溶液所消耗的体积,mL M------------------氧化锌的摩尔质量,g/mol, 即MZnO=81.39g/mol (二)以基准碳酸钙(CaCO3)标定(指示剂:钙指示剂) 标定流程:准称工作基准试剂碳酸钙(0.35~0.4g)于100mL烧杯中 ↓←少量水湿润,盖上表面皿 滴加盐酸溶液(20%)使之刚好完全溶解(可加热助溶) ↓冷却 转移入250毫升容量瓶中,加水至刻度,混匀 ↓ 准确移取25.00毫升(含Ca2+溶液)于锥形瓶 ↓←加甲基红指示剂一滴 滴加氨水(10%)至微黄色 ↓ 加20毫升氨~氯化铵缓冲溶液(PH=10) ↓←加一米粒大的钙指示剂 用EDTA溶液滴定至溶液由紫红色变为纯蓝色,即为终点。 记录EDTA溶液消耗的体积 ↓ 同时做空白实验 三、计算:CEDTA=[m*(V1/250)X1000]/[(V2-V0)*MCaCO3] 式中: m--------CaCO3的质量,g V1---------含Ca2+标准溶液所取的体积 V2----------------滴定时,EDTA标准溶液所消耗的体积,mL V0-----------------空白滴定时,EDTA标准溶液所消耗的体积,mL M------------------CaCO3的摩尔质量,g/mol, 即MCaCO3=100.09g/mol
化学需氧量(COD)的测定 实验原理 在强酸性溶液中,准确加入过量的重铬酸钾标准溶液,加热回流,将水样中还原性物质(主要是有机物)氧化,过量的重铬酸钾以试亚铁灵作指示剂,用硫酸亚铁铵标准溶液回滴,根据所消耗的重铬酸钾标准溶液量计算水样化学需氧量。 实验仪器 1.500mL全玻璃回流装置。2.加热装置(电炉)。3.25mL或50mL酸式滴定管、锥形瓶、移液管、容量瓶等。 实验试剂 (1)重铬酸钾标准溶液(0.2500mol/L):称取预先在120℃下烘干2h的基准或优质纯重铬酸钾6.129g溶于水中,移入500mL容量瓶,稀释至标线,摇匀。 (2)试亚铁灵指示液:称取1.485g水合邻菲啰啉(C12H8N2·H2O)、0.695g硫酸亚铁(FeSO4·7H2O)溶于水中,稀释至100mL,贮于棕色瓶内。 (3)硫酸亚铁铵标准溶液(0.1 mol/L):称取39.5g硫酸亚铁铵溶于水中,边搅拌边缓慢加入20mL浓硫酸,冷却后移入1000mL容量瓶中,加水稀释至标线,摇匀。临用前,用重铬酸钾标准溶液标定。 标定方法:准确吸取10.00mL重铬酸钾标准溶液于300mL锥形瓶中,加水稀释至110mL左右,缓慢加入30mL浓硫酸,混匀。冷却后,加入3滴试亚铁灵指示液(约0.15mL),用硫酸亚铁铵溶液滴定,溶液的颜色由黄色经蓝绿色至红褐色即为终点。
式中:c——硫酸亚铁铵标准溶液的浓度(mol/L); V——硫酸亚铁铵标准溶液的用量(mL)。 (4)硫酸-硫酸银溶液:于500mL浓硫酸中加入5g硫酸银。放置1—2d,不时摇动使其溶解。 (5)硫酸汞:结晶或粉末。 六、测定步骤 (1)取20.00mL混合均匀的水样(或适量水样稀释至20.00mL)置于250mL磨口的回流锥形瓶中,准确加入10.00mL重铬酸钾标准溶液及数粒小玻璃珠或沸石,连接磨口回流冷凝管,从冷凝管上口慢慢地加入30mL硫酸-硫酸银溶液,轻轻摇动锥形瓶使溶液混匀,加热回流2h(自开始沸腾时计时)。 (2)冷却后,用90mL水冲洗冷凝管壁,取下锥形瓶。溶液总体积不得少于140mL,否则因酸度太大,滴定终点不明显。 (3)溶液再度冷却后,加3滴试亚铁灵指示液,用硫酸亚铁铵标准溶液滴定,溶液的颜色由黄色经蓝绿色至红褐色即为终点,记录硫酸亚铁铵标准溶液的用量。 (4)测定水样的同时,取20.00mL重蒸馏水,按同样操作步骤作空白试验。记录滴定空白时硫酸亚铁铵标准溶液的用量。 七、数据处理
VcVVLmgOCOD10008)()/,(102
