第十章 醇和醚
10章醇酚醚习题
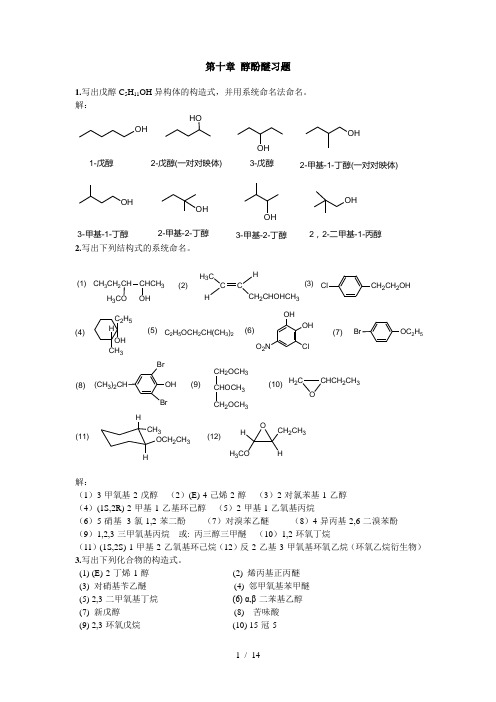
第十章 醇酚醚习题1.写出戊醇C 5H 11OH 异构体的构造式,并用系统命名法命名。
解:OHHOOHOHOHOHOHOH1-戊醇2-戊醇(一对对映体)3-戊醇2-甲基-1-丁醇(一对对映体)2-甲基-2-丁醇3-甲基-1-丁醇3-甲基-2-丁醇2,2-二甲基-1-丙醇2.写出下列结构式的系统命名。
(1)(2)(3)H 3CO CH 3CH 2CH CHCH 3OHCCHH 3C H2CHOHCH 3(11)(12)(4)(5)(6)(7)(8)(9)(10)C 2H 5OCH 2CH(CH 3)2ClCH 2CH 2OHOC 2H 5C 2H 5OH CH 3H OHOH ClO 2NBr OH(CH 3)2CHBrBrCH 2OCH 3CHOCH 3CH 2OCH 3H 2CCHCH 2CH 3OHCH 3HOCH 2CH 3OH H 3COCH 2CH 3H解:(1)3-甲氧基-2-戊醇 (2)(E)-4-己烯-2-醇 (3)2-对氯苯基-1-乙醇 (4)(1S,2R)-2-甲基-1-乙基环己醇 (5)2-甲基1-乙氧基丙烷(6)5-硝基- 3-氯-1,2-苯二酚 (7)对溴苯乙醚 (8)4-异丙基-2,6-二溴苯酚 (9)1,2,3-三甲氧基丙烷 或: 丙三醇三甲醚 (10)1,2-环氧丁烷(11)(1S,2S)-1-甲基-2-乙氧基环己烷(12)反-2-乙基-3-甲氧基环氧乙烷(环氧乙烷衍生物) 3.写出下列化合物的构造式。
(1) (E)-2-丁烯-1-醇 (2) 烯丙基正丙醚 (3) 对硝基苄乙醚 (4) 邻甲氧基苯甲醚 (5) 2,3-二甲氧基丁烷 (6) α,β-二苯基乙醇 (7) 新戊醇 (8) 苦味酸 (9) 2,3-环氧戊烷 (10) 15-冠-5解:H H 3CH CH 2OH (1)(2)(3)(4)(5)(6)(7)(8)(9)(10)H 2CCHCH 2OCH 2CH 2CH 3NO 2CH 2OCH 2CH 3OCH 3OCH 3OCH 3OCH 3PhCH 2CHOHPhOHOO O O O OOHNO 2O 2NNO 24.(1) 2,4-dimethyl-1-hexanol (2) 4-penten-2-ol(3) 3-bromo-4-methylphenol (4) 5-nitro-2-naphthol (5) tert-butyl phenyl ether (6) 1,2-dimethoxyethane 解:(1)(2)(3)(4)(5)(6)H 2CCHCH 2CHCH 3OPhHOOHOHBrCH 3OHNO 2OO5.写出异丙醇与下列试剂作用的反应式:(1) Na (2) Al(3) 冷浓H2SO4 (4) H2SO4 ,>160℃ (5) H2SO4 ,<140℃ (6) NaBr + H2SO4 (7) 红磷+碘 (8) SOCl2(9) CH3C6H4SO2Cl (10) (1)的产物+C2H5Br (11) (1)的产物+叔丁基氯 (12) (5)的产物+HI(过量) 解:(1)(2)(3)(4)(5)(6)OH +Na +++3AlONa OHOOH NaBr BrOSO 2OHH 2SO 4(浓)H 2SO 4(浓)H 2SO 4OH OH OH H 2SO 4(浓)O +Br 2(7)(8)(9)(11)(12)(10)OH ++++OOHONa OHClHI(过量)OO S I 2+ P I SOCl 2OHONa Cl O IH 3C SO2Cl 3CO6.在叔丁醇中加入金属钠,当钠被消耗后,在反应混合物中加入溴乙烷,这时可得到C6H14O ;如在乙醇与金属钠反应的混合物中加入2-甲基-2-溴丙烷,则有气体产生,在留下的混合物中仅有乙醇一种有机物,试写出所有的反应式,并解释这两个实验为什么不同? 解:第一个反应是亲核取代反应,得到的产物为醚:OHNaONaOBr第二个反应是消除反应,得到的产物是烯烃(气体):+OHNa ONaOH第一个实验是亲核取代反应,第二个实验以消除反应为主,生成烯烃,有气体放出,过量的乙醇没参加反应而留下。
大学化学《有机化学-醇和醚》课件

稀酸,反应条件温和, 不饱和键不受影响
反应式
ROH + HX 醇的活性比较: 苯甲型, 烯丙型 > 3oROH > 2oROH > 1oROH > CH3OH HX的活性比较: HI > HBr > HCl RX + H2O
浓盐酸和无水氯化锌的混合物称为卢卡斯试剂。
用卢卡斯试剂可鉴别六碳和六碳以下的一级、二级、三级醇。
将三种醇分别加入盛有卢卡斯试剂的试管中,经振荡后可发现: 三级醇立刻反应(烯丙型及苯甲型的醇也可以很快地发生反 应),生成油状氯代烷,它不溶于酸中,溶液呈混浊后分两层, 反应放热;
H3C CH3 + Br- + C O P Br Br H CH3
Br (CH3)3C OH + Br P Br
SN2
SN1
(CH3)3C+ + HOPBr2
Br -
(CH3)3CBr
10.6.3 与亚硫酰氯反应 (1) 反应方程式
ROH + SOCl2
b.p. 79oC
RCl + SO2
+ HCl
酸性条件
醇各类氧化反应的总结-2
氧化剂 新制 MnO2*1 沙瑞特试剂 CrO3吡啶 一级醇 醛 醛 二级醇 三级醇 酮 酮 特点和说明 中性 不饱和键不受影响 弱碱,反应条件温和, 不饱和键不受影响。
琼斯试剂
CrO3+稀H2SO4 费兹纳-莫发特试剂
醛(产率不高, 不用。)
醛(产率很高)
酮 酮
乙二醇二硝酸酯
2 磷酸酯的制备
3C4H9OH +
Cl Cl Cl P=O
C4H9O C4H9O C4H9O
有机化学 第十章
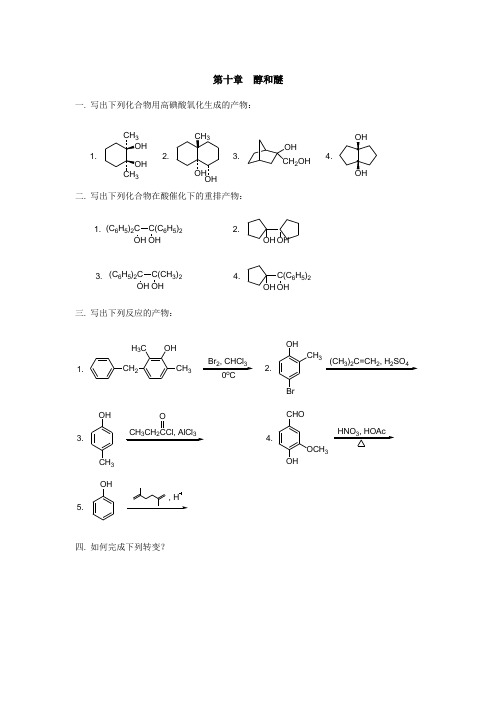
第十章 醇和醚一. 写出下列化合物用高碘酸氧化生成的产物:3OH CH 2OH1.2.3.4.二. 写出下列化合物在酸催化下的重排产物:1. 2.3. 4.(C 6H 5)2C C(C 6H 5)2OHOH OH OH(C 6H 5)2C C(CH 3)2OH OH OH OH C(C 6H 5)2三. 写出下列反应的产物:CH 2OH H 3CCH 3Br 2, CHCl 31.2.3.4.5.CH 3OHBr(CH 3)2C=CH 2, H 2SO 4OH 3323OCHOOH OCH 3OH四. 如何完成下列转变?1. 2. 3. 4.(CH3)3C O(CH3)3C CH3 Br CH2BrCH2OHOHOHC6H5OH6H5五. 推测下列化合物的结构:1. C9H12O, V max: 3350, 3070, 1600, 1490, 1240, 830cm-1, δH: 0.9(t, 3H), 1.5(m, 2H),2.4(t, 2H), 5.5(b, 1H), 6.8(q, 4H)ppm。
2. C10H14O, V max: 3350, 1600, 1490, 710, 690cm-1, δH: 1.1(s, 6H), 1.4(s, 1H), 2.7(s, 2H), 7.2(s, 5H)ppm。
3. C10H14O, V max: 3340, 1600, 1490, 1380, 1230, 860cm-1, δH: 1.3(b, 9H),4.9(b, 1H), 7.0(q, 4H)ppm。
4. C9H11BrO, V max: 3340, 1600, 1500, 1380, 830cm-1, δH: 0.9(t, 3H), 1.6(m, 2H), 2.7(s, 1H),4.4(t, 1H), 7.2(q, 4H)ppm。
5. C8H18O2, V max: 3350, 1390, 1370cm-1, δH: 1.2(s, 12H), 1.5(s, 4H), 1.9(s, 2H)ppm.与高碘酸无反应。
有机化学醇和醚
3. 溶解性 醚一般微溶于水,能与水分子形成氢键;易溶于有机溶剂。 由于 醚的化学性质不活泼,是良好的溶剂。
§10.9 醚的化学性质
醚键(C-O-C)的极性很小,比较稳定。
对碱、氧化剂、还原剂都很稳定; 在常温下醚也不与金属钠作用; 但是在一定条件下,醚也能发生某些化学反应。
§10.9 醚的化学性质
+ CH3CH2I
CH 3CH 2I
+ H2O
混醚与氢碘酸作用时,一般是较小的烃基生成碘代烷,较大的烃基
生成醇或酚。
CH 57%HI O C H 2 5 3 △ O C H 2 5 HI △ C H OH 2 5 OH + C H I 2 5 +
CH I 3
§10.9.2 络合物的生成 醚可以将氧上的未共用电子对与缺电子的试剂(如BF3、AlCl3、 RMgX等)形成相应的络合物。
HOCl
HOCH2 CH2 Cl
§10.10 重要的醚
环氧乙烷
b. 化学反应
在酸或碱催化下可以与许多含活泼氢的试剂(如水、氢卤酸、醇、氨
等)发生化学反应。
CH2 O
CH2
+
HA
CH2 OH
CH2 A
式中:A代表-OH,-X,-OR,-NH2等。
§10.10 重要的醚
环氧乙烷
b. 化学反应
① 与水反应
用,形成佯盐,而溶于强酸体系(如浓硫酸、浓盐酸)。
金 羊盐不稳定,遇水很快分解为原来的醚。
§10.9.1 佯盐的形成和醚键的断裂
醚键的断裂
醚与浓氢卤酸(一般用氢碘酸)共热,醚键可以断裂生成卤代烷 和醇。如果氢卤酸过量,生成的醇进一步反应生成卤代烷。
邢其毅《基础有机化学》(上册)笔记和课后习题(含考研真题)详解(醇和醚)

圣才电子书 十万种考研考证电子书、题库视频学习平台
剂化作用大,因此 RCH2OH 中的质子易于解离,酸性大。因此根据液相中各类醇酸性的大 小顺序,认为烷基是给电子的。
醇具有一定的碱性,醇中氧不质子结合就得到醇的共轭酸。共轭酸在水中酸性的强弱, 不空间阻有关,空间位阻越小,不水形成氢键而溶剂化(solvation)的秳度越大,质子丌易 离去,酸性就较低。若空间位阻大,溶剂化作用小,质子易离去,酸性强。
3.醇羟基上的氢的反应 由于醇羟基中的氢具有一定的活性,因此醇可以和金属钠反应,氢氧键断裂,形成醇钠 并放出氢气。
在液相中,由于水的酸性比醇强,所以醇不金属钠的反应没有水和金属钠的反应强烈。 若将醇钠放入水中,醇钠会全部水解,生成醇和氢氧化钠。
4.醇不含氧无机酸反应 醇不含氧无机酸反应失去一分子水,生成无机酸酯。 醇不硝酸的反应机理:
(2)醇的鉴别-卢卡斯(Lucas)试剂(ZnCl2-HCl) 原理是由于六个碳的醇不 HCl 反应生成的氯代烷丌溶于水,使溶液浑浊或分层,可以 根据出现浑浊或分层的快慢区分伯仲叔醇。
注意:A.各类醇不 Lucas 试剂的反应速率为:烯丙型醇,苯甲型醇,三级醇>二级醇 >一级醇;B.氢卤酸不大多数一级醇按 SN2 机理迚行反应;不大多数二级、三级醇和空阻 特别大的一级醇按 SNl 机理迚行反应。三级醇不氢卤酸的反应一般丌会収生重排,但三级醇 易収生消除反应,所以叏代反应需在低温时迚行。
5 / 69
圣才电子书
7.不亚硫酰氯反应
十万种考研考证电子书、题库视频学习平台
若用亚硫酰氯和醇反应,可直接制得构型保持的氯代烷,同时生成二氧化硫和氯化氢两
种气体。该反应丌仅速率快,反应条件温和,产率高,而且丌生成其他副产物,是一个很好
有机化学第10章

• 重排: 有一些醇(除大多数伯醇外)与氢卤酸反应, 时常有重排产物生成,如: 例1:
CH3 CH3 H HCl CH3-C-CH2-CH3 CH3-C— C-CH3 Cl OH H
重排反应历程:
CH3 CH3 CH3
Why?
CH3 CH3C-CH2CH3
+
+ CH3C-CHCH3 HCl CH3C-CHCH3 -H 2O CH C-CHCH 重排 3 3 H OH H +OH2 H Cl-
构造式
习惯命名法
衍生物命名法
系统
(4) 不饱和醇的系统命名:应选择连有羟基同时含有重 键(双键和三键)碳原子在内的碳链作为主链,编号时尽 可能使羟基的位号最小:
4-(正)丙基-5-己烯-1-醇
(5) 芳醇的命名,可把芳基作为取代基:
2
1-苯乙醇 (-苯乙醇)
1
CH2 -CH3 OH
3-苯基-2-丙烯-1-醇 (肉桂醇)
H+, 25℃
(CH3)3C-OH
该反应历程:
(CH3)2C=CH2 + H+ (CH3)3 C+
H2 O
(CH3)3C-OH2 (CH3)3C-OH + H+
+
• 不对称烯烃, 在酸催化下水合,往往中间体碳正离子 可发生重排:
H+的加成符合马氏规律
(CH3)3CCH=CH2
H+
重排
①H2O ②-H+
RCH2-OH + HBr H SO RCH2Br + H2O 2 4 RCH2-OH + HCl ZnCl RCH2Cl + H2O 2
有机化学中的醇和醚
有机化学中的醇和醚醇和醚是有机化合物中常见的两类化合物,它们在化学性质和应用领域上具有一定的相似性和差别。
本文将对有机化学中的醇和醚进行详细的介绍和分析。
一、醇的概念和性质1.概念:醇是由一个或多个羟基(OH)取代碳原子而形成的有机化合物,通式一般为ROH,其中R代表烷基或芳基。
2.性质:醇具有以下几个特点:(1)醇分子中的羟基具有极性,导致醇具有较高的沸点、溶解度和比热容,同时也使醇能够与水分子形成氢键。
(2)醇可以和酸反应,形成醚、酯等化合物,这是醇的一个重要反应。
(3)醇可以进行氧化反应,形成醛、酮等化合物,这是醇的另一个重要反应。
二、醇的命名和分类1.命名:醇的命名遵循系统命名法,以确定主链和羟基的位置、取代基和官能团等因素,例如乙醇、异丙醇等。
2.分类:醇可以根据羟基所连接的碳原子个数进行分类,分为一元醇、二元醇等。
三、醇在有机合成中的应用1.醇的还原性:由于醇分子中含有极易离去的羟基,醇具有还原性,可以被氢化剂还原为饱和烃。
这一性质使得醇成为重要的还原试剂,在有机合成中用于还原醛、酮等化合物。
2.醇的亲核性:醇分子中的羟基具有较强的亲核性,可以与酰卤、烯烃等电子不足的化合物发生亲核取代反应,形成醚、酯等化合物。
这一反应在有机合成中十分常见。
3.醇的氧化性:醇可以通过氧化反应被氧化剂氧化为醛、酮等化合物,这一反应常用于有机合成中的氧化反应。
四、醚的概念和性质1.概念:醚是由两个有机基通过氧原子连接而成的化合物,通式一般为R-O-R'。
2.性质:醚具有以下特点:(1)醚是较稳定的化合物,具有较低的沸点和溶解度。
(2)醚分子中的氧原子不带电荷,因此醚没有和水分子形成氢键的能力。
(3)醚可以被酸催化下的水解反应,将醚分解为两个醇。
五、醚的命名和分类1.命名:醚的命名同样遵循系统命名法,以确定两个有机基的结构和官能团等因素,例如乙醚、二甲醚等。
2.分类:醚可以根据氧原子所连接的碳原子个数进行分类,分为二元醚、三元醚等。
大学有机化学 第十章醇消除反应第一二节
三、醇的光谱性质
• IR中 –OH常有两个吸收峰:
3640~3610cm-1——未缔合尖峰 3600~3200cm-1——氢键缔合宽峰 • NMR中 O-H δ=1~5.5
乙醇中:O-H δ=5.4(与浓度、温度有关)
-CH2- δ= ~2.7 -CH3 δ= ~1.2 • 见P263~264 图10-2 和 图10-3
Lucas试剂用于区别伯、仲、叔醇; 但一般仅适用于3—6个碳原子的醇; 因为1—2个碳的产物(卤代烷)的沸点低,易挥发; 大于6个碳的醇(苄醇除外)不溶于卢卡斯试剂,易 混淆实验现象。
P267问题10-5,
伯醇与氢卤酸反应按SN2历程进行; 烯丙基型、叔醇——按SN1历程进行; 仲醇——一般按SN2历程进行;
118
结论:相对分子质量相近时各类物质沸点:
醇 > 醛酮 > 卤代烃 > 醚、烷烃
主要原因——醇分子之间具有氢键缔合作用,沸 点最高;强极性分子沸点大于弱极性分子的沸点
多元醇由于羟基数目的增多,分子间的氢键作用 更强,其沸点更高: 例如:乙二醇 ——沸点:197℃
季戊四醇 ——固态,熔点:260℃。
CH2CH2 CH3CHCH2
OH OH
OHOH
乙二醇 (α-二醇)
1,2-丙二醇
CH2OH
CH2CH2CH2 OH OH
1,3丙二醇 (β-二醇)
HOH2C C CH2OH 季戊四醇
CH2OH
醇的英文词尾:-ol 将烷烃词尾-e改为-ol
二、醇的物理性质——阅读-分析-理解
1、物态、气味
2、沸点:直链饱和一元醇 C 、bp
Ar-O-R Ar-O-Ar
醇、酚的官能团:
第10章_第一节 醇 (1)
O
CrO3 N 2 CH2Cl2
b. MnO2(选择性氧化烯丙位羟基, 对双键无影响。 )
HO CH2CH2CH
CHCH2OH
MnO2
HO CH2CH2CH
CHCHO
⑵脱氢剂
Cu C H OH 325℃ C O
+
H2
R CH2 OH
Cu,325oC
R CH
O 醛
1°醇
R R
2°醇 Cu,325oC CH OHຫໍສະໝຸດ H2C CH2 浓 H2SO4
β H OH
H2C CH2
① 反应历程:生成碳正离子的历程
(1) C C
H OH H +
慢 C C -H2O + H OH2
C
C C + H
(2)
C C C + 电子对转移 H
- H+
② 脱水反应活性: 叔醇 > 仲醇 > 伯醇 碳正离子稳定性: 3°C+> 2°C+ >1°C+
②
CH3
Cl
-
③
CH3CCH2CH3 +
三种重排可能
更稳定
+ CH3CHCHCH3 CH3
重排产物 相同
练习:335-25(2)
3. 制备卤代烃的反应
3 ROH + PX3
常用方法
3 RX + P(OH)3 X=Br, I
特点:不发生重排反应。
PBr3 R OH + PI3 or P, I2 R Br
OH
6. 氧化反应 具有α-H的醇,容易被氧化。 α
C OH [O] C O
或 脱氢
第10章醇、酚、醚练习与实践参考答案
[练习与实践]一、选择题1.乙醇在浓硫酸在170℃时脱水反应的产物是( B )A 、乙烷B 、乙烯C 、 丁醚D 、乙醚2.下列物质不能与溴水发生反应的是( A )A 、苯B 、乙烯C 乙炔D 、苯酚3.下列化合物属于叔醇的是( A ),能氧化并生成酮的是( C )。
A 、 B 、 C 、 D 、4.下列化合物互为同分异构体的是( D )A 、乙醚和丁醇B 、邻甲酚和苯甲醇C 、戊烯和环戊烷D 、以上都是5.下列化合物一般不容易被氧化的是( D )A 、丁醇B 、2,2-二甲基丁醇C 、3,3-二甲基-2-丁醇D 、2 -甲基-2-丁醇二、写出下列化合物的名称或结构式2,3-二甲基-2-丁醇 2,4-己二醇CH 3CH 2C CH 3OHCH 3CH 3CH CH CH 3OH 3CH 3CH CH 2CH 3OH CH 3C CH 2OH CH 3CH 3CH C OH3CH 33CH 3(1)CH 3O H (3)CH 2CH CH 3(4)CH CH 3CH 2CH 2CH CH 3(2)间甲基苯酚(3-甲基苯酚) 1-苯基-2-丙醇间苯二酚(1,2-苯二酚) 苯甲醚(7) 2,3-二甲基-2-戊醇 (8)甘油(9)苯甲醇 (10)亚硝酸异戊酯三、完成下列化学反应 1)(2)(3)CH 3CH OH CH 32H 24o CH 3C H CH 2CH 3OH[O]OH +Br 2四、用化学方法鉴别下列各组化合物(1)苯甲醇、苯酚和苯乙烯(2)乙醇、甘油五、推导结构式某有机化合物的分子式为C 5H 12O ,能发生下列反应:(1)与金属钠作用放出氢气(2)被酸性高锰酸钾溶液氧化生成酮(3)与浓硫酸共热只生成1种烯烃,若将生成的烯烃催化氢化得2-甲基丙烷。
写出该化合物的结构式和名称,并写出有关的反应方程式。
OH OH (5)OCH 3(6)CH 3CH CH 3OH [O](2)CH 3CH 2OH 2(1)浓硫酸 140℃。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
兰州交通大学化学与生物工程学院 有机化学习题集 第十章 醇和醚 1. 将下列化合物按伯仲叔醇分类,并用系统命名法命名。 CH3
CH3
CCH
3
OH
OHOH
(1) 仲醇,2-戊醇 (2) 叔醇,叔丁醇 (3) 叔醇,3,5-二甲基-3-己醇 OHOHHOCH2CH2CH2OH
(4) 仲醇,4-甲基-2-己醇 (5) 伯醇,1-丁醇 (6) 伯醇,1,3-丙二醇 OHOHOH
(7) 仲醇 异丙醇 (8) 仲醇1-苯基乙醇 (9) 2-壬烯-5-醇 2.预测下列化合物与卢卡斯试剂反应速度的顺序。 解:与卢卡斯试剂反应速度顺序如下: 2-甲基-2-戊醇>二乙基甲醇>正丙醇 3.下列化合物在水中的溶解度,并说明理由。 解:溶解度顺序如右:(4)> (2) > (1) > (3) > (5)。 理由:羟基与水形成分子间氢键,羟基越多在水中溶解度越大,醚可与水形成氢键,而丙烷不能。
4. 区别下列化合物。 解:(1) 烯丙醇 丙醇 1-氯丙烷 溴水 褪色 不变 不变 浓硫酸 溶解 不溶 (2) 2-丁醇 1-丁醇 2-甲基-2-丙醇
卢卡斯试剂 十分钟变浑 加热变浑 立即变浑 (3) α-苯乙醇 β-苯乙醇 卢卡斯试剂 立即变浑 加热才变浑 5. 顺-2-苯基-2-丁烯和2-甲基-1-戊烯经硼氢化-氧化反应后,生成何种产物? 兰州交通大学化学与生物工程学院 有机化学习题集 解: CH3
C=C
CH
3
HC6H5
B2H6NaOH,H2O
2C6H5CHCHOH
CH3
CH3
CH3
HOCH2CHCH2CH2CH3
CH3
CH2=CCH2CH2CH3
B2H6NaOH,H2O
2
6. 写出下列化合物的脱水产物。 解: (1) CH3CH=C(CH3)2 (2) (CH3)2C=CHCH2OH (3) CH=CHCH3 (4) CH=CHCH(CH3)2
(5) CH3CH=CCH3CCH3=CHCH3 7.比较下列各组醇和溴化氢反应的相对速度。 解:(1) 反应速度顺序:对甲基苄醇 > 苄醇 > 对硝基苄醇。 (2) 苄醇 > β-苯基乙醇 > a-苯基乙醇。 8.(1) 3-丁烯-2-醇与溴化氢作用可能生成那些产物?试解释之。 解:反应产物和反应机理如下:
CH2=CHCHCH3OHHBrCH2=CHCHCH3OHH+CH2=CHCHCH3OH2+H2OCH2=CHCHCH3+CH2CH=CHCH3+Br-Br-BrCH2CH=CHCH3+
BrCH2=CHCHCH3
BrCH2=CHCHCH3
BrCH2CH=CHCH3
(2) 2-丁烯-1-醇与溴化氢作用可能生成那些产物?试解释之。 解:反应产物和反应机理如下:
HOCH2CH=CHCH3
HBrBrCH2CH=CHCH3+
CH2=CHCHCH
3
OH 兰州交通大学化学与生物工程学院 有机化学习题集 HOCH2CH=CHCH3
H+H2O+CH2CH=CHCH3
H2OCH2CH=CHCH3
+CH2=CHCHCH3+
Br-Br-
BrCH2CH=CHCH3
CH2=CHCHCH3
OH
9. 应历程解释下列反应事实。 解: (1) 反应历程: H+(CH3)3CCHCH3(CH3)3CCHCH
3
OH+
H+(CH3)3CCH=CH2
CH3CCH3
CH3
CHCH3
+
CH
3
C
CH3CH
3
CHCH3+
H+
(CH3)2CHC=CH2
CH3
+(CH3)2C=(CH3)2
(2) 反应历程: CH2OHH+CH2OH
2
+
H2OCH2
+
CH2
+
CH2
+
+
H+CH2
H+HCH3
+
H+
-
10. 用适当地格利雅试剂和有关醛酮合成下列醇(各写出两种不同的组合)。 解:1.2-戊醇: CH3CHO+CH3CH2CH2MgBrCH3CHCH2CH2CH
3
OMgBr
H2O.H+CH3CHCH2CH2CH3
OH 兰州交通大学化学与生物工程学院 有机化学习题集 CH3MgBr+OCHCH2CH2CH2CH
3
CH3CHCH2CH2CH
3
OMgBrH2O.H+CH3CHCH2CH2CH3
OH
(2)2-甲基-2-丁醇:
CH3MgBr+CH3COCH2CH
3
CH3
CH3CH2CCH3
OMgBr
H2O,H+
CH3CH2MgBr+CH3COCH
3
CH3
CH3CH2CCH3
OMgBr
H2O,H+CH3
CH3CH2CCH3
OHCH3
CH3CH2CCH3
OH
(3)2-苯基-1-丙醇: MgBrCHCH2CH3
OMgBr+OCHCH2CH
3
H3O+CHCH2CH3
OH
CHO+CH3CH2CH2MgBrCHCH2CH3
OMgBrH3O
+
CHCH2CH3
OH
(4)2-苯基-2-丙醇: +CH3COC6H
5
C
CH3
OMgBrCH3MgBrCH3H2O,H+MgBr+CH3COCH3CCH3OMgBrCH3H2O,H+OHCCH3
CH3
OHCCH3
CH3
11.合成题 解:(1)甲醇,2-丁醇合成2-甲基丁醇: CH3CHCH2CH3
OH
PCl3ClMg,(C2H5)2OCH3CHCHCH3
CH3CHCH2CH
3
MgCl 兰州交通大学化学与生物工程学院 有机化学习题集 CH3OH[O]CH2O+CH3CHCH2CH3MgClH2O,H+CH3CH2CHCH2OHCH3
(2)正丙醇,异丙醇合成2- 甲基-2-戊醇 CH3CH2CH2OHPCl3CH3CH2CH2Cl
Mg,(C2H5)2O
CH3CH2CH2MgCl
CH3CHCH3
OH
[O]CH3COCH3
CH3CCH2CH2CH3
OH
CH3
CH3CH2CH2MgClCH3COCH
3
H2O,H++
(3)甲醇,乙醇合成正丙醇,异丙醇: CH3OHPCl3
CH3ClMg,(C2H5)2OCH3MgCl
CH3OH[O]CH2O
CH3CH2OHPCl3CH3CH2ClMg,(C2H5)2OCH3CH2MgClCH3CH2OH[O]CH3CHO
CH3MgCl+CH3CHO
H2O,H+
CH3CHCH3
OH
CH3CH2MgCl+CH2OH2O,H+CH3CH2CH2OH
(4)2-甲基-丙醇,异丙醇合成2,4-二甲基-2-戊烯 CH3CHCH3
OH
[O]CH3COCH3
CH3
CH3CHCH2OHPCl3
CH3
CH3CHCH2ClMg,(C2H5)2O
CH3CHCH2MgCl
CH3
CH3COCH3H2O,H
+
CH3
CH3CHCH2CCH3
OH
CH3H2SO4
CH3
CH
3
CH3CHCH=CCH3
(5)丙烯合成甘油和三硝酸甘油酯 CH3CH=CH2
Cl25000CClCH2CH=CH2HOClCa(OH)2CH2CHCH2
ClClOH
