药物合成课件还原反应
精选《药物合成反应》第一章卤化反应课件资料

δ CH3(CH2)5CH
δ CH2
BH3 THF 0 oC
CH3(CH2)5CH H
CH2 BH2
Br2 MeONa MeOH 0 oC
CH3(CH2)5CH 2 CH2 Br (94%)
(2)若C*--B为手性,则被X2 置换时构型反转
(B2H6)
BH3 THF 25 0C
※ BH2
I2 MeONa MeOH 0 0C
加成
CC
2
R Nu
R4
Me HBr Me
Me
H Br
anti (协同历程)
Me
Ph
H HBr
CC
H
CH3
Ph
H
CC
+
H Br H CH3
Ph
HH
CC
H Br
CH3
(H标记)
(二历程差别与 (anti):(syn)=9:1 Me
Ph基存在有关M) e HBr
H
MM离ee子对历程HB协r同历程
Br Me
R
H
CC
I2 / OH
H
B(OH)2
R OH CC
H I
H B(OH)2
X2=(Br2, Cl2)
易成三圆环 I半径大,极性大
RX CC
H X
H B(OH)2
X RC H
X C
H B(OH)2
X RC H
B(OH)2 CH
X2 RCH CH2
x2 cat
RCH CH2 (加成)
X
X
x
(取代)
HX ROH
HBr RCH CH2 h
RX
RCH2CH2Br
药物合成反应3 PPT资料共68页

2.仲胺的制备 氨或伯胺与卤代烃反应可得各种胺的混合物。如 用仲卤代烷与氨或伯胺反应,由于立体位阻,主 要得仲胺,及少量叔胺。如:
25.11.2019
仲胺也可以用还原烃化制备。伯胺与羰基化 合物缩合生成Schiff 碱,再用Raney 镍或铂 催化氢化,得到仲胺的收率—般较好。
25.11.2019
常用保护羟基方法有: 1.酯化法 反应后可通过碱性水解除去。 2.苄醚法 反应完成后可在催化剂上加氢氢解除去。 3.四氢吡喃醚法 醇与二氢吡喃(DHP)在酸存在下反应即可引入 四氢吡喃基(形成四氢吡喃醚即THP)。同样在 温和的酸性条件水解,保护基被除去。 4.三芳基甲醚保护基
25.11.2019
冠状动脉扩张药派克昔林(perhexiline)中间体二苯酮的合 成:
冠状动脉扩张药普尼拉明(prenylamine)中间体二苯丙酸 的制备:
镇痛药四氢帕马丁(tetrahydropalmatine,延胡索乙素)中 间体3,4-二甲氧基苯丙腈的合成:
25.11.2019
1.反应机理 Friedel-Crafts 烃化反应是碳正离子对芳环
25.11.2019
理想保护基的要求是:
①引入保护基的试剂应易得、稳定及无毒; ②保护基不带有或不引人手性中心; ③保护基在整个反应过程中是稳定的; ④保护基的引入及脱去,收率是定量的; ⑤脱保护后,保护基部分与产物容易分离。围绕 这些要求,人们在经过几十年的努力后,今天仍 不时有新的保护基团的研究工作报道,为有机合 成提供更加巧妙的手段。
溶剂对烃化位置有较大影响: 酚类在DMSO、DMF、醚类、醇类中烃化时,主 要得酚醚(O-烃化产物),而在水、酚或三氟乙醇中 烃化时,则主要得到C-烃化产物。
还原反应

9 还原反应通过还原反应,可将不饱和结构转化为饱和结构,将羰基化合物转化为醇,等等,可以实现多种官能团的转化,在药物合成中有着广泛的应用。
本章主要内容为,碳-碳(杂)不饱和结构的还原,多种含氧不饱和结构的化学还原以及氢解等,催化多相加氢等大工业生产常见的还原过程以及生物法还原不在本章重点讨论范围之内。
9.1多相催化加氢、催化转移氢化和均相催化加氢多相催化加氢可以完成从酰卤、炔烃、酮、硝基物、芳烃到羧酸,几乎所有不饱和结构的还原。
多相催化加氢以氢气为氢源,适应面广,但有时需加压,而且当底物中存在多个活性基团时,存在还原的选择性问题。
不同官能团被还原的反应活性不同,催化剂及反应条件也不同。
通常情况下,表9.1的内容可作为催化加氢活性顺序(及反应条件)的参考。
表9.1 不同官能团加氢难易顺序表(易→难)当底物分子中含多个可还原基团时,处在表的前部的基团将被优先还原。
例如还原不饱和醛的羰基,可用加氢法,如果是还原其双键,则加氢法不合适。
催化加氢反应示例:Finasteride中间体的合成。
与多相催化加氢用氢气作氢源不同,催化转移氢化的氢源为有机化合物,通常为不饱和脂环烃、不饱和萜类或醇,如环己烯、alpha-蒎烯和异丙醇等。
所用催化剂可以是钯黑或钯/碳,铂和铑的活性较低,而镍一般用于醇作氢源的反应。
催化转移氢化主要适用于碳-碳不饱和键、硝基、偶氮基、亚胺基和氰基的还原,也可用于碳-卤键、苄基及烯丙基的氢解。
具有反应条件温和,操作简单,基团选择性好等优点。
表9.2列举了更多的应用实例。
表9.2 一些催化转移氢化应用实例均相催化加氢的主要特点是催化剂以分子态溶解在反应介质中,起催化作用,其氢源为氢气。
选择性好,反应条件温和。
催化剂一般为第VIII族过渡元素Rh、Ru、Ir、Co以及Pt等的配合物。
常见的配体是Cl、CN、PPh3、CO和胺等给电子体。
在药物合成中,均相催化法主要应用于碳-碳双键的选择性还原,见表9.3。
还原反应(2)
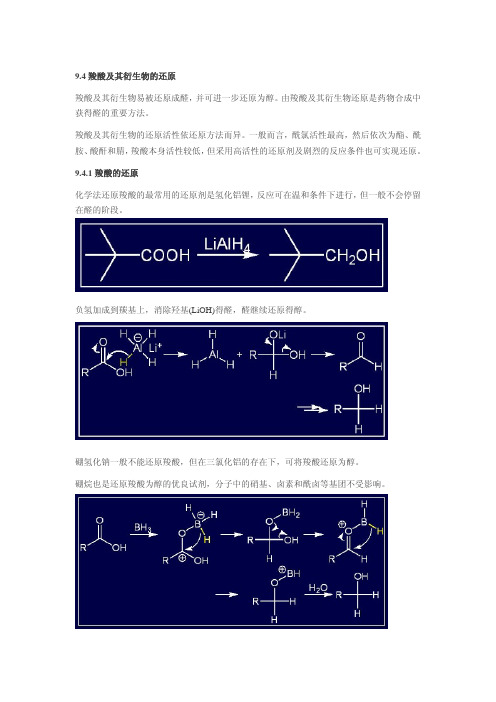
9.4 羧酸及其衍生物的还原羧酸及其衍生物易被还原成醛,并可进一步还原为醇。
由羧酸及其衍生物还原是药物合成中获得醛的重要方法。
羧酸及其衍生物的还原活性依还原方法而异。
一般而言,酰氯活性最高,然后依次为酯、酰胺、酸酐和腈,羧酸本身活性较低,但采用高活性的还原剂及剧烈的反应条件也可实现还原。
9.4.1 羧酸的还原化学法还原羧酸的最常用的还原剂是氢化铝锂,反应可在温和条件下进行,但一般不会停留在醛的阶段。
负氢加成到羰基上,消除羟基(LiOH)得醛,醛继续还原得醇。
硼氢化钠一般不能还原羧酸,但在三氯化铝的存在下,可将羧酸还原为醇。
硼烷也是还原羧酸为醇的优良试剂,分子中的硝基、卤素和酰卤等基团不受影响。
硼烷还原羧基的速度比还原其它基团快,因此,控制硼烷的用量及反应温度,可以在底物分子中含氰基、酯基或醛、酮羰基时还原羧基。
硼烷还原羧基的反应速度,脂肪酸大于芳香酸,位阻小的酸大于位阻大的酸。
脂肪酸酯反应速度很慢,芳香酸酯几乎不反应。
9.4.2 酰卤的还原化学法还原酰卤为醛的最常用的还原剂是金属氢化合物,如三叔丁氧基氢化铝锂或三丁基锡氢。
在低温下,还原芳酰卤和杂环酰卤的收率较高,而且不影响底物分子中的硝基、氰基、酯基、双键和醚键等。
负氢加成到羰基上、消除卤素(卤化锂)得醛。
9.4.3 酯和酰胺的还原依反应条件的不同,酯可被还原为醇、醛和双分子偶联反应。
(1) 酯还原为醇已有多种化学方法可将酯还原为醇,其中应用最为广泛的是金属氢化合物,其中又以氢化铝锂为最。
①金属氢化合物作还原剂酯用0.5eq.的氢化铝锂还原,可得伯醇。
负氢加成到羰基上,消除烷氧基(烷氧基锂)得醛,醛继续还原得醇。
在氢化铝锂还原时加入三氯化铝或定量的乙醇(用氯或烷氧基替换其1~3个氢原子),可以提高其还原的选择性。
如以下alpha,beta-不饱和酯的还原,若单用氢化铝锂还原,则生成饱和醇。
②金属钠/醇作还原剂:Bouveault-Blanc反应高级脂肪酸酯用金属钠和无水醇直接还原生成相应的伯醇的反应,称为Bouveault-Blanc反应。
药物合成反应-还原反应共59页文档

21、静念园林好,人间良可辞。 22、步步寻往迹,有处特依依。 23、望云惭高鸟,临木愧游鱼。 24、结庐在人境,而无车马喧;问君 何能尔 ?心远 地自偏 。 25、人生归有道,衣食固其端。
▪
26、要使整个人生都过得舒适、愉快,这是不可能的,因为人类必须具备一种能应付逆境的态度。——卢梭
▪
27、只有把抱怨环境的心情,化为上进的力量,才是成功的保证。——罗曼·罗兰
▪
28、知之者不如好之者,好之者不如乐之者。——孔子
▪
29、勇猛、大胆和坚定的决心能够抵得上武器的精良。——达·芬奇
▪
30、意志是一个强壮的盲人,倚靠在明眼的跛子肩上。——叔本华
谢谢!
59
药物合成反应(全)

H 快
B C H CH OH 慢
CH X-X
CH2 OH
X2 快
C X
C O
三、醛酮α位的卤代反应
四溴环己二烯酮(α,β不饱和酮的α卤代剂,不发生
双键加成反应)
O Br Br
+
O
O Br
+
OH Br Br
Br
Br
Br
Br
(选 择 性 溴 化 试 剂 )
三、醛酮α位的卤代反应
1 通过烯醇酯的卤化反应
心肌梗死等症。 本品化学名为1,4-二氢-2,6-二甲基-4-2-硝基苯基)-吡 啶-3,5-二羧酸二乙酯 化学结构式为:
CH3 CH2 OOC H3 C N H COOCH2 CH3 CH3 NO2
合成路线如下
NO2 CHO KNO3 H2SO4 NO2 CHO CH3 COCH2 COOCH2 CH3 NH4 OH H3 C N H CH3 CH3 CH2 OOC COOCH2 CH3
5.6 molSO2Cl2/Et2O 0.7 molSO2Cl2/Et2O
一、醇的卤素置换反应
3 与卤代磷反应
R-OH + PX3 X R O P X HX R-X + O H P X X
4 与NCS反应
H3C HOH2CH2C H CH2OH
NCS CH3SCH3
H3C HOH2CH2C
H CH2Cl
化学药物的合成方法分类?
全合成:由结构简单的原料经过一系列单元反应制备化学药 物的方法;在药物发展上发挥了重要作用。 半合成:对已经具有一定基本结构的产物经过化学修饰或结 构改造得到疗效更高、毒副作用更小的新药。
水杨酰苯胺(Salicylanilide)的合成
药物合成教学资料氧化反应PPT课件
目
CONTENCT
录
• 氧化反应基本概念与分类 • 药物合成中常见氧化反应 • 氧化反应机理与影响因素 • 实验方法与操作技巧 • 结果分析与讨论 • 药物合成中氧化反应应用实例 • 总结与展望
目
CONTENCT
录
• 氧化反应基本概念与分类 • 药物合成中常见氧化反应 • 氧化反应机理与影响因素 • 实验方法与操作技巧 • 结果分析与讨论 • 药物合成中氧化反应应用实例 • 总结与展望
注意事项三
实验结束后要及时清洗实验仪器和试剂瓶,避免 残留物对下次实验造成影响。
安全规范一
穿戴好实验服和护目镜等个人防护用品。
安全规范二
严格按照实验步骤进行操作,不要随意更改实验 条件。
安全规范三
遇到异常情况时要立即停止实验,并及时向教师或实验 室管理员报告。
实验注意事项及安全规范
注意事项一
实验过程中要保持通风良好,避免吸入有害 气体。
醇在氧化剂作用下,羟基被氧化成醛基或酮基。
常见氧化剂
铬酸、高锰酸钾、氧气等。
实例
乙醇在铬酸作用下氧化成乙醛。
醛或酮的氧化成羧酸
02
01
03
反应机理
醛或酮在强氧化剂作用下,羰基被氧化成羧基。
常见氧化剂
硝酸、高锰酸钾、重铬酸钾等。
实例
乙醛在硝酸作用下氧化成乙酸。
醛或酮的氧化成羧酸
02
01
03
反应机理
步骤二
在恒温水浴锅中加热反应混合 物,同时通入氧气或空气进行
氧化反应。
步骤三
反应完成后,将反应混合物进 行冷却、过滤、洗涤等操作,
得到目标产物。
药物合成反应(全)
加成反应
总结词
加成反应是一种在药物合成中常见的反应类型,涉及有机化合物中的双键或三键与其它原子或基团结合生成新分 子的过程。
详细描述
在药物合成中,加成反应通常用于制备含有双键或三键的化合物。例如,烯烃中的双键可以与卤素、醇、酸等发 生加成反应,生成相应的卤代烃、醇、酯等化合物。此外,炔烃中的三键也可以与氢气等发生加成反应,生成烯 烃或烷烃。
详细描述
光化学反应通常需要在特定的光源照射下进行,利用光能激发分子使其跃迁至激发态,进而发生化学变化。光化 学反应具有高选择性、高活性和环保等优点,因此在药物合成中常用于合成一些具有特定结构的化合物。
酶催化反应
总结词
酶催化反应是一种利用酶作为催化剂来加速生物体内生化反应的特殊反应。
详细描述
酶是生物体内的一种蛋白质,具有高度专一性和高效性,能够加速生物体内的生化反应。酶催化反应 具有高选择性、高活性和低污染等优点,因此在药物合成中常用于合成一些具有复杂结构的天然产物 或类似物。
压力条件
01
02
03
常压反应
大多数药物合成反应在常 压下进行,操作简便,设 备要求低。
பைடு நூலகம்
加压反应
在高压下,可以提高反应 速度和产率,缩短反应时 间。但加压设备成本高, 操作复杂。
真空反应
在真空条件下,可以降低 反应温度,减少副反应, 提高产物纯度。但真空设 备成本高,操作复杂。
溶剂选择与控制
溶剂的种类
实验废弃物的处理与环保
实验废弃物的分类
根据废弃物的性质和危害程度,将其分为一般废弃物、有害废弃物和危险废弃 物,并采取相应的处理措施。
废弃物处理
对于一般废弃物,可进行简单的分类和处置;对于有害废弃物和危险废弃物, 应按照相关规定进行无害化处理和处置,以降低对环境和人体健康的危害。
第七章 还原反应2
Copyright © 2004 Pearson Education, Inc., publishing as Benjamin Cummings
第一节 还原反应机理
一.非均相催化氢化反应 1.基本过程 五个连续的步骤:底物分子向催化剂界面扩散;底 物分子在催化剂表面吸附(包括物理吸附和化学吸 附);底物分子在催化剂表面进行化学反应;产物分 子由催化剂表面解吸;产物分子由催化剂界面向介 质扩散。 通常决定总反应速度的主要是吸附和解吸两步。
Copyright © 2004 Pearson Education, Inc., publishing as Benjamin Cummings
第二节不饱和烃的还原 一 炔、烯烃的还原1多相催化氢化
③铂(Pt)为催化剂
铂 Na2PtCl6 + 2HCl + 6NaOH H2PtCl6 + NaBH4 载体铂 PtO2 Adams Pt Pt + 2HCOONa + 6NaCl + 4H2O
亚当斯催化剂 (NH4)2PtCl6 + 4NaNO3 PtO2 + 4NaCl + 2NH4Cl + 4NO2 + O2
第一节 还原反应机理
一.非均相催化氢化反应 4.催化转移氢化反应 通常所用的供氢体主要为不饱和脂环烃、不饱和萜 类及醇类,如环己烯、环已二烯、四氢化萘、α-蒎 烯、乙醇、异丙醇和环己醇等。最常用而易得的供 氢体为环己烯和四氢化萘。常用而有效的催化剂是 钯黑和钯碳,而铂、铑等催化剂的活性较低。 Raney镍仅用于醇类。
《药物合成反应》第一章 卤化反应
精品课程
药物合成反应
材料与化学工程系
药物合成反应
医药工业与制药工程
• 医药行业是按国际标准划分的15类国际化 产业之一,被称为“永不衰落的朝阳产业”
• 包括医药工业和医药商业
• 医药工业按原材料来分,又可分为化学制 药业、中药业、生物制药业及医疗器械业
药物合成反应
医药工业发展前景
• 随着社会的的现代化发展要求,对药的品 种、质量、效果等相应地提出了越来越高 的要求
• 随着中国步入老龄化社会,对医药的需求 带来相当大的机会
• 医药产业已成为世界经济强国竞争的焦点, 世界上许多国家都把建立制药学科视为国 家强盛的现状
• 中国医药工业的现状
药物合成反应
一 不饱和烃卤加成反应 1.卤素对烯烃的加成
(加成)
药物合成反应
F2:加成反应激烈,副产物多,实用性小; I2:C-I键不稳定,易消除,不实用; Cl2和Br2常用,重要,资源丰富,且活泼
程度适中,反应相对易控制; Cl2来自于氯碱工业,Br2来自于海洋。
药物合成反应
• (2)反应机理(两种机理,形成两类产品) • 以anti为主,但比例影响因素较多
• 在1999年制药工程专业招生时,全国共有 34所高等院校设置制药工程专业,其中医 药类院校13所,理工类院校12所,综合性 大学9所,招生人数为1165人。
• 2004年5月,国内已有121所高校设置了制 药工程专业,
药物合成反应
分布状况
• 制药工程专业在各省市的分布不是十分均衡的
• 最多的江苏省有10所以上的高校设置了制药工程 专业,但是全国却有近1/5的省、自治区则没有设 置该专业。
