中国农业大学有机化学课件第十八章 周环反应
高等有机化学周环反应
H R1
R1
H
C CH CH CH CH2
C CH CH CH CH2
R2 1 2 3 4 5 [1,5] s迁移 R2 1 2 3 4 5
H
1
2
hv
3
[1,3] s迁移
1) S-S 或 A-A相连, 且分子轨道能量尽可能相近,这是能量近似原则; 2)相同对称性的连线不能相交,即两条SS 或两条 AA不能在相关图上交叉。
m1 m2
m1 m2
C2 s 键: C2 对称,m1对称
C2 p 键: C2 反对称,m1对称
* 周环反应中顺旋保持C2对称性, 而对旋保持m1对称性.
COCH3
1 2 COCH3
3H
12 CH2 CH
CH2 CH
1
2
3 CH CH3
CH2
[3,3] s迁移
3
1 23 CH2 CH CH CH3
CH2 CH CH2 1 23
那么、为什么上述s 迁移反应有时需要加热,有时需要光照呢? [1, j] s 迁移:此反应经过环状过渡态,其中转移基团氢于迁移起点和终点都相
4n+2 p电子的环加成反应:
HOMO 2 (A)
LUMO 3 (S)
LUMO p* (A)
HOMO p (S)
m1
m1
对于第一种情况,两种分子的两个分子轨道对m1对称元素是反对称的,对 于后一种情况,两者是对称的。因此两种情况对称性是一致的,轨道对称性是
允许的,反应顺利进行。但是丁二烯的分子轨道理论计算结果表明:
第十八章 协同反应

过程中起着极其重要作用。
Company Logo
18.1
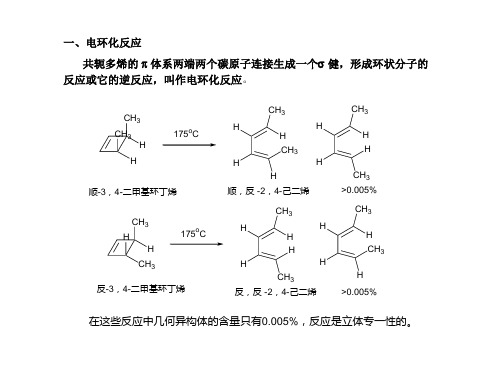
电环化反应
直链共轭多烯的π分子轨道的一些特点 1) π分子轨道的数目与参与共轭体系的碳原子数是一 致的。 2) 对镜面( δv)按对称-反对称-对称交替变化。 3)结(节)面数由0→1→2…逐渐增多。 4) 轨道数目n为偶数时,n /2为成键轨道,n /2为反 键轨道。n为奇数时,(n-1)/2为成键轨道,(n-1)/2 为反键轨道,1个为非键轨道。
Company Logo
18.1
π4
电环化反应
LUMO
π4
π3 LUMO
HOMO
π3 π2 π1
π2
HOMO
π1
基 态
激发态
1,3 — 丁二烯的π分子轨道
Company Logo
18.1
电环化反应
3、 电环化反应立体选择性的解释
①丁二烯的电环合反应 加热时, HOMO如下, 顺旋生成产物
丁二烯在基态(加热)环化时,顺旋允许,对旋禁阻。 光照时, HOMO如下, 对旋生成产物
Company Logo
自由基反应和离子型反应的共同特点:
反应物 反应活性中间体 产物
1912年 Claisen重排 1928年 Diels —Aldler反应 1940年 Cope重排 共同特点:
反应物
产物
Company Logo
周环反应的共同特点:
1. 反应过程中没有自由基或离子这一类活性中间体产生; 旧键断裂与新键生成同时进行。 2. 反应条件一般只需要加热或光照,反应速率极少受溶剂
Bπ * Aπ
LUMO 热反应(对称性禁阻) HOMO
Company Logo
光照条件下,到处于激发态的乙烯分子中的一个电子跃 迁π*轨道上去,因此,乙烯的HOMO是π*,另一乙烯分子基 态的LUMO也是π*,两者的对称性匹配是允许的,故环加成 允许。
有机合成机理1周环反应机理

分子轨道对称守恒原理和前线轨道理论是近代有机化学中的重大
成果之一。为此,轨道对称守恒原理创始人之一R.霍夫曼和前线轨
道理论的创始人福井谦一共同获得了1981年的诺贝尔化学奖。
1.σ-键的形成 当两个原子轨道沿着键轴方向对称重叠时,可形成两个σ-键的分
子轨道。对称性相同的原子轨道形成σ-成键轨道,对称性不同的原 子轨道形成σ*反键轨道。
以丁二烯为例讨论——丁二烯电环化成环丁烯时,要求: 1.C1—C2,C3—C4沿着各自的键轴旋转,使C1和C4的轨道结合形 成一个新的σ-键。 2.旋转的方式有两种,顺旋和对旋。 3.反应是顺旋还是对旋,取决于分子是基态还是激发态时的HOMO 轨道的对称性。 丁二烯在基态(加热)环化时,起反应的前线轨道HOMO是ψ2 所以丁二烯在基态(加热)环化时,顺旋允许,对旋禁阻。
25 ℃ 顺旋
CH3 Ph
CH3
CH3 H H CH3
顺旋 H3C H H
hυ 对旋 CH3
HH CH3 CH3
二、4n+2个π电子体系的电环化
以己三烯为例讨论,处理方式同丁二烯。先看按线性组合的己三烯的六个分子轨道。
ψ6
E6
ψ5
E5
ψ4
E4
E
ψ3
E3
ψ2
E2
ψ1
E1
基态 激发态
从己三烯为例的π轨道可以看出: 4n+2π电子体系的多烯烃在基态(热反应时)ψ3为HOMO,电环化
时对旋是轨道对称性允许的,C1和C6间可形成σ-键,顺旋是轨道对称 性禁阻的,C1和C6间不能形成σ-键。
顺旋(禁阻)
对旋(允许)
ψ3 己三烯的热环合
130 ℃
CH3 H
第二十一章周环反应PPT课件

.
25
但在光的作用下,丁二烯及其衍生物按对旋的方式变为环丁烯及
其衍生物。这一反应大多数是形成关环化和物,而逆向开环反应则 不易发生。这是由于双烯比烯吸收光的力量更强,因此双烯容易被 激化。由于逆向反应是热禁阻的,所以应当预料到,产物非常稳定。 这是合成环系的有效方法。
.
27
环加成反应
两分子烯烃或多烯烃变成环状化合物的反应叫做环加成。 例如:
[4+2]环化加成反应(热反应)允许
.
37
[4+2] 环 化 加 成 反 应 具 有 下 列 特 点 :
(i)是可逆的反应。利用逆反应有时可以得到一些用别
的方法难以合成的化合物。例如:
(ii)加成时是立体专一性的,无例外的都是顺 式加成。
(iii)如亲双烯分子上还有其它的不饱和基团时,加成后不饱 和基团是靠近于新产生的双键一面。它是一个经验规则,称为 阿尔德规则,也称不饱和性最大积累规则。[夏炽中译[美]F.A. 凯里等“高等有机化学“A卷P367]。例如,两个分子的环戊二 烯合成反应时,一个分子供给一个双键,作为亲双烯使用。 加 成时生成二环戊二烯, 理论上应有两种取向: 一种是外型 (Oxo)的, 即原有的双键和新生成的双键处在离的较远的位 置; 另一种是双键处在离的较近的位置, 这叫作内型(Endo) 的,双烯合成主要产生内型产物。(邢其毅主编”基础有机化 学示范教学“P308,胡宏纹讲的”周环反应“解释为次基轨道 的结果)。
Woodward和Hoffman指出:“当反应物与产物的轨道 对称性相合(轨道对称性匹配或者说相位相同)时,反应 易于发生,并不相合时,反应难于发生。”顺旋时反应物 与产物对称性相合。前线轨道理论,只看HOMO的两头 的相位,不管中间。
有机反应中的周环反应PPT共69页

有机反应中的周环反应
31、别人笑我太疯癫,我笑他人看不 穿。(名 言网) 32、我不想听失意者的哭泣,抱怨者 的牢骚 ,这是 羊群中 的瘟疫 ,我不 能被它 传染。 我要尽 量避免 绝望, 辛勤耕 耘,忍 受苦楚 。我一 试再试 ,争取 每天的 成功, 避免以 失败收 常在别 人停滞 不前时 ,我继 续拼搏 。
33、如果惧怕前面跌宕的山岩,生命 就永远 只能是 死水一 潭。 34、当你眼泪忍不住要流出来的时候 ,睁大 眼睛, 千万别 眨眼!你会看到 世界由 清晰变 模糊的 全过程 ,心会 在你泪 水落下 的那一 刻变得 清澈明 晰。盐 。注定 要融化 的,也 许是用 眼泪的 方式的 光荣可 以被永 远肯定 。
谢谢
11、越是没有本领的就越加自命不凡。——邓拓 12、越是无能的人,越喜欢挑剔别人的错儿。——爱尔兰 13、知人者智,自知者明。胜人者有力,自胜者强。——老子 14、意志坚强的人能把世界放在手中像泥块一样任意揉捏。——歌德 15、最具挑战性的挑战莫过于提升自我。——迈克尔·F·斯特利
周环反应18综述

周环反应主要内容一、引言二、周环反应的分类及理论解释分类:1.电环化反应(electrocyclic reactions)2.环加成反应(cycloaddition reactions)3.(T -键迁移反应(sigmatropic rearrangement)理论解释:1.前线轨道理论2.分子轨道对称性守恒3.芳香过渡态理论三、总结引言在本科学习过两类反应:离子反应:通过键的异裂而产生的C+、C为中间体自由基反应:通过键的均裂而产生的C为中间体但是,有没有其它类型的反应呢?1928年Diels-Alder反应,研究相当深入,应用广泛但这类反应没有检测到反应中间体,不服从上述两种反应机理,不受溶剂极 性影响,不被酸碱催化,也不受自由基引发剂或淬灭剂的影响,是一类很特殊的有机反应,一度认为是没有机理的反应,困惑化学界50多年(从1912年Claisen 反应起)。
1958年Vogel 报道了一个有趣的反应:1961年荷兰Leiden 大学Prof.Haringa 研究己三烯关环时,得到的是CH —、H — 反式的关环产物该校Oosterhoff 教授认为,加热和光照所引起的化学反应的立体化学不同可能 是由于受到其他因素(如共轭己三烯的轨道对称性)的影响,并进一步提出是受 最高占据轨道和节点数控制的。
这一见解Haringa 作为脚注发表在四面体上。
这已经接近了分子轨道对称性守恒大门,可以说已经踏入了一只脚。
120°Ccis-tra nsMe而得不到更稳定的:tran s-tra n或者不稳定的:CO 2MeCO COMe2 GO Me与此同时,美国Woodwarc和Eschenmoser正领导全世界来自19个国家的100 位科学家进行V B12全合成工作,历时12年,于1972年宣告完成,轰动一时,是有机合成的杰作,传为佳话。
在合成过程中,注意到己三烯在关环反应中,在光、热不同条件下,产物的立体化学完全不同,Woodwarc称之为“the very pretty set of facts ” (一组绝妙的事实),他抓住这个事实,深入研究,并与年轻的量子化学博士后Hoffman合作,发现了“分子轨道对称性守恒原理”,或称W—H规则。
有机化学理论课 第十八章 分子轨道理论简介

第十八章分子轨道理论简介一、教学目的和要求(1)了解分子轨道理论的原理。
(1)了解周环反应的一般规律。
(2)了解分子轨道对称守恒原理在有机合成中的作用。
二、教学重点与难点分子轨道理论的原理,周环反应的理论。
三、教学方法和教学学时1、教学方法:以课堂讲授为主,结合必要的课堂讨论。
教学手段以板书和多媒体相结合。
2、教学学时:2学时四、教学内容第一节电环化反应第二节环加成反应第三节σ迁移反应第四节周环反应的理论一、电环化反应机理二、环加成反应机理三、σ键迁移反应机理五、课后作业、思考题习题:1、2、4、6、11。
§18-1 周环反应的理论一、周环反应前面各章讨论的有机化学反应从机理上看主要有两种,一种是离子型反应,另一种是自由基型反应,它们都生成稳定的或不稳定的中间体。
还有另一种机理,在反应中不形成离子或自由基中间体,而是由电子重新组织经过四或六中心环的过渡态而进行的。
这类反应表明化学键的断裂和生成是同时发生的,它们都对过渡态作出贡献。
这种一步完成的多中心反应称为周环反应。
周环反应:反应中无中间体生成,而是通过形成过渡态一步完成的多中心反应。
反应物——→产物周环反应的特征:(1) 多中心的一步反应,反应进行时键的断裂和生成是同时进行的(协同反应)。
例如:(2) 反应进行的动力是加热或光照。
不受溶剂极性影响,不被酸碱所催化,不受任何引发剂的引发。
(3) 反应有突出的立体选择性,生成空间定向产物。
例如:二、周环反应的理论 (一) 轨道和成键周环反应的过程,广泛的应用轨道来描述,这些轨道往往是用图形来表示。
有机化学中涉及最多的原子轨道为1p 轨道和2s 轨道。
原子轨道线形组合成分子轨道。
当两个等价原子轨道组合时,总是形成两个新的分子轨道,一个是能量比原子轨道低的成键轨道,另一个是能量比原子轨道高的反键轨道。
(二)分子轨道对称守恒原理原子轨道组合成分子轨道时,遵守轨道对称守恒原理。
即当两个原子轨道的对称性相同(位相相同)的则给出成键轨道,两个原子轨道的对称性不同(位相不同)的则给出反键轨道。
第18章周环反应-ye

共轭多烯的分子轨道及有关概念
成键轨道、反键轨道、非键轨道 最高占有轨道(HOMO)、最低未占轨道( LUMO )、 单占轨道(SOMO) 电子在分子轨道中的排列遵循:能量最低原理、鲍 里不相容原理、洪特规则 离域分子轨道、离域键、定域分子轨道、定域键 离域能( DE ) = 离域的 E -定域的 E (分子中所有 电子能量之和称为E) 节 ( 结 ) 面、对称性、对称、反对称、不对称、镜面、 C2旋转轴
+
H H
Ph
C
CH2 H
2016年3月2日
温州医学院药学院
对反应情况作出解释
H + Br H
内向对旋
Cl 7 Br 2 1 3 4 H 6 5H
+
H2O
OH Br
H + Br H
Cl 7 Br 2 1 3 4 H 6 5H
H + Br H
OH
H2O -H+
Br
+
外向对旋
H H
+
Cl
2016年3月2日
1s atom ic orbital H:H bonding m ole cular orbital
1s atom ic orbital
分子轨道数等于参与组合的原子轨道数。 按能量由低到高依次分别为成键轨道、非 键轨道和反键轨道。
温州医学院药学院
2016年3月2日
原子轨道有两种组合方式。 1S波函数相位相同时,相互增强,形成 成键轨道。
温州医学院药学院
电环化反应选择规则的应用实例
CH 3 H 3C H
CH 3
175oC
