使用氨基柱分析食品中的糖类
单糖及氨基糖的毛细柱气相色谱分析
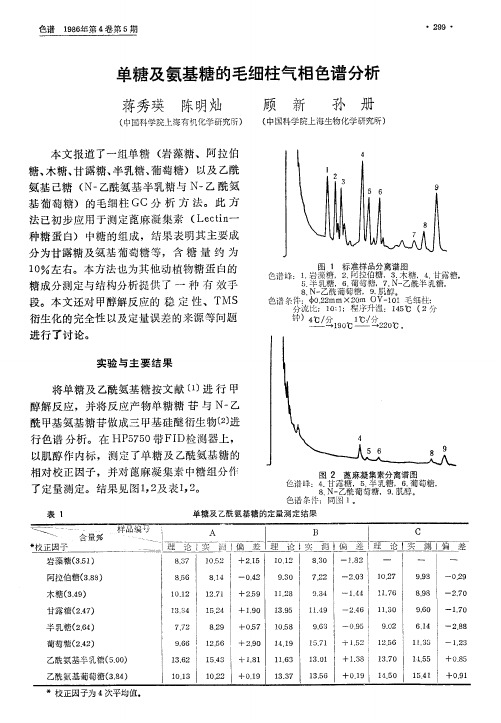
表 1
单 糖 及 乙酰 氨 基 糖 的 定 量 测 定 结 果
表 2 蓖麻凝集素中糖组分测定
结果讨论 (一) 甲醇解反应的稳 定性问题: 由于 单糖的结构不 同,在反应中活性各不相同, 对酸度和温度敏感性不 同[3],我们选用较为 激 烈的条件,以保证 甲醇解完全。 (二)TMS衍 生 物 的完全性和稳定性 问题:我们做了乙酰氨基糖的 TMS衍生物
的红外光谱图,无-OH峰吸收,但有-OSi (CH3),吸收,证明糖的 TMS是基本完全的。 另外,该衍生物在潮湿空气 中易水解,故对 该类化合物进行衍生化 反应时须注意容器及
试剂的干燥。 (三) 定量 方法的误差来源:1.样品纯
度问题:我们选用的标准糖及 内标物均为生 化试剂 ,其纯度不高,给方法带来一定的系 统误差。2.糖的TMS衍生物对 FID响应普 遍较小[4],我们得到了与文献报道相同的结 果。3.峰面积采用半峰宽的人工测量是影响 方法精度和准确度的主要 因素之一。
单糖及氨基糖的毛细柱气相色谱分析
蒋秀瑛 陈明灿
顾新 孙册
ቤተ መጻሕፍቲ ባይዱ
(中国科学院上海有机化学研究所) (中国科学院上海生物 化学研究所)
本文报道了一组单糖 (岩藻糖、阿拉伯 糖、木糖、甘露糖、半乳糖、葡萄糖)以及乙酰 氨基己糖 (N-乙酰氨基半乳糖与 N-乙酰氨 基葡萄糖)的毛细柱GC分 析 方 法。此 方 法已初步应用于测定蓖麻凝集素 (Lectin一 种糖蛋 白) 中糖的组成,结果表明其主要成 分为甘露糖及氨基葡萄糖等,含 糖 量 约 为 10%左右。本方法也为其他动植物糖蛋 白的 糖成分测定与结构分析提供了一 种 有 效手 段。本文还对甲醇解反应的 稳 定 性、TMS 衍生化的完全性 以及定量误差的来源等问题 进行了讨论。
Amide80系列色谱柱分离糖类中文1

基本概念见第 2-1 节。图 3 和 4 显示了柱效和保留随 柱温的不同而异。
-4-
分钟
图 10 环槐聚糖的分离
色谱柱:
洗脱液: 流速: 温度: 检测:
TSKgel Amide-80
4.6mm ID x 25cm 乙腈 / 水 = 57/43 1.0mL/min 25℃ RI
分钟
图9 色谱柱:
洗脱液: 流速: 温度: 检测:
β-环糊精酸水解产物的分离
TSKgel Amide-80 4.6mm ID x 25cm 乙腈/水 = 55/45 1.0mL/min 25℃ RI
3-2 影响谱带增宽的因素
(1) 流速
第 2-2 节中描述了流量对理论塔板高度的影响。请 参见图 3、图 5 和 图 6。
进样量 (μg)
图8
进样量与峰面积之间的关系
色谱柱:
洗脱液: 流速: 温度: 检测: 样品:
TSKgel Amide-80 4.6mm ID x 25cm 乙腈/水 = 80/20 1.0mL/min
80℃
RI 1. 赤藓糖醇 2. 葡萄糖 3. 木糖
3. 方法开发
如前一节所述,有必要对各种流动相条件进行研究,以优 化保留和选择性。以下给出了使用 TSKgel Amide-80 柱进 行方法开发时的一些指南。
TSKgel Amide-80 4.6mm ID x 25cm 乙腈/水 = 80/20 1.0mL/min
80℃
RI 1.鼠李糖 2. 岩藻糖 3. 木糖 4. 果糖 5. 甘露糖 6. 葡萄糖 7. 蔗糖 8. 麦芽糖
4-2 寡糖的分离 (环槐聚糖:环 β-1, 2-葡聚糖)
环槐聚糖的分析如图 10 所示,17 聚体至 24 聚体程度的 环槐聚糖得到分离。
氨基柱分离糖先后顺序

氨基柱分离糖先后顺序氨基柱是一种常用的色谱柱,用于糖类物质的分离。
糖是生物体内最重要的能量供应物质之一,具有广泛的生理功能。
糖类物质的分离对于研究其结构和功能具有重要意义。
本文将以氨基柱分离糖的先后顺序为标题,介绍氨基柱在糖类物质分离中的应用。
一、氨基柱的基本原理氨基柱是一种通过亲水作用分离糖类物质的色谱柱。
其基本原理是利用氨基官能团与糖分子中的羟基之间的氢键作用,实现糖类物质的分离。
由于糖类物质中的羟基数量和位置的不同,使得不同的糖类物质在氨基柱上具有不同的保留时间,从而实现分离。
二、单糖的分离单糖是糖类物质中的基本单位,包括葡萄糖、果糖、半乳糖等。
在氨基柱上,单糖的分离通常通过调节流动相的pH值、离子强度和有机溶剂含量来实现。
例如,在弱酸性条件下,将流动相的pH值调节到适当的范围,可以实现对单糖的有效分离。
此外,还可以通过梯度洗脱的方式,根据不同单糖的亲和力来实现它们的分离。
三、二糖的分离二糖是由两个单糖分子通过糖苷键连接而成的糖类物质,包括蔗糖、乳糖、麦芽糖等。
在氨基柱上,二糖的分离通常需要调节流动相的pH值、离子强度、有机溶剂含量以及洗脱梯度等参数。
通过这些参数的调节,可以实现对不同二糖的有效分离。
同时,根据二糖的结构特点,还可以采用亲水性降低的有机溶剂作为流动相,以增强分离效果。
四、寡糖的分离寡糖是由若干个单糖分子通过糖苷键连接而成的糖类物质,包括麦芽三糖、低聚果糖等。
在氨基柱上,寡糖的分离通常需要更加复杂的条件。
除了调节流动相的pH值、离子强度、有机溶剂含量以及洗脱梯度等参数外,还需要根据寡糖分子的大小和结构特点来选择合适的分离条件。
此外,还可以采用亲水性降低的有机溶剂作为流动相,并采用温度梯度的方法来增强分离效果。
五、多糖的分离多糖是由大量单糖分子通过糖苷键连接而成的糖类物质,包括淀粉、纤维素等。
在氨基柱上,多糖的分离需要更加复杂的条件。
通常需要采用多种分离技术的组合,如尺寸排阻色谱、亲和色谱等。
色谱法在糖类化合物分析中的应用

第2期王静等:色谱法在糖类化台物分析中的应用糖类化合物的传统检测方法采用柱后衍生和可见光检测器检测.近年来常用灵敏度较低的示差折光检测器直接测定,样品毋需衍生化。
为了提高分析灵敏度,可采用衍生化的方法将样品组分制备成具有紫外吸收或能发出荧光的衍生物,用紫外检测器、二极管阵列检测器或荧光检测器,虽然样品制备操作繁杂,但分析灵敏度可大大提高。
高效液相色谱分析糖类化合物用固定相一般认为CaIbohydm把柱和氨基键合周定相具有较好的分离效果,前者为w砒t∞公司的品脾.价格昂贵.常用的氨基键合固定相品牌有:AM矾msⅡ,x.1,陇}mBorbN如.sph耐80出N心,HypersilN心,P0】y髀m60.5N屿,眦N玛。
大多数单糖、低聚糖在氨基柱上可得到满意的分离。
但是某些还原糖容易与固定相的氨基发生化学反应,产生席夫碱,使氨基柱的使用寿命缩短,而且氨基柱所需平衡时间较长。
离子交换色谱也可用于糖的分离。
糖在水溶液中虽不以离子形式存在,但可通过形成离子配合物的方式间接实现糖韵分离,糖的硼酸盐化合物即可采用阳离子交换树脂柱分离。
另有报道使用价格低廉的硅胶柱和十八烷基键合固定相(‰)分离糖,效果较好,前者流动相需加氨类调节荆,后者用水做流动相。
高效液相色谱分析糖类化合物用流动相一般为水和乙腈、甲醇的二元混合溶液或三元混合溶液,配比视组分的多少,分子量范围,结构组成等而定,还可采用梯度洗脱改善分离、缩短分析时间。
但无论流动相配比如何变化,采用反相化学键合相色谱体系分析单糖、低级糖,其出峰顺序有规律地依赖于分子量的大小,且相同分子量的酮糖较醛糖保留时问短。
6凝胶渗透色谱法测定多糖分子量m滞瑚】高效液相凝胶渗透色谱法测定多糖分子量因具有快速、高分辨率和重现性好的特点已被广泛采用。
不同分子量的多糖按照其大小顺序先后流出色谱柱,通过一系列不同分子量标准多糖测得的校正曲线得出相应的分子量。
凝胶渗透色谱测定多糖分子量所用柱填料为刚性或半刚性水溶性凝胶,填料表面孔径范围可以从2—250m。
高效液相色谱法检测乳制品中果糖_葡萄糖_蔗糖和乳糖的含量

Determination of fructose, glucose, sucrose and lactose in dairy products by high performance liquid chromatography
LI Jing- fang, ZHANG Su- wen, PENG Mei- chun, PENG Can ( Hunan Avadairy CorpLtd , Changsha 410200 , China) Abstract: HPLC method was established to determine the fructose, glucose, sucrose and lactose in dairy products These four kinds of sugars were simultaneously assayed on a NH2 column by using a differential refract- meter detector and a mobile phase of acetonitrile- water( 75∶25 ) The linear range of this method ranged from 2 mg / mL to 20 mg / mL The relative standard deviation was 290 %, 141 %, 140 %, 279 % for fructose, glucose, sucrose and lactose respectively The 10461 %, 10456 %, 9787 % This method was proved to be accurate average recovery was correspondingly 9496 %, and rapid Key words: HPLC; fructose; glucose; sucrose; lactose 中图分类号: TS2527 文献标识码: A 文 章 编 号: 1002-0306 ( 2011 ) 06-0391-03
使用氨基柱分析食品中的糖类

LC-Vp 系统 包括脱气机 DGU14A;泵 LC-10ADvp (1 台); 自动进样器 SIL-HTC; 柱温箱 CTO-10Avp;示 差折光检测器 RID-10A
分析条件
分析柱:Asahipak NH2-50 4E (内径 4.6mm×长 250mm) 保护柱:Asahipak NH2-50G 4A (内径 4.6mm×长 10mm) 流动相:乙睛:水 (7:3) 流量:0.8mL/min 柱温:40℃ RID 池温:40℃ 检测时间:15min 进样体积:10μL
实验可以看出,该方法的稳定性良好,对实际样品进行检测也得到了很好的结果。
0.3
0.3
0.3
0.3
0.2
0.2
0.2
0.2
Volts
果糖 葡萄糖
Volts Volts
Volts
0.1
果糖 葡萄糖 蔗糖 棉子糖
0.1
0.1
0.1
(棉子糖)
蔗糖
0.0
0.0
0.0
0.0
0
1
2
3
4
5
6
7
8
9 10 11 12 13 14 15
标样 葡萄糖,果糖,蔗糖,棉子糖
标样配制 将葡萄糖,果糖,蔗糖,棉子糖标样溶解于水中,配制成 25mg/mL、20mg/mL、 15mg/mL、
10mg/mL 和 5mg/mL 的混标液。各进样 10μL,各重复 2 次。分别制作各组分的标准曲线。并计 算各组分的相关系数和最低检出限。结果见表 1。 精密度试验
取 15mg/mL 的混标样,进样 10μL,连续测定 6 次,色谱图如图 1。各组分保留时间和面积 的相对标准偏差见表 2。 实际样品分析
糖柱分离原理、分类

糖柱糖柱专为糖和有机酸的高效分离设计。
顾名思义就是分析分离糖类物质的色谱柱,分离原理是基于配体交换反应,糖分子上每一个羟基都带有一个非常弱的负电荷,而端基异构碳上所带的羟基可被去质子化,从而带上一个很强的负电荷。
糖分子上的这些负电荷与树脂表面上的金属离子的正电荷之间的相互作用使糖被保留,从而达到分离。
目前使用较多的糖类分析柱有聚合物基质的磺化柱和氨基硅胶色谱柱,其中聚合物磺化色谱柱又分为磺化氢型(如UniPS 5-10H)、磺化钙型(如UniPS 5-10Ca)、磺化钠型(如UniPS 5-10 Na)等等,常见的糖柱有:Ca 柱——对于一般的甜味剂分析来说,钙型柱是首选的柱。
它已经过优化,可用于分析单糖类,还可提供二糖类、三糖类和四糖类的分离。
300 x 7.8 mm 柱主要用于定量高果糖玉米糖浆中的葡萄糖和果糖,以及进行单糖类常规分析。
250 x 4.0 mm 柱适合糖醇分离。
Pb 柱——铅型柱专门用于分离纤维素衍生单糖。
它用于分析木制品的戊糖和己醣,尤其是纤维二糖、葡萄糖、木糖、半乳糖、树胶醛醣和甘露糖。
它还可很好地分辨乳制品中的蔗糖、乳糖和果糖。
H 柱——氢型柱用于含有羧酸、挥发性脂肪酸、短链脂肪酸、醇类、酮类以及许多中性新陈代谢副产物的溶液中的碳水化合物进行分析。
最常用于有机酸分析,此柱还可用于发酵监测、生物流体分析和乙酰氨基糖分离。
Na 柱——钠型柱已针对含高浓度盐(例如甜菜糖)的样本中的糖分析进行优化。
它与盐相容,所以在分析前不需要对样品进行脱盐处理。
K 柱——钾型柱已针对玉米糖浆和酿造麦汁等样本中的单糖、二糖、三糖分析进行优化。
它可很好地分离葡萄糖、麦芽糖和麦芽三糖。
Ag 柱——银型柱可提供快速、高分辨率的寡糖分析。
它可在大约25 分钟的时间内对寡糖(Dp-11)进行分离。
氨基柱——氨基柱一般用于分离各种单糖,不宜分离含醛基,羰基的化合物,还原糖,可用于分离非还原糖。
糖柱所配套的检测器:示差折光、蒸发光散射检测器(ELSD)、脉冲安培检测器。
高效液相色谱蒸发光散射检测器测定保健食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖和木糖

高效液相色谱蒸发光散射检测器测定保健食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖和木糖尚姝;冯有龙【摘要】目的:建立高效液相色谱-蒸发光散射法同时测定保健食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖、木糖的方法。
方法采用Sepax HP-Amino(300mm×4.6 mm,5μm)色谱柱,流动相为乙腈-水(70∶30),流速为1.0 mL·min-1,柱温为35℃;使用蒸发光散射检测器检测,漂移管的温度105℃,载气流速2.2 mL·min-1。
结果果糖、葡萄糖、蔗糖、麦芽糖、乳糖和木糖进样量分别在1.0328~10.328μg(r=0.9989),1.5085~15.085μg(r=0.9997),1.0199~10.199μg(r=0.9998),1.5094~30.187μg(r=0.9995),2.9992~59.984μg (r=0.9996),5.05~50.5μg (r=0.9996)范围内与峰面积的对数呈现良好的线性关系;平均回收率(n=6)分别为96%,105%,103%,95%,98%和99%;重复性实验,6种糖含量的 RSD(n=6)分别为2.95%,2.52%,1.75%,1.62%,2.23%和1.85%。
结论该方法操作简单、快速、准确,适用于多种保健食品中糖的分析。
%Obj ective A method for the simultaneous determination of 6 sugars such as fructose,glucose,sucrose,maltose,lactose and xylose in functional foods was described by using high performance liquid chromatography with evaporative light scattering de-tection(ELSD).Methods Sepax HP-Amino column (300 mm×4.6mm,5μm)was adopted,the mobile phase was composed of acetonitrile-water(70∶30)at a flow rate of 1.0 mL·min-1 ,and the column temperature was set at 35 ℃;The conditions of ELSD were as follows:the temperature of the drifting tube 105 ℃,the flow rate of nebulizer gas 2.2 mL·min-1 .ResultsThe logarithm of samples size of fructose,glucose,sucrose,maltose,lactose and xylose had good linearity with the logarithm of peak ar-ea in the ranges of 1.032 8-10.328μg(r=0.998 9),1.508 5-15.085μg (r=0.999 7),1.019 9-10.199μg(r=0.999 8),1.509 4-30.187μg (r=0.999 5),2.999 2-59.984μg(r=0.999 6),and 5.05-50.5μg (r=0.999 6),respectively;The average recoveries were 96%,105%,103%,95%,98% and 99%,respectively;Repeatability experiments showed that RSD values of their contents were2.95%,2.52%,1.75%,1.62%,2.23% and 1.85%,respectively.Conclusion This method was simple,fast,and accurate for the analysis offructose,glucose,sucrose,maltose,lactose and xylose in functional foods.【期刊名称】《西北药学杂志》【年(卷),期】2014(000)001【总页数】5页(P27-31)【关键词】高效液相色谱法;蒸发光散射;保健食品;果糖;葡萄糖;蔗糖;麦芽糖;乳糖;木糖【作者】尚姝;冯有龙【作者单位】江苏省食品药品检验所,南京 210008;江苏省食品药品检验所,南京 210008【正文语种】中文【中图分类】R927.2糖是植物和动物的主要能源物质,也是生命过程中必需的营养素[1],在生命过程中提供能量、增强人体的免疫功能、控制和调节细胞的分裂和生长[2]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Minutes
图 1 糖标准样品的色谱
0
1
2
3
4
5
6
7
8
9 10 11 12 13 14 15
Minutes
图 2 实际样品色谱图
重复性
1
2
3
保留时间
4
5
6 平均
RSD/%
1
2
3
4 面积
5
6 平均
RSD/%
表 2 精密度实验结果
果糖 5.804 5.797 5.785 5.772 5.862 5.862 5.813 0.668 869505 887332 870326 880015 875419 869991 875431 1.44
使用氨基柱分析食品中的糖类
摘要 对几种常见的低分子量的糖类进行了分析,实验采用了比较便宜的常规分析柱氨基柱作
为分离手段,并研究了该方法的稳定性。
关键词 HPLC 低分子量糖类 氨基柱
糖是自然界分布最广泛的有机化合物群之一,是生物的能源,具有非常重要的作用。糖主 要分布在植物、食品中,是决定食品风味的最主要的成分之一,因此,糖类的分析具有非常重 要的意义。目前,糖类分离的手段主要是采用液相色谱,检测手段主要为示差折光检测器。
取 15mg/mL 的混标样,进样 10μL,连续测定 6 次,色谱图如图 1。各组分保留时间和面积 的相对标准偏差见表 2。 实际样品分析
称取样品大枣提取液 50mg,溶解于 1mL 水中,0.45um 膜过滤后,进样 10μL,重复 3 次。 色谱图见图 2。
52
结果讨论
表 1 糖标准样品线性及最低检出限
棉子糖 12.035 12.014 12.026 12.026 11.943 12.067 12.014 0.314 747302 772964 756541 770132 759981 760213 761189
2.39
53
标样 葡萄糖,果糖,蔗糖,棉子糖
标样配制 将葡萄糖,果糖,蔗糖,棉子糖标样溶解于水中,配制成 25mg/mL、20mg/mL、 15mg/mL、
10mg/mL 和 5mg/mL 的混标液。各进样 10μL,各重复 2 次。分别制作各组分的标准曲线。并计 算各组分的相关系数和最低检出限。结果见表 1。 精密度试验
果糖 葡萄糖 蔗糖 棉子糖
回归方程 Y=1.46×10-4X-0.035 Y=1.89×10-4X-0.14 Y=1.946×10-4X-0.26 Y=0.31×10-4X+0.12
相关系数 0.9997 0.99996 0.99991 0.99997
最低检测限 LOD(mg/ml) 0.18 0.57 0.03 0.14
葡萄糖 6.875 6.878 6.859 6.848 6.933 6.874 6.876 0.429 801027 829150 812294 809956 814235 802516 811529 2.44
蔗糖 8.299 8.296 8.280 8.272 8.267 8.283 8.283 0.152 918445 935894 921689 919942 932021 923510 925250 1.33
仪器
LC-Vp 系统 包括脱气机 DGU14A;泵 LC-10ADvp (1 台); 自动进样器 SIL-HTC; 柱温箱 CTO-10Avp;示 差折光检测器 RID-10A
分析条件
分析柱:Asahipak NH2-50 4E (内径 4.6mm×长 250mm) 保护柱:Asahipak NH2-50G 4A (内径 4.6mm×长 10mm) 流动相:乙睛:水 (7:3) 流量:0.8mL/min 柱温:40℃ RID 池温:40℃ 检测时间:15min 进样体积:10μL
实验可以看出,该方法的稳定性良好,对实际样品进行检测也得到了很好的结果。
0.3
0.3
0.3
0.3
0.2
0.2
0.2
0.2
Volts
果糖olts
0.1
果糖 葡萄糖 蔗糖 棉子糖
0.1
0.1
0.1
(棉子糖)
蔗糖
0.0
0.0
0.0
0.0
0
1
2
3
4
5
6
7
8
9 10 11 12 13 14 15
糖的种类非常的庞大,从分子量来看,有从分子量仅为 180 的单糖到分子量为几百万的多 糖,即使同样的单糖,还包含各种各样的不同糖类,如葡萄糖,氨基糖,山梨糖醇,糖醛酸等, 而且它们还有多种异构体。因此,分析糖类有不同的分离方法和检测方法。多糖主要采用凝胶 色谱法;分离单糖和低聚糖主要采用分配色谱法和配位体交换色谱法。检测手段绝大部分为示 差折光检测器。本实验采用了比较便宜的分离柱氨基柱 Asahipak NH2-50 4E 为分离手段,并研 究了该方法的稳定性。
