运用碘量法测定铜精矿中的锡
间接碘量法测定铜合金中铜含量实验报告

间接碘量法测定铜合金中铜含量实验报告一、实验目的二、实验原理间接碘量法是一种根据一定的分析方法,通过加热剂溶液通过蒸馏的方式使碘变成气体,再通过测量气体中的碘的含量来确定原液的浓度的一种分析方法。
其中,在铜合金实验中,先将铜合金中的干粉与63mL的硝酸混合,加热提取,经过滤分离以去除杂质,再加入碘酸将铜成分转化成铜碘,再通过真空蒸馏使铜碘分解,蒸发成无色无气体状的气体,最后通过对无色无气状的气体中的碘的测量含量,从而可以得到该样品中铜的浓度,以及样品中铜含量的值。
三、实验步骤1. 将1.2克的铜合金干粉加入滤瓶中,再加入70mL的稀硝酸中,加入搅拌棒混合;2. 将混合液定容至100mL,灌入石蜡封口的真空蒸馏收集管中,加热提取;3. 通过滤筛将提取液经过筛分由杂质;4. 将滤分后的液体容量调节至30mL,并加入3-3.5mL的碘酸;5. 用真空抽引真空蒸馏仪,真空蒸馏仪加热,使气体通过Co柱进行洗净;6. 将洗净后的气体浓度在Na柱上进行测定,记录碘浓度对应的原液碘浓度;7. 根据测定的碘浓度,计算实验样品中铜含量的含量。
四、实验结果实验结果如下所示:样品中铜含量:98.7 mg/L五、实验分析通过本次实验,可以得知样品中铜含量为98.7 mg/L,说明本次实验结果符合预期目标。
本次实验使用真空蒸馏装置,使铜碘分解蒸发,最后通过对无色无气状的气体中的碘的测量含量,从而可以得到该样品中铜的浓度,以及样品中铜含量的值。
六、讨论本次实验使用的真空蒸馏装置的操作非常简单,样品处理效率较高,实验结果符合预期,说明该实验是可靠的。
另外,此类实验有可能受到干扰因素的影响,从而影响实验结果的准确性,所以在实验中需要注意控制各个方面因素,以保证最终得出的实验结果准确可信。
铜合金中锡的分析作业指导书
(1+1)
浓
1%
30%
饱和溶液
固体
50%
试剂名称
碘化钾溶液
淀粉溶液
F标准溶液0.02mol/L
要求
20%
1%
准确称取F 0.7133克于250ml烧杯中,加入氢氧化钠1克,碘化钾10克,用水溶解后,移到1000ml容量瓶中,以水稀至刻度摇匀。
4.2分析方法
4.2.1称取试样0.5~1.0克于250ml三角瓶中,加入(1+1)盐酸10ml,再加入过氧化氢数ml,加热使试样溶解,待试样全溶后,加热煮沸,驱尽过量过氧化氢。
4.2.4然后根据下列公式计算铜合金中锡的含量:
锡=
T锡XV
X100%
G
锡——F标准溶液对锡的滴定度,克/ml.
G——称试样重量(克)
V——滴定时耗F标准溶液的ml数
编写人
审核人
批准人
编写日期
审核日期
批准日期
1.0目的
测定铜合金中锡的含量,为后序加工提供质量保证。
2.0适用范围
适用于本公司铜合金中锡的测定。
3.0职责
化验室:按作业规范对测试需求进行化验分析;
铸造车间:提供测试样品,根据化验结果采取相应措施。
4.0测试内容:
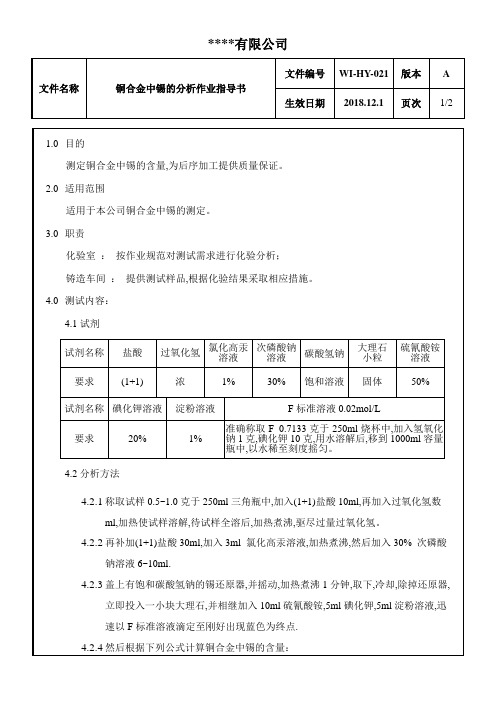
4.1试剂
试剂名称
盐酸
过氧化氢
氯化高汞溶液
次磷酸钠溶液ห้องสมุดไป่ตู้
碳酸氢钠
大理石
小粒
硫氰酸铵溶液
4.2.2再补加(1+1)盐酸30ml,加入3ml氯化高汞溶液,加热煮沸,然后加入30%次磷酸钠溶液6~10ml.
4.2.3盖上有饱和碳酸氢钠的锡还原器,并摇动,加热煮沸1分钟,取下,冷却,除掉还原器,立即投入一小块大理石,并相继加入10ml硫氰酸铵,5ml碘化钾,5ml淀粉溶液,迅速以F标准溶液滴定至刚好出现蓝色为终点.
碘量法测铜分析方法-【word】可编辑

碘量法测铜分析方法一:分析方法称取样品0.5g于250ml锥形瓶中,用水湿润摇匀,加入10ml饱和氯酸钾+硝酸溶液,在电热板上溶样,溶至近干取下稍冷加入5ml硫酸,继续加热溶解至冒烟,取下冷却再加入混合酸10ml煮沸3分钟左右,取下冷却用30ml水洗杯壁,加入脲素小许并煮沸2分钟,取下冷却加1:1氨水中和至有红色沉淀出现,再用饱和氟化氢铵溶液调至红色沉淀消失并过量1ml,加入碘化钾5ml,用标准溶液滴定至浅黄色,加入淀粉指示剂2ml,再滴定至浅兰色,加硫氰酸钾指标剂2ml使兰色加深,继续滴定至兰色消失为终点。
二:试剂:1:氯酸钾+硝酸饱和溶液:把100g氯酸钾加入400ml硝酸溶液中配成饱和溶液。
2:硫酸+硝酸混合液:3份硫酸+7份硝酸混匀。
3:饱和氟化氢铵溶液:把50g氟化氢铵加入100ml蒸馏水中配成饱和溶液。
4:脲素:5:50%碘化钾溶液:称取50g碘化钾溶入100ml蒸馏水中摇匀。
6:淀粉指示剂:称取0.5g可溶性淀粉,加30ml蒸馏水加热溶解完后补加70ml蒸馏水摇匀。
7:硫氰酸钾指示剂:称取20g硫氰酸钾加100ml蒸馏水揺匀。
8:1:1氨水溶液:1份氨水+1份蒸馏水混匀。
9:铜标准溶液:标准称取1.000g铜标准加1:1硝酸20ml,加热溶解,再加入1:1硫酸5ml继续加热化烟后取下冷却,加蒸馏水100ml使盐类溶解。
移入1000ml容量瓶中,定容摇匀。
此溶液每ml含1mg铜。
10:标准滴定溶液:称取分析纯硫代硫酸钠12.5g,加入无水碳酸钠0.1g,用蒸馏水100ml溶解后移入1000ml容量瓶中,定容摇匀一星期后标定。
11:标定:吸取铜标准溶液15ml,加30%三氯化铁溶液2ml,用氨水中和出现氢氧化铁(红色)沉淀,滴加饱和氟化氢铵溶液使红色沉淀消失,加5ml碘化钾溶液,用硫代硫酸钠标准溶液滴至淡黄色,加2ml淀粉指示剂滴至浅兰色,补加硫氰酸钾指示剂2ml摇动使兰色加深继续滴至兰色消失为终点。
碘量法测定铜精矿中铜分析误差探讨

碘量法测定铜精矿中铜分析误差探讨赵荣龙,陈俊华,朱子贤(云南铜业股份有限公司西南铜业分公司,云南昆明650102)摘要:文章阐述了碘量法测定铜分析中常见的干扰因素及消除方法,提出了对滴定过程中主张淀粉加入时机为溶液浅黄色刚好消失的观点。
关键词:碘量法;淀粉;误差作者简介:赵荣龙(1985-),男,云南大理人,主要研究方向:实验室有色金属元素分析。
Metallurgy and materials云南铜业股份有限公司西南铜业分公司是国内著名的铜冶炼企业,铜精矿作为公司的主要原料,分析结果直接用于结算。
文章讨论的碘量法是常量铜分析的经典分析方法,反应原理为Cu 2+与I -定量反应生成CuI 和I 2,硫代硫酸钠标准溶液滴定析出碘而间接计算试样中铜的含量。
反应方程式如下:2Cu 2++4I -=2CuI ↓+I 2I 2+2S 2O 3-2=2I -+S 4O 6-由于CuI 沉淀表面会吸附游离I 2影响滴定终点判断,会影响准确度故在接近化学计量点时,加入少量KSCN ,使CuI 沉淀转变成溶解度更低的CuSCN ,(Ksp ,CuI=1.1×10-10,Ksp ,CuSCN=1.1×10-14)使被吸附的I 2从沉淀表面置换出来。
CuI+SCN -=CuSCN ↓+I -对分析而言,碘量法的分析原理是毫无争议的,但在分析过程中经常出现分析结果偏离预期的情况,如何对该分析方法的准确运用成为当今的研究方向。
文中主要探讨了分析过程中各干扰因素对铜分析结果的影响及消除方法。
根据淀粉与碘反应机理和吸附作用,文章认为可以在滴定至浅黄色刚好消失时加入淀粉,这是与国标法不一致的地方。
1试样的分解在试样分解过程中,样品发生跳溅、样品分解不充分,均会对分析结果造成影响。
试样分解过程中分析人员不能离开样品,不时观察样品,若发现样品发生跳溅,及时移至低温电炉。
分解试样在发烟之前试样不要完全蒸干,对于分解不完全的样品应根据情况选择合适的试剂进行再分解,直到样品分解完全。
WLTILECL-WI-01-06HA 铜及铜合金中锡含量的测定检测实施细则.

一、检测依据:GB/T5121.10-2008《铜及铜合金化学分析方法第10部分:锡含量的测定》二、检测前的准备:1、对样品状况及有效性进行检查,对被测样品进行分组、编号。
2、对仪器设备正常性和环境条件的适用性进行检查。
在检测前检查各仪器设备是否处于正常工作状态,对仪器设备使用记录本上应进行检测前记录,对在使用过程中仪器设备出现的故障及异常情况也要进行详细的笔记。
三、在检测过程中发生异常现象的处理办法:在检测过程中,若发现被测样品损坏或出现首次测量超差,检测结果离散性太大等异常情况,应立即对所用试剂、仪器及操作方法、环境条件进行检查,找出原因重新对该样品进行检测。
四、在检测过程中发生意外事故的处理办法:1、在检测过程中若发生停电、停气、停水或其他非人力可避免的自然灾害,应检查这种情况对检测结果的影响,若无影响,则在恢复正常后继续测试,若有影响,则需重新进行样品制备测试。
2、检测过程中,若检测仪器设备发生意外损坏,则应在对仪器设备进行修理检定后重新对样品进行测试。
五、检测结束后的工作检测结果后应对被测样品有效性进行检查,对样品状况进行描述,对仪器设备正常性进行检查,同时进行台面清理工作。
六、最短工作日:本项产品检测的最短工作日为十天。
七、实施细则:1. 范围本方法规定了铜及铜合金中锡含量的测定。
本方法适用于铜及铜合金中的锡含量的测定。
测定范围:>0.50%~10.00%。
2.试样制备在送检样品中任取样品,制备成厚度不大于1mm的碎屑,试样严格按GB/T5121.10-2008《铜及铜合金化学分析方法第10部分:锡含量的测定》中表4进行称取试样精确至0.0001g。
试料量、酸量用量和标准滴定溶液浓度如下表1:表1 试料量、酸量用量和标准滴定溶液浓度3.仪器设备与试剂3.1试剂除非另有说明,在分析中仅适用确认为分析纯的试剂和蒸馏水或去离子水或相当纯度的水。
碳酸钙、过氧化氢(ρ1.10g/mL)、盐酸(1+1)、氨水(1+1)、三氯化铁(FeCl3•6H2O)溶液(10g/L)、氯化汞溶液(5g/L)、次磷酸钠(NaH3PO3•H2O)溶液(614g/L)、硫氰酸胺溶液(500g/L)、碘化钾溶液(100g/L)、碳酸氢钠饱和溶液。
碘量法测定铜的含量

碘量法测定铜的含量一、实验目的1、掌握铜矿石的溶样方法;2、掌握碘量法测定铜的方法。
二、实验原理试料经盐酸、硝酸分解后,用乙酸氨溶液调节溶液PH值为3.0~4.0,用氟化氢铵掩蔽铁,加入碘化钾与二价铜作用,析出的碘以淀粉为指示剂,用硫代硫酸钠标准溶液滴定。
三、试剂1.碘化钾2.铜片(≥99.99%):将铜片放入微沸的冰乙酸(P=1.05g/mL)中,微沸1min,取出后用水和无水乙酸分别冲洗二次以上,在100℃烘箱中烘4min。
冷却,置于磨口瓶中备用。
3.溴水4.氟化氢铵5.盐酸(P=1.19g/ml)6.硝酸(P=1.42g/ml)7.硫酸(P=1.84g/ml)8.高氯酸(P=1.67g/ml)9.冰乙酸(P=1.05g/ml)10.硝酸(1+1)11.氟化氢铵饱和溶液(贮存于聚乙烯瓶中)12.乙酸铵溶液(300g/L):称取90g乙酸铵,置于400ml烧杯中,加入150ml水和100ml冰乙酸,溶解后,用水稀释至300ml,混匀,此溶液PH值为5;13.硫氰酸钾溶液(40%):称取4g硫氰酸钾于400ml烧杯中,加100ml水溶解后(PH<7),加入2g碘化钾溶解后,加入2ml淀粉溶液,滴加碘溶液(0.04mol/L)至刚好呈蓝色,再用硫代硫酸钠标准溶液滴至蓝色刚好消失。
14.淀粉溶液(1%):称取1g可溶性淀粉,用少量水调成糊状,再用刚煮沸的水稀释至100ml,再加热煮沸,冷却后转入试剂瓶中。
15.三氯化铁(100g/L)16.铜标准溶液:称取1.000g铜片,置于500ml锥形烧杯中,缓慢加入40ml硝酸(1+1)盖上表面皿,低温加热使其完全溶解,取下,用水洗表面皿及杯壁,冷却至室温。
将溶液移入500ml容量瓶中,用水洗涤烧杯,洗液并入容量瓶中,用水稀释至刻度,混匀。
此溶液1ml含2.0mg铜。
17.硫代硫酸钠标准溶液⑴制备称取100g硫代硫酸钠置于1000ml烧杯中,加入500ml无水碳酸钠(4g/L)溶液,移入10L棕色试剂瓶中,用煮沸并冷却的蒸馏水稀释至约10L,加入10ml三氯甲烷,静止两周,使用时过滤,补加1ml三氯甲烷。
氨水二次分离-碘量法测定铜锡钛合金中的铜含量

氨水二次分离⁃碘量法测定铜锡钛合金中的铜含量①庞文林(湖南有色金属研究院,湖南长沙410100)摘㊀要:为测定铜锡钛合金中的铜含量,采用盐酸⁃硝酸⁃过氧化氢溶解该合金,在氯化铵存在时,以铁盐作载体,用氨水沉淀分离锡和钛等元素,经二次沉淀分离消除沉淀对铜的吸附作用;蒸发除铵㊁醋酸酸化,在pH=3.5 4.0时铜被碘化钾定量还原,释放出当量之碘,用硫代硫酸钠标准溶液滴定㊂加入标准溶液后铜回收率在97.05% 102.60%之间,标准偏差在0.5%以内,此方法准确可靠,干扰少,重现性好,可用于实际样品的分析检测,对实际分析工作有指导作用㊂关键词:铜锡钛合金;氨水二次分离;硫代硫酸钠;碘量法;铜;锡;钛中图分类号:O655文献标识码:Adoi:10.3969/j.issn.0253-6099.2018.05.031文章编号:0253-6099(2018)05-0119-03DeterminationofCopperContentinCu⁃Sn⁃TiAlloybyMethodofSecondaryAmmoniumHydroxideSeparationandIodimetryPANGWen⁃lin(HunanResearchInstituteofNonferrousMetals,Changsha410100,Hunan,China)Abstract:Cu⁃Sn⁃Tialloywasdissolvedinamixtureofhydrochloricacid,nitricacidandhydrogenperoxidefordeterminingtheCucontenttherein.Inthepresenceofammoniumchlorideandwithironsaltsasthecarrier,mostoftinandtitaniumwerefirstlyseparatedbyprecipitationwithammoniumhydroxide.Then,secondaryseparationbyprecipitationwasadoptedforeliminationofcopperadsorption.AmmoniawaseliminatedbyevaporationandaceticacidwasusedtoregulatepHvaluetotherangeof3.5 4.0.Thecopperwasthenreducedbypotassiumiodideandanequivalentofiodinewasreleased,whichwastitratedwithsodiumthiosulfatestandardsolution.ItisshownthattheCurecoverywaswithintherangeof97.05% 102.60%,withthestandardvariancelessthan0.5%.Itisconcludedthatsuchmethodpresentedinthispaperisaccurateandreliablewithlessinterferenceandgoodreproducibility,whichcanbeadoptedintheactualsampleanalysisandmeasurement.Keywords:Cu⁃Sn⁃Tialloy;secondaryseparationwithammoniumhydroxide;sodiumhyposulfite;iodimetry;Cu;Sn;Ti㊀㊀铜锡钛合金是生产铜锡钛焊粉的主要原料,精确控制铜锡钛含量对生产高性能焊粉至关重要㊂铜的测定方法有滴定法[1]㊁电化学分析法[1]㊁吸光光度法[2]㊁原子吸收光谱法[3]和原子发射光谱法等[4]㊂高含量的铜须采用滴定法测定,常用的滴定法有碘量法[5]和EDTA络合滴定法[6],其中碘量法的选择性优于EDTA络合滴定法㊂铜锡钛焊粉中的铜含量比较高(约55%),适合用滴定法测定㊂本文以盐酸⁃硝酸⁃过氧化氢体系溶解样品,采用氢氧化物共沉淀法分离杂质,经二次沉淀分离消除氢氧化物沉淀对铜吸附的影响㊂1㊀实验原料及方法1.1㊀试㊀剂1)铜标准溶液(2mg/mL):准确称取纯金属铜(99.99%)1.0000g于250mL烧杯中,加入1+1硝酸20mL,低温溶解㊂然后加热浓缩至5mL,加入1+1硫酸30mL,加热至冒浓烟,冷却,吹入少量水,再冒浓烟㊂冷却,加入100mL水,加热溶解盐类,冷却,移入500mL容量瓶中,以水稀释至刻度,摇匀,备用㊂2)硫代硫酸钠标准溶液(0.04mol/L):称取100g硫代硫酸钠(Na2S2O3㊃5H2O)溶于预先煮沸冷却的水中,加无水碳酸钠2g,移入10L棕色试剂瓶中㊂用同样煮沸冷却的水稀释至10L,摇匀㊂于暗处静置一周后标定㊂标定:吸取50.00mL铜标准溶液置于250mL锥形烧杯中,加氯化铵4 5g,滴加1+1氨水中和至铜铵络离子的蓝色出现,加冰醋酸至蓝色消失,并过量5mL,加碘化钾2 3g,轻轻摇动后,迅速以硫代硫酸钠标准溶液滴定至黄色变浅,加入0.5%淀粉①收稿日期:2018-04-07作者简介:庞文林(1964-),男,湖南长沙人,工程师,主要从事有色冶金分析检测工作㊂第38卷第5期2018年10月矿㊀冶㊀工㊀程MININGANDMETALLURGICALENGINEERINGVol.38ɴ5October2018溶液5mL,继续滴定快到终点时,加入25%硫氰酸钾溶液3mL,激烈摇动至蓝色加深,再滴定至蓝色恰好消失为终点㊂按下式计算硫代硫酸钠准溶液对铜的滴定度:f=ρV11000ˑV2(1)式中f为与1.00mL硫代硫酸钠标准溶液相当的以克表示的铜质量,g/mL;ρ为铜标准溶液浓度,mg/mL;V1为铜标准溶液体积,mL;V2为所消耗硫代硫酸钠标准溶液体积,mL㊂3)淀粉溶液(0.5%):称取0.5g可溶性淀粉置于200mL烧杯中,用少量水调成糊状,将100mL沸水徐徐倒入其中,继续煮沸至透明,取下冷却㊂现用现配㊂4)硫氰酸钾溶液(25%):称取25g硫氰酸钾置于300mL烧杯中,加入100mL水溶解(pH<7),加入2g碘化钾,待溶后,加入2mL淀粉溶液,滴加碘溶液(0.04mol/L)至刚好呈蓝色,再用硫代硫酸钠标准溶液滴定至蓝色刚好消失㊂5)氯化铁溶液:称取48g氯化铁(FeCl3㊃6H2O)于25mL烧杯中,加少量盐酸及水溶解后,以水稀释至500mL,铁浓度20mg/mL㊂盐酸㊁硝酸㊁硫酸㊁过氧化氢㊁冰醋酸㊁氯化铵㊁碘化钾㊁碳酸钠等试剂均为分析纯试剂;实验用水为蒸馏水㊁去离子水或相当纯度的水㊂1.2㊀铜锡钛合金粉主要成分铜锡钛合金粉主要成分见表1㊂表1㊀铜锡钛合金粉主要成分(质量分数)/%铜锡钛铝砷铋铅铁镍镉锰5515170.10.010.050.10.10.10.10.011.3㊀实验方法称取0.2g试样于250mL烧杯中,加入15mL盐酸㊁5mL硝酸㊁1mL双氧水,盖上表面皿,低温加热溶解试样㊂吹水洗表面皿,低温蒸至近干,加10mL盐酸,再低温蒸至近干㊂取下加水40mL,微热使盐类溶解,加氯化铵5g㊁氯化铁溶液2mL(相当于铁40mg),用氨水中和至沉淀完全并过量20mL,加热煮沸1min,取下补加5mL氨水,放置30min㊂过滤于300mL锥形烧杯中,以5%氨水⁃氯化铵洗液洗涤烧杯和沉淀各3次,滤液保留㊂沉淀用洗液洗入原烧杯中,用热水洗净滤纸,加10mL盐酸(1+1)微热溶解沉淀,加热溶解后,加水至30mL,用氨水中和至沉淀完全并过量10mL,加热煮沸1min,取下补加5mL氨水,放置30min㊂取下,经原滤纸过滤于原承接滤液的烧杯中,涤液洗涤烧杯和沉淀各3 4次㊂将滤液浓缩至30mL,加冰醋酸5mL,煮沸2min,冷却㊂沿杯壁加入少量水,加碘化钾2 3g,轻轻摇动后,迅速以硫代硫酸钠标准溶液滴定至黄色变浅,加入0.5%淀粉溶液5mL,继续滴定快到终点时,加入25%硫氰酸钾溶液3mL,激烈摇动至蓝色加深,再滴定至蓝色恰好消失为终点㊂1.4㊀铜含量计算方法铜含量wCu按下式计算:wCu=fV3mˑ100%(2)式中V3为滴定时消耗硫代硫酸钠标准溶液的体积,mL;m为试样量,g㊂2㊀实验结果讨论2.1㊀溶样酸的选择试验采用单一的盐酸溶解铜锡钛合金粉,结果样品溶解速度缓慢,大部分样品不溶解㊂采用单一的硝酸溶解样品,样品中的锡水解,产生偏锡酸盐包裹样品,样品同样溶解不完全㊂采用盐酸⁃硝酸⁃双氧水低温溶解样品,溶样速度快,只需几分钟样品就溶解完全,溶液清亮㊂2.2㊀氢氧化铁沉淀对铜吸附的影响铜钛锡合金粉中的锡㊁钛对铜的测定有干扰,锡和钛在低酸度情况下均会水解而包裹铜,使滴定终点不明显㊂在含有铵盐的氨性溶液中,以铁盐为载体共沉淀锡㊁钛,可以消除锡㊁钛和其他杂质对铜测定的影响㊂氢氧化物共沉淀负载锡和钛消除铁㊂按实验方法进行,取铜标准溶液120.00mg,采取补加不同量的铁,研究了氢氧化铁沉淀对铜吸附的影响,结果见表2㊂表2㊀铁加入量对铜回收的影响铁加入量mg铜测定值/mg一次过滤二次过滤0119.24119.9810118.64119.9620118.09119.9530117.98120.0840117.82119.83实验证明,一次过滤,氢氧化铁沉淀对铜有一定的吸附,且吸附作用随着铁加入量增加而越发明显㊂二次沉淀分离时,氢氧化铁沉淀对铜的吸附量很少,对铜的吸附影响可以忽略不计㊂2.3㊀氢氧化铁沉淀对锡和钛共沉淀的作用在含有铵盐的溶液中,以铁盐为载体共沉淀锡㊁钛的过程中,补加的铁盐太多,生成的氢氧化铁沉淀量太021矿㊀冶㊀工㊀程第38卷大,对铜的吸附作用增强造成铜的损失;补加的铁盐太少,不能完全负载样品中的锡和钛,使其进入滤液中,从而干扰铜的测定㊂按照实验方法,取铜标准溶液120.00mg,各加入锡标准溶液40mg㊁钛标准溶液40mg㊂采取补加不同量的铁,将两次过滤的滤液合并用盐酸酸化,经ICP⁃AES测定滤液中残留的锡和钛的含量,同时二次沉淀后的滤渣用盐酸溶解,经ICP⁃AES测定吸附的铜量,结果见表3㊂表3㊀铁加入量对锡㊁钛分离效果的影响铁加入量/mg滤液残留锡量/mg滤液残留钛量/mg滤渣吸附铜量/mg03.851.250.02101.210.270.04200.820.00130.05300.0110.0010.01400.0090.00080.06实验表明,当加入的铁量为40mg时,氢氧化铁沉淀基本能够负载绝大部分的钛㊁锡,且对铜基本没有吸附作用,对测定结果不产生干扰㊂本实验选择的铁补加量为40mg㊂2.4㊀混合干扰元素对铜测定的影响铜锡钛合金中除了绝大部分的铜㊁锡和钛金属外,还含有少量的铝㊁砷㊁铋㊁铅㊁铁㊁镍㊁镉㊁锰等杂质元素㊂铅㊁铁㊁铝在氨性溶液中可形成沉淀而被过滤除去㊂极少量的砷㊁锑等不干扰测定,残留的极少部分锡和钛不干扰铜的测定㊂2.5㊀样品加标回收实验为考察方法的稳定性,对2个铜锡钛合金粉样品进行了加入标准溶液的回收实验,结果见表4㊂表4㊀样品加标回收实验结果样品编号样品中铜含量/mg标准溶液中铜含量/mg测定值/mg回收率/%1108.8210.00118.6398.1020.00128.98100.802112.9610.00123.22102.6020.00132.3797.05㊀㊀从表4可以看出,加入标准溶液后铜回收率在97.05% 102.60%之间,满足实际样品的分析检测要求㊂2.6㊀精密度实验按照实验方法,随机抽取3个铜锡钛合金粉样品连续6次重复测定,以验证精密度,结果见表5㊂表5㊀精密度实验数据样品编号铜含量/%123456平均值标准偏差/%1#56.7856.4957.0856.9056.8756.4356.760.252#58.2158.7358.5657.8958.4758.8758.460.363#61.9862.2061.6461.3762.0861.7761.840.31从表5数据可知,实验标准偏差在0.5%以内,可以满足测定要求㊂3㊀结㊀㊀论采用盐酸⁃硝酸⁃过氧化氢体系溶解样品,氢氧化物共沉淀法分离杂质,经二次沉淀分离消除氢氧化物沉淀对铜吸附的影响;蒸发除铵㊁醋酸酸化,在pH=3.5 4.0时铜被碘化钾定量还原,释放出当量之碘,用硫代硫酸钠标准溶液滴定㊂此方法干扰少,重现性好,结果准确稳定,可以用于实际样品的分析检测以及现场产品检验㊂参考文献:[1]㊀栾日坚,张㊀珂,马㊀明,等.电位滴定分析方法在地质样品主量元素检测中的应用[J].中国无机分析化学,2017,7(1):22-27.[2]㊀常㊀芳,李利群,陈海清.吸光光度法测定电解锌粉的电解液中铜[J].理化检验(化学分册),2005,41(4):271-273.[3]㊀张卫卫.基于火焰原子吸收法实现多金属矿中铅锌铜的测定[J].世界有色金属,2016(23):56-57.[4]㊀范丽新,王㊀杰.电感耦合等离子体原子发射光谱法(ICP⁃AES)测定铜磁铁矿中Al,Ni,Cu,Mg,Pb,Zn6种元素[J].中国无机分析化学,2015,5(1):53-55.[5]㊀王㊀成,肖丽梅,葛钰玮.碘量法测定铜锍及含铜烧结物料中铜[J].冶金分析,2011,31(1):62-65.[6]㊀刘和连,许㊀方,黄海平.EDTA络合滴定法测定黄铜中铜和锌[J].冶金分析,2015,35(5):70-73.引用本文:庞文林.氨水二次分离⁃碘量法测定铜锡钛合金中的铜含量[J].矿冶工程,2018,38(5):119-121.121第5期庞文林:氨水二次分离⁃碘量法测定铜锡钛合金中的铜含量。
碘量法测定铜

铜的测定——碘量法
1.方法要点:试样以盐酸—过氧化氢溶解,在磷酸溶液中,碘化钾与铜生成Cu2I2并析出定量的碘,以硫代硫酸钠标准滴定溶液滴定。
2.主要反应:2Cu2++4I-= Cu2I2↓+I2 I2+2S2O32-=S4O62-+2I-
Cu2I2+2SCN-= Cu2(SCN)2↓+2I-
3.试剂:盐酸溶液(1+1);氨水(1+1);30%过氧化氢;磷酸;碘化钾;淀粉溶液;硫氰酸钠溶液(100g/L);硫代硫酸钠标准滴定溶液(0.1mol/L)。
4.分析步骤:称取0.2000g试样于500mL锥形瓶中,加入5mL盐酸溶液,5mL过氧化氢溶液,加热溶解并煮沸2-3min。
冷却,加30ml水,用氨水溶液中和至有氢氧化铜出现,滴加磷酸至沉淀恰好溶解并过量5mL,冷却至室温。
加入2g碘化钾,稍摇动。
加入100mL 水,立即用硫代硫酸钠标准滴定溶液滴定至浅黄色时,加2-3mL淀粉溶液,继续滴至蓝色消失,再加10mL硫氰酸钠溶液,继续滴至蓝色恰好消失为终点。
5.计算:C*V⨯0.06355
ω(Cu)=—————————⨯100%
M
式中:C——硫代硫酸钠溶液的物质的量浓度
V——消耗硫代硫酸钠溶液的体积
M——称取试样的质量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
运用碘量法测定铜精矿中的锡
摘要:文章分析碘量法应用在铜精矿内锡的测定试验中,简述试验过程,并讨论样本分解、分离铜元素以及碘量法可用性等方面的内容。
最终判断此方法具备可用性。
关键词:碘量法;锡;铜
引言:使用碘量法检测铜精矿内锡含量时,铜元素影响是比较受重视的问题,其影响状况复杂,干扰程度也有差异。
对此,曾推出混合掩蔽铜的处理方式,但存在明显的局限性,测定结果不佳。
为保障测定效率与准确性,对碘量法的应用效果进行检验。
一、碘量法测定锡试验过程
(一)试验准备
此类试验的主要试剂包含:一是锌粉,纯度达到工业级别,粒度小于。
二是铝粒,其质量分数达到以上。
三是洗液,溶液试剂内,每升含有
氨水以及氯化铵。
四是锡标准液,含量为。
精确称量,质量分数同样超过,放在规格为的烧杯容器内,添加的盐酸以及的清水,加热到全部溶解,自然冷却到室温状态。
吹洗表皿后,放到
的容量瓶内,进行稀释定容,混合均匀。
五是淀粉,称量淀粉,放在
烧杯内,添加的清水,直至混合成浆状。
搅拌中,添加的氢氧化钠溶液,浓度含量为。
静置至少五分钟后,添加碘化钾,进行混合溶解,用水进行稀释,定容至,混合均匀。
六是碘酸钾标准滴定溶液,其
,称量的碘酸钾以及的无水碳酸钠,一同放置在烧杯内,添加的清水,进行加热拌和,直到全部溶解后,添加
碘化钾,继续搅拌溶解处理。
自然冷却后,添加清水进行稀释,定容到,混合均匀。
标定过程为:称取的锡标准溶液,放入的锥形容量瓶内,添加的还原铁粉以及清水、的盐酸,保持低温加热状态,直到全部溶解后,加铝前加。
构建二氧化碳的气流屏障,流水下稍冷,关闭二氧化碳,添加铝粒,轻晃容量瓶,确保大多数铝粒被溶解后,进行加热处理,直到煮沸,消除其中的气泡。
受到二氧化碳气体的保护,逐渐冷却到室温状态后,暂停补充二氧化碳,取下容量瓶。
添加淀粉,基于碘酸钾标准,进行滴定检测,直到呈现浅蓝色为止。
而后开展空白试验。
(二)试验方法
称取锡与铜,放在烧杯内,添加三氯化铁与高锰酸钾、硝酸,进行加热处理,直到。
自然冷却,清水冲洗器皿及杯壁,直至。
滴入氨水,直到形成红色的胶状沉淀物,过量。
放置半个小时后,使用中速滤纸处理,使用洗液,连续洗涤次,把淀粉和滤纸同时去除,放置在规格的瓷坩埚上进行烘干及灰化处理,自然冷却。
添加锌粉,混合均匀后,添加氢氧化钠以及锌粉、氯化钠,放置在马弗炉上,保持一刻钟的时间。
移出瓷坩埚,自然冷却。
把瓷坩埚转移到事先添加还原铁粉以及盐酸的容量瓶内,接上还原设备,进行低温加热,直至全部溶解。
连接气流保护,稍冷后停止通,添加铝粉,持续摇晃容量瓶,直到大多数铝粒被溶解,进行低温加热,直到铝粒全部溶解。
连接气流保护,放置在冷却水内进行冷却。
关上气体,移出锥形容量瓶,添加淀粉,进行碘酸钾滴定,直到表现出浅蓝色[1]。
随同完成空白试验。
二、碘量法测定锡试验结果
(一)试验条件的影响
其一,氨水添加量对试验结果的影响。
提取锡与铜,放置在容量瓶内,根据上述试验方式,变量为“氨水过量”,单位是,得到的测量结果为:变量是0时,测定锡含量是,外在现象是有轻微褪色的情况。
其他变量条件下,变量为,锡含量为;变量为,锡含量
是;变量为,对应锡含量是;变量为,锡含量是。
这四种的试验表现均是稳定状态。
由此可判断,在滴入氨水,直到形成红色胶状的沉淀物,锡测量结果相对较低,而且滤液内铜离子是,表示测定物质内有为铜离子,会干扰测定结果。
但在氨水过量处于区间时,都能保障测定准确性,本次试验选择过量值是。
其二,铜离子。
提取锡与不确定量铜放入容量瓶内,共进行四组试验,铜添加量分别是,锡添加量不变。
氨水分离铜,测出的锡含量各自对应、、、;不分离铜的情况下,测定出的锡含量分别为:、、、。
由此能看出,在铜含量不足的试验条件下,不会干扰到测定结果,但其超过,便会产生干扰,而且在铜添加量不断上升的过程,干扰程度随之明显,导致测定结果不确定。
经过氨水分离处理后,能获得较为正常的测定结果。
其三,铜分离程度。
称取锡与铜放入的容量瓶内,根据试验设定,通过滤液经控制值,使用硫,代替硫酸钠溶液,完成测定铜含量的任务。
进行三组试验,在滤液内测定出的铜含量分别为、、,除铜率各自对应、、。
通过上述试验数据来看,样本通过分离处理后,除铜率均能超过,而且样本内铜含量不足,不会对锡测定结果产生干扰。
其四,锡回收率。
锡含量作为变量,与铜放入容量瓶内,进行试验测定,记录锡回收率。
试验中,锡添加量分别为、、、、以及;测定锡含量为、、、、、;对应回收率为、、、、、。
根据上述试验结果来看,在锡含量不足的试验条件下,测定结果相对较少。
在锡含量超过
后,测定结果比较稳定。
继而表示碘量法能较为准确地测出铜精矿内锡超过
的样本[2]。
(二)共存离子的影响
铜精矿样本中,溶液的锡、铁以及锰、铋元素,都能通过氨水实现沉淀,因而选择分别观察各元素对锡测定结果的干扰情况。
提取锡的标准溶液,放入烧杯内,添加三氯化铁,分别放入锰和铋。
经过试验结果对比分析,在锰含量为锡的倍,以及铋为锡的倍情况下,不会给锡测定结果造成干扰,而且回收率能保持在区间内,确保回收效果。
(三)样本分析
提取样本放入规格烧杯内,适当添加清水进行润湿,按照上述的试验方法,进行测定试验。
一方面,试验方式精密度。
结果现实,碘量法的测定标准偏差是,符合试验要求。
另一方面,试验方式准确度。
采用本试验方式和铍载分离,进行样本测试,偏差在以内,说明结果准确。
结束语:碘量法和铍载分离对比来看,其一,后者能实现完全分离,前者仅能做到局部分离,但在溶液值处于区间内,便可以保持基本分离效果,对最后测定结果无干扰。
其二,碘量法的分析速度更快,而且拥有环保的特性。
总之,碘量法值得推广应用。
参考文献:
[1]涂满娣,戴金兰,刘德峰,等.均值-标准差质量控制图用于短碘量法测定进口铜精矿中铜含量的应用[J].福建分析测试,2021,(01):51-53+58.
[2]颜立新,刘金优,冯晓青,等.铜精矿中铜的电解重量法测定及其与碘量法测定的比较[J].中国无机分析化学,2019,(04):31-35.。
