仿制药详细研发流程
仿制药研发流程解析

仿制药研发流程解析仿制药指的是通过对已经上市的原研药进行研究复制,具有与原研药相同的活性成分、药理作用、适应症和剂型等相似特征的药物。
仿制药的研发流程相对复杂,包含多个环节和步骤。
以下是一个对仿制药研发流程进行解析的详细说明。
第一阶段:研究规划和确定1.研究目标确定:选定要研发的原研药,根据国内药物市场和竞争现状,制定相关研究目标。
2.研究规划:制定详细的研究计划,包括研究方法、时间、费用等。
3.资源配置:确定研究所需的各种资源,包括研究团队、实验设备、药物原料等。
第二阶段:文献研究和药物获取1.文献研究:对与原研药相关的文献进行深入研究,了解其药理作用、化学结构、药代动力学等相关信息。
2.药物获取:获得原研药,可以通过购买、委托生产等方式获得。
第三阶段:质量与一致性研究1.质量研究:对原研药进行质量研究,包括物理性质、化学性质、纯度等方面的测试,确保仿制药的质量符合要求。
2.一致性研究:通过对原研药和仿制药的比较研究,验证仿制药与原研药在药效、生物等方面的一致性。
第四阶段:制剂开发1.剂型选择:根据原研药的剂型和市场需求,确定仿制药的剂型。
2.成分选择和配方设计:根据原研药的成分和配方,设计仿制药的成分和配方。
3.制剂工艺开发:根据设计的配方,开发制剂工艺,包括原料的加工、配方的配制、制剂的制备等。
4.质量控制:制定质量控制标准,确保仿制药的质量符合要求。
第五阶段:临床试验1.申报临床试验:根据国家药物监管机构的规定,申报临床试验。
2.临床试验设计:设计临床试验方案,包括试验目标、试验方法、样本大小等。
3.招募试验对象:根据试验方案,招募符合条件的试验对象。
4.临床试验实施:按照临床试验方案,进行试验药物的给药和治疗,并记录试验数据。
5.临床试验数据分析:对试验数据进行统计分析,评估仿制药的疗效和安全性。
第六阶段:申报和审批1.申报荷尔蒙研究和申报药品注册:根据临床试验结果,编写荷尔蒙研究报告和药品注册申请,并提交给国家药物监管机构进行审批。
仿制药研发流程

仿制药研发流程仿制药(generic drugs)是指在原创药物(brand-name drugs)专利保护期过后,其他企业根据原创药物的化学结构和制造工艺开发出来的药物。
仿制药的研发流程通常包括以下几个步骤。
第一步是购买原创药物的专利权。
仿制药企业首先需要购买原创药物的专利权,才能合法地开展仿制药的研发工作。
这是仿制药研发的第一步,也是最基础的一步。
第二步是进行文献调研。
仿制药企业需要对原创药物的相关文献进行深入研究,了解原创药物的化学成分、制造工艺、药效等方面的信息。
通过文献调研,仿制药企业可以对仿制药的研发方向和重点进行确定。
第三步是进行药物分析和铺路工作。
仿制药企业需要对原创药物进行药物分析,确定其化学结构和药物特性。
同时还要进行工艺开发和试验研究,确定仿制药的制造工艺和生产条件。
这一步骤是仿制药研发的关键性步骤,需要耗费大量的时间和精力。
第四步是进行仿制药的临床试验。
仿制药企业需要提交临床试验申请,并按照相关的法规和规定进行试验。
临床试验阶段包括药物的安全性和有效性试验,需要各种类型的临床试验数据来支持仿制药的上市申请。
第五步是申请仿制药的上市许可。
仿制药企业需要提交仿制药的上市申请,包括药物的临床试验数据、质量控制和生产工艺等信息。
申请通过后,仿制药企业就可以合法地生产和销售仿制药。
第六步是生产和销售仿制药。
仿制药企业在获得上市许可后,就可以开始生产和销售仿制药。
企业需要建立完善的生产和质量控制体系,确保仿制药的质量稳定和安全有效。
仿制药的研发流程比较复杂,需要企业在技术、法规和市场等多个方面进行充分的考虑和准备。
在研发过程中,企业需要投入大量的人力、物力和资金,同时还要面对法律法规的严格监管和市场竞争的压力。
但是,仿制药的研发也有其优势,例如可借鉴原创药物的临床试验数据和药物研发经验,缩短研发周期和降低研发成本,提供更多的选择和降低药物价格。
总的来说,仿制药的研发流程包括购买专利权、文献调研、药物分析和铺路工作、临床试验、上市许可申请以及生产和销售等步骤。
仿制药详细研发流程
3)工艺研究:是否微粉化,制粒是干法、湿法、直接压片、包衣目的等
4)方法
常规方法:重量、水分测定、HPLC等
仪器分析:X-光衍射、扫描电镜
四
处方工艺研究
工艺参数研究
1、处方工艺摸索:
1)辅料相容性试验
2)处方筛选
3)工艺参数研究
2、小试验证三批
1)固体口服制剂可用A01、A02.....
2)液体口服可用B01、B02.........
3)注射剂可用C01、C02...........
4)医疗器械可用D01、D02....等)
1)三批重现性样品
2)验证工艺
3、初试一批
1)样品全检
2)工艺参数验证
4、中试三批
1)三批全检
2)用于稳定性考察
5、注册三批(BE)
五
质量研究1Leabharlann 质量研究方法的确定(初试、中试样品)
2、质量标准的方法学验证
1)质量标准的初步验证(对照品、杂质、原料、参比、小试)
2)系统的方法学验证(初试、中试样品)
1、综述资料
2、药学研究资料
3、药理毒理研究资料
4、BE试验资料
九
向省局提交注册申请
1、省局形式审查
2、省局现场核查(研制现场、生产现场、临床试验现场)
十
资料移交总局
2、总局审评中心审评
2、总局审评过程或有因的核查和抽样检验
十一
完整性审评
1、补充后续稳定性资料
2、完整性通过
十二
批准上市
1、售后
说明:
1、原辅料检验(原料研究溶解性、晶型、粒径、水合物、
仿制药研发流程范文

仿制药研发流程范文第一步:确定仿制药的目标和研发策略。
在仿制药的研发过程中,首先需要明确确定仿制药的目标,即要仿制的原研药物,同时要确定研发的策略,包括选定合适的仿制药的技术路线、合理安排研发计划等。
第二步:进行原研药物的分析与评价。
在确定了仿制药的目标之后,需要对原研药物进行全面的分析与评价。
这包括对原研药物的药效学、药代动力学、药物相互作用等进行研究,了解原研药物的药理学特性和临床疗效。
第三步:建立仿制药物的质量标准。
在研发仿制药物之前,需要建立仿制药物的质量标准。
这包括制定合适的质量控制方法、建立合理的质量标准体系等。
同时还需要进行原研药物的样品收集和分析,以便进行仿制药物的比较研究。
第五步:进行仿制药物的生产和临床试验。
在经过前面几个步骤的研究之后,需要进行仿制药物的生产和临床试验。
生产过程包括药物原料的采购和加工、药品生产的工艺流程的优化等。
临床试验阶段,需要进行药物在人体内的安全性和有效性的评价。
第六步:仿制药物的注册和上市。
当仿制药物通过临床试验,并获得相关数据支持时,可以提交注册材料,并经过相关部门的审查和批准,最终获得仿制药物的注册证书。
之后,该仿制药物可以上市销售。
第七步:仿制药物的监管和维护。
在仿制药物上市后,相关部门将对其进行监管,对其质量和安全性进行抽检。
同时,还需要进行仿制药物的生产和质量管理,确保其质量和安全性的稳定。
总结起来,仿制药研发流程包括确定研发目标和策略、原药物分析与评价、制定质量标准、制剂开发、生产和临床试验、注册和上市等步骤。
其中,每一个步骤都需要严格的研究和规范操作,以确保仿制药物的质量和安全性。
仿制药研发具体流程

仿制药研发具体流程随着新药研发难度的加大及研发成本的不断上涨,仿制药逐渐成为制药企业的新宠。
仿制药研发相比新药研发,其流程较为简单,成本也相对较低,因此受到了市场的青睐。
本文将从仿制药研发的起步阶段、流程、仿制药上市销售以及质量控制等方面对其展开分析。
1、仿制药研发的起步阶段仿制药研发的起端就是现有药物的信息源。
首先,研发人员需要对原研药进行充分的了解,包括其化学分子结构、药理学特性、临床应用疗效、副作用及安全风险等,这些信息的获取可以通过查阅文献、产品说明书、专利等方式得到,并对其进行分析和评估。
根据得到的信息,设计出仿制药的研究方案和定位,包括药物的分子结构设计、制品制备、药效实验、原料药的纯化和标准化等。
2、仿制药研发流程(1)药物开发方案的制定在得到原研药的信息后,仿制药研发的下一步就是制定药物开发方案。
此时设计方案需要考虑的关键因素就是如何利用现有技术实现唯一和创新的药物分子结构的设计和制备。
方案中通常包括生产的需求量、产品的成本、投资成本、生产工艺和质量标准等方面。
此外,对于仿制药开发,还需要结合当前市场需求以及已有的同类仿制药的研究结果,进行合理的市场分析和定位。
(2)药物分子结构的优化与确定对于仿制药的研制而言,药物分子的结构设计是十分重要的一环。
一般来讲,仿制药的分子结构和原研药是相似的,但不是完全相同,通常会对分子结构进行优化设计以提高其功效或减少不良反应。
对于拥有自主知识产权的原研药而言,仿制药可通过降低药物剂量、改变毒副反应等方面的改进提高其市场竞争力,并推动现有药物技术的发展。
(3)药物质量标准的制定药物质量标准的制定是药品研制的重要一环,这是确保药品质量和安全的基础。
仿制药的质量标准一般可参考原研药,这有利于保持仿制药与原研药的一致性。
此外,在制定质量标准时,需要将临床实践和新技术的发展考虑进去,并结合仿制药的研发目标制定个性化标准。
(4)仿制药临床试验仿制药进入临床试验需要提供大量的生产样品,并对药品进行安全和有效性的严格测试分析以验证研制的仿制药是否具有预期的药效,同时也需要对其不良反应和副作用情况进行监测,以确保患者的安全。
仿制药研发流程范文

仿制药研发流程范文1.市场调研和申请:在决定仿制其中一种药物之前,制药公司会进行市场调研,了解目标市场的需求情况和潜在竞争对手。
在确定了仿制目标后,制药公司需要向药品监管机构提交仿制药药物申报书,并进行注册和批准等法律程序。
2.获取原创药品信息:仿制药的研发需要基于原创药品的研究成果和技术信息,因此制药公司需要通过一些合法渠道获取原创药品的相关技术文献、专利信息、研究报告等。
这些信息对于制定仿制策略和确定研发路径至关重要。
3.仿制策略制定:制药公司需要根据市场需求和原创药品的特点,制定合理的仿制策略。
仿制策略可能包括选择合适的仿制原料和工艺、确定合理的剂量和给药途径、调整制剂类型、改进药物的生物利用度和稳定性等。
4.临床前研究:仿制药需要进行一系列的临床前研究,包括体内和体外的药理学评价、药代动力学研究、毒理学评价等。
这些研究旨在评估仿制药药物的活性、代谢途径、药动学参数和安全性。
5.临床试验:仿制药的临床试验分为三个阶段,即I、II和III期。
在I期临床试验中,会重点评估仿制药药物的安全性和耐受性。
在II期临床试验中,会扩大患者样本量,评估仿制药药物的疗效和安全性。
III 期临床试验是最后一个阶段,是对大规模患者进行的多中心试验,用于评估仿制药在实际使用条件下的疗效和安全性。
6.保密与质量控制:在仿制药研发过程中,保持信息的保密性和数据的完整性非常重要。
制药公司需要建立严格的质量控制系统,确保仿制药的质量满足相关标准和要求。
7.生产与注册:仿制药经过临床试验后,制药公司可以开始规模化生产,并申请药物注册。
注册成功后,仿制药可以正式在市场上销售和推广。
8.后续监测和改进:仿制药上市后,制药公司需要进行后续的监测和改进工作。
他们需要监测仿制药的安全性和疗效,并及时采取措施解决可能出现的问题。
总之,仿制药研发的流程包括市场调研和申请、获取原创药品信息、仿制策略制定、临床前研究、临床试验、保密与质量控制、生产与注册以及后续监测和改进等步骤。
详解仿制药研发具体流程
详解仿制药研发具体流程目录一、珠述二、仿制药研发项目汇总3三、仿制药的研发具体步骤:5(一)产品信息调研(二)前期准备1、参比制剂的采购2、原料采购3、色谱柱及对照品米购4、辅料米购5、包材的米购(三)处方工艺研究1、原辅料及参比制剂的检验2、处方工艺摸索3、初步验证工艺4、中试生产及工艺验证(四)质量研究1、质量研究项目的选择及方法初步确定2、质量标准的方法学验证3、质量对比研究4、质量标准的制定(五)稳定性研究(中试产品)(六)药理蠹理研究(七)申报资料的撰写、整理(八)申报临床及申报现场核查(九)临床研究(+)申报生产一、珠述根据药品注册管理办法附件二的规定,仿制药即是已有国家药品标准的原料药或者制剂,该类药物国已批准生产或上市销售,经过国外广泛使用,其安全性、有效性已经得到较充分证实。
如今的新法规对仿制药提出了新的要求,主要是以下几点:1、规对被仿制药品的选择原则,即参比制剂的选择问题。
2、增加批准前生产现场的检查。
3、按照CTD格式要求提供申报资料,使申报规,统一。
4、强调了对比研究,是判断两者质量是否一致的重要方法之一。
5、强化了工艺验证,目的是确保大生产时能始终如一地按照申报工艺生产出质量包定的产品。
6、提出了晶型的要求,晶型的不同,溶解度和稳定性不同。
分析上述新要求和参考指导原则,从而得出结论:仿制药研发的目的是做到规模化生产,强调本地化,以实现“替代性”。
要做到“同”。
方法为对比研究。
1.安全性“同”:对丁安全性,口服固体制剂控制的主要为有关物质,而液体制剂除控制有关物质外,还需对防腐剂、氧化剂等对人体有影响的物质进行控制。
因此,必须要将防腐剂含量测定定入质量标准。
研究的容:静态上应包括杂质谱的对比,单个杂质的对比,杂质总量的对比。
动态上的对比为影响因素试验、加速试验的对比,即稳定性对比研究。
2.有效性“同”:对丁口服固体制剂,口服混悬剂(包括干混悬剂),溶出曲线是主要的控制指标[1];对丁口服溶液剂,防腐剂、矫味剂、氧化剂、增溶剂及稳定剂的选用非常重要,控制点为口感、渗透压、PH及有无絮凝现象;对丁局部用制剂(如鼻喷雾剂),粒度分布、渗透压及黏度是主要控制指标。
简述仿制药的研发流程
简述仿制药的研发流程简述仿制药的研发流程(1)产品信息调研:1、参比制剂的采购:2、原料采购:3、色谱柱及对照品采购: 4、辅料采购5、包材的采购(2)前期准备:1、原辅料及参比制剂的检验:2、处方工艺摸索3、初步验证工艺4、中试生产及工艺验证(3)处方工艺研究:1、中试批量: 2、中试生产 3、工艺验证(4)质量研究:1、质量研究项目的选择及方法初步确定2、质量标准的方法学验证3、质量对比研究(稳定性研究期间)(5)稳定性研究:1、影响因素试验2、包材相容性试验3、加速试验 4、长期试验5、稳定性研究结果的评价(6)药理毒理研究:1、药理毒理资料进行整理归纳总结2、试验委托(7)申报资料的撰写、整理:1、综述资料2、药学研究资料3、药理毒理研究资料 4、临床试验资料(8)申报现场审核:1、将资料和电子申报表报省局,准备现场核查。
2、动态三批现场工艺核查,抽样送检省药检所复检。
(9)临床研究:1、固体口服制剂做生物等效性2、溶液剂一般可免临床 3、局部用制剂一般需做临床试验(10)申报生产:临床试验完成后,整理资料,申报省局。
试述申报资料撰写要求:申报资料项目:一、综述资料包括:1.药品名称。
2.证明性文件。
3.立题目的与依据。
4.对主要研究结果的总结及评价。
5.药品说明书样稿、起草说明及最新参考文献。
6.包装、标签设计样稿。
二、药学研究资料7.药学研究资料综述。
8.药材来源及鉴定依据。
9.药材生态环境、生长特征、形态描述、栽培或培植(培育)技术、产地加工和炮制方法等。
10.药材标准草案及起草说明,并提供药品标准物质及有关资料。
11.提供植物、矿物标本,植物标本应当包括花、果实、种子等。
12.生产工艺的研究资料、工艺验证资料及文献资料,辅料来源及质量标准。
13.化学成份研究的试验资料及文献资料。
14.质量研究工作的试验资料及文献资料。
15.药品标准草案及起草说明,并提供药品标准物质及有关资料。
详解仿制药研发具体流程
详解仿制药研发具体流程目录一、综述2二、仿制药研发项目汇总3三、仿制药的研发具体步骤:5(一)产品信息调研5(二)前期准备(约一个月完成):51、参比制剂的采购52、原料采购53、色谱柱及对照品采购54、辅料采购:65、包材的采购:6(三)处方工艺研究61、原辅料及参比制剂的检验62、处方工艺摸索63、初步验证工艺84、中试生产及工艺验证8(四)质量研究91、质量研究项目的选择及方法初步确定92、质量标准的方法学验证103、质量对比研究124、质量标准的制定14(五)稳定性研究(中试产品)14(六)药理毒理研究16(七)申报资料的撰写、整理16(八)申报临床及申报现场核查17(九)临床研究17(十)申报生产17一、综述根据药品注册管理办法附件二的规定,仿制药即是已有国家药品标准的原料药或者制剂,该类药物国内已批准生产或上市销售,经过国内外广泛使用,其安全性、有效性已经得到较充分证实。
如今的新法规对仿制药提出了新的要求,主要是以下几点:1、规范对被仿制药品的选择原则,即参比制剂的选择问题。
2、增加批准前生产现场的检查。
3、按照CTD格式要求提供申报资料,使申报规范,统一。
4、强调了对比研究,是判断两者质量是否一致的重要方法之一。
5、强化了工艺验证,目的是确保大生产时能始终如一地按照申报工艺生产出质量恒定的产品。
6、提出了晶型的要求,晶型的不同,溶解度和稳定性不同。
分析上述新要求和参考指导原则,从而得出结论:仿制药研发的目的是做到规模化生产,强调本地化,以实现“替代性”。
要求是做到“同”。
方法为对比研究。
1.安全性“同”:对于安全性,口服固体制剂控制的主要为有关物质,而液体制剂除控制有关物质外,还需对防腐剂、氧化剂等对人体有影响的物质进行控制。
因此,必须要将防腐剂含量测定定入质量标准。
研究的内容:静态上应包括杂质谱的对比,单个杂质的对比,杂质总量的对比。
动态上的对比为影响因素试验、加速试验的对比,即稳定性对比研究。
仿制药研发流程
仿制药研发流程仿制药的研发流程是一个系统性的、繁琐的过程,大致可以分为以下几个步骤:1.目标药物选择:仿制药的研发通常是在已有的原研药物上进行的,因此首先需要选择目标药物。
选择的标准包括药物的临床需求、市场竞争状况、产业链配套能力等。
2.医药文献调研:了解目标药物的研究背景,包括药物的化学结构、药理学特性、临床应用情况、不良反应等信息。
同时,还需要对原料药、制剂、药理学、药代动力学等方面的文献进行调研,为后续的研发工作提供基础。
3.原料药供应与质量评价:开始寻找原料药的供应商,并进行质量评价。
原料药的质量对于药物的研发至关重要,需要对供应商的生产工艺、质量管理体系等进行彻底的审查。
4.药物优选及剂型选择:根据目标药物的特性、药理学特点、市场需求等因素,选择药物的优选剂型。
药物剂型的选择包括口服制剂、注射制剂、外用制剂等。
5.药物配方设计与试制:通过调整药物的剂型与剂量,设计合理的药物配方。
配方设计需要考虑药物的物理化学性质、药理学特点、稳定性等因素。
设计好的配方进行试制实验,根据试制结果进行必要的调整。
6.药物稳定性评价与优化:对试制出的样品进行药物稳定性评价,包括物理稳定性、化学稳定性、生物稳定性等。
根据评价结果,优化药物的配方和工艺。
7.药物工艺研究:根据药物的成分和性质,开展药物工艺研究。
包括原料评估、制剂制备工艺优化、工艺验证等。
8.生物等效性评价:对仿制药进行生物等效性评价,即与原研药物在体内的药代动力学和生理学效应的比较。
该评价确定了仿制药与原研药的相似性,是否能替代原研药物。
9.临床试验:在完成前期研发工作后,进行临床试验,验证药物的安全性和有效性。
临床试验分为三期,包括对健康志愿者的试验、对患者的试验等。
试验结果需要向监管部门提交并获得批准。
10.生产资质申请:在完成临床试验,获得相关数据支持后,向药品监管部门提交仿制药上市注册申请。
注册申请需要包含药物研发相关的数据和资料。
11.上市与销售:获得相关资质后,仿制药可以正式上市销售。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2)验证工艺
3、初试一批
1)样品全检
2)工艺参数验证
4、中试三批
1)三批全检
2)用于稳定性考察
5、注册三批(BE)
五
质量研究
1、质量研究方法的确定(初试、中试样品)
2、质量标准的方法学验证
1)质量标准的初步验证(对照品、杂质、原料、参比、小试)
2)系统的方法学验证(初试、中试样品)
3、国内外上市情况(生产注册情况)
4、专利规避
5、稳定性、临床、不良反应、说明书等资料
6、原辅料、对照品、杂质信息
二
前期准备
1、参比制剂的采购(原研)
2、原辅料采购(证照、资质、合成工艺、发票、继供能力)
3、对照品、杂质采购
4、仪器、色谱柱、试剂等采购(准备)
5、包材的采购(可放置中试之前)
三
处方前研究
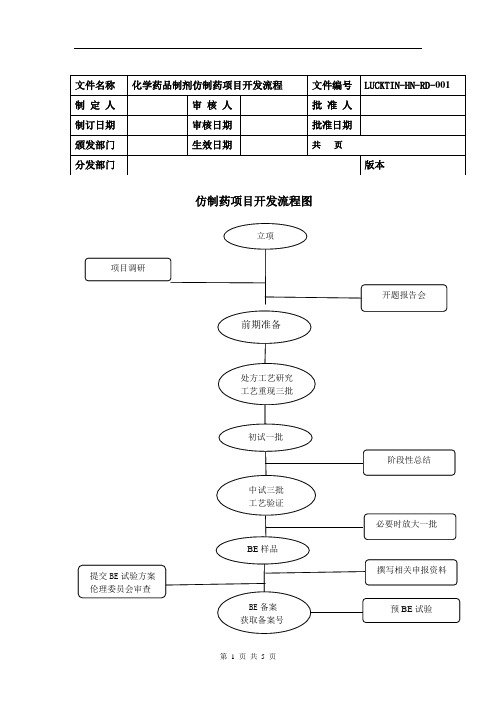
仿制药项目开发流程图
文件名称
化学药品制剂仿制药项目开发流程
文件编号
LUCKTIN-HN-RD-001
制 定 人
审 核 人
批 准 人
制订日期
审核日期
批准日期
颁发部门
生效日期
共 页
分发部门
版本
仿制药研发具体流程
项目
内容
备注
一
品种调研
(立项)
1、原研信息(规格、处方组成、工艺、来源等)
2、质量标准(原研、药典、首仿)
3、质量对比研究(初试1验(含参比制剂)/低温冻融试验
2、包材相容性试验
3、加速试验(含参比制剂)
4、长期试验(含参比制剂)
5、稳定性研究结果的评价
七
BE试验
1、提交BE方案,伦理委员会审核
2、通过审核,提交BE备案,获取备案号
3、预BE试验,正式BE试验
八
申报资料的撰写、整理
1)固体口服制剂可用A01、A02.....
2)液体口服可用B01、B02.........
3)注射剂可用C01、C02...........
4)医疗器械可用D01、D02....等)
1、综述资料
2、药学研究资料
3、药理毒理研究资料
4、BE试验资料
九
向省局提交注册申请
1、省局形式审查
2、省局现场核查(研制现场、生产现场、临床试验现场)
十
资料移交总局
2、总局审评中心审评
2、总局审评过程或有因的核查和抽样检验
十一
完整性审评
1、补充后续稳定性资料
2、完整性通过
十二
批准上市
1、售后
说明:
2)处方组成:辅料种类、规格及资料来源, 不同规格处方或比例是否一致
3)工艺研究:是否微粉化,制粒是干法、湿法、直接压片、包衣目的等
4)方法
常规方法:重量、水分测定、HPLC等
仪器分析:X-光衍射、扫描电镜
四
处方工艺研究
工艺参数研究
1、处方工艺摸索:
1)辅料相容性试验
2)处方筛选
3)工艺参数研究
2、小试验证三批
1、进度计划及预算,参见项目开题报告附件;
2、1-14项,填写主要内容汇总,如有需要,可另附表,附表按编号命名及排序。
3、备注:文件编号XKY-HN-RD-***
RD—研发
HN—海南
XKY—北京鑫开元医药科技有限公司
指导性的文件编号可采用XKY-HN-RD-001、002、003...
项目编号可采用XKY-HN-RD-***
1、原辅料检验(原料研究溶解性、晶型、粒径、水合物、
化学稳定性、引湿性等)
2、方法初步确定(方法建立的原则是筛选出杂质检测能力强的色谱条件并进行有针对性的部分项目方法学验证,用对照品、杂质、原料、参比制剂验证,为各项研究建立适宜的评价方法)
3、原研制剂的逆向研究
1)物理性质:规格、重量、形状、硬度等
